一种用于靶向PSMA的EuK二聚体化合物、衍生物及其应用的制作方法
一种用于靶向psma的euk二聚体化合物、衍生物及其应用
技术领域
1.本发明涉及药物化学、放射性药物化学和临床核医学技术领域,尤其涉及一种用于靶向psma的euk二聚体化合物、衍生物及其应用。
背景技术:
2.在全球范围内,前列腺癌是一种严重威胁男性健康的恶性肿瘤,其发病率仅次于肺癌,并且发病率呈现为快速上升的状态,它已经成为男性肿瘤类疾病的主要死亡原因之一。如何尽早对前列腺患者进行精准分期,并辅以有效的治疗手段以降低死亡率,是本领域研究重点。
3.前列腺特异性膜抗原(prostate-specific membrane antigen,psma)是一种ii型跨膜蛋白,在前列腺癌细胞的细胞膜上表达高度上调,上调程度可以达到正常组织中的100~1000倍,且其上调程度与肿瘤的恶性程度、前列腺癌的gleason评分成正相关。在近些年的研究中,psma作为前列腺癌诊疗的靶点,已广泛应用于前列腺癌的临床诊疗实践中,有多个以psma为靶点的检查、治疗探针及治疗药物被报道,包括正电子发射计算机断层扫描技术(positron emission tomography,pet)和单光子发射计算机断层扫描技术(single photon emission computed tomography,spect)的显像剂以及放射性治疗核素标记的药物已经大量应用于临床,如
68
ga-psma-11、
18
f-dcfpyl、
18
f-psma-1007、
177
lu-psma-617、
123
i-mip-1072、
131
i-mip-1095和
211
at标记的euk衍生物等。
4.组织的病理分型对于疾病的诊断、治疗及预后评估具有重大意义,因而穿刺活检依然是前列腺癌诊断的“金标准”。但在穿刺过程中,为了拿到可用的组织用于病例分析,减少假阳性等,在穿刺手术过程中需要进行多次穿刺,对临床医生的经验要求较高,操作繁琐,且对于远处转移病灶很难通过现有手段通过穿刺活检得到可用于病例分析的样本。并且,病理分析需要数小时甚至几天的时间,时间较长,不能用于外科手术中。
5.[
18
f]psma-1007在之前的研究中被用于指导前列腺癌的穿刺手术,因其脂溶性较高主要通过肝脏排泄,这有效的排除了尿液对膀胱的干扰,可以更准确地识别前列腺癌的原发灶。但是由于
18
f短半衰期的限制(109.8min),留给手术医生的可用于进行穿刺手术的时间窗较短,同时正电子核素能量较高,还需要考虑对医务人员的辐射损伤,不利于在临床中进行推广,因此,这种
18
f核素引导患者穿刺的方法并不实用。
[0006]
此外,核素及其标记的放射性治疗前列腺癌及相关疾病的药物是目前研究的热点,如
223
ra,特别是金属核素
225
ac标记psma,但
225
ac使用高能加速器生产、靶材料来源受限,产量有限、价格贵。
技术实现要素:
[0007]
为了解决上述问题,本发明提供一种具有高活性、高肿瘤靶/非靶比值的用于靶向psma的euk二聚体化合物、衍生物及其应用,以实现更好地诊断、检测以及治疗前列腺癌及相关疾病的效果。
[0008]
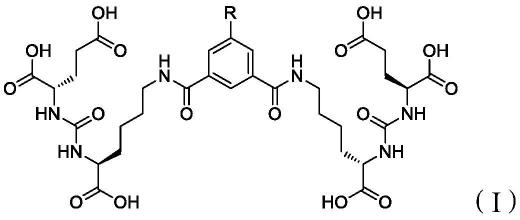
本发明首先提供一种euk二聚体化合物或其药用可接受的衍生物,所述euk二聚体化合物的结构如式(i)所示:
[0009][0010]
其中,r为
123
i、
124
i、
125
i、
127
i、
131
i或
211
at。
[0011]
本发明发现所述化合物标记上述放射性同位素后半衰期均相对较长,可作为psma靶向药物,对前列腺肿瘤进行pet、spect成像或核素治疗,同时可进一步用于首次或重复穿刺快速病理检测,为后续治疗提供良好的指导。在核素治疗方面,
211
at可用中能加速器生产,产量高且价格便宜。
[0012]
当用于显像时,选择r为
123
i、
124
i、
125
i或
131
i的euk二聚体化合物或其药用可接受的衍生物。
[0013]
当用于制备治疗试剂时,选择r为
131
i或
211
at的euk二聚体化合物或其药用可接受的衍生物。
[0014]
本发明进一步提供所述euk二聚体化合物或其药用可接受的衍生物的制备方法:
[0015]
当所述euk二聚体化合物或其药用可接受的衍生物中的r为
123
i、
124
i、
125
i、
131
i或
211
at时,其反应途径如下:
[0016][0017]
各步骤的反应试剂和条件如下:
[0018]
(a)1,4-二氧六环,双三苯基磷二氯化钯,六正丁基二锡,回流;
[0019]
(b)lioh,meoh/h2o,r.t.;
[0020]
(c)2,3,5,6-四氟苯酚,dcc(n,n'-二环己基碳二亚胺),r.t.;
[0021]
(d)h-lys-otbu-ureido-glu(otbu)2,ch2cl2,et3n,r.t.;
[0022]
(e)hcl(1m),h2o2(3%),[
123/124/125/131
i]nai,na
211
at,r.t.;
[0023]
(f)ch2cl2/cf3cooh=1/1(v/v),r.t.,过夜。
[0024]
当所述euk二聚体化合物或其药用可接受的衍生物中的r为
127
i时,其反应途径如下:
[0025][0026]
上述各步骤的反应试剂和条件如下:
[0027]
(a)2,3,5,6-四氟苯酚,dcc(n,n'-二环己基碳二亚胺),r.t.;
[0028]
(b)h-lys-otbu-ureido-glu(otbu)2,ch2cl2,et3n,r.t.;
[0029]
(c)ch2cl2/cf3cooh=1/1(v/v),r.t.,过夜。
[0030]
本发明进一步提供所述的euk二聚体化合物或其药用可接受的衍生物作为psma靶向抑制剂的应用。
[0031]
本发明进一步提供一种psma靶向抑制剂,含有所述的euk二聚体化合物或其药用可接受的衍生物。
[0032]
本发明进一步提供r为
123
i、
124
i、
125
i或
131
i时的euk二聚体化合物或其药用可接受的衍生物作为靶向psma的肿瘤显像剂的应用。
[0033]
本发明进一步提供一种靶向psma的肿瘤显像剂,含有r为
123
i、
124
i、
125
i或
131
i时的euk二聚体化合物或其药用可接受的衍生物。
[0034]
本发明发现,当r为
123
i、
125
i或
131
i时,所述euk二聚体化合物或其药用可接受的衍生物作为spect类靶向psma的肿瘤显像剂;当r为
124
i时,所述euk二聚体化合物或其药用可接受的衍生物作为pet类靶向psma的肿瘤显像剂。
[0035]
本发明进一步提供一种检测试剂,其含有
123
i、
124
i、
125
i、
131
i或
211
at时的euk二聚体化合物或其药用可接受的衍生物。
[0036]
优选地,所述检测试剂为快速穿刺病理阳性检测试剂。
[0037]
本发明进一步提供r为
123
i、
124
i、
125
i、
131
i或
211
at时的euk二聚体化合物或其药用可接受的衍生物在制备前列腺癌及相关疾病的检测试剂中的应用。
[0038]
本发明进一步提供一种前列腺癌及相关疾病的肿瘤核素治疗药物,其含有r为
131
i或
211
at时的euk二聚体化合物或其药用可接受的衍生物。
[0039]
本发明进一步提供r为
131
i或
211
at时的euk二聚体化合物或其药用可接受的衍生物在制备前列腺癌及相关疾病的肿瘤核素治疗药物中的应用。
[0040]
本发明提供的一种用于靶向psma的euk二聚体化合物、衍生物及其应用,在放射性核素标记后,通过小鼠体内分布实验表明,其主要通过肾脏排谢,而在非靶组织和器官代谢快、摄取低。该类化合物与前列腺特异性膜抗原(psma)有很高的亲和性,适合用于前列腺癌诊断、分期、治疗和疗效评估,以及用于穿刺活检中影像引导和快速病理分析。
附图说明
[0041]
为了更清楚地说明本发明或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0042]
图1为本发明实施例1~7化合物的合成路线,图中,a~e表示各步骤的反应试剂及
nmr(600mhz,chloroform-d)δ8.58(t,j=1.8hz,1h),8.35
–
8.26(m,2h),3.95(s,6h),1.57
–
1.51(m,6h),1.36
–
1.31(m,6h),1.16
–
1.09(m,6h),0.89(t,j=7.3hz,9h).
[0055]
实施例2合成化合物2
[0056][0057]
将化合物1(329mg,0.68mmol)溶解于甲醇溶液中,向其中加入氢氧化锂的水溶液,在50℃条件下反应过夜。反应结束后,用1m盐酸溶液中和反应液,减压旋蒸除去甲醇,然后经减压抽滤得到213mg产物2,为白色固体,产率68.7%。1h nmr(400mhz,dmso-d6)δ13.20(s,2h),8.39(dd,j=2.2,1.1hz,1h),8.22(d,j=1.7hz,2h),1.51(q,j=8.0hz,6h),1.30(q,j=7.3hz,6h),1.18
–
1.07(m,6h),0.85(t,j=7.3hz,9h).
[0058]
实施例3合成化合物3
[0059][0060]
将化合物2(200mg,0.44mmol)溶解于ch2cl2溶液中,依次加入2,3,5,6-四氟苯酚(284mg,1.71mmol)与dcc(408mg,1.98mmol),室温下搅拌8h。反应结束后,抽滤除去不溶物,经减压旋蒸除去溶剂后得到粗产物,粗产物经柱色谱分离纯化后,得到319mg化合物3,为无色油状液体,产率96.6%。1h nmr(400mhz,chloroform-d)δ8.93(t,j=1.8hz,1h),8.66
–
8.49(m,2h),7.08(tt,j=9.8,7.0hz,2h),1.61
–
1.53(m,6h),1.36(q,j=7.3hz,6h),1.24
–
1.15(m,6h),0.91(t,j=7.3hz,9h).
[0061]
实施例4合成标记前体4
[0062][0063]
将化合物3(284mg,0.38mmol)溶解于二氯甲烷溶液中,加入2-[3-[1-叔丁酯-(5-氨基戊基)]-脲基]-戊二酸二叔丁酯(479mg,0.98mmol)与三乙胺,室温下搅拌8h。反应结束后,减压旋蒸除去溶剂后得到粗产物,粗产物经柱色谱分离纯化后,得到417mg化合物4,为白色固体,产率80.7%。1h nmr(400mhz,dmso-d6)δ8.51(t,j=5.6hz,2h),8.18(s,1h),7.97(d,j=1.6hz,2h),6.28(t,j=8.3hz,4h),4.08
–
3.91(m,4h),3.31
–
3.19(m,4h),2.22(dq,j=19.3,10.2,9.5hz,4h),1.93
–
1.78(m,2h),1.66(dtd,j=15.0,9.0,6.4hz,4h),1.59
–
1.49(m,12h),1.41
–
1.35(m,54h),1.33
–
1.29(m,10h),1.13
–
1.07(m,6h),0.85(t,j=7.3hz,9h).hrms:m/z计算[c
68h119
n6o
16
sn]
+
为1395.77100,谱图显示为1395.76770。
[0064]
实施例5合成化合物5
[0065][0066]
将5-碘间苯二甲酸(584mg,2.00mmol)溶解于ch2cl2溶液中,依次加入2,3,5,6-四氟苯酚(499mg,3.00mmol)与dcc(826mg,4.00mmol),室温下搅拌8h。反应结束后,抽滤除去不溶物,经减压旋蒸除去溶剂后得到粗产物,粗产物经柱色谱分离纯化后,得到1063mg化合物5,为米白色固体,产率90.3%。1h nmr(600mhz,chloroform-d)δ8.97(t,j=1.6hz,1h),8.83(d,j=1.6hz,2h),7.09(tt,j=9.8,7.0hz,2h).
[0067]
实施例6合成化合物6
[0068][0069]
将化合物5(375mg,0.63mmol)溶解于二氯甲烷溶液中,加入2-[3-[1-叔丁酯-(5-氨基戊基)]-脲基]-戊二酸二叔丁酯(696mg,1.42mmol)与三乙胺,室温下搅拌8h。反应结束后,减压旋蒸除去溶剂后得到粗产物,粗产物经柱色谱分离纯化后,得到789mg化合物6,为白色固体,产率88.1%。1h nmr(600mhz,dmso-d6)δ8.63(t,j=5.6hz,2h),8.30(t,j=1.6hz,1h),8.28(d,j=1.5hz,2h),6.28(dd,j=13.4,8.3hz,4h),4.06
–
4.01(m,2h),3.98(m,2h),3.25(q,j=6.6hz,4h),2.28
–
2.15(m,4h),1.86(dddd,j=13.8,8.8,6.9,5.2hz,2h),1.71
–
1.60(m,4h),1.53(tt,j=14.1,7.5hz,6h),1.40
–
1.36(m,59h),1.32(m,4h).hrms:m/z计算[c
56h91
n6o
16
ina]
+
为1253.54284,谱图显示为1253.53943。
[0070]
实施例7合成标准品7
[0071][0072]
将化合物6(101mg,0.082mmol)溶于7ml二氯甲烷中,搅拌下加入3ml三氟乙酸,室温下反应过夜。反应结束后,经减压旋蒸除去溶剂,加入乙酸乙酯后析出白色固体,固体经乙酸乙酯洗涤3次,石油醚洗涤3次,干燥后得到72mg化合物7,为白色固体,产率98.2%。1h nmr(400mhz,dmso-d6)δ12.42(s,6h),8.66(t,j=5.6hz,2h),8.29(m,3h),6.31(t,j=8.0hz,4h),4.15
–
4.01(m,4h),3.24(q,j=6.6hz,4h),2.31
–
2.17(m,4h),1.92(tt,j=14.1,6.1hz,2h),1.69(tt,j=14.2,8.2hz,4h),1.53(dh,j=19.8,7.0,6.5hz,6h),1.33(p,j=7.7hz,4h).hrms:m/z计算[c
32h42
n6o
16
i]-为893.17075,谱图显示为893.17108。
[0073]
实施例8 125
i标记化合物[
125
i]7的制备
[0074]
称取0.3mg锡前体(化合物4)于玻璃瓶中,加入250μl乙醇使其溶解,随后加入
[
125
i]nai溶液,再依次加入100μl稀盐酸(1m)和100μl h2o2(3%)溶液,在室温条件下反应20min。反应结束后,用碳酸氢钠固体中和反应液,取上层清液进hplc分析,hplc条件为:venusil mp c18 column(agela technologies,4.6mm
×
250mm),1ml/min,uv=254nm,ch3cn/h2o(含0.1%三氟乙酸)=90/10。随后,反应液用氮吹仪吹干,向其中加入300μl三氟乙酸,在50℃条件下反应10min。反应结束后,用氮吹仪将三氟乙酸除尽,向其中加入ch3cn/h2o(v/v,26/74)的混合溶液750μl后,进液相分析和分离,hplc条件为:venusil mp c18 column(agela technologies,4.6mm
×
250mm),1ml/min,uv=254nm,ch3cn/h2o(含0.1%三氟乙酸)=26/74。终产物[
125
i]7通过与对应稳定化合物的共进样分析,进一步对
125
i标记的化合物进行了验证,结果参见图3。
[0075]
实施例9标准品7与psma亲和力测定
[0076]
1)用hepes缓冲溶液(50mm)将待测化合物稀释至不同浓度:
[0077]
400μm、40μm、4μm、400nm、40nm、4nm、0.4nm、0.04nm。
[0078]
2)依次在黑色96酶标板中加入25μl梯度浓度的待测化合物、25μl naag(160μm)和50μl psma重组蛋白溶液(0.4μg/ml)。在酶标仪中混合均匀后,转移至摇床中,在37℃条件下孵育1小时。孵育结束后,每孔加入100μl opa检测试剂,避光孵育3分钟,在ex/em=350/450nm的条件下测定荧光强度。
[0079]
3)通过cheng-prusoff方程,将实验测得的ic
50
值转化为ki。
[0080]
标准品化合物7的抑制psma蛋白酶活性曲线参见图4,结果表明,化合物7与psma的亲和力很高,ki值为38.77
±
8.01pm。
[0081]
实施例10荷瘤鼠体内生物分布实验
[0082]
为了评估[
125
i]7在肿瘤和主要组织器官中的分布,在22rv1荷瘤小鼠中进行了生物分布实验。21只22rv1荷瘤小鼠随机分为7组(n=3/组)。通过尾静脉向小鼠注射[
125
i]7溶液(15μci,100μl)。按规定时间处死3只小鼠(1h、6h、12h、1d、3d、5d、7d),取肿瘤及主要组织器官(血、尿、心、肺、肝、脾、肾、膀胱、肿瘤、脑、肌肉、骨、唾液腺、小肠),称量湿重并测量放射性计数,经时间衰减校正后计算相应的放射性值(%id/g)。[
125
i]7在荷瘤鼠体内生物分布实验结果见图5,结果表明,[
125
i]7在22rv1肿瘤中具有较高的摄取值,注射72小时后,肿瘤部位还有明显的放射性滞留,对于放射性卤素治疗及穿刺病理检查都是有利的。
[0083]
实施例11荷瘤鼠micro-spect/ct小鼠体内生物分布实验
[0084]
分别取右侧前肢腋下接种了22rv1细胞与pc3细胞的裸鼠(即22rv1荷瘤小鼠和pc3荷瘤小鼠)用于spect/ct成像研究。spect/ct图像通过hispect软件重建,并通过vivoquant 2.5软件进行分析。
[0085]
在实验组中,选择三只22rv1荷瘤小鼠注射[
125
i]7的生理盐水溶液(45μci,100μl)。将小鼠按规定时间置于麻醉箱内,使用1.0%异氟烷/空气混合物保持麻醉,进行micro-spect/ct图像采集,结果见图6中的图(a)。根据图(a)可得,[
125
i]7可以和psma高表达的22rv1肿瘤特异性结合,在肿瘤中有明显的摄取和保留,注射72小时后,肿瘤部位还有明显的放射性滞留。
[0086]
在对照组中,选择三只pc3荷瘤小鼠注射[
125
i]7的生理盐水溶液(45μci,100μl)。将小鼠按规定时间置于麻醉箱内,使用1.0%异氟烷/空气混合物保持麻醉,进行micro-spect/ct图像采集,结果见图6中的图(b)。根据图(b)可得,[
125
i]7不与psma低表达的pc3细
胞结合,表明[
125
i]7与psma是特异性结合。
[0087]
在抑制组中,选择三只22rv1荷瘤小鼠经尾静脉共注射抑制剂zj43(50mg/kg)与[
125
i]7(45μci,100μl)的生理盐水溶液。将小鼠按规定时间置于麻醉箱内,使用1.0%异氟烷/空气混合物保持麻醉,进行micro-spect/ct图像采集,结果见图6中的图(c)。根据图(c)可得,[
125
i]7可以被抑制剂zj43明显抑制,在肿瘤和肾脏没有放射性信号浓集,表明[
125
i]7与psma是特异性结合。
[0088]
在本发明中,[
123/124/131
i]7的效果与[
125
i]7的效果相当,由于篇幅有限,在此不再一一列举。
[0089]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1