一种海洋来源的萘啶类抗炎活性化合物及其制备方法
1.本发明涉及海洋生物及医药技术领域,具体地说,涉及一种从海洋海绵aaptos suberitoides中分离得到的萘啶类抗炎活性化合物及其制备方法。
背景技术:
2.炎症是机体对各种外源性或内源性损伤所做出的一种防御性反应。如果炎症得不到有效控制,就会导致类风湿性关节炎、动脉粥样硬化、糖尿病甚至癌症等各种疾病。目前,临床上所用的抗炎药物主要有非甾体抗炎药及糖皮质激素,但是这两类药物在长期大量使用后均存在一些严重的不良反应。因此,开发更加安全有效的新型抗炎药物具有广阔的临床应用前景。
3.巨噬细胞是人体内一种重要的免疫细胞,在启动炎症反应和抵抗外界侵染中起着较为关键的作用。巨噬细胞感受外界刺激(如病毒、物理伤害以及药物等)后能够产生一系列炎症物质,包括细胞因子(il-6、il-12等)、趋化因子以及炎症介质。一部分物质会表现出促炎特性,这些物质是导致炎症反应加重的重要因素。因此,想要控制炎症反应的加重以及缓解炎症反应的发展,抑制巨噬细胞分泌炎症物质已是研究的热点之一。lps是十分重要的致炎因子,它能够刺激体内的巨噬细胞合成和释放多种内源性活性因子,进而诱发炎症。利用lps处理巨噬细胞是常用的体外炎症模型造模手段。
4.aaptos suberitoides属于aaptos属(porifera,demospongiae,suberitida,suberitidae),广泛分布于越南、日本、印度尼西亚和加勒比海浅水水域。以往的化学研究表明,其主要化学成分为aaptamine类生物碱,至今未见其抗炎活性的相关报道。
技术实现要素:
5.本发明的目的在于提供一种海洋来源的萘啶类抗炎活性化合物,第二目的是提供海洋来源的萘啶类抗炎活性化合物的制备方法。
6.本发明的第一目的采用以下技术方案实现:
7.一种海洋来源的萘啶类抗炎活性化合物,其特征在于:所述化合物是从海绵aaptos suberitoides中分离得到的,其分子式为c
10
h8n2o3,结构式为:
[0008][0009]
该化合物命名为:4-carbomethoxy-5-keto-1,6-naphthyridine。
[0010]
本发明的第二目的采用以下技术方案实现:
[0011]
本发明所述萘啶类抗炎活性化合物的制备方法,包括以下步骤:
[0012]
1、原料处理:将冷冻保存的海绵样品用粉碎机粉碎后,在室温下用甲醇动态冷浸提取3次,每次浸泡3天;合并3次提取液,40℃温度条件下减压浓缩;然后,用无水甲醇溶解脱盐3次,制得浸膏;
[0013]
2、减压硅胶柱层析:将浸膏溶解于1.5-3倍重量的纯甲醇中,再用浸膏重量1-3倍的100-200目硅胶拌样后上减压硅胶柱;再分别用石油醚与乙酸乙酯体积配比为100:1、50:1、25:1、10:1、5:1、2:1、1:1、1:2、1:4的石油醚乙酸乙酯溶液和二氯甲烷与甲醇体积配比为20:1、10:1、5:1、0:1的二氯甲烷甲醇溶液进行梯度洗脱,分别收集各部分的洗脱液并浓缩,用tlc薄层色谱监测并合并相同的部分;
[0014]
3、ods柱层析:取步骤2中体积配比为1:2的石油醚乙酸乙酯溶液洗脱得到的组分,过ods柱,再分别用浓度为甲醇与水体积配比为1:4、3:7、4:6、5:5、6:4、7:3、8:2的甲醇溶液进行梯度洗脱,分别收集各部分的洗脱液并浓缩,用tlc薄层色谱监测并合并相同的部分;
[0015]
4、高效液相色谱分离:取步骤3中体积配比为3:7甲醇溶液洗脱得到的组分通过高效液相分析用ods c18柱制备可得所述化合物,保留时间为25.0分钟,即制得所述化合物。
[0016]
优选的,步骤2中,所述减压硅胶柱的填料硅胶为200-300目。
[0017]
优选的,步骤4中,所述ods c18柱采用ymc ods c18柱,型号为10
×
250mm,填料粒径为5μm,流动相为乙腈/水15:85v/v,流速为1.5ml/min。
[0018]
有益效果:本发明所述的萘啶类抗炎活性化合物是从海绵aaptossuberitoides中分离出来的新化合物,该化合物的制备方法简单易行,人工合成也易于实现。通过核磁共振(nmr)、质谱(ms)等方法,结合相关文献对比鉴定化合物结构,鉴定该海绵来源新化合物为4-carbomethoxy-5-keto-1,6-naphthyridine;同时,采用griess法对化合物进行抗炎活性测试,并采用rt-qpcr和western blot法对化合物抗炎活性机制进行探究,发现该化合物可显著抑制lps诱导的raw264.7细胞炎症,通过mapk信号通路调控炎症,降低促炎因子il-1β、il-6和tnf-αmrna水平以及inos和cox2蛋白水平的表达,从而抑制炎症的发生。本发明首次披露该具有良好抗炎活性的新化合物,为开发利用我国海洋生物资源及抗炎新药的研发提供了科学依据。
附图说明
[0019]
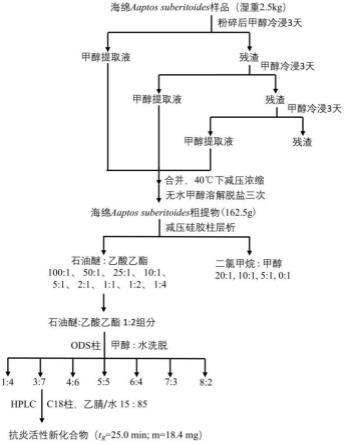
图1为本发明所述化合物的制备方法工艺流程图。
[0020]
图2为本发明所述化合物的高分辨质(hresims)谱图。
[0021]
图3为本发明所述化合物的核磁共振氢(1h nmr)谱图。
[0022]
图4为本发明所述化合物的核磁共振碳(
13
c nmr)谱图。
[0023]
图5为本发明所述化合物的核磁共振氢(1h-1
h cosy)谱图。
[0024]
图6为本发明所述化合物的核磁共振氢(hsqc)谱图。
[0025]
图7为本发明所述化合物的核磁共振氢(hmbc)谱图。
[0026]
图8为本发明所述化合物对raw264.7细胞产生no的影响的示意图。
[0027]
raw264.7细胞以1
×
105ml-1
浓度种于24孔板,化合物(40μg/ml、80μg/ml)37℃预处理细胞1h后,lps(1μg/ml)37℃处理24h,使用no检测试剂盒即griess法对细胞培养上清中no含量进行检测;测定样本在520nm处的吸光度,用样品和标准品的吸光度作图;
##
p<0.01vs.对照组,有统计学意义;
***
p<0.001vs.lps单独处理组,有统计学意义。
[0028]
图9为本发明所述化合物对raw264.7细胞毒活性的示意图。
[0029]
以不同浓度化合物(20μg/ml、40μg/ml、60μg/ml、80μg/ml、100μg/ml)37℃处理细胞48h或以不同浓度化合物预处理细胞1h后,lps(1μg/ml)37℃处理48h;
*
p<0.05,有统计学意义。
[0030]
a.化合物单独处理对raw264.7细胞的影响。
[0031]
b.化合物+lps共同处理对raw264.7细胞的影响。
[0032]
图10为本发明所述化合物降低lps诱导的raw264.7细胞中促炎因子mrna表达水平的示意图。
[0033]
化合物(40μg/ml、80μg/ml)37℃预处理细胞1h后,lps(1μg/ml)37℃处理24h,处理后从所有组中提取rna并逆转录为cdna,将逆转录后的cdna用试剂盒进行rt-qpcr,用cq值(2-δδcq
法)绘图,用β-actin基因归一化计算各基因的相对表达;
####
p<0.0001vs.对照组,有统计学意义,
****
p<0.0001vs.lps单独处理组,有统计学意义。
[0034]
a.tnf-α的相对表达;b.il-1β的相对表达;c.il-6的相对表达。
[0035]
图11为本发明所述化合物降低lps激活的raw264.7细胞中促炎因子inos和cox2的mrna和蛋白表达的示意图。
[0036]
化合物(40μg/ml、80μg/ml)37℃预处理细胞1h后,lps(1μg/ml)37℃处理24h;处理后从所有组中提取rna并逆转录为cdna,将逆转录后的cdna用试剂盒进行rt-qpcr;用cq值(2-δδcq
法)绘图;用β-actin基因归一化计算各基因的mrna相对表达;对于蛋白表达,从细胞中获取蛋白并进行western blotting,用三个独立的灰度扫描值计算表达水平;用gapdh基因归一化计算各基因的蛋白相对表达。
##
p<0.01,
###
p<0.001,
####
p<0.0001vs.对照组,有统计学意义;
**
p<0.01,
***
p<0.001,
****
p<0.0001vs.lps单独处理组,有统计学意义。
[0037]
a.inos的mrna相对表达;b.cox2的mrna相对表达;c.inos和cox2的western blot图;d.inos的蛋白相对表达;e.cox2的蛋白相对表达。
[0038]
图12为本发明所述化合物对lps激活的raw264.7细胞mapks通路的影响的示意图。
[0039]
化合物(40μg/ml、80μg/ml)37℃预处理细胞1h后,lps(1μg/ml)37℃处理24h;对于蛋白表达,从细胞中获取蛋白并进行western blot,用三个独立的灰度扫描值计算表达水平;用蛋白质的总蛋白和磷酸化蛋白归一化计算相对表达。
###
p<0.001,
####
p<0.0001vs.对照组,有统计学意义;
***
p<0.001,
****
p<0.0001vs.lps单独处理组,有统计学意义。
[0040]
a.mapks通路的western blot图;b.p-p38/p38的蛋白相对表达;c.p-erk/erk的蛋白相对表达;d.p-jnk/jnk的蛋白相对表达。
具体实施方式
[0041]
下面结合附图和具体实施方式对本发明作进一步说明。
[0042]
实施例:
[0043]
本实施例所述海洋来源的萘啶类抗炎活性化合物,其特征在于:所述化合物是从海绵aaptos suberitoides中分离得到的,其分子式为c
10
h8n2o3,结构式为:
[0044][0045]
该化合物命名为:4-carbomethoxy-5-keto-1,6-naphthyridine。
[0046]
所述海绵aaptos suberitoides于2012年采自于西沙永兴岛海域,并将其于-20℃冷冻保存。
[0047]
如图1所示,所述萘啶类抗炎活性化合物的制备方法包括以下步骤:
[0048]
1、原料处理:将冷冻保存的湿重2.5kg的海绵样品用粉碎机粉碎后,在室温下用甲醇动态冷浸提取3次,每次浸泡3天;合并3次提取液,40℃温度条件下减压浓缩;然后,用无水甲醇溶解脱盐3次,制得浸膏162.5g(海绵aaptos suberitoides粗提物);
[0049]
2、减压硅胶柱层析:将浸膏溶解于1.5-3倍重量的纯甲醇中,再用浸膏重量1-3倍的100-200目硅胶拌样后上减压硅胶柱,所述硅胶减压柱的填料硅胶为200-300目;再分别用石油醚与乙酸乙酯体积配比为100:1、50:1、25:1、10:1、5:1、2:1、1:1、1:2、1:4的石油醚乙酸乙酯溶液和二氯甲烷与甲醇体积配比为20:1、10:1、5:1、0:1的二氯甲烷甲醇溶液进行梯度洗脱,分别收集各部分的洗脱液并浓缩,用tlc薄层色谱监测并合并相同的部分;
[0050]
3、ods柱层析:取步骤2中体积配比为1:2的石油醚乙酸乙酯溶液洗脱得到的组分,过ods柱,再分别用浓度为甲醇与水体积配比为1:4、3:7、4:6、5:5、6:4、7:3、8:2的甲醇溶液进行梯度洗脱,分别收集各部分的洗脱液并浓缩,用tlc薄层色谱监测并合并相同的部分;
[0051]
4、高效液相色谱分离:取步骤3中体积配比为3:7甲醇溶液洗脱得到的组分通过高效液相分析用ods c18柱(所述ods c18柱采用ymc ods c18柱,型号为10
×
250mm,填料粒径为5μm,流动相为乙腈/水15:85v/v,流速为1.5ml/min)制备可得所述化合物,保留时间为25.0分钟,即制得所述化合物。
[0052]
化合物结构解析
[0053]
取制备的萘啶类抗炎活性化合物,通过核磁共振(nmr)、质谱(ms)等方法,并结合相关文献对比,对其结构进行鉴定,结果如下:该化合物为棕色针状结晶,由高分辨质谱确定分子式为c
10
h8n2o3([m+h]
+
m/z 205.0612;计算值205.0608),如图2所示。氢谱中显示两组耦合质子信号8.96,7.45(each,1h,d,j=4.3hz)和δ
h 7.52,6.67(each,1h,d,j=9.0hz),如图3所示;如图6所示,hsqc谱图确定4个氢质子分别连与次甲基碳δc154.8,118.8,134.0,106.2。碳谱低场区还显示4个季碳信号(δ
c 141.6,117.0,160.8,154.8),如图4所示。以上信号为1,6-萘啶生物碱的特征性信号。另外,氢谱中在δh3.85处还显示一个甲氧基信号与δ
c 52.6相关,碳谱中还显示一个羰基碳信号(δ
c 168.0)。如图7所示,在hmbc谱图中,h-2(δ
h 8.96)与c-3(δ
c 118.8),c-4(δ
c 141.6),和c-8a(δ
c 154.8)相关,h-3(δ
h 7.45)与c-2(δ
c 154.8),c-9(δ
c 168.0),和c-4a(δ
c 117.0)相关,h-7(δ
h 7.52)与c-5(δ
c 160.8),c-8(δ
c 106.2)和c-8a(δ
c 154.8)相关,h-8(δ
h 6.67)与c-4a,c-7(δ
c 134.0)相关,甲氧基信号(δ
h 3.85)与c-4和c-9相关。
[0054]
由以上相关信号推测,本发明所述萘啶类抗炎活性化合物的结构与文献报道的3,5-dicarbomethoxy-1,6-naphthyridine结构相似,不同之处在于c-5的羰基被酮基替代。因
此,本发明所述萘啶类抗炎活性化合物确定为4-carbomethoxy-5-keto-1,6-naphthyridine。
[0055]
表1:化合物的1d、2d nmr数据(500m,dmso-d6)
[0056]
positionδh,mult(j in hz)δchmbc1
ꢀ‑ꢀ
28.96(d,j=5.4hz)154.8c-3,4,8a37.45(d,j=6.0hz)118.8c-2,4a,94 141.6 4a 117.0 5 160.8 6
ꢀ‑ꢀ
77.52(d,j=9.0hz)134.0c-5,8,8a86.67(d,j=9.0hz)106.2c-4a,,7,8a,8a 154.8 9 168.0 9-och33.85(s)52.6c-4,9
[0057]
抗炎活性测定实验
[0058]
细胞:小鼠来源的巨噬细胞株raw264.7,培养于含10%的胎牛血清、100u/ml青霉素、链霉素的1640培养液,置于5%co2、37℃培养箱中培养,1-2天换液1次。待细胞生长至70%-80%融合度后进行传代,2-3d传代1次。
[0059]
1、cck8法检测化合物对raw264.7细胞活力的影响
[0060]
取对数生长期细胞,调整raw264.7细胞悬液浓度为5
×
104ml
-1
,加入96孔板内,每孔100μl,置于5%co2、37℃培养箱中培养过夜,之后加入终浓度分别为0、20μg/ml、40μg/ml、60μg/ml、80μg/ml、100μg/ml的化合物,每组设3个复孔,继续培养48h。每孔加入cck8试剂10μl,继续培养2h。终止培养,在酶标仪a450nm处测量各孔的吸光度值,计算化合物对细胞的抑制率。
[0061]
2、化合物对lps诱导的raw264.7细胞释放no的影响
[0062]
取对数生长期细胞,调整细胞悬液浓度为1
×
105ml
-1
,取1ml加于24孔细胞培养板内,置5%co2、37℃培养箱中培养过夜,根据预实验结果,每孔分别加入40μg/ml、80μg/ml的化合物孵育1h后,再加入或不加入终浓度为1μg/ml的lps,置培养箱中继续培养24h。取细胞上清,通过griess试剂法,酶标仪a540nm处检测细胞培养上清中的no含量。
[0063]
3、化合物对lps诱导的raw264.7细胞mrna表达的影响
[0064]
取对数生长期细胞,调整细胞悬液浓度为2.5
×
105ml
-1
,取2ml加于6孔细胞培养板内,置5%co2、37℃培养箱中培养过夜。每孔分别加入40、80μg/ml的化合物孵育1h后再加入或不加入终浓度为1μg/ml的lps,置培养箱中继续培养24h。处理后用trizol试剂提取总rna。使用逆转录试剂盒将分离的总rna逆转录为cdna。从genebank中获得序列,采用ncbi设计引物,引物见表1,在荧光定量pcr仪上采用相应的引物、cdna等材料按步骤进行扩增,采用2
‑△△
ct
相对定量法进行基因表达分析,如下表所示:
[0065][0066]
4、化合物对lps诱导的raw264.7细胞蛋白表达的影响
[0067]
取对数生长期细胞,调整细胞悬液浓度为2.5
×
105ml
-1
,取2ml加于6孔细胞培养板内,置5%co2、37℃培养箱中培养过夜。每孔分别加入40μg/ml、80μg/ml的化合物孵育1h后再加入或不加入终浓度为1μg/ml的lps,置培养箱中继续培养24h。将ripa缓冲液加入细胞中,提取总蛋白,然后用bca蛋白检测试剂盒估算蛋白浓度。将10μg的蛋白质加入sds-page进行分离并转膜,5%脱脂牛奶室温封闭1-2h,然后在4℃与稀释的一级抗体孵育过夜。用1
×
tbst溶液洗膜,并用辣根过氧化物酶偶联二级抗体在室温下孵育1h,再次洗涤。最后,通过ecl化学发光法显影成像并分析结果。
[0068]
5、统计分析
[0069]
所有数据均用x
±
s表示。与对照组比较,差异有统计学意义(
#
p<0.05,
###
p<0.001,
####
p<0.0001);与lps处理组比较(
*
p<0.05,
**
p<0.01,
***
p<0.001,
****
p<0.0001)。vs.对照组,有统计学意义;采用one-way anova检验。
[0070]
实验结果解析:
[0071]
1、化合物对lps诱导的raw264.7细胞no含量的影响
[0072]
通过实验测定了化合物对lps诱导的raw264.7细胞产生no水平的影响。如图8所示,与对照组相比,lps刺激导致raw264.7细胞中no含量显著增加;与lps处理组比较,化合物+lps处理组均显著降低no水平。在浓度为40μg/ml、80μg/ml时,与lps处理组相比,raw264.7细胞no的释放量分别减少了62%、72%。
[0073]
2、化合物对raw264.7细胞活力的影响
[0074]
在深入研究化合物的抗炎作用之前,采用cck8法测定化合物(图9a)或与lps共处理(图9b)对细胞活性的影响。图9a的结果显示,化合物在20μg/ml、40μg/ml、60μg/ml、80μg/ml、100μg/ml浓度下均无细胞毒性。与对照组相比,在100μg/ml浓度下,细胞存活率仍高达91%。
[0075]
为了研究化合物与lps合用对raw264.7细胞的毒性作用,用不同浓度(20μg/ml、40μg/ml、60μg/ml、80μg/ml、100μg/ml)的化合物与lps(1μg/ml)共处理细胞24h,cck8法测定细胞活性。结果显示,当化合物与lps合用时,当浓度达到80μg/ml时,对raw264.7细胞的毒性作用无显著性差异。因此,根据raw264.7细胞no的产生和细胞毒性结果,选择40μg/ml、80μg/ml的化合物进行进一步的实验。
[0076]
3、化合物对lps诱导的raw264.7细胞分泌促炎细胞因子的影响
[0077]
据研究,raw264.7细胞受lps刺激后,产生炎症,释放大量的促炎细胞因子如tnf-α、il-6、il-1β等。为了确定化合物是否具有抗炎活性,采用rt-qpcr方法检测il-1β、il-6和tnf-α的mrna表达水平。如图10所示,与对照组相比,lps处理组tnf-α、il-1β和il-6的mrna表达水平显著升高;与lps处理组相比,化合物+lps处理组显著降低了lps诱导的tnf-α(图10a)、il-1β(图10b)和il-6(图10c)mrna的表达。这些结果表明了化合物在转录水平上抑制了促炎细胞因子的表达。
[0078]
4、化合物对lps诱导的raw264.7细胞中促炎因子inos和cox-2表达的影响
[0079]
inos促进no的合成,cox-2催化花生四烯酸合成pge2。no和pge2均可引起炎症部位的细胞损伤。因此,抑制inos和cox-2的表达可以减轻炎症反应。为观察化合物是否具有抑制inos和cox-2表达的作用,采用rt-qpcr和western blotting方法分析cox-2和inos的mrna和蛋白水平表达。
[0080]
如图11a、b所示,与对照组相比,lps处理组细胞中inos和cox-2的mrna表达均显著升高;与lps处理组相比,化合物+lps处理组显著降低上述细胞因子的基因表达水平,化合物(80μg/ml)+lps处理组甚至低于空白对照组。
[0081]
如图11c、d、e所示,与对照组相比,lps处理组细胞中inos的表达增加了1.44倍;化合物在80μg/ml时,其抑制率为27%。此外,lps处理组cox-2的表达较未处理的对照组增加1.78倍,化合物(40和80μg/ml)+lps处理组cox-2的表达分别降低41%和56%。
[0082]
因此,化合物的抗炎作用与其抑制inos和cox-2的表达有关。
[0083]
5、化合物对lps诱导的raw264.7细胞mapk信号通路的影响
[0084]
丝裂原活化蛋白激酶(mapk)信号通路在炎症中起关键作用。mapks的磷酸化与cox-2和inos的激活有关。因此,为了研究和证实化合物是否通过mapk信号通路抑制lps刺激的raw 264.7细胞产生no,抑制cox-2和inos的表达,进行了western blot实验。结果表明,如图12所示,与对照组相比,lps诱导p38、erk和jnk的磷酸化水平分别增加1.5倍、2.1倍和1.8倍。与lps处理组相比,化合物在40μg/ml时使erk1和jnk的磷酸化水平分别降低36%和43%,而对p38的磷酸化水平无抑制作用。此外,当浓度为80μg/ml时,化合物使p38、erk、jnk的磷酸化水平分别降低53%、58%、51%。由此提示化合物通过mapk信号通路抑制lps诱导的raw 264.7细胞的炎症反应。
[0085]
本发明中所述的参考文献如下:
[0086]
[1]kim s,choi h s,ko y,et al.5-hydroxymaltol derived from beetroot juice through lactobacillus fermentation suppresses inflammatory effect and oxidant stress via regulating nf-kb,mapks pathway and nrf2/ho-1 expression[j].antioxidants,2021,10(8):1324.
[0087]
[2]trang d t,tai b h,hang d t t,et al.four new aaptamine alkaloids from marine sponge aaptos aaptos.nat prod res.2022 oct;36(19):5022-5031.
[0088]
[3]qianqian h,shuang m,na n,et al.a review of the secondary metabolites from the marine sponges of the genus aaptos.natural product communications,2020,15(9):1-12.
[0089]
综上所述,本发明所述的萘啶类抗炎活性化合物通过核磁共振(nmr)、质谱(ms)等
方法,结合相关文献对比鉴定化合物结构,鉴定该海绵来源新化合物为4-carbomethoxy-5-keto-1,6-naphthyridine;同时,采用griess法对化合物进行抗炎活性测试,并采用rt-qpcr和western blot法对化合物抗炎活性机制进行探究,发现该化合物可显著抑制lps诱导的raw264.7细胞炎症,通过mapk信号通路调控炎症,降低促炎因子il-1β、il-6和tnf-αmrna水平以及inos和cox2蛋白水平的表达,从而抑制炎症的发生。本发明首次披露该具有良好抗炎活性的新化合物,为开发利用我国海洋生物资源及抗炎症新药的研发提供了科学依据。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1