一种孤儿受体GPR151的新用途
一种孤儿受体gpr151的新用途
技术领域
1.本发明属于生物医药技术领域,涉及一种孤儿受体gpr151的新用途,具体涉及孤儿受体gpr151在筛选或制备预防、诊断或治疗结肠炎的药物中的应用。
背景技术:
2.炎症性肠病(inflammatory bowel disease,ibd)是一种消化道内的慢性炎症性疾病,包括克罗恩病(crohn's disease,cd)和溃疡性结肠炎(ulcerative colitis,uc),典型症状为:腹泻、直肠出血、腹痛、疲劳和体重减轻。目前造成ibd的因素主要包括遗传因素、免疫系统的异常反应及外界环境刺激。通常针对ibd的治疗主要包括内科治疗和外科手术治疗两种方式。内科治疗一般采用糖皮质激素和tnf抑制剂等药物治疗,但会出现治疗无效或耐药或严重的副作用等情况。因此,从新的角度深入研究炎症性肠病的治疗以寻找有效的药物作用靶点具有重要的理论和实际意义。
3.孤儿受体gpr151为a类视紫红质家族的成员之一,gpr151最初被鉴定为与gpcr10、gpcr-2037、galrl类甘丙肽受体具有同源性。视紫红质样家族的序列结构系统发育分析将gpr151与galr1(甘丙肽受体1)、galr2、galr3和kisspeptin受体(kiss1r/gpr54)一起归为“第14类”中。另外,可比性序列分析将gpr151归为更广泛的包括生长抑素、阿片类药物、甘丙肽和kisspeptin受体“sog”亚家族中。gpr151表达分布广泛,在许多组织,如胃肠道黏膜、小肠、结肠、脾脏、肺等中均有表达。目前有研究报道gpr151在脊髓中表达显著升高,从而介导神经病理性疼痛。然而,尚未有报道gpr151直接参与结肠炎等炎症的发生发展。
技术实现要素:
4.针对现有技术的不足,本发明提供一种孤儿受体gpr151的新用途,通过实验发现可将gpr151作为靶点,可以将抑制其表达和功能的抑制剂作为结肠炎的有效治疗药物。
5.本发明是通过以下技术方案实现的:
6.一种孤儿受体gpr151在筛选或制备预防、诊断或治疗结肠炎的药物中的应用,将孤儿受体gpr151作为靶点。
7.一种孤儿受体gpr151的抑制剂在制备预防、诊断或治疗结肠炎的药物中的应用。
8.优选地,所述抑制剂为抑制gpr151 mrna的核酸分子,所述核酸分子为sirna或shrna;
9.所述sirna或shrna具有如seq id no.5所示的序列。
10.优选地,所述sirna采用甲氧基或胆固醇进行修饰。
11.优选地,所述抑制剂为抑制gpr151 mrna的重组载体,包括能转录出抑制gpr151 mrna的核酸分子sirna或shrna的序列以及载体,所述序列嵌入载体中;
12.所述sirna或shrna具有如seq id no.5所示的序列。
13.优选地,所述载体为慢病毒载体或腺相关病毒载体。
14.一种预防、诊断或治疗结肠炎的药物组合物,包括孤儿受体gpr151的抑制剂。
15.优选地,还包括药学上可接受的载体。
16.本发明的有益效果如下:
17.本发明通过挖掘公共geo数据库,利用r语言分析,最终挑选出未被报道有抗炎功能且能通过实验验证的基因gpr151。随后,通过tnbs诱导小鼠结肠炎模型,提取结肠的mrna进行qpcr检测,发现gpr151 mrna水平在tnbs诱导的结肠炎模型维持阶段升高2倍左右,提示gpr151可能在结肠炎炎症维持阶段发挥作用。通过抑制gpr151表达或抑制其功能都能够有效缓解结肠炎,说明gpr151参与结肠炎的发生发展。综上,本发明通过实验发现可将gpr151作为靶点,可以将抑制其表达和功能的抑制剂作为结肠炎的有效治疗药物。
附图说明
18.图1为实施例1中tnbs诱导的小鼠结肠炎模型中各参数变化:a为tnbs诱导小鼠结肠炎后小鼠体重的变化,b为tnbs诱导小鼠结肠炎后小鼠结肠长度的变化,c为tnbs诱导小鼠结肠炎后小鼠结肠中gpr151基因表达的变化;图中数据代表means
±
sem(n=3或4);与指定组相比,
*
p<0.05,
***
p<0.001;
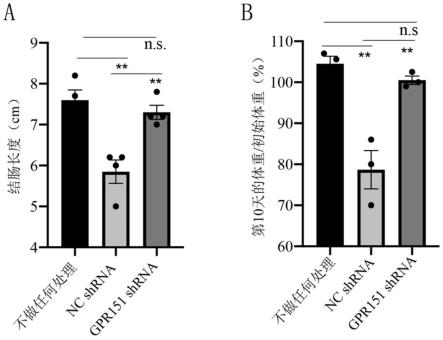
19.图2为实施例2中gpr151shrna抑制tnbs诱导的结肠炎的进展:a为gpr151-shrna对结肠炎小鼠结肠长度的影响,b为gpr151-shrna对结肠炎小鼠体重的影响;图中数据代表means
±
sem(n=3或4);与指定组相比,
**
p<0.01;
20.图3为实施例2中敲除gpr151基因后抑制tnbs诱导小鼠结肠炎的进展:a为各组小鼠的结肠组织标本,b为敲除gpr151基因对结肠炎小鼠结肠长度的影响,c为敲除gpr151基因对结肠炎小鼠体重的影响,d为he染色结果;图中数据代表means
±
sem(n=3或4);与指定组相比,
*
p<0.05,
**
p<0.01,
***
p<0.001。
具体实施方式
21.下面结合附图与具体实施例对本发明做进一步详细说明。
22.实施例1
23.tnbs(2,4,6-三硝基苯磺酸)与乙醇灌肠一次致炎是目前最为常用的结肠炎模型建立方法。tnbs处理小鼠可建立模拟临床结肠炎的临床前模型,其产生的免疫反应是th1介导的,特征在于cd4
+
t细胞、嗜中性粒细胞和巨噬细胞的浸润,形成横向进展的炎症,导致透壁结肠炎。该模型持续时间较长,可充分体现急性炎症向慢性炎症迁延转化过程,并且其与临床上的结肠炎具有极高的相似度。因此本实施例通过tnbs诱导小鼠结肠炎模型,提取结肠的mrna进行qpcr检测,以观察gpr151在tnbs诱导的结肠炎的发生发展阶段的表达,具体步骤如下:
24.1、tnbs诱导小鼠结肠炎模型的建立
25.将禁食24h、不禁饮的c57bl/6j小鼠随机分成50%酒精对照组、tnbs结肠炎模型组,每组4只。
26.(1)50%酒精对照组:给予50%酒精100μl灌肠1次。
27.(2)tnbs模型组:给予2.5% tnbs/50%酒精100μl灌肠1次后,于第5天结束实验。
28.监测各组小鼠每天的体重变化,小鼠处死后收集结肠组织标本,记录结肠的长度,rt-pcr法检测小鼠结肠组织中gpr151 mrna表达水平。
29.2、rna提取及实时荧光定量pcr
30.按照trizol法抽提总rna,测定浓度后取1μg总rna,参考vazyme公司hiscriptⅱ1st strand cdna synthesis kit的说明进行逆转录反应。得到的cdna产物稀释8倍用于实时荧光定量pcr的模板,每个pcr体系加入2μl模板,参考vazyme公司aceq qpcr sybr green master mix的说明进行,所用引物序列如下表1所示。结果分析采用2-δδct
法分析。
31.表1引物序列
32.序列名称seq id序列gpr151forward15
’‑
cctagtagctccaagtcagaca-3’gpr151reverse25
’‑
accttaggtggtctttgagtctc-3’gapdh forward35
’‑
aaatggtgaaggtcggtgtgaac-3’gapdh reverse45
’‑
caacaatctccactttgccactg-3’33.3、实验结果
34.(1)tnbs诱导小鼠产生结肠炎
35.tnbs经灌肠的方式诱导小鼠结肠炎的产生,如图1中a所示,tnbs模型组与50%酒精对照组(ctrl)相比,从给药后第3天开始体重显著降低(n=4,
*
p<0.05)。实验结束时处死小鼠并取小鼠结肠,测量小鼠结肠长度,如图1中b所示,结果表明,与50%酒精对照组相比,tnbs模型组小鼠结肠长度显著变短(n=4,
*
p<0.05)。体重减轻和结肠缩短说明tnbs诱导小鼠产生炎症,结肠炎模型建立成功。
36.(2)tnbs诱导的小鼠结肠炎模型中gpr151基因表达增加
37.利用tnbs经灌肠的方式诱导小鼠结肠炎产生。到第5天实验结束时,取小鼠结肠,通过qpcr分析结肠中gpr151基因表达情况。如图1中c所示,tnbs模型组的结肠中gpr151 mrna表达均显著性增加(n=3,
***
p<0.001),gpr151mrna水平在tnbs诱导的结肠炎模型维持阶段升高2倍左右。这表明gpr151参与结肠炎的发生发展。
38.实施例2抑制gpr151的表达对结肠炎的影响
39.1、设计合成小鼠gpr151 shrna
40.通过美国国立生物技术信息中心(ncbi)数据库中获取小鼠gpr151 mrna的序列全长(nm_181543.1),根据rnai原理,结合设计软件,设计针对小鼠gpr151基因转录本的3个候选shrna,经blast比对检查以保证和其他基因没有同源性,再进行化学合成。
41.2、筛选高效靶向gpr151-shrna
42.以2
×
105(个/孔)细胞数接种于24孔板中,待细胞生长汇合度达到70%~90%时,进行gpr151-shrna干扰效率筛选实验。转染48h后收集细胞,通过qpcr鉴定gpr151-shrna的干扰效果。
43.结果表明,3个候选shrna中只有1个候选shrna的干扰效率大于60%,所以最终选定了该干扰效率大于60%的候选shrna。该gpr151-shrna的靶序列信息如下表2所示。
44.表2gpr151-shrna及nc-shrna(对照)的靶序列信息
[0045][0046]
3、gpr151 shrna对结肠炎进展的影响
[0047]
将c57bl/6j小鼠随机分成nc-shrna对照组、gpr151-shrna组,同时设置不做任何处理的正常对照组,每组3只,具体步骤如下:
[0048]
(1)nc-shrna对照组:小鼠注射nc-shrna(如seq id no.6所示);
[0049]
(2)gpr151-shrna组:小鼠注射gpr151-shrna(如seq id no.5所示);
[0050]
(3)正常对照组:小鼠不做任何处理。
[0051]
给c57bl/6j小鼠连续3周腹腔注射gpr151-shrna或nc-shrna后,同时在第3天注射shrna 1h后,给予2.5% tnbs/50%酒精100μl灌肠1次,到第4周时实验结束。监测小鼠每天的体重变化,收集结肠组织标本,记录结肠的长度,he染色观察小鼠结肠组织炎症程度并评分,rt-pcr法检测小鼠结肠组织中gpr151 mrna表达水平。
[0052]
如图2中a、b所示,与nc-shrna组相比,小鼠注射gpr151-shrna能够明显抑制tnbs引起的结肠炎(
**
p<0.01,n=3或4)。
[0053]
4、gpr151基因敲除鼠(gpr151ko鼠)对结肠炎进展的影响
[0054]
将wt c57bl/6小鼠和gpr151ko小鼠给予小鼠灌肠2.5% tnbs 1次,监测小鼠的体重变化直至第5天实验结束。
[0055]
如图3中a、b所示,与wt c57bl/6j小鼠相比,gpr151ko小鼠可显著地抑制结肠炎引起的小鼠结肠长度缩短(
*
p<0.05,n=3)。如图3中c所示,与wt c57bl/6j小鼠相比,gpr151ko小鼠可显著地抑制结肠炎引起的小鼠体重下降(
**
p<0.01或
***
p<0.001,n=4)。图3中d的he染色结果显示,与wt c57bl/6j小鼠相比,gpr151ko小鼠明显抑制tnbs引起的免疫细胞浸润。以上这些结果表明抑制gpr151表达能够缓解tnbs诱导的结肠炎的进展。
[0056]
本实施例研究发现,通过抑制gpr151表达或抑制其功能可以有效缓解结肠炎,说明gpr151参与结肠炎的发生发展。另外针对gpr151基因转录本设计了shrna,并将其与腺相关病毒载体进行重组连接,构建gpr151基因干扰的重组腺相关病毒载体,此干扰病毒用以证明抑制gpr151表达能够缓解结肠炎的进展。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1