一种基于荧光定量PCR检测人MTHFRC677T位点多态性的试剂盒的制作方法
一种基于荧光定量pcr检测人mthfr c677t位点多态性的试剂盒
技术领域
1.本发明属于单核苷酸多态性检测领域,具体涉及一种基于荧光定量pcr检测人mthfr c677t位点多态性的试剂盒。
背景技术:
2.人类基因组dna中5,10-亚甲基四氢叶酸还原酶(mthfr)是叶酸和甲硫氨酸在人体内代谢途径中的关键酶之一,可将5,10-亚甲基四氢叶酸还原为5-甲基四氢叶酸。一方面作为甲基的传递体参与体内嘌呤和嘧啶的合成及dna、rna、蛋白质的甲基化;另一方面在甲硫氨酸合成酶的催化下,以维生素b
12
为辅酶,使血液中的同型半胱氨酸再甲基化生成甲硫氨酸,从而维持体内正常的同型半胱氨酸水平。
3.研究发现,mthfr基因c677t位多态性可导致mthfr的耐热性和活性下降,从而引起同型半胱氨酸甲基化受阻,出现高同型半胱氨酸血症。高同型半胱氨酸可损伤血管内皮细胞,并引起低密度脂蛋白氧化和血小板凝集,从而破坏血管平滑肌细胞的正常功能及机体的凝血和纤溶系统,从而加速动脉粥样硬化和血栓形成,引发多种疾病,如脑卒中、h型高血压、冠心病等。同时发现,高同型半胱氨酸血症可引起细胞死亡、诱导dna链断裂、氧化应激和细胞凋亡,干扰胚胎细胞的正常周期和诱发胚胎细胞凋亡,从而引发出生缺陷的发生。
4.此外,mthfr c677t基因多态性影响叶酸的正常代谢,从而增加叶酸拮抗剂的毒副作用。甲氨蝶呤是抗叶酸代谢药物,是目前很多肿瘤(急性细胞性白血病)和风湿病的一线用药,临床用药过程发现相同剂量的甲氨蝶呤用在不同的患者身上时其毒副反应不一。研究结果表明677位tt纯合子对氨甲喋呤治疗的毒性反应比677c的基因型严重得多。
5.另外,c677t基因多态性还影响到5-氟尿嘧啶的化疗效果。5-氟尿嘧啶为嘧啶类似物,属于抗代谢药的一种,对消化道癌及其他实体癌有良好疗效。5-氟尿嘧啶对胃肠道肿瘤化疗效果的研究发现,677位tt基因型携带者化疗有效率显著高于tc和cc基因型携带者。
6.由此可见,通过对个体mthfr基因c677t位点基因型进行检测可以提示个体发生脑卒中等心脑血管疾病及新生儿缺陷的风险,并预测甲氨蝶呤和5-氟尿嘧啶等化疗药物的治疗疗效和毒副作用。
7.对于该突变位点的检测,目前主要有sanger测序法、pcr-rflp法、芯片法、荧光定量pcr法等方法,然而上述检测方法存在检测过程繁琐,周期过长,成本较高,判读复杂或者易引起交叉污染而出现假阳性以及灵敏度低等缺点。现有技术中也公开了采用pcr-fret法对突变位点进行检测,通过设计一对用来扩增目标序列特异引物和一对作为目标序列的检测信号fret探针,两个独立的特异寡核苷酸序列都标记上荧光基团。当两个探针都结合上去才能检测到荧光信号,fret探针再进行熔解曲线分析,通过熔解曲线来判断mthfr基因多态性(c677t)。然而,上述方法需设计两条不同的fret探针才能进行检测,检测程序复杂,且增加了检测成本。
技术实现要素:
8.为了克服上述现有技术的不足,本发明的目的在于提供一种基于荧光定量pcr检测人mthfr c677t位点多态性的试剂盒,该试剂盒采用新引物对和双标荧光探针对mthfr c677t位点多态性进行准确检测。
9.本发明解决上述技术问题的技术方案如下:
10.本发明提供了一种基于荧光定量pcr检测人mthfr c677t位点多态性的试剂盒,所述试剂盒包括基于mthfr基因c677t的snp位点设计的特异性引物和荧光探针;其中,所述探针的两端分别标记有荧光报告基团/荧光淬灭基团;
11.进一步的,所述特异性引物和荧光探针的序列如下:
12.mthfr基因c677t正向扩增引物:gagctttgaggctgacctgaag;
13.mthfr基因c677t反向扩增引物:cctcaaagaaaagctgcgtgat;
14.mthfr基因677c探针:5’tgaaatcggctccc 3’;
15.mthfr基因677t探针:5’atgaaatcgactccc 3’;
16.进一步的,所述mthfr基因677c探针5’端的荧光报告基团为vic,3’端的荧光淬灭基团为quencher和mgb;
17.进一步的,所述mthfr基因677t探针5’端的荧光报告基团为fam,3’端的荧光淬灭基团为quencher和mgb;
18.进一步的,所述试剂盒还包括如下组分中的一种或几种:pcr反应液、酶反应液、c677t位点反应液、无核酸酶水;
19.进一步的,所述pcr反应液包括缓冲液、mgcl2和dntps;所述酶反应液主要为taq酶;
20.进一步的,所述c677t位点反应液包括上游引物、下游引物、677c探针、677t探针,其配比为1:1:2:1;
21.进一步的,所述试剂盒的使用包括如下步骤:pcr试剂准备、dna样品提取、pcr扩增、判定样品型别;
22.进一步的,所述pcr扩增的循环条件如下:
23.60℃ 30s,收集荧光;
24.95℃ 10min;
25.95℃ 15s,60℃ 1min,收集荧光,40个循环;
26.60℃ 30s,收集荧光;
27.升温速率0.06℃/s;
28.进一步的,所述样品型别的判定标准如下:
29.若结果显示为gg型(红点),则样品型别对应为cc型;
30.若结果显示为ga型(绿点),则样品型别对应为ct型;
31.若结果显示为aa型(蓝点),则样品型别对应为tt型;
32.若三者均不显示,则样品上样量不足或漏加,需重新加样上机。
33.本发明的有益效果在于:
34.(1)与测序法等相比,本发明提供的试剂盒采用了全新引物对和双标荧光探针,具有更快的检测时效性;
35.(3)本发明的试剂盒操作简便且能有效防止污染:pcr荧光检测时间(从标本处理开始)仅为2~3小时;pcr荧光检测是全封闭操作,加样后可不再打开管盖,大大避免了污染发生;
36.(2)本发明提供的检测方法具有灵敏度高、特异性好、可重复性强、检测结果快速客观且可节约成本等优点,在个体化代谢用药领域具有极大的应用前景。
附图说明
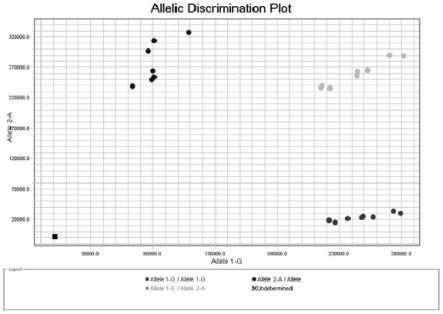
37.图1显示为本发明试剂盒检测23例待测样本的等位基因分型图;
38.图2显示为3例阳性对照样本的扩增曲线图。
具体实施方式
39.以下结合实例说明本发明,但不限制本发明。在本领域内,技术人员对本发明所做的简单替换或改进均属于本发明所保护的技术方案内。
40.实施例1:
41.试剂盒包括以下组分:
42.pcr反应液、酶反应液、c677t位点反应液、无核酸酶水;
43.pcr反应液包括10
×
缓冲液、25mm mgcl2和10mm dntps;酶反应液包括taq酶,c677t位点反应液包括上游、下游引物及677c探针、677t探针,配比分别为1:1:2:1;上游引物为400nm,下游引物为400nm,677c探针为800nm,677t探针为400nm。
44.本实施例中使用的mthfr c677t位点的引物和探针的核苷酸序列可参见表1。
45.表1 c677t位点反应液
46.mthfr-fgagctttgaggctgacctgaagmthfr-rcctcaaagaaaagctgcgtgat677c-px1-tgaaatcggctccc-y1677t-px2-atgaaatcgactccc-y1
47.注:x1、x2为荧光报告基团,y1为荧光淬灭基团。
48.试剂盒的使用:
49.一、检测方法
50.1、pcr试剂准备(试剂准备区)
51.1.1从冰箱中取出试剂盒,平衡至室温,各组分充分融解,c677t位点反应液用手轻弹混匀(勿涡旋震荡),低速离心5s。
52.1.2计算当次试验所需要的反应数(n):n=标本数+阴性对照(1t)(无核酸酶水)+阳性对照(3t)(试剂盒未提供,可用阳性临床样本替代),并根据下表反应体系配置方法计算当次实验所需要的各种试剂量。
53.在本实施例中,各组分需要的量为:
[0054][0055]
1.3将各组分震荡混匀,低速离心5s,按照19μl/孔分装至八联管内备用。
[0056]
2、dna提取(样品制备区)
[0057]
2.1将待测样品(一般为外周静脉全血)在涡旋混匀器上混匀,取200μl加入ep管。
[0058]
2.2加入20μl proteinase k溶液,混匀。
[0059]
2.3加200μl缓冲液gb,充分点到混匀,56℃放置10min,其间颠倒混匀数次,溶液应变清亮。
[0060]
2.4加入200μl无水乙醇,充分颠倒混匀,此时可能会出现絮状沉淀。
[0061]
2.5将上一步所得溶液和絮状沉淀都加入一个吸附柱cb3中(吸附柱cb3放入收集管中),12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb3放入收集管中。
[0062]
2.6向吸附柱cb3中加入500μl缓冲液gd(使用前请先检查是否已加入无水乙醇),12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb3放入收集管中。
[0063]
2.7向吸附柱cb3中加入600μl缓冲液pw(使用前请先检查是否已加入无水乙醇),12000rpm离心30s,倒掉收集管中的废液,将吸附柱cb3放入收集管中。
[0064]
2.8重复操作步骤2.7
[0065]
2.9 12000rpm离心2min,倒掉废液。将吸附柱cb3置于室温放置2min,以彻底晾干吸附材料中残余的漂洗液。
[0066]
2.10将吸附柱cb3转入1.5ml离心管中,向吸附膜中间位置悬空滴加70μl洗脱缓冲液tb,室温放置2min,12000rpm离心2min,将溶液收集到离心管中。用超微量紫外分光光度计nanodrop one测浓度及纯度,根据标本要求稀释并保存。
[0067]
2.11加样:将提取好的待测样品dna稀释到20ng/μl。用带滤芯吸嘴分别吸取待测样品dna、无核酸酶水(阴性质控)、gg/ga/aa阳性对照样本各1μl加入八联管各孔中,盖紧管盖,低速离心数秒后转移至pcr扩增区。
[0068]
3、pcr扩增区
[0069]
abi prism 7500仪器设置
[0070]
a)打开“set up”窗口,按样品对应顺序设置阴性质控(negative control)、阳性对照(positive control allel1/allel1、allel1/allel2、allel2/allel2)以及待测样品(unknown),并在“sample name”一栏中设置样品名称。探针检测模式设置为:fam/vic。
[0071]
b)打开run method窗口,设置循环条件如下:
[0072]
60℃30s,收集信号
[0073]
95℃10min
[0074]
95℃15s,60℃60s,40个循环,每个循环收集一次信号
[0075]
60℃30s,收集信号
[0076]
保存文件,运行。
[0077]
二、结果判读
[0078]
阴性对照:fam检测通路无扩增曲线明显对数增长期,vic检测通路无扩增曲线明显对数增长期;
[0079]
gg型阳性对照:结果分析显示为gg型;
[0080]
ga型阳性对照:结果分析显示为ga型;
[0081]
aa型阳性对照:结果分析显示为aa型;
[0082]
以上要求需在同一次试验中同时满足,否则,本次试验无效,需重新进行。
[0083]
结果说明:
[0084]
根据仪器显示结果判定样品型别,若结果显示为gg型(红点),则样品型别对应为cc型;若结果显示为ga型(绿点),则样品型别对应为ct型;若结果显示为aa型(蓝点),则样品型别对应为tt型。若三者均不显示,则样品上样量不足或漏加,需重新加样上机。
[0085]
以上所述的仅是本发明的优选实施方式,应当指出,对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1