人尿液来源的诱导的体节前中胚层祖细胞及其用途
本技术涉及人尿液来源的尿液细胞诱导的体节前中胚层祖细胞(uipsm)、由uipsm细胞形成的类体节结构、产生uipsm细胞和类体节结构的方法及其用途。
背景技术:
1、终末分化的体细胞可以成功地重新编程为多能干细胞,拓宽了成体细胞重新编程为干细胞的研究领域(takahashi等人,2007;takahashi和yamanaka,2006)。此外,诱导多能干细胞(ipsc)具有向胚层分化的潜力,但其致瘤性的风险限制了其应用,而致瘤性归因于ipsc诱导分化的细胞,效率不能达到100%。其次,对人体细胞而言,成纤维细胞、血细胞、羊膜细胞、皮肤上皮干细胞、近端小管(hk2)细胞系、周细胞来源细胞、内皮细胞、胰腺外分泌细胞等多种细胞都是重编程诱导起始的来源,而这些细胞的获取会对受试者造成一定程度的损伤。
2、此外,非侵入性获得的尿液细胞可以被重新编程为诱导多能干细胞(ipsc)和神经祖细胞(npc)(wang等人,generation of integration-free neural progenitor cellsfrom cells in human urine,nat methods 10,84-89,2013;zhou等人,generation ofhuman induced pluripotent stem cells from urine samples,nat-protoc 7,2080-2089,2012),提示尿液细胞作为一种起始细胞具有很强的可塑性,可作为诱导分化的起始细胞,在临床应用中具有一定的优势。
3、脊椎动物胚胎表现出高度保守的组织空间格局特征。双命运神经中胚层祖细胞(nmp)最令人信服的证据来自具有自我更新能力的尾芽细胞群,这些细胞将迁移至神经管和预定体节中胚层位置进行发育(henrique等人,2015)。体节前中胚层细胞(psm)是一种来源于尾侧外胚层(cle)的轴向干细胞,可以沿着前后轴形成体节,这决定了胚胎发育过程中体轴的延伸(henrique等人,2015;saito和suzuki,2020)。轴旁中胚层(又称体节中胚层)细胞可发育为骨骼谱系、肌细胞谱系和真皮细胞谱系,并进一步分化为肌肉骨骼系统,但由于伦理和技术的限制,在人胚胎中很难获得自我更新的psm细胞。因此,体外构建自我更新的psm祖细胞对躯体发生的研究具有重要意义。然而,由于伦理和技术的限制,很难在人胚胎中获得自我更新的psm细胞。
4、尽管人类胚胎干细胞(es)可以分化为psm,并在确定的条件培养基中聚集后生成三维“原肠胚”模型(beccari等人,2018;moris等人,2020),原肠胚形成的发生使其不能很好的模仿体节发生过程,因此不是研究相关疾病的好模型。该结果主要归因于主动聚集的细胞缺乏psm特性,如体节中胚层细胞的自我更新和多潜能分化。因此,产生自我更新的psm细胞以构建类体节结构来模拟胚胎早期发育中的体节发生是至关重要的。
技术实现思路
0、发明概述
1、本公开表明,尿液细胞可以被重新编程为体节前中胚层祖细胞,其能稳定扩增并分化为中胚层谱系细胞。体节前中胚层祖细胞还能够自组装形成类体节结构,以模拟体节发生。
2、所产生的体节前中胚层祖细胞在本文中被指定为尿液来源尿液细胞诱导的体节前中胚层祖细胞(缩写为uipsm)。uipsm细胞高表达体节前中胚层相关基因,具有体节前中胚层转录特征表达谱。重要的是,uipsm细胞退出多能状态,降低了肿瘤形成的风险,同时保留了分化为体节前中胚层谱系细胞的潜力。
3、uipsm细胞可以在体外自组装以产生类体节(uisomitoid)结构,这是一种uipsm自组装的类似于体节的“喙尾”结构。uisomitoid结构模仿了胚胎早期发育过程中体节形成中类似组织的建立,主要涉及基于干细胞的胚胎模型(scme)研究方向。uisomitoid结构可以更好地模拟胚胎体节发生的前后轴和分子钟的建立。
4、在一个方面,本文提供了一种诱导尿液细胞以获得体节前中胚层祖细胞(uipsm细胞)的方法。具体地,该方法可以包括以下步骤:
5、(a)培养尿液细胞并从培养的尿液细胞中选择上皮样细胞;
6、(b)用载体转化上皮样细胞;
7、(c)在补充有wnt激动剂、dot1l抑制剂和生长因子(一种或多种)的基础培养基中诱导经转化的上皮样细胞。
8、在一些实施方案中,从自一个或多个受试者收集的上尿路尿液样品中获得所述尿液细胞。
9、在一些实施方案中,将尿液细胞用regm培养基培养,并且在培养过程中主要富集上皮样细胞和间充质细胞类型。
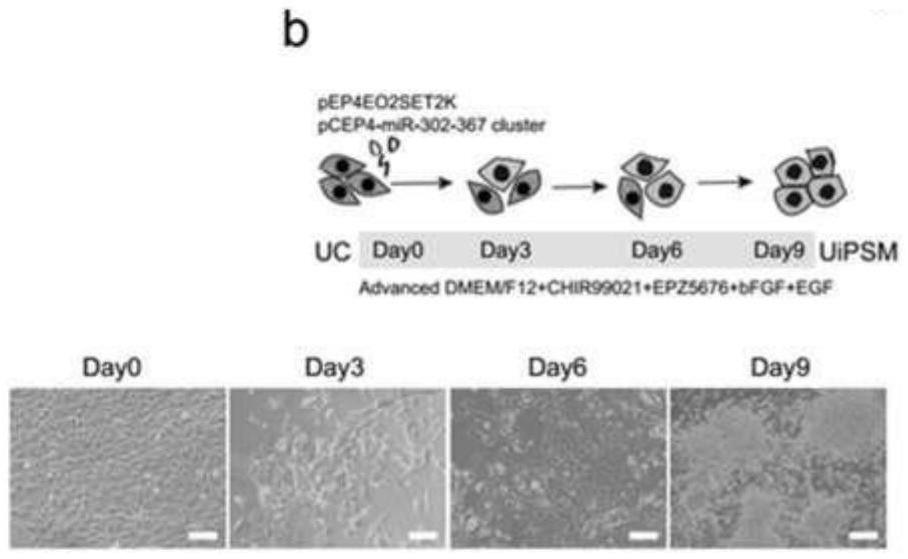
10、在一些实施方案中,所述上皮样细胞通过用一种或多种载体电穿孔进行转化,以使细胞易感于随后的诱导。例如,所使用的载体可以是pep4e02set2k和pcep4-mir-302-367。在一些实施方案中,尿液细胞的状态在电穿孔后2天内恢复。
11、在一些实施方案中,所使用的生长因子选自fgf(例如bfgf),egf、vegf、pdgf、tgf-β、pd-ecgf、tnf、hgf、igf(例如igf 1)、bmp、红细胞生成素、csf、m-csf及其片段或变体。
12、在一些实施方案中,用于诱导上皮样细胞的基础培养基是advanced dmem/f12。
13、在一些实施方案中,wnt激动剂是chir99021。
14、在一些实施方案中,dot1l抑制剂是epz5676。
15、在一些实施方案中,诱导在约7至12天的时间段内进行。
16、在一个方面,本文提供了体节前中胚层祖细胞(uipsm细胞)通过本文所述的方法获得。uipsm细胞有能力分化为体节前中胚层谱系细胞,如骨骼肌细胞、成骨细胞、软骨细胞和成软骨细胞。
17、在一个方面,本文提供了一种类体节结构,其包括如上所述的来源于尿液细胞的体节前中胚层祖细胞。具体地说,所述类体节结构是通过体外扩增和分化所述体节前中胚层祖细胞而产生的。优选地,类体节结构是自组织的“喙尾”结构。
18、在一个方面,本文提供了产生如上所述的类体节结构的方法,该方法包括:
19、(a)将一定量的(例如400个)uipsm细胞接种在低粘附板的孔中,用于在48小时期间聚集;
20、(b)在含有wnt激动剂和nodal抑制剂的培养基中使聚集的细胞伸长达7天;
21、(c)从平板上获得“喙-尾”3d类体节结构。
22、在一些实施方案中,wnt激动剂是chir99021。
23、在一些实施方案中,nodal抑制剂是sb431542。
24、在一个方面,本文提供了尿来源的体节前中胚层祖细胞(uipsm细胞)在诱导骨骼肌细胞、成骨细胞和软骨细胞分化中的用途。
25、在一个方面,本文提供了一种用于从尿液细胞诱导为体节前中胚层祖细胞(uipsm细胞)的重编程系统。
26、一般来说,本公开涉及以下实施方案:
27、1.一种诱导尿液细胞产生体节前中胚层祖细胞的方法,包括以下步骤:
28、(a)将活的尿液细胞培养一段合适的时间以出现上皮样细胞,并分离所述上皮样细胞;
29、(b)在补充有wnt激动剂、dot1l抑制剂和一种或多种生长因子的基础培养基中诱导所述上皮样细胞达足够长的时间以形成颗粒化的集落;和
30、(c)从所述集落中获得体节前中胚层祖细胞。
31、2.实施方案1的方法,其中在步骤(b)之前,用一种或多种能够改善细胞的渗透性以用于诱导或增强细胞重编程的载体预处理上皮样细胞。
32、3.实施方案2的方法,其中所述载体表达一种或多种以下因子:oct4、sox2、sv40lt、klf4、mirna 302、mirna 303、mirna 304、mirna305、mirna 306和mirna 307。
33、4.实施方案2或3的方法,其中在预处理后,进一步培养上皮样细胞以恢复其能力。
34、5.前述实施方案中任一项的方法,其中所述尿液细胞是从自一个或多个供体受试者收集的上尿路尿液样品中分离的。
35、6.前述实施方案中任一项的方法,其中在步骤(a)中,将尿液细胞在regm培养基中培养。
36、7.前述实施方案中任一项的方法,其中在步骤(b)中,所述基础培养基为dmem、dmem/f12或advanced dmem/f12。
37、8.前述实施方案中任一项的方法,其中所述生长因子选自fgf(例如bfgf)、egf、vegf、pdgf、tgf-β、pd-ecgf、tnf、hgf、igf(例如igf1)、bmp、红细胞生成素、csf、m-csf及其片段或变体。
38、9.前述实施方案中任一项的方法,其中所述生长因子是bfgf和egf。
39、10.前述实施方案中任一项的方法,其中所述wnt激动剂是chir99021,和/或所述dot1l抑制剂是epz5676。
40、11.根据实施方案10的方法,其中所述基础培养基为advanced dmem/f12,其补充有浓度范围为约2-4μm(例如3μm、2.5-3μm、3-3.5μm)的chir99021、浓度范围为约4-6μm(例如5μm、4.5-5μm、5-5.5μm)的epz5676、浓度范围为约4-6ng/μl(例如5ng/μl、4.5-5ng/μl、5-5.5ng/μl)的bfgf和浓度范围为约4-6ng/μl(例如5ng/μl、4.5-5ng/μl和5-5.5ng/μl)的egf。
41、12.前述实施方案中任一项的方法,其中步骤(b)中的诱导进行约7-12天的时间段,例如约7天、约8天、约9天、约10天、约11天和约12天。
42、13.通过前述实施方案中任一项的方法获得或能获得的体节前中胚层祖细胞。
43、14.一种培养实施方案13的体节前中胚层祖细胞的方法,包括在补充有wnt激动剂、tgf-β抑制剂和一种或多种生长因子的基础培养基中培养所述体节前中胚层祖细胞。
44、15.实施方案14的方法,其中所述基础培养基为dmem、dmem/f12或advanced dmem/f12。
45、16.实施方案14或15的方法,其中所述wnt激动剂是chir99021,和/或所述tgf-β抑制剂是a8301。
46、17.实施方案14-16中任一项的方法,其中所述生长因子选自fgf(例如bfgf)、egf、vegf、pdgf、tgf-β、pd-ecgf、tnf、hgf、igf(例如igf1)、bmp、红细胞生成素、csf、m-csf及其片段或变体。
47、18.实施方案17的方法,其中所选择的生长因子是bfgf和egf。
48、19.根据实施方案18的方法,其中限定的培养基是advanced dmem/f12,其补充有浓度范围为约2-4μm(例如,3μm、2.5-3μm、3-3.5μm)的chir99021、浓度范围为约4-6μm(如,5μm、4.5-5μm、5-5.5μm)的a8301、浓度范围为约4-6ng/μl(例如5ng/μl、4.5-5ng/μl、5-5.5ng/μl)的bfgf和浓度范围为约4-6ng/μl(例如5ng/μl、4.5-5ng/μl、5-5.5ng/μl)的egf。
49、20.根据实施方案14-19中任一项的方法,进一步包括将培养的体节前中胚层祖细胞传代。
50、21.通过实施方案14-20中任一项的方法获得或能获得的体节前中胚层祖细胞。
51、22.一种用于将体节前中胚层祖细胞分化为骨骼肌细胞的方法,包括:
52、(a)将所述体节前中胚层祖细胞在补充有wnt激动剂、tgf-β抑制剂和一种或多种生长因子的基础培养基中接种过夜;
53、(b)在补充有ksr、its、neaa、β-me、igf-1、hgf、chir99021、vc、dex和sb431542的基础培养基中诱导细胞;和
54、(c)在补充有ksr、马血清、neaa、β-me、igf-1和hgf的基础培养基中诱导细胞。
55、23.实施方案22的方法,其中在步骤(b)中,所述基础培养基补充有约15%ksr、约1%its、约1%neaa、约0.1μmβ-me、约4ng/ml igf-1、约10ng/ml hgf、约3μm chir99021、约50ng/ml vc、约0.5ng/ml dex和约2nm sb431542。
56、24.根据实施方案22或23的方法,其中在步骤(c)中,所述基础培养基补充有约15%ksr、约2%马血清、约1%neaa、约0.1μmβ-me、约4ng/ml igf-1和约10ng/ml hgf。
57、25.实施方案22-24中任一项的方法,其中在步骤(b)中,诱导进行12-18天的时间段,例如15天、12天、13天、14天、16天、17天和18天。
58、26.实施方案22-25中任一项的方法,其中在步骤(c)中,进行诱导直到骨骼肌纤维束完全存在。
59、27.一种用于将体节前中胚层祖细胞分化为成骨细胞的方法,包括:
60、(a)将所述体节前中胚层祖细胞在补充有wnt激动剂、tgf-β抑制剂和一种或多种生长因子的基础培养基中接种过夜;和
61、(b)在补充有fbs、vc、β-甘油磷酸盐和1-硫代甘油的基础培养基中诱导细胞。
62、28.实施方案27的方法,其中在步骤(b)中,所述基础培养基补充有约10%fbs、约50ng/ml vc、约100nmβ-甘油磷酸盐和约1μm 1-硫代甘油。
63、29.一种用于将体节前中胚层祖细胞分化为软骨细胞的方法,包括:
64、(a)将所述体节前中胚层祖细胞在补充有wnt激动剂、tgf-β抑制剂和一种或多种生长因子的基础培养基中接种过夜;和
65、(b)在补充有fbs、its、丙酮酸钠、vc、β-甘油磷酸盐、tgf-β3和bmp2的基础培养基中诱导细胞。
66、30.实施方案29的方法,其中在步骤(b)中,所述基础培养基补充有约10%fbs、约1%its、约1%丙酮酸钠、约50ng/ml vc、约0.1nmβ-甘油磷酸盐、约4ng/ml tgf-β3和约20ng/ml bmp2。
67、31.实施方案27-30中任一项的方法,其中所述诱导进行约15天。
68、32.实施方案22-31中任一项的方法,其中所述基础培养基是dmem/f12或dmem。
69、33.实施方案22-32中任一项的方法,其中所述培养基在诱导期间每2-3天交换一次。
70、34.一种用于产生类体节结构的方法,包括:
71、(a)接种实施方案13或21的体节前中胚层祖细胞并培养足够的时间以形成紧密的球形细胞聚集体;
72、(b)在补充有wnt激动剂和nodal抑制剂的基础培养基中伸长细胞聚集体;和
73、(c)从板上分离伸长的结构。
74、35.实施方案34的方法,其中在步骤(a)中,在补充有wnt激动剂、tgf-β抑制剂和一种或多种生长因子的培养基中进行培养。
75、36.实施方案35的方法,其中所述培养基是补充有chir99021、a8301、bfgf和egf的advanced dmem/f12。
76、37.实施方案36所述的方法,其中所述培养基为advanced dmem/f12,其补充有浓度范围为约2-4μm(例如,3μm、2.5-3μm、3-3.5μm)的chir99021、浓度范围为约4-6μm(如,5μm、4.5-5μm、5-5.5μm)的a8301、浓度范围为约4-6ng/μl(例如5ng/μl、4.5-5ng/μi、5-5.5ng/μl)的bfgf和浓度范围为4-6ng/μl(例如5ng/μl、4.5-5ng/μi、5-5.5ng/μl)的egf。
77、38.实施方案34的方法,其中在步骤(b)中,基础培养基是补充有chir99021和sb431542的advanced dmem/f12。
78、39.实施方案38的方法,其中chir99021的浓度范围为约2-4μm(例如3μm、2.5-3μm、3-3.5μm),且sb431542的浓度范围为约5-15μm(如10μm、5-10μm、10-15μm)。
79、40.实施方案34-39中任一项的方法,其中在培养约48小时后形成紧密的球形细胞聚集体。
80、41.实施方案34-40中任一项的方法,其中所述细胞聚集体被伸长达7-12天的时间段,例如约7天、约8天、约9天、约10天、约11天和约12天。
81、42.实施方案34-41中任一项的方法,其中用于接种的细胞数为约200-1000个细胞,例如300个细胞、400个细胞、500个细胞、600个细胞、700个细胞、800个细胞、900个细胞和1000个细胞(优选约400个细胞)。
82、43.通过实施方案34-42中任一项的方法产生的类体节结构。
83、44.实施方案43的类体节结构,其中该结构模拟伸长的胚胎尾芽并构建前后轴。
84、45.一种组合物,其包含实施方案13或21的体节前中胚层祖细胞或实施方案44的类体节结构。
85、46.实施方案44的类体节结构在对中胚层谱系的人类疾病建模中的用途。
86、47.实施方案44的类体节结构在筛选药物中的用途,所述药物包括基于小分子、蛋白质和抗体的治疗物。
87、48.实施方案13或21的体节前中胚层祖细胞或实施方案45的组合物在治疗需要肌肉再生、软骨再生、脊髓再生或相关再生的受试者中疾病或病症中的用途。
88、49.一种用于治疗受试者中需要肌肉再生、软骨再生和/或脊髓再生的疾病或病症的方法,包括向受试者施用(例如植入)实施方案13或21的体节前中胚层祖细胞或实施方案45的类体节结构。
89、50.一种用于将尿液细胞重编程为体节前中胚层祖细胞的试剂盒,包括:
90、基础培养基,其为advanced dmem/f12;
91、用于诱导尿液细胞的试剂的组合,包括chir99021、epz5676、bfgf和egf,或chir9902、a8301、bfgf和egf;以及
92、任选地,用于收集尿液细胞或采集上皮样细胞的工具。
93、51.一种用于分化实施方案13或21的体节前中胚层祖细胞的试剂盒,包括:
94、基础培养基,其为dmem/f12或dmem;和
95、选自下组的试剂的组合:
96、(a)ksr、its、neaa、β-me、igf-1、hgf、chir99021、vc、dex和sb431542;
97、(b)ksr、马血清、neaa、β-me、igf-1和hgf;
98、(c)fbs、vc、β-甘油磷酸盐和1-硫代甘油;和
99、(d)fbs、its、丙酮酸钠、vc、β-甘油磷酸盐、tgf-β3和bmp2。
100、通过下面参考附图对几个实施方案的详细描述,本公开的前述和其他特征和优点将变得更加明显。
- 还没有人留言评论。精彩留言会获得点赞!