作为组蛋白脱乙酰酶6抑制剂的1,3,4-噁二唑硫羰基化合物及包含该化合物的药物组合物的制作方法
本发明涉及具有组蛋白脱乙酰酶6(hdac6)抑制活性之1,3,4-噁二唑硫羰基化合物、其立体异构体、其药学可接受的盐;所述化合物用于制备治疗性药物的用途;使用所述化合物治疗疾病的方法;包含所述化合物的药物组合物;及其制备方法。
背景技术:
1、在细胞中,诸如乙酰化的翻译后修饰在生物过程之枢纽中充当非常重要的调节模块,且亦由数种酶严格控制。作为构成染色质的核心蛋白,组蛋白以轴形式起作用,dna卷绕在其周围,且因此有助于dna凝聚。此外,组蛋白的乙酰化与脱乙酰化之间的平衡在基因表达中起到非常重要的作用。
2、作为用于自构成染色质之组蛋白蛋白质的赖氨酸残基移除乙酰基的酶,已知组蛋白脱乙酰酶(hdac)与基因沉默相关联且诱发细胞周期停滞、血管生成抑制、免疫调节、细胞凋亡等(hassig等人,curr.opin.chem.biol.1,300-308(1997))。另外,据报导,hdac酶功能的抑制通过降低癌细胞存活相关因子的活性及活化体内癌细胞死亡相关因子来诱导癌细胞自行凋亡(warrell等人,natl.cancer inst.90,1621-1625(1998))。
3、就人类而言,已知18种hdac且根据与酵母hdac的同源性将其分为四类。在此情况下,使用锌作为辅因子的十一种hdac可分成三类:第i类(hdac1、2、3、8)、第ii类(iia:hdac4、5、7、9;iib:hdac6、10)和第iv类(hdac11)。此外,七种第iii类hdac(sirt 1至7)使用nad+代替锌作为辅因子(bolden等人,nat.rev.drug discov.5(9),769-784(2006))。
4、各种hdac抑制剂当前处于临床前或临床开发阶段,但迄今为止仅非选择性hdac抑制剂被称为抗癌剂。伏瑞斯特(vorinostat;saha)和罗米地辛(romidepsin;fk228)已获批作为皮肤t细胞淋巴瘤的治疗剂,而帕比司他(panobinostat;lbh-589)已获批作为多发性骨髓瘤的治疗剂。然而,已知非选择性hdac抑制剂一般在高剂量下会产生副作用,例如疲劳、恶心等(piekarz等人,pharmaceuticals 3,2751-2767(2010))。据报导,所述副作用是由对第i类hdac之抑制引起的。归因于所述副作用等原因,非选择性hdac抑制剂在除抗癌剂以外的其他领域中的药物开发上受到限制(witt等人,cancer letters 277,8-21(2009))。
5、同时,据报导,选择性抑制第ii类hdac将不显示在抑制第i类hdac时出现的毒性。在开发选择性hdac抑制剂之情况下,将有可能解决由对hdac之非选择性抑制引起的诸如毒性等的副作用。因此,有机会开发选择性hdac抑制剂作为各种疾病的有效治疗剂(matthias等人,mol.cell.biol.28,1688-1701(2008))。
6、已知hdac6(一种第iib类hdac)主要存在于细胞质中且含有微管蛋白,因此涉及多种非组蛋白底物(hsp90、皮层肌动蛋白(cortactin)等)的脱乙酰化(yao等人,mol.cell18,601-607(2005))。hdac6具有两个催化域,其中c末端的锌指域可结合至泛蛋白化蛋白质。已知hdac6具有多种非组蛋白蛋白质作为底物,且因此在各种疾病中起重要作用,所述疾病例如是癌症、炎性疾病、自体免疫性疾病、神经疾病、神经退化病症及其类似疾病(santo等人,blood 119,2579-2589(2012);vishwakarma等人,internationalimmunopharmacology 16,72-78(2013);hu等人,j.neurol.sci.304,1-8(2011))。
7、各种hdac抑制剂共同具有的结构特征包括封端基团、接头基团和锌结合基团(zbg),如以下伏立诺他(vorinostat)之结构中所示。许多研究人员已通过封端基团和接头基团之结构修饰来进行关于酶之抑制活性及选择性的研究。在所述基团以外,已知锌结合基团在酶抑制活性及选择性方面起更重要的作用(wiest等人,j.org.chem 78,5051-5055(2013);methot等人,bioorg.med.chem.lett.18,973-978(2008))。
8、
9、大部分锌结合基团为异羟肟酸或苯甲酰胺。在本文中,异羟肟酸衍生物展示出强hdac抑制作用,但存在低生物利用率及严重脱靶活性的问题。苯甲酰胺包括苯胺,且因此存在可能在活体内产生有毒代谢物的问题(woster等人,med.chem.commun.,onlinepublication(2015))。
10、因此,与具有副作用的非选择性抑制剂不同,需要开发选择性hdac6抑制剂,该选择性hdac6抑制剂含有具有经改良之生物利用率的锌结合基团,同时不引起副作用,以便治疗癌症、炎性疾病、自体免疫性疾病、神经疾病、神经退化病症及其类似疾病。
11、相关的现有技术
12、专利文献
13、国际未审查之专利公开案第wo 2011/091213号(公开于2011年7月28日):acy-1215
14、国际未审查之专利公开案第wo 2011/011186号(公开于2011年1月27日):tubastatin
15、国际未审查之专利公开案第wo 2013/052110号(公开于2013年4月11日):sloan-k
16、国际未审查之专利公开案第wo 2013/041407号(公开于2013年3月28日):cellzome
17、国际未审查之专利公开案第wo 2013/134467号(公开于2013年9月12日):kozi
18、国际未审查之专利公开案第wo 2013/008162号(公开于2013年1月17日):novartis
19、国际未审查之专利公开案第wo 2013/080120号(公开于2013年6月06日):novartis
20、国际未审查之专利公开案第wo 2013/066835号(公开于2013年5月10日):tempero
21、国际未审查之专利公开案第wo 2013/066838号(公开于2013年5月10日):tempero
22、国际未审查之专利公开案第wo 2013/066833号(公开于2013年5月10日):tempero
23、国际未审查之专利公开案第wo 2013/066839号(公开于2013年5月10日):tempero
技术实现思路
1、技术问题
2、本发明的一个目的是提供具有选择性hdac6抑制活性的1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐。
3、本发明的另一目的是提供一种药物组合物,其包括具有选择性hdac6抑制活性的1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐。
4、本发明的又另一目的是提供一种用于制备所述化合物的方法。
5、本发明的又另一目的是提供一种含有所述化合物的药物组合物。
6、本发明的又另一目的是提供一种含有所述化合物的药物组合物,其是用于预防或治疗hdac6活性相关疾病。本文中,hdac6活性相关疾病可包括传染性疾病,赘瘤,内分泌病,营养及代谢疾病,精神及行为障碍,神经疾病,眼睛及眼附件疾病,循环系统疾病,呼吸系统疾病,消化道问题,皮肤及皮下组织疾病,肌肉骨胳系统及结缔组织疾病,或畸形、变形和染色体畸变。
7、本发明的又另一目的是提供一种其在制备用于预防或治疗hdac6活性相关疾病的药物中的用途。
8、本发明的又另一目的是提供一种用于治疗hdac6活性相关疾病的方法,该方法包括施用治疗有效量之化合物或含有所述化合物的药物组合物。
9、针对问题的技术方案
10、本发明人已发现具有组蛋白脱乙酰酶6(hdac6)抑制活性的噁二唑化合物且已将其用于抑制或治疗hdac6活性相关疾病,由此完成本发明。
11、在下文中将更详细地描述本发明。揭示于本发明中的各种要素的所有组合属于本发明的范畴内。另外,可发现本发明的范畴不限于以下特定描述。
12、1,3,4-噁二唑硫羰基化合物
13、根据所述目的,本发明中所提供的化合物可如以下(1)至(3)中所示。
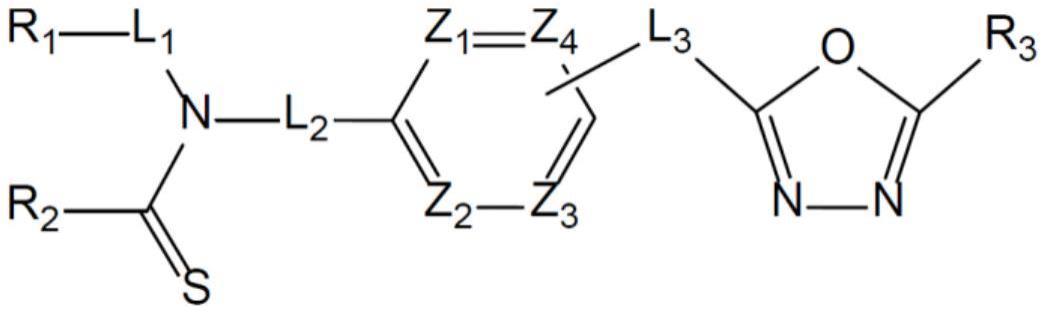
14、(1)一种由下式i表示的1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐:
15、
16、在式i中,
17、l1、l2和l3各自独立地为单键或-(c1-c4亚烷基)-;
18、r1为-h、-(c1-c4烷基)、-(c1-c4烷基)-o(c1-c4烷基)、-(c1-c4烷基)-c(=o)-o(c1-c4烷基)、-(c3-c7环烷基)、-(c2-c6环杂烷基)、-芳基、-杂芳基、-金刚烷基、
19、在r1中,
20、-(c1-c4烷基)中之至少一个h可被-t或-oh取代,
21、-芳基或-杂芳基中之至少一个h可各自独立地被-t、-oh、-o(c1-c4烷基)、-ocf3、-o-芳基、-nrdre、-(c1-c4烷基)、-cf3、-cf2h、-c(=o)-(c1-c4烷基)、-c(=o)-o(c1-c4烷基)、-c(=o)-nrdre、-s(=o)2-(c1-c4烷基)、-芳基、-杂芳基、取代,其中中之至少一个h可被-t、-(c1-c4烷基)、-cf3或-cf2h取代,
22、-(c3-c7环烷基)、-(c2-c6环杂烷基)、-金刚烷基、中之至少一个h可各自独立地被-t、-oh或-(c1-c4烷基)取代;
23、r2为-nrarb、-orc、-杂芳基、
24、在r2中,
25、中之至少一个h可被-t、-oh、-o(c1-c4烷基)、-nrdre、-(c1-c4烷基)、-cf3、-cf2h、-cn、-芳基、-杂芳基、-(c1-c4烷基)-芳基或-(c1-c4烷基)-杂芳基取代,其中-芳基、-杂芳基、-(c1-c4烷基)-芳基或-(c1-c4烷基)-杂芳基中之至少一个h可被-t、-oh、-cf3或-cf2h取代;
26、r3为-ct3或-ct2h;
27、y1、y2、y4和y7各自独立地为=ch-、-chrf-、-nrf-、-o-、-c(=o)-或-s(=o)2-;
28、y3、y5和y6各自独立地为-ch-或-n-;
29、z1至z4各自独立地为n或crz,
30、在z1至z4中,
31、z1至z4中之至少三个不可同时为n,且rz为-h、-t或-o(c1-c4烷基);
32、z5和z6各自独立地为-ch2-或-o-;
33、z7和z8各自独立地为=ch-或=n-;
34、z9为-nrg-或-s-;
35、ra和rb各自独立地为-h、-(c1-c4烷基)、-(c1-c4烷基)-oh、-(c1-c4烷基)-nrdre、-芳基、-(c1-c4烷基)-芳基、-杂芳基、-(c1-c4烷基)-杂芳基、-(c3-c7环烷基)、-(c2-c6杂环烷基)或
36、在ra和rb中,
37、-(c1-c4烷基)、-(c1-c4烷基)-oh或-(c1-c4烷基)-nrdre中之至少一个h可被-t取代,
38、-芳基、-(c1-c4烷基)-芳基、-杂芳基、-(c1-c4烷基)-杂芳基、-(c3-c7环烷基)或-(c2-c6杂环烷基)中之至少一个h可被-t、-oh、-o(c1-c4烷基)、-(c1-c4烷基)、-cf3、-cf2h或-cn取代,
39、中之至少一个h可被-t、-oh、-o(c1-c4烷基)、-(c1-c4烷基)、-cf3、-cf2h、-cn、-(c2-c6杂环烷基)、-芳基、-(c1-c4烷基)-芳基或-杂芳基取代;
40、rc为-(c1-c4烷基)、-芳基、-(c1-c4烷基)-芳基、-杂芳基或-(c1-c4烷基)-杂芳基,
41、在rc中,
42、-(c1-c4烷基)中之至少一个h可被-t或-oh取代,
43、-芳基、-(c1-c4烷基)-芳基、-杂芳基或-(c1-c4烷基)-杂芳基中之至少一个h可被-t、-oh、-cf3或-cf2h取代;
44、rd和re各自独立地为-h、-(c1-c4烷基)、-芳基或-(c1-c4烷基)-芳基,
45、在rd和re中,
46、-(c1-c4烷基)中之至少一个h可被-t或-oh取代,
47、-芳基或-(c1-c4烷基)-芳基中之至少一个h可被-t、-oh、-cf3或-cf2h取代;
48、rf为-h、-(c1-c6烷基)、-(c1-c4烷基)-oh、-(c1-c4烷基)-o-(c1-c4烷基)、-c(=o)-(c1-c4烷基)、-c(=o)-o(c1-c4烷基)、-(c1-c4烷基)-c(=o)-o(c1-c4烷基)、-nrdre、-(c1-c4烷基)-nrdre、-s(=o)2-(c1-c4烷基)、-芳基、-(c1-c4烷基)-芳基、-(c2-c4烯基)-芳基、-杂芳基、-(c1-c4烷基)-杂芳基、-c(=o)-(c3-c7环烷基)、-(c2-c6杂环烷基)或-(c1-c4烷基)-c(=o)-(c2-c6杂环烷基),
49、在rf中,
50、-(c1-c6烷基)、-(c1-c4烷基)-oh、-(c1-c4烷基)-o-(c1-c4烷基)、-c(=o)-(c1-c4烷基)、-c(=o)-o(c1-c4烷基)、-(c1-c4烷基)-c(=o)-o(c1-c4烷基)、-nrdre、-(c1-c4烷基)-nrdre或-s(=o)2-(c1-c4烷基)中之至少一个h可被-t取代,
51、-芳基、-(c1-c4烷基)-芳基、-(c2-c4烯基)-芳基、-杂芳基、-(c1-c4烷基)-杂芳基、-c(=o)-(c3-c7环烷基)、-(c2-c6杂环烷基)或-(c1-c4烷基)-c(=o)-(c2-c6杂环烷基)中之至少一个h可被-t、-oh、-(c1-c4烷基)、-cf3或-cf2h取代;
52、rg为-h或-(c1-c4烷基);
53、q为-o-或单键;
54、为单键或双键,限制条件为当为双键时,y1为=ch-;
55、a至e各自独立地为0、1、2、3或4的整数,限制条件为a和b不能一起为0,且c和d不能一起为0;
56、f为1或2的整数;且
57、t为f、cl、br或i。
58、(2)如上述(1)之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐:
59、在式i中,
60、l1、l2和l3各自独立地为单键或-(c1-c2亚烷基)-;
61、r1为-(c1-c4烷基)、-(c6-c12芳基)或包括至少一个选自o、n和s中的杂原子的-(c3-c10杂芳基),
62、在r1中,
63、-(c1-c4烷基)中之至少一个h可被-t或-oh取代,
64、-(c6-c12芳基)或包括至少一个选自o、n和s中的杂原子的-(c3-c10杂芳基)中之至少一个h可各自独立地被-t、-cf3或-cf2h取代;
65、r2为包含至少一个选自o、n和s中的杂原子的-(c3-c10杂芳基)、
66、r3为-ct3或-ct2h;
67、y1、y2、y4和y7各自独立地为=ch-、-chrf-、-nrf-、-o-、-c(=o)-或-s(=o)2-;
68、y3、y5和y6各自独立地为-ch-或-n-;
69、z1至z4各自独立地为n或crz,
70、在z1至z4中,
71、z1至z4中的至少三个不可同时为n,
72、rz为-h、-t或-o(c1-c4烷基);
73、rf为-h、-(c1-c6烷基)、-c(=o)-(c1-c4烷基)或-(c2-c6杂环烷基);
74、为单键或双键,限制条件为当为双键时,y1为=ch-;
75、a至e各自独立地为0、1、2、3或4的整数,限制条件为a和b不能一起为0,且c和d不能一起为0;
76、f为1或2的整数;且
77、t为f、cl、br或i。
78、在本发明中,表示所述式的键联部分。
79、在本发明中,表示单键或双键。换言之,可为作为单键或作为双键。
80、在本发明中,“单键”是指其中两个原子共有具有所形成之键的一对电子的键。
81、在本发明中,“cm-cn”(其中m和n各自独立地为1或大于1的整数)可意谓碳的数目,例如,“c1-c4烷基”表示具有1至4个碳原子的烷基。
82、在本发明中,“烷基”意谓直链或分支链饱和烃基,且例如“c1-c4烷基”可包括甲基、乙基、正丙基、异丙基、正丁基、仲丁基、叔丁叔丁基、异丁基等。
83、在本发明中,“亚烷基”意谓衍生自限定的烷基(包括直链和分支链两者)的二价官能基,且例如“c1-c4亚烷基”可包括亚甲基(-ch2-)、亚乙基(-ch2ch2-)、亚正丙基(-ch2ch2ch2-)、亚正丁基(-ch2ch2ch2ch2-)等。
84、在本发明中,“杂芳基”意谓在环中具有至少一个杂原子的芳族官能基,且该杂原子可包括选自o、n和s中的至少一者。杂芳基可包括环中具有3个至10个碳原子的杂芳基。杂芳基可为4元或更多元环,例如5元至6元环。举例而言,“杂芳基”可为呋喃、噻吩、噻唑、噻二唑、吡咯、吡唑、吡啶、嘧啶、咪唑、三唑、三嗪、哒嗪、吡嗪或其类似者,但不限于此。
85、在本发明中,“杂环烷基”意谓在环中具有至少一个杂原子的环烷基。杂原子可包括选自o、n和s中的至少一者。杂环烷基可包括环中具有3个至10个碳原子的杂环烷基。杂环烷基可为3元或更多元环,例如3元至6元环。举例而言,“杂环烷基”可为环氧丙烷、氧杂环丁烷、四氢呋喃、四氢吡喃、氮杂环丁烷、吗啉、硫代吗啉二氧化物、哌嗪、哌啶、噁二唑、吡咯烷等,但不限于此。
86、在本发明中,t意谓卤素原子,且可为f、cl、br或i。
87、在本发明中,药学可接受的盐可指医药学行业中常规使用的盐,例如由钙、钾、钠、镁或其类似物制备的无机离子盐;由盐酸、硝酸、磷酸、溴酸、碘酸、过氯酸、硫酸等制备的无机酸盐;由乙酸、三氟乙酸、柠檬酸、顺丁烯二酸、丁二酸、乙二酸、苯甲酸、酒石酸、反丁烯二酸、杏仁酸、丙酸、乳酸、乙醇酸、葡萄糖酸、半乳糖醛酸、麸氨酸、戊二酸、葡糖醛酸、天冬氨酸、抗坏血酸、碳酸、香草酸、氢碘酸等制备的有机酸盐;由甲磺酸、乙磺酸、苯磺酸、对甲苯磺酸、萘磺酸等制备的磺酸盐;由甘氨酸、精氨酸、赖氨酸等制备的氨基酸盐;由三甲胺、三乙胺、氨、吡啶、甲吡啶等制备的胺盐;及其类似者,但本发明中意谓的盐的类型不限于这些所列的盐。
88、本发明的由式i表示之1,3,4-噁二唑硫羰基化合物的“立体异构体”可包括非对映异构体及光学异构体(对映异构体),其中光学异构体不仅可包括对映异构体,而且包括对映异构体及甚至外消旋体两者的混合物。异构体可通过根据相关技术(例如柱层析法、hplc或其类似技术)分离。替代地,由式i表示之1,3,4-噁二唑硫羰基化合物的各立体异构体可通过使用已知系列的光学纯起始材料和/或试剂立体特异性合成。
89、(3)如上述(1)或(2)之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐,其中所述化合物是选自表1中所示的化合物1至46中的化合物。
90、表1
91、
92、
93、
94、
95、制备式i之1,3,4-噁二唑硫羰基化合物的方法
96、由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐可根据由反应式1至4表示的制备方法且其中甚至亦可以包括本领域技术人员显而易知之制备方法来进行制备。
97、在下文中,在反应式中,x1至x4可依次与式i的z1至z4相同,且其他符号可由与反应式中之式i的符号相同的符号表示,且未特定描述的那些可与式i中所定义相同。因此,将省略任何冗余描述。
98、在以下反应式1至反应式4中,由“x”表示之取代基可意谓离去基。
99、在以下反应式1至反应式4中,“pg”可表示胺保护基且例如,pg可为叔丁氧基羰基(boc)。
100、<反应式1>
101、
102、在反应式1中,由“r2”表示的式1-1-4化合物可意谓其中伯氨基或仲氨基引入至r2的化合物,在式i的定义中,r2为单价取代基。
103、根据反应式1,可通过式1-1-1化合物与式1-1-2化合物之间的取代反应制备式1-1-3化合物,然后式1-1-4化合物与式1-1-5化合物可进行反应以制备式1-1-6化合物。
104、通过反应式1制备的化合物可为化合物1、2、3、7、35等。
105、<反应式2>
106、
107、在反应式2中,r5可与如式i中的rf所定义相同。
108、根据反应式2,可通过使式1-1-3化合物、式1-1-5化合物以及引入包括保护基(pg)之氨基的螺环化合物进行反应来制备式1-2-1化合物。此后,可移除保护基以制备式1-2-2化合物,且接着可进行还原胺化反应或取代反应以制备式1-2-3化合物。
109、通过反应式2制备的化合物可为10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、36、37、38、44、45、46等。
110、<反应式3>
111、
112、在反应式3中,r4可为(其中y1和y7可各自独立地表示-n-),且r5可与如式i中的rf所定义相同。
113、根据反应式3,可通过使式1-1-3化合物、式1-1-5化合物以及引入包括保护基(pg)之氨基的r4化合物进行反应来制备式1-3-1化合物。此后,可移除保护基以制备式1-3-2化合物,且接着可进行还原胺化反应或取代反应以制备式1-3-3化合物。
114、通过反应式3制备之化合物可为化合物4、5、39、40、41、42、43等。
115、<反应式4>
116、
117、根据反应式4,可使式1-4-1化合物与2,4-双(4-甲氧基苯基)-1,3,2,4-二硫杂二磷杂环丁烷-2,4-二硫化物(2,4-bis(4-methoxyphenyl)-1,3,2,4-dithiadiphosphetan-2,4-disulfide,lawesson试剂)反应以制备式1-4-2或式1-4-3化合物。
118、替代地,可使式1-4-2化合物与1-甲氧基-n-三乙基铵基磺酰基-甲酰亚胺酯(1-methoxy-n-triethylammoniosulfonyl-methanimidate,burgess试剂)反应以制备式1-4-3化合物。
119、通过反应式4制备之化合物可为化合物6、8、9等。
120、包括由式i表示之1,3,4-噁二唑硫羰基化合物的组合物、其用途及使用其的治疗方法
121、本发明提供一种药物组合物,其包括由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐作为活性成分。
122、另外,本发明提供一种用于预防或治疗组蛋白脱乙酰酶6活性相关疾病的药物组合物,其包含由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐作为活性成分。
123、本发明的药物组合物选择性抑制组蛋白脱乙酰酶6,由此显示在预防或治疗组蛋白脱乙酰酶6活性相关疾病方面的显著作用。
124、组蛋白脱乙酰酶6活性相关疾病可包括:诸如朊病毒病之传染性疾病;诸如良性肿瘤(例如骨髓发育不良综合征)或恶性肿瘤(例如,多发性骨髓瘤、淋巴瘤、白血病、肺癌、结肠直肠癌、结肠癌、前列腺癌、尿道上皮癌、乳腺癌、黑色素瘤、皮肤癌、肝癌、脑癌、胃癌、卵巢癌、胰腺癌、头颈癌、口腔癌或神经胶质瘤)之赘瘤;内分泌病、营养及代谢疾病,诸如威尔逊病、淀粉样变性病或糖尿病;诸如抑郁或雷特综合征等的精神及行为障碍;神经疾病,诸如中枢神经系统萎缩(例如亨廷顿病、脊髓性肌萎缩(sma)、脊髓小脑共济失调(sca)、神经退化疾病(例如阿尔茨海默病)、动作障碍(例如帕金森病)、神经病变(例如遗传性神经病变(charcot-marie-tooth病)、偶发性神经病变、炎性神经病变、药物诱导的神经病变)、运动神经病变(例如肌肉萎缩性侧索硬化(als))、中枢神经系统脱髓鞘疾病(例如多发性硬化(ms))或其类似疾病;眼睛及眼附件疾病,诸如葡萄膜炎;循环系统疾病,诸如心房纤维性颤动、中风或其类似疾病;呼吸系统疾病,诸如哮喘;消化系统疾病,诸如酒精性肝病、炎性肠疾病、克罗恩病、溃疡性肠疾病或其类似疾病;皮肤及皮下组织疾病,诸如银屑病;肌肉骨胳系统及结缔组织疾病,诸如类风湿性关节炎、骨关节炎、全身性红斑狼疮(sle)或其类似疾病;或畸形、变形及染色体畸变,诸如常染色体显性多囊性肾病,且亦包括与组蛋白脱乙酰酶之异常功能相关的其他症状或疾病。
125、对于施用,除由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐之外,本发明的药物组合物可进一步包含至少一种类型的药学可接受的载剂。本文中所使用之药学可接受的载剂可包括盐水溶液、灭菌水、林格溶液(ringer'ssolution)、缓冲盐水、右旋糖溶液、麦芽糊精溶液、丙三醇、乙醇及其至少一种组分之混合物,且可视需要添加其他常规添加剂(例如抗氧化剂、缓冲溶液、抑菌剂等)来一起使用。另外,可添加稀释剂、分散剂、表面活性剂、黏合剂及润滑剂以调配成诸如水溶液、悬浮液、乳液等可注射剂型、丸剂、胶囊、粒剂或片剂。因此,本发明的组合物可为贴片、液体药品、丸剂、胶囊、颗粒剂、片剂、栓剂等。此类制剂可根据此项技术中用于调配之常规方法或揭示于雷明顿药物科学(remington's pharmaceutical science)(最新版本),merck publishingcompany,easton pa中的方法制备,且此类组合物可视每种疾病或组分调配成多种制剂。
126、本发明的组合物可根据目标方法经口或非经肠施用(例如,静脉内、皮下、腹膜内或局部施用),其中其剂量视患者之体重、年龄、性别、健康状况、膳食、给药时间、给药方法、排泄率、疾病的严重程度及其类似因素而在其范围内变化。本发明的由式i表示之1,3,4-噁二唑硫羰基化合物的每日剂量可为约1至约1000mg/kg,优选约5至约100mg/kg,且可通过划分化合物之每日剂量,一日一次或一日若干次来进行施用。
127、除了由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐以外,本发明的药物组合物可进一步包括至少一种展示相同或类似医药作用的活性成分。
128、本发明可提供一种预防或治疗组蛋白脱乙酰酶6活性相关疾病的方法,其包括施用治疗有效量之由式i表示的1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐。
129、如本文所用,术语“治疗有效量”可指有效预防或治疗组蛋白脱乙酰酶6活性相关疾病的由式i表示之1,3,4-噁二唑硫羰基化合物的量。
130、另外,本发明可提供一种用于选择性抑制hdac6的方法,其通过将由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐施用至包括人类之哺乳动物中来进行。
131、根据本发明的预防或治疗组蛋白脱乙酰酶6活性相关疾病的方法可不仅包括在症状表现之前处理疾病本身,并且还包括通过施用式i表示之1,3,4-噁二唑硫羰基化合物来抑制或避免此类症状。在管理疾病方面,某一活性成分之预防剂量或治疗剂量可视疾病或病状的性质和严重程度以及施用活性成分的途径而变化。其剂量及频率可视个别患者之年龄、体重及反应而变化。适合的剂量和用法可易于由本领域技术人员自然地考虑此类因素而选择。另外,除施用由式i表示之1,3,4-噁二唑硫羰基化合物之外,本发明的用于预防或治疗组蛋白脱乙酰酶6活性相关疾病的方法可进一步包括施用治疗有效量的有助于治疗疾病的额外活性剂,其中该额外活性剂可与式i之化合物一起展示协同作用或佐剂作用。
132、本发明提供由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐在制备用于治疗组蛋白脱乙酰酶6活性相关疾病的药物中的用途。用于制备药物的由式i表示之1,3,4-噁二唑硫羰基化合物可与可接受之佐剂、稀释剂、载剂等组合,且可与其他活性剂一起制备成复合药剂,由此具有协同作用。
133、若不彼此矛盾,则本发明的用途、组合物及治疗性方法中所提及的事项可同样适用。
134、本发明的有利效果
135、根据本发明,由式i表示之1,3,4-噁二唑硫羰基化合物、其立体异构体或其药学可接受的盐可选择性抑制hdac6,因此具有预防或治疗组蛋白脱乙酰酶6活性相关疾病的显著极佳作用。
- 还没有人留言评论。精彩留言会获得点赞!