以抗TIGIT抗体治疗癌症的方法与流程
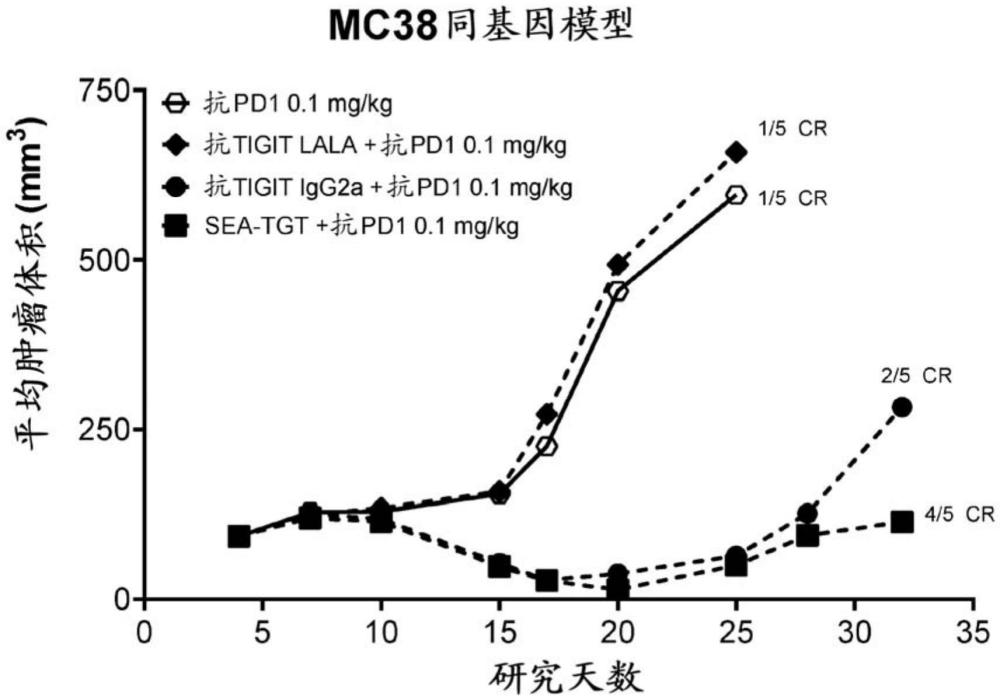
本文提供了以抗tigit抗体与抗pd-1抗体和/或抗pd-l1抗体的组合治疗癌症的方法。
背景技术:
1、具有ig结构域和itim结构域的t细胞免疫受体(“t-cell immunoreceptor withig and itim domains”,tigit)是在t细胞亚群,例如活化、记忆和调节t细胞以及自然杀伤(nk)细胞上表达的免疫细胞接合子。tigit是ig超家族蛋白质内cd28家族的成员,且充当限制t细胞增殖和活化以及nk细胞功能的共抑制分子。tigit通过与cd226(也称为dnax辅助分子-1,或“dnam-1”)竞争同一组配体来介导它的免疫抑制作用:cd155(也称为脊髓灰质炎病毒受体或“pvr”)和cd112(也称为脊髓灰质炎病毒受体相关2或“pvrl2”)。levin等人,eur:immunol.,2011,41:902-915。因为cd155对tigit的亲和力高于它对cd226的亲和力,所以在tigit存在下cd226信号传导受到抑制,由此限制t细胞增殖和活化。
2、在患有某些癌症(例如黑素瘤)的患者中,tigit表达在肿瘤抗原(ta)特异性cd8+t细胞和cd8+肿瘤浸润性淋巴细胞(til)上上调。在表达tigit配体(cd155)的细胞存在下阻断tigit增加ta特异性cd8+t细胞和cd8+til两者的增殖、细胞因子产生和脱粒。chauvin等人,j clin invest.,2015,125:2046-2058。因此,tigit代表用于刺激患者的抗肿瘤t细胞反应的潜在治疗目标,不过仍需要阻断tigit和促进抗肿瘤反应的改良方法,且需要以抗tigit抗体(无论呈单一疗法形式还是与其它剂(例如抗体)组合)治疗癌症的改良方法。
3、提供了以抗tigit抗体与抗pd-1抗体和/或抗pd-l1抗体的组合治疗癌症的改良方法。
技术实现思路
1、实施方案1.一种治疗癌症的方法,所述方法包括向患有癌症的受试者施用(1)抗tigit抗体,和(2)抗pd-1抗体或抗pd-l1抗体;其中所述癌症的样品中的pd-l1水平如通过综合阳性评分(combined positive score,cps)所测量小于10,或如通过总比例评分(total proportion score,tps)所测量小于50%,或如通过肿瘤细胞评分(tumor cellscore,tc)所测量小于50%,或如通过肿瘤浸润性免疫细胞染色(tumor-infiltratingimmune cell staining,ic)所测量小于10%,且其中所述抗tigit抗体包含具有增强的效应功能的fc区。
2、实施方案2.如实施方案1的方法,其中如通过cps所测量,所述癌症的pd-l1表达水平小于5,或小于3,或小于1。
3、实施方案3.如实施方案1或实施方案2的方法,其中如通过tps所测量,所述癌症的pd-l1表达水平小于40%,或小于30%,或小于20%,或小于10%,或小于5%,或小于3%,或小于1%。
4、实施方案4.如实施方案1-3中任一项的方法,其中如通过tc所测量,所述癌症的pd-l1表达水平小于40%,或小于30%,或小于20%,或小于10%,或小于5%,或小于3%,或小于1%。
5、实施方案5.如实施方案1-4中任一项的方法,其中如通过ic所测量,所述癌症的pd-l1表达水平小于5%,或小于3%,或小于1%。
6、实施方案6.如实施方案1-5中任一项的方法,其中:
7、a)所述癌症是非小细胞肺癌且所述tps<1%;
8、b)所述癌症是头颈部鳞状细胞癌(hnscc)且所述cps<1;
9、c)所述癌症是尿路上皮癌且所述cps<10;
10、d)所述癌症是胃癌且所述cps<1;
11、e)所述癌症是食管癌且所述cps<10;
12、f)所述癌症是宫颈癌且所述cps<1;或
13、g)所述癌症是三阴性乳腺癌且所述cps<10。
14、实施方案7.如实施方案6的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是派姆单抗(pembrolizumab)或纳武单抗(nivolumab)。
15、实施方案8.如实施方案1-5中任一项的方法,其中所述癌症是非小细胞肺癌,且所述tps<50%。
16、实施方案9.如实施方案8的方法,所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是西米普利单抗(cemiplimab)。
17、实施方案10.如实施方案1-5中任一项的方法,其中:
18、a)所述癌症是尿路上皮癌且ic<5%;
19、b)所述癌症是三阴性乳腺癌且ic<1%;或
20、c)所述癌症是非小细胞肺癌且ic<10%;或
21、d)所述癌症是非小细胞肺癌且tc<50%。
22、实施方案11.如实施方案10的方法,所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是阿特珠单抗(atezolizumab)。
23、实施方案12.如实施方案1-11中任一项的方法,其中所述抗pd-1抗体或抗pd-l1抗体以亚治疗剂量施用。
24、实施方案13.一种治疗癌症的方法,所述方法包括向患有癌症的受试者施用(1)抗tigit抗体,和(2)抗pd-1抗体或抗pd-l1抗体;其中所述抗tigit抗体包含具有增强的效应功能的fc区,且其中所述抗pd-1抗体或抗pd-l1抗体以亚治疗剂量施用。
25、实施方案14.如实施方案12或实施方案13的方法,其中所述抗pd-1抗体或抗pd-l1抗体的亚治疗剂量:a)低于针对所治疗癌症的所述抗体的单一疗法剂量和/或b)包含比针对所治疗癌症的单一疗法给药频率更低的所述抗体给药频率。
26、实施方案15.如实施方案12-14中任一项的方法,其中所述抗体的所述亚治疗剂量包括低于针对所治疗癌症的所述抗体的所述单一疗法剂量的剂量。
27、实施方案16.如实施方案15的方法,其中所述亚治疗剂量是在针对所治疗癌症的所述单一疗法剂量的5%与90%之间,或5%与80%之间,或5%与70%之间,或5%与60%之间,或5%与50%之间,或5%与40%之间,或5%与30%之间的所述抗体的剂量。
28、实施方案17.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是派姆单抗,且其中所述单一疗法剂量是200mg或400mg。
29、实施方案18.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是纳武单抗,且其中所述单一疗法剂量是240mg、360mg或480mg。
30、实施方案19.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是西米普利单抗,且其中所述单一疗法剂量是350mg。
31、实施方案20.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿维单抗(avelumab),且其中所述单一疗法剂量是800mg。
32、实施方案21.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是德瓦鲁单抗(durvalumab),且其中所述单一疗法剂量是10mg/kg或1500mg。
33、实施方案22.如实施方案14-16中任一项的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿特珠单抗,且其中所述单一疗法剂量是840mg、1200mg或1680mg。
34、实施方案23.如实施方案12-22中任一项的方法,其中所述抗体的所述亚治疗剂量包含比针对所治疗癌症的单一疗法给药频率更低的所述抗体给药频率。
35、实施方案24.如实施方案23的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是派姆单抗,且其中所述单一疗法给药频率是每3周或每6周。
36、实施方案25.如实施方案24的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是派姆单抗,且其中所述单一疗法剂量是每3周200mg或每6周400mg。
37、实施方案26.如实施方案23的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是纳武单抗,且其中所述单一疗法给药频率是每2周或每3周或每4周。
38、实施方案27.如实施方案26的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是纳武单抗,且其中所述单一疗法剂量是每2周240mg、每3周360mg或每4周480mg。
39、实施方案28.如实施方案23的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是西米普利单抗,且其中所述单一疗法给药频率是每3周。
40、实施方案29.如实施方案23的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿维单抗,其中所述单一疗法给药频率是每2周。
41、实施方案30.如实施方案23的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是德瓦鲁单抗,其中所述单一疗法给药频率是每2周或每4周。
42、实施方案31.如实施方案30的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是德瓦鲁单抗,且其中所述单一疗法剂量是每2周10mg/kg或每4周1500mg。
43、实施方案32.如实施方案23的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿特珠单抗,其中所述单一疗法给药频率是每2周、每3周或每4周。
44、实施方案33.如实施方案32的方法,其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿特珠单抗,且其中所述单一疗法剂量是每2周840mg、每3周1200mg或每4周1680mg。
45、实施方案34.如实施方案1-33中任一项的方法,其中所述癌症选自小细胞肺癌、早期小细胞肺癌、肾细胞癌、尿路上皮癌、三阴性乳腺癌、胃癌、肝细胞癌、神经胶母细胞瘤、卵巢癌、头颈部鳞状细胞癌、食管鳞状细胞癌(escc)和非高微卫星不稳定性(非高msi)结直肠癌。
46、实施方案35.一种治疗癌症的方法,所述方法包括向患有癌症的受试者施用(1)抗tigit抗体,和(2)抗pd-1抗体或抗pd-l1抗体;其中所述抗tigit抗体包含具有增强的效应功能的fc区,且其中所述癌症选自小细胞肺癌、早期小细胞肺癌、肾细胞癌、尿路上皮癌、三阴性乳腺癌、胃癌、肝细胞癌、神经胶母细胞瘤、卵巢癌、头颈部鳞状细胞癌、食管鳞状细胞癌(escc)和非高微卫星不稳定性(非高msi)结直肠癌。
47、实施方案36.如实施方案34或实施方案35的方法,其中所述方法是尿路上皮癌的一线治疗。
48、实施方案37.如实施方案1-36中任一项的方法,其中所述癌症包含降低所述抗pd-1抗体或抗pd-l1抗体的功效的突变。
49、实施方案38.一种治疗癌症的方法,所述方法包括向患有癌症的受试者施用(1)抗tigit抗体,和(2)抗pd-1抗体或抗pd-l1抗体;其中所述抗tigit抗体包含具有增强的效应功能的fc区,且其中所述癌症包含降低所述抗pd-1抗体或抗pd-l1抗体的功效的突变。
50、实施方案39.如实施方案37或实施方案38的方法,其中所述癌症包含egfr基因中的突变和/或alk基因中的突变和/或ros1基因中的突变。
51、实施方案40.如实施方案37-39中任一项的方法,其中所述癌症是非小细胞肺癌,且其中所述癌症包含egfr基因中的突变和/或alk基因中的突变。
52、实施方案41.如实施方案40的方法,其中所述方法包括施用抗pd-1抗体,其中所述抗pd-1抗体是派姆单抗或纳武单抗;或其中所述方法包括施用抗pd-l1抗体,其中所述抗pd-l1抗体是阿特珠单抗。
53、实施方案42.如前述实施方案中任一项的方法,其中所述抗tigit抗体包含与fcγriiia、fcγriia和fcγri中的至少一者的结合增强的fc。
54、实施方案43.如实施方案42的方法,其中所述抗tigit抗体包含与至少fcγriiia的结合增强的fc。
55、实施方案44.如实施方案42的方法,其中抗tigit抗体包含与至少fcγriiia和fcγriia的结合增强的fc。
56、实施方案45.如实施方案42的方法,其中所述抗tigit抗体包含与至少fcγriiia和fcγri的结合增强的fc。
57、实施方案46.如实施方案42的方法,其中所述抗tigit抗体包含与fcγriiia、fcγriia和fcγri的结合增强的fc。
58、实施方案47.如实施方案42-46中任一项的方法,其中所述抗tigit抗体的所述fc与fcγriib的结合减弱。
59、实施方案48.如前述实施方案中任一项的方法,其中所述抗tigit抗体在重链恒定区中包含取代s293d、a330l和1332e。
60、实施方案49.如前述实施方案中任一项的方法,其中所述抗tigit抗体未岩藻糖基化。
61、实施方案50.如前述实施方案中任一项的方法,其中所述方法包括施用抗tigit抗体的组合物,其中所述组合物中至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%的所述抗体未岩藻糖基化。
62、实施方案51.如前述实施方案中任一项的方法,其中所述抗tigit抗体的所述fc包含相对于相同同型的对应野生型fc具有增强的adcc和/或adcp活性的fc。
63、实施方案52.如前述实施方案中任一项的方法,其中所述抗tigit抗体包含:
64、a)重链cdr1,所述重链cdr1包含选自seq id no:7-9的氨基酸序列;
65、b)重链cdr2,所述重链cdr2包含选自seq id no:10-13的氨基酸序列;
66、c)重链cdr3,所述重链cdr3包含选自seq id no:14-16的氨基酸序列;
67、d)轻链cdr1,所述轻链cdr1包含seq id no:17的氨基酸序列;
68、e)轻链cdr2,所述轻链cdr2包含seq id no:18的氨基酸序列;以及
69、f)轻链cdr3,所述轻链cdr3包含seq id no:19的氨基酸序列。
70、实施方案53.如前述实施方案中任一项的方法,其中所述抗tigit抗体包含重链cdr1、cdr2和cdr3以及轻链cdr1、cdr2和cdr3,所述cdr包含以下序列:
71、a)分别seq id no:7、10、14、17、18和19;或
72、b)分别seq id no:8、11、14、17、18和19;或
73、c)分别seq id no:9、12、15、17、18和19;或
74、d)分别seq id no:8、13、16、17、18和19;或
75、e)分别seq id no:8、12、16、17、18和19。
76、实施方案54.如前述实施方案中任一项的方法,其中所述抗tigit抗体包含包括选自seq id no:1-5的氨基酸序列的重链可变区和包括seq id no:6的氨基酸序列的轻链可变区。
77、实施方案55.如前述实施方案中任一项的方法,其中所述抗tigit抗体包含包括选自seq id no:20-24的氨基酸序列的重链和包括seq id no:25的氨基酸序列的轻链。
78、实施方案56.如前述实施方案中任一项的方法,其中所述抗tigit抗体以亚治疗剂量施用。
79、实施方案57.如实施方案56的方法,其中所述抗tigit抗体的所述亚治疗剂量a)低于针对所治疗癌症的所述抗tigit抗体的所述单一疗法剂量和/或b)包含比针对所治疗癌症的单一疗法给药频率更低的所述抗tigit抗体给药频率。
80、实施方案58.如实施方案56或实施方案57的方法,其中所述抗tigit抗体的所述亚治疗剂量包括低于针对所治疗癌症的所述抗tigit抗体的所述单一疗法剂量的剂量。
81、实施方案59.如实施方案56-58中任一项的方法,其中所述亚治疗剂量是在针对所治疗癌症的所述单一疗法剂量的5%与90%之间,或5%与80%之间,或5%与70%之间,或5%与60%之间,或5%与50%之间,或5%与40%之间,或5%与30%之间的所述抗tigit抗体的剂量。
82、实施方案60.如实施方案56-59中任一项的方法,其中所述抗tigit抗体的所述亚治疗剂量包含比针对所治疗癌症的单一疗法给药频率更低的所述抗tigit抗体给药频率。
83、实施方案61.如前述实施方案中任一项的方法,其中所述方法包括施用抗pd-1抗体。
84、实施方案62.如实施方案61的方法,其中所述抗pd-1抗体选自派姆单抗、纳武单抗、ct-011、bgb-a317、西米普利单抗、信迪利单抗(sintilimab)、替雷利珠单抗(tislelizumab)、tsr-042、pdr001或特瑞普利单抗(toripalimab)。
85、实施方案63.如实施方案1-60中任一项的方法,其中所述方法包括施用抗pd-l1抗体。
86、实施方案64.如实施方案63的方法,其中所述抗pd-l1抗体选自德瓦鲁单抗、bms-936559、阿特珠单抗或阿维单抗。
- 还没有人留言评论。精彩留言会获得点赞!