靶向密蛋白3的嵌合抗原受体和治疗癌症的方法与流程
发明领域本发明涉及嵌合抗原受体(car),其包含结合细胞连接蛋白的至少一个表位的抗原结合蛋白,其中所述细胞连接蛋白位于细胞-细胞连接内,并且在癌细胞中,其中所述细胞连接蛋白的所述一个或多个表位仅可由所述car胞外域接近和/或由所述car胞外域结合。
背景技术:
0、发明背景
1、过继t细胞疗法是对癌症患者具有可治愈潜力变革性药物。为了为患者设计这些有力的自体细胞疗法,使用了外周血来获得t细胞,然后对其进行遗传修饰。将嵌合抗原受体(car)引入这些细胞使它们特异性与选择的抗原结合。离体扩增这些经修饰的细胞并再输注到患者中,目的是运输至表达匹配的抗原的癌细胞并随后杀死这些癌细胞(yeku等人,am soc clin oncol educ book.2017;37:193-204;mcbride等人,wiley interdiscip revnanomed nanobiotechnol.2019;11(5):e1557)。
2、car是合成抗原受体,其重定向t细胞特异性、功能和持久性。car由与t细胞激活结构域(例如,cd3复合物的ζ链)和共刺激结构域(例如,cd28或4-1bb)融合的抗原结合蛋白的抗原特异性区(诸如单链可变片段(scfv))构成。这种配置促进抗原特异性激活并增强人原代t细胞的增殖和抗凋亡功能。
3、已证明car-t细胞针对一系列液体肿瘤b细胞恶性肿瘤的引人注目的疗效;早期临床试验结果表明了在多发性骨髓瘤中的活性(sadelain等人,nature.2017;545(7655):423-31;june等人,n engl j med.2018;379(1):64-73;brudno等人,nat rev clinoncol.2017;15(1):31-46)。2017年fda批准用于淋巴瘤和白血病的cd19 car-t重新激发了开发用于实体瘤的car-t细胞的集中努力。然而,迄今为止,car-t细胞疗法在实体瘤中表现的疗效有限。
4、为了针对实体癌生成安全而有效的t细胞疗法,t细胞必须在整个制备过程中保持高而有效的杀伤潜力、能够运输至肿瘤,并克服免疫抑制性肿瘤微环境(tme)。主要的成功因素之一是抗原靶标的选择。通常,选择用于靶向的抗原在癌细胞表面上以足够的量表达,而正常组织表达仍然很低,以确保与健康细胞的低交叉反应性(脱靶效应和中靶效应两者)。实体瘤中的car免疫疗法仍然富有挑战性,很大程度上是由于缺乏其表达限于恶性组织的适当的表面抗原。抗原靶标的肿瘤外表达有引起中靶毒性的可能,其具有取决于受影响的器官组织的不同程度的严重性(watanabe等人,front immunol.2018;9:2486;park等人,sci rep.2017;7(1):14366)。
5、因此,需要鉴定出用于car免疫疗法的新靶标,特别是用于生成针对实体瘤和癌症的t细胞疗法的新靶标。
6、发明概述
7、根据第一方面,本文提供了嵌合抗原受体(car),其包含:
8、a)胞外域,其包含分离的密蛋白3(claudin-3)结合蛋白,其与人密蛋白3上的不连续表位结合,所述不连续表位至少包含seq id no:13的n38和e153;
9、b)跨膜结构域;和
10、c)一个或多个胞内信号传导结构域。
11、在进一步的方面,提供了包含多肽的嵌合抗原受体(car),该多肽包含:
12、a)包含密蛋白3结合结构域的胞外域,所述密蛋白3结合结构域包含重链可变区(vh),所述重链可变区包含seq id no:1的重链互补决定区1(cdrh1)序列;seq id no:2的重链互补决定区2(cdrh2)序列;seq id no:3的重链互补决定区3(cdrh3)序列;
13、b)跨膜结构域;和
14、c)一个或多个胞内信号传导结构域。
15、在进一步的方面,提供了分离的密蛋白3结合蛋白,其与人密蛋白3上的不连续表位结合,所述不连续表位至少包含seq id no:13的n38和e153。
16、在进一步的方面,提供了密蛋白3结合蛋白,其包含重链可变区(vh),所述重链可变区包含seq id no:1的重链互补决定区1(cdrh1)序列;seq id no:2的重链互补决定区2(cdrh2)序列;seq id no:3的重链互补决定区3(cdrh3)序列。
17、在进一步的方面,本文提供了多肽,其包含本文公开的car或密蛋白3结合蛋白的氨基酸序列。
18、根据其他方面,本文提供了包含编码本文公开的car或密蛋白3结合蛋白的序列的多核苷酸、包含本文公开的多核苷酸序列的载体以及包含本文公开的多核苷酸序列和/或载体的载体生产者细胞。
19、在另一个方面,本文提供了免疫效应细胞,其包含本文公开的car、多肽、多核苷酸和/或载体。
20、在另一个方面,本文提供了药物组合物,其包含本文公开的免疫效应细胞或密蛋白3结合蛋白,以及药学上可接受的赋形剂。
21、在另一个方面,本文提供了生成包含本文公开的car的免疫效应细胞的方法;所述方法包括将本文公开的多肽、多核苷酸和/或载体引入至免疫效应细胞中。
22、在另一个方面,本文提供了本文公开的car、密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物,其用于治疗癌症。
23、在另一个方面,本文提供了治疗受试者的癌症的方法,所述方法包括向受试者施用治疗有效量的本文公开的car或密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。
24、在另一个方面,本文提供了增加对患有癌症的受试者中的癌细胞的细胞毒性的方法,所述方法包括向受试者施用有效量的本文公开的car或密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。
25、在另一个方面,本文提供了减少患有癌症的受试者中癌细胞数量的方法,所述方法包括向受试者施用有效量的本文公开的car或密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。
26、在另一个方面,本文提供了本文公开的car或密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物在制备用于治疗癌症的药物中的用途。
27、在另一个方面,本文提供了本文公开car或密蛋白3结合蛋白、多肽、多核苷酸、载体、免疫效应细胞或药物组合物,其用于疗法。
技术实现思路
0、概述
1、新表位或新抗原(癌症特异性突变或仅由癌细胞表达的蛋白质)的识别对开发抗癌疗法是重要的。此类新表位允许将癌细胞与健康的、非癌细胞区分,并允许抗癌剂和患者自身的免疫系统被独特地靶向,而健康的、非癌细胞仍然不受影响。一种相似的但特异性较低的方法是靶向肿瘤相关联的自身抗原——与健康的、非癌细胞相比,在癌细胞中上调或过表达的蛋白质或其他细胞组分。然而,这些方法的缺点是真正的癌症特异性新表位很少且不易预测,而靶向肿瘤相关联的自身抗原可能会由于其在健康的非癌细胞中表达而导致脱靶效应。
2、为了解决这些缺点,本文提供了嵌合抗原受体(car),其结合细胞连接蛋白的至少一个表位,其中所述细胞连接蛋白位于细胞-细胞连接之内,并且在癌细胞中,其中所述细胞连接蛋白的所述至少一个表位仅可由所述car胞外域接近而结合。。此类一个或多个表位在癌细胞和健康的、非癌细胞两者,以及在有组织的组织之内的细胞上均存在或表达;而在有组织的组织之内的细胞中,由于它们不可接近而结合和/或不可用于结合而使脱靶效应减少。
3、嵌合抗原受体(car)
4、在各种实施方案中,提供了基因工程化的受体,其将免疫效应细胞重定向至表达本文所述表位的癌细胞。这些基因工程化的受体(本文称为嵌合抗原受体(car))是将对期望的抗原/表位的基于抗体的特异性与t细胞受体激活胞内域结合,以生成表现出特异性细胞免疫活性的嵌合蛋白的分子。术语“嵌合”描述了由来自不同起源的不同蛋白质或dna的部分构成。
5、在特定的实施方案中,本文提供了嵌合抗原受体(car),其包含:
6、a)包含密蛋白3结合结构域的胞外域,所述密蛋白3结合结构域包含重链可变区(vh),所述重链可变区包含seq id no:1的重链互补决定区1(cdrh1)序列;seq id no:2的重链互补决定区2(cdrh2)序列;seq id no:3的重链互补决定区3(cdrh3)序列;
7、b)跨膜结构域;和
8、c)一个或多个胞内信号传导结构域。
9、car的抗原结合结构域与靶细胞表面上的靶抗原接合,导致car聚集,并向含有car的细胞递送激活刺激。car的主要特性是它们能够重定向免疫效应细胞特异性,从而触发增殖、细胞因子产生、吞噬作用或产生能够以不依赖于主要组织相容性(mhc)的方式介导表达靶抗原的细胞的细胞死亡的分子,这利用了单克隆抗体、可溶性配体或细胞特异性共受体的细胞特异性靶向能力。
10、胞外域
11、在各种实施方案中,car包含胞外结合结构域,其包含抗原结合结构域(例如,密蛋白3特异性结合结构域);跨膜结构域;一个或多个共刺激信号传导结构域;以及一个或多个胞内信号传导结构域。
12、如本文所用,术语“嵌合抗原受体”(“car”)指工程化受体,其包含胞外抗原结合结构域(通常衍生自单克隆抗体或其片段,例如,以单域抗体(sdab)形式的vh域或以scfv形式的vh域和vl域),以及任选的间隔区、跨膜区和一个或多个胞内效应域。在特定的实施方案中,car进一步包含抗原结合结构域和胞内信号传导结构域之间的铰链区。car还可以包含任何胞外结合结构域、跨膜结构域、共刺激结构域和/或胞内信号传导结构域之间的铰链域或间隔域。car还被称为嵌合t细胞受体或嵌合免疫受体(cir)。car遗传地引入到造血细胞,诸如t细胞中,以重定向t细胞对期望的细胞表面抗原的特异性,这导致了car-t疗法。如本文所用,术语“间隔域”指发挥将跨膜结构域连接至胞外抗原/靶标结合结构域的功能的寡肽或多肽。该区域还可以称为“铰链域”或“茎域”。间隔物的大小可以根据靶表位的位置而变化,以在car:靶标/抗原结合后具有最佳功能。在一些情况下,不希望受到任何理论的束缚,可以通过在car:靶标/抗原结合后维持设定距离(例如,14nm)来达到最佳功能。
13、在特定的实施方案中,car包含胞外结合结构域,其包含与表位特异性结合的抗原结合蛋白,该表位存在于多种细胞上,但仅在靶细胞,例如癌细胞上可接近而结合和/或可用于结合。如本文所用,术语“结合结构域”、“抗原结合结构域”、“胞外域”、“胞外结合结构域”、“抗原特异性结合结构域”和“胞外抗原特异性结合结构域”可互换地使用,并提供具有特异性结合至感兴趣的靶抗原/表位的能力的car。结合结构域可以衍生自天然的、合成的、半合成的或重组来源。
14、如本文所用,术语“抗原结合蛋白”指蛋白质、抗体、抗体片段(例如,fab、scfv等)和其他抗体衍生的蛋白质构建体,诸如包含能够结合靶抗原的域抗体(dab)和sdab的那些。术语“抗原结合蛋白”和“表位结合蛋白”在本文可互换地使用。这不包括天然同源配体或受体。在一些实施方案中,抗原结合蛋白能够结合密蛋白3(也称为rvp1、hrvp1、c7orf1、cpe-r2、cpetr2),其可以称为“密蛋白3结合蛋白”或“密蛋白3特异性结合蛋白”。“密蛋白3结合蛋白”指蛋白质、抗体、抗体片段(例如,fab、scfv等)和其他抗体衍生的蛋白质构建体,诸如包含能够结合密蛋白3,优选人密蛋白3的域(例如,dab、sdab等)的那些。
15、如本文所用,术语“抗原”指被抗原结合蛋白选择性识别的大分子的结构。抗原包括但不限于包含一个或多个t细胞表位的蛋白质(含有或不含多糖)或蛋白质组合物。
16、如本文所用,术语“表位”指与抗原结合蛋白的特定结合结构域形成接触的抗原部分,也称为互补位。表位可以是线性的,或构象的/不连续的。构象表位或不连续表位包含由其他序列分隔的氨基酸残基,即,不在抗原的一级序列中的连续序列中的氨基酸残基,并且可以通过多肽链的三级折叠来组装。尽管残基可以来自多肽链的不同区域,但它们在抗原的三维结构中非常接近。在多聚体抗原的情况下,构象或不连续表位可以包括来自不同肽链的残基。表位之内包含的特定残基可通过计算机建模程序或通过本领域已知的方法(诸如x射线晶体学)获得的三维结构来确定。表位作图可以使用本领域技术人员已知的各种技术进行,包括但不限于出版物中描述的那些技术,这些出版物诸如methods in molecularbiology‘epitope mapping protocols’,mike schutkowski和ulrich reineke(volume524,2009),以及johan rockberg和johan nilvebrant(volume 1785,2018)。非限制性示例性方法包括基于肽的方法,诸如肽扫描(pepscan),通过这种方法,使用诸如elisa的技术,或例如在噬菌体上,通过肽或蛋白质突变体的大文库展示,筛选了一系列重叠肽的结合。详细的表位信息可以通过结构技术确定,这些结构技术包括但不限于x射线晶体法、溶液核磁共振(nmr)光谱法和低温电子显微法(cryo-em)。诱变,诸如丙氨酸扫描,是另一种有效的方法,通过这种方法,结合丢失分析用于表位作图。另一种方法是氢/氘交换(hdx)组合蛋白酶解和液相色谱质谱(lc-ms)分析来表征不连续表位或构象表位。
17、在特定的实施方案中,car的胞外结合结构域包含抗体或其抗原结合结构域。
18、术语“抗体”在本文中以最广泛的含义使用,指具有免疫球蛋白样域(例如igg、igm、iga、igd或ige)的分子,并且包括单克隆、重组、多克隆、嵌合、人、人源化、多特异性抗体(包括双特异性抗体和异源缀合抗体);dab、sdab、抗原结合抗体片段、fab、f(ab’)2、fv、二硫键连接的fv、scfv、二硫键连接的scfv、双抗体、tandabs等,以及任何前述分子的修饰版本(对于替代性的“抗体”格式的汇总,参见holliger和hudson 2005naturebiotechnology 23(9):1126-1136)。
19、术语“全抗体”、“整个抗体”或“完整抗体”在本文中可互换地使用,指具有大约150,000道尔顿的分子量的异四聚体糖蛋白。完整抗体由通过共价二硫键连接的两条相同的重链(hc)和两条相同的轻链(lc)构成。这个h2l2结构折叠而形成三个功能性域,包含两个抗原结合片段(称为“fab”片段)和“fc”可结晶片段。fab片段由氨基末端的可变域(重链可变(vh)或轻链可变(vl))和羧基末端的恒定域(ch1(重)和cl(轻))构成。fc片段由成对的ch2和ch3区二聚化形成的两个域构成。fc可以通过与免疫细胞上的受体结合或通过结合c1q(经典补体途径的第一个组分)来引发效应功能。五类抗体igm、iga、igg、ige和igd由不同的重链氨基酸序列定义,分别称为μ、α、γ、ε和δ,每条重链可以与κ或者λ轻链配对。血清中的大多数抗体属于igg类,并且有四种人igg的同种型(igg1、igg2、igg3和igg4),其序列主要在铰链区中不同。
20、可以使用多种方法获得全人抗体,例如使用能够产生人抗体库基于酵母的文库或转基因动物(例如,小鼠)。可以使用基于facs(荧光激活细胞分选)的方法或通过使用标记抗原在珠子上捕获,来选择在其表面上呈递与感兴趣的抗原结合的人抗体的酵母。可以用感兴趣的抗原和对经修饰以表达人免疫球蛋白基因的转基因动物进行免疫,使用b细胞分选技术分离抗原特异性人抗体。然后,可以表征使用这些技术产生的人抗体的期望的特性,诸如亲和力、可开发性和选择性。
21、替代性的抗体形式包括替代性的支架,其中抗原结合蛋白的一个或多个cdr可以排列到合适的非免疫球蛋白蛋白质支架或骨架上,诸如,亲和体(affibody)、spa支架、ldl受体a类域、avimer(参见例如,美国专利申请公开号2005/0053973、2005/0089932和2005/0164301号)或egf域。
22、在整个本说明书中,可变域序列和全长抗原结合序列之内的(例如,抗体重链序列或抗体轻链序列之内的)可变域区域中的氨基酸残基根据kabat编号惯例进行编号。相似地,实施例中使用的术语“cdr”、“cdrl1”、“cdrl2”、“cdrl3”、“cdrh1”、“cdrh2”和“cdrh3”按照kabat编号惯例。对于进一步的信息,参见kabat等人,sequences of proteins ofimmunological interest,4th ed.,u.s.department of health and human services,national institutes of health(1987)。
23、对于本领域技术人员将显而易见的是,对于可变域序列和全长抗体序列中的氨基酸残基有替代性的编号惯例。对于cdr序列还有替代性的编号惯例,例如chothia等人,1989nature 342(6252):877-83中列出的那些。抗原结合蛋白的结构和蛋白质折叠可以意指其他残基被认为是cdr序列的一部分,并且技术人员将如此理解。
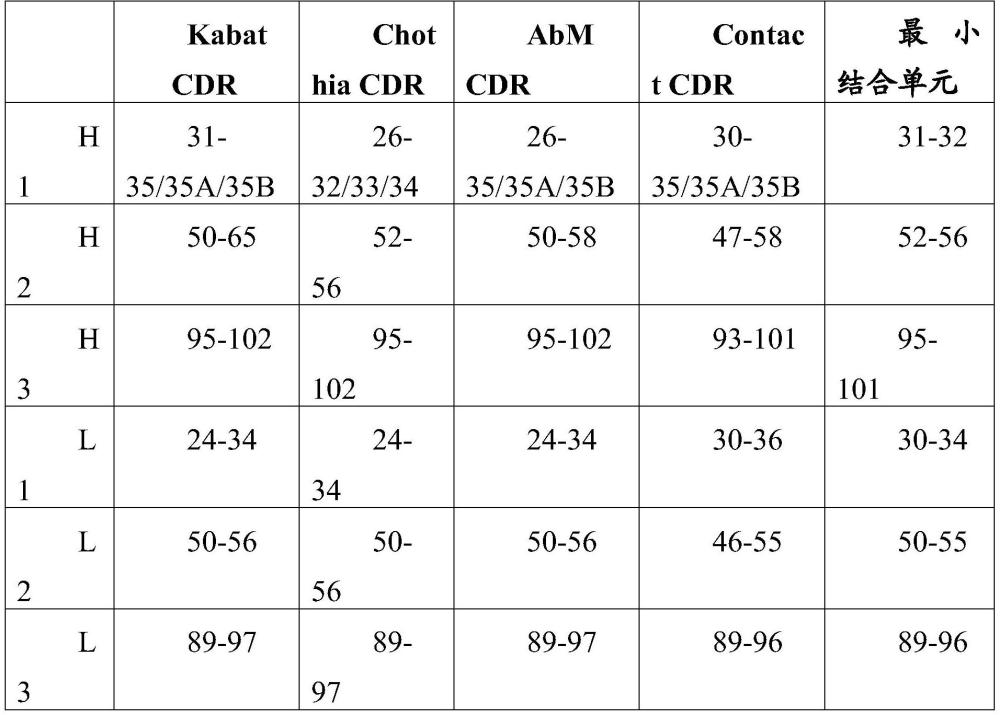
24、技术人员可获得的cdr序列的其他编号惯例包括“abm”(巴斯大学)和“contact”(英国伦敦大学学院)方法。可以确定使用kabat、chothia、abm和contact方法中的至少两种的最小重叠区,以提供“最小结合单元”。最小结合单元可以是cdr的子部分。
25、下表1代表了对每个cdr或结合单元使用每种编号惯例的一个定义。下表1中使用kabat编号方案以对可变域氨基酸序列进行编号。应当注意的是,一些cdr定义可以根据所使用的各个出版物而不同。
26、表1
27、
28、示例性密蛋白3结合蛋白包含以下cdr中任一个或组合:
29、seq id no:1的cdrh1;
30、seq id no:2的cdrh2;
31、seq id no:3的cdrh3;
32、seq id no:4的cdrl1;
33、seq id no:5的cdrl2;和/或
34、seq id no:6的cdrl3,
35、或
36、来自seq id no:7的cdrh1,cdrh2,cdrh3;和/或
37、来自seq id no:8的cdrl1,cdrl2,cdrl3,
38、或
39、来自seq id no:7的cdrh1,cdrh2,cdrh3;和
40、来自seq id no:8的cdrl1,cdrl2,cdrl3。
41、cdr可通过至少一个氨基酸取代、缺失或添加进行修饰,其中变体抗原结合蛋白基本上保持未修饰蛋白的生物学特性。
42、应当理解,每个cdr h1、h2、h3、l1、l2、l3可以单独修饰或与以任何排列或组合与任何其他cdr组合进行修饰。在一个实施方案中,通过取代、缺失或添加多至3个氨基酸,例如1个或2个氨基酸,例如1个氨基酸来修饰cdr。通常,修饰是取代,特别是保守取代,例如如下表2中所示。
43、表2
44、 侧链 成员 疏水性的 met、ala、val、leu、ile 中性亲水性的 cys、ser、thr 酸性的 asp、glu 碱性的 asn、gln、his、lys、arg 影响链取向的残基 gly、pro 芳香族的 trp、tyr、phe
45、例如,在变体cdr中,包含作为替代性的定义(例如kabat或chothia)的一部分的cdr的侧翼残基可以用保守氨基酸残基取代。
46、包含如上所述的变体cdr的此类抗原结合蛋白在本文中可以称为“功能性cdr变体”。
47、在一个实施方案中,密蛋白3结合蛋白包含重链可变区(vh),所述重链可变区包含seq id no:1的重链互补决定区1(cdrh1)序列;seq id no:2的重链互补决定区2(cdrh2)序列;seq id no:3的重链互补决定区3(cdrh3)序列。在一个实施方案中,密蛋白3结合蛋白进一步包含轻链可变区(vl),所述轻链可变区包含seq id no:4的轻链互补决定区1(cdrl1)序列;seq id no:5的轻链互补决定区2(cdrl2)序列;seq id no:6的轻链互补决定区3(cdrl3)序列。在特定的实施方案中,本文提供的car的胞外域包含本文公开的密蛋白3结合蛋白。
48、在一个实施方案中,本公开的密蛋白3结合蛋白显示出人密蛋白3和来自另一物种的密蛋白3(诸如小鼠密蛋白3和/或食蟹猴密蛋白3)之间的交叉反应性。在一个实施方案中,本文所述的密蛋白3结合蛋白特异性地结合人、食蟹猴和鼠密蛋白3。这特别有用,因为药物在人中测试之前,药物开发通常需要在小鼠系统中测试先导药物候选物。提供可以结合人和小鼠物种的药物允许技术人员在这些系统中测试结果,并使用相同的药物对数据进行并排比较。这避免了需要寻找针对小鼠密蛋白3有作用的药物和针对人密蛋白3有作用的单独药物的复杂化,并且还避免了需要比较使用不同药物的人和小鼠中的结果。还设想了疾病模型诸如狗或猴子,诸如食蟹猴中使用的其他物种之间的交叉反应性。
49、“抗原结合结构域”指抗原结合蛋白上能够特异性与抗原结合的域,这可以是单个可变域,或其可以是如可在标准抗体上发现的成对的vh/vl域。sdab或scfv域也可以提供抗原结合位点。在一个实施方案中,抗原结合蛋白是密蛋白3结合蛋白。在一个实施方案中,密蛋白3结合蛋白是sdab并且包含重链可变区(vh)。在一个实施方案中,密蛋白3结合蛋白是scfv并且包含重链可变区(vh)和轻链可变区(vl)。在一些实施方案中,vl位于vh的n末端处,或vh位于vl的n末端处。在一些实施方案中,vl和vh经由肽键彼此直接融合或经由肽接头彼此连接。
50、不同轻链或重链的框架区的序列在物种(诸如人)之内相对保守。抗体的框架区,即组成的轻链和重链的组合的框架区,用于在三维空间中定位和对齐cdr。cdr主要负责与抗原的表位结合。
51、“单克隆抗体”是由b淋巴细胞的单个克隆或已将单个抗体的轻链和重链基因转染到其中的细胞产生的抗体。单克隆抗体通过本领域技术人员已知的方法产生,例如通过制备来自骨髓瘤细胞与免疫脾细胞的融合的杂交抗体形成细胞。单克隆抗体包括人源化单克隆抗体。
52、“嵌合抗体”是一种工程化ab,其含有与衍生自受体ab的轻链和重链恒定区缔合的衍生自供体ab的天然存在的可变区(轻链和重链)。因此,在某些实施方案中,本文考虑的car包含抗原结合结构域,其是嵌合抗体或其抗原结合结构域。
53、在一些实施方案中,抗体是与人密蛋白3蛋白特异性结合的人抗体(诸如人单克隆抗体)或其片段。
54、在一个实施方案中,car包含“人源化”抗体或抗体结合片段。“人源化抗体”指一种具有cdr的工程化抗体,其cdr衍生自非人供体免疫球蛋白,该分子的其余免疫球蛋白衍生部分衍生自一种(或多种)人免疫球蛋白。此外,可以改变框架支撑残基以保留结合亲和力(参见例如,queen等人,proc.natl acad sci usa.1989;86(24):10029-10032和hodgson等人,biotechnology,1991;9(5):421-5)。通过与供体抗体的核苷酸和氨基酸序列的同源性,合适的人受体抗体可以是选自常规数据库的人受体抗体,例如,选自kabat数据库、losalamos数据库和swiss protein数据库。特征在于与供体抗体的框架区(基于氨基酸)的同源性的人抗体可以适合于提供用于插入供体cdr的重链恒定区和/或重链可变框架区。可以以相似的方式选择能够提供轻链恒定区或可变框架区的合适的受体抗体。应当注意的是,受体抗体重链和轻链不需要起源于相同的受体抗体。ep-a-0239400和ep-a-054951中详述了产生此类人源化抗体的方法的非限制性实例。
55、查询核酸序列和主题核酸序列之间的“百分比同一性”是以百分比表示的“同一性”值,这是在已经使用合适的算法或软件(诸如blastn、fasta、clustalw、muscle、mafft、emboss needle、t-coffee和dnastar lasergene)进行成对全局序列比对后,在查询序列的整个长度上使用合适的算法或软件(诸如blastn、fasta、dnastar lasergene、genedoc、bioedit、emboss needle或emboss infoalign)计算出的。重要的是,查询核酸序列可以通过本文的一项或多项权利要求中定义的核酸序列来描述。
56、查询氨基酸序列和主题氨基酸序列之间的“百分比同一性”是以百分比表示的“同一性”值,这是在已经使用合适的算法/软件(blastp、fasta、clustalw、muscle、mafft、emboss needle、t-coffee和dnastar lasergene)进行成对全局序列比对后,在查询序列的整个长度上使用合适的算法或软件(诸如blastp、fasta、dnastar lasergene、genedoc、bioedit、emboss needle或emboss infoalign)计算出的。重要的是,查询氨基酸序列可以通过本文的一项或多项权利要求中定义氨基酸序列来描述。
57、查询序列可以是与主题序列100%相同的,或与主题序列相比,其可以包括多至一定整数数量的氨基酸或核苷酸改变,使得同一性%小于100%。例如,查询序列与主题序列是至少50%、60%、70%、75%、80%、85%、90%、95%、96%、97%、98%或99%相同的。此类改变包括:至少一个氨基酸缺失、取代(包括保守取代和非保守取代),或插入,并且其中所述改变可以发生在查询序列的氨基末端或羧基末端位置处或这些末端位置之间的任何位置处,单独散布在查询序列中的氨基酸或核酸之间,或者散布在查询序列之内的一个或多个连续组中。
58、可以在查询序列的整个长度上(包括cdr)确定百分比(%)同一性。替代性地,百分比同一性可以排除一个或多个或所有cdr,例如所有cdr与主题序列100%相同,并且百分比同一性变异在查询序列的其余部分,例如,框架序列中,这使得cdr序列固定且完整。
59、本领域技术人员应当理解,本文公开的vh和/或vl域可以并入(例如,以sdab或scfv的形式)至car-t疗法中。
60、组织结构的无组织化(disorganisation)是癌症的标志,并且所得的细胞-细胞连接的扰乱可以导致表位在癌组织和癌细胞中变得可接近/可用,否则这些表位将“隐藏”在有组织的或健康的组织中[corsini等人(2018)oncotarget]。细胞-细胞接触的改变还导致细胞极性的丧失以及暴露出许多胞外信号,诸如来自生长因子的信号——在缺乏顶端-基底极性的情况下,不仅在顶端区域接收生长信号的上皮细胞倾向于通过由有丝分裂轴的错误方向促进平面外分裂而增殖。
61、在一些实施方案中,car包含胞外域,该胞外域包含结合位于细胞-细胞连接之内的细胞连接蛋白(例如,密蛋白3)的至少一个表位的抗原结合蛋白,其中所述细胞连接蛋白(例如,密蛋白3)的至少一个表位仅当细胞连接蛋白错误定位于细胞-细胞连接之外并由此暴露于细胞表面时,才可由所述car胞外域接近而结合。错误定位于细胞-细胞连接之外的细胞连接蛋白,指细胞连接蛋白的异常定位,使得细胞连接蛋白不只限于细胞-细胞连接,例如,紧密连接。作为说明性的和非限制性的实例,细胞连接蛋白(例如,密蛋白3)错误定位于癌中的细胞-细胞连接之外,并且暴露于可以被本文公开的car或抗体识别和结合的细胞表面。比较而言,在健康的或非癌组织中,位于紧密连接内的细胞连接蛋白(例如,密蛋白3)正确地受限于紧密连接,从而阻止靶向细胞连接蛋白的car或抗体的接近。
62、因此,在健康(非癌)细胞和癌细胞两者上表达的细胞连接蛋白上发现了由本文所述的car靶向的表位。然而,当由car胞外域的抗原结合蛋白结合的细胞连接蛋白的表位错误定位于或存在于细胞-细胞连接之外,而将细胞连接蛋白暴露于细胞表面时(例如,癌细胞或无组织的组织中的细胞),所述表位可用于结合和/或可接近而结合。或者,当细胞-细胞连接受损(例如,有漏洞(leaky))或被扰乱时,在癌细胞中由car胞外域的抗原结合蛋白结合的表位可用于结合和/或可接近而结合。例如,在健康的、非癌细胞或有组织的组织之内的细胞中,一个或多个表位可以被隐藏,因为它们位于细胞-细胞连接之内,使得car胞外域、抗体或抗原结合片段与所述表位结合被阻断。因此,在健康的、非癌细胞中,或在健康的、非癌细胞之间的细胞-细胞连接中,或在位于有组织的组织之内的细胞之间的细胞-细胞连接中,一个或多个表位对于car胞外域的结合是不可接近的/不可用的。
63、因此,不希望受任何特定理论的束缚,假设本文所述的car胞外域结合存在于健康的、非癌细胞和癌细胞两者中的一个或多个表位,但仅在癌细胞中或在无组织的组织中的细胞之间所述表位是可接近而结合和/或可用于结合的(参见图1)。对于由car胞外结合结构域结合的此类接近和可用性,可以是由于细胞连接蛋白的构象变化而导致形成了或暴露出car胞外域结合的一个或多个表位,例如,通过展开细胞连接蛋白中的埋藏的环,或通过在癌细胞中将在健康的、非癌细胞或有组织的组织中没有发现非常接近的氨基酸聚集在一起。或者,可用性和/或接近可以是由于与健康的非癌细胞或有组织的组织中相比,癌细胞中的细胞连接蛋白不在与结合配偶体的复合物中,或不与结合配偶体接合。应当理解,位于细胞-细胞连接之内的细胞连接蛋白可以包含特别有吸引力的表位,以在这方面用car来靶向,有组织的组织中的完整的或未受损的(例如,未被扰乱的)细胞-细胞连接阻止了car的接近,并导致所述表位不可接近和/或不可用于结合。
64、因此,在某些实施方案中,一个或多个表位存在于健康的、非癌细胞中并且不可被car胞外域接近而结合,和/或当所述细胞-细胞连接在健康的、非癌细胞之间时,一个或多个表位位于细胞-细胞连接中并且不可被car胞外域接近而结合。在进一步的实施方案中,car胞外域受到空间位阻而不结合健康的、非癌细胞中的一个或多个表位和/或受到空间位阻而不结合位于健康的、非癌细胞之间的细胞-细胞连接中的一个或多个表位。
65、因此,在一个实施方案中,细胞-细胞连接被扰乱,诸如与有组织的组织中的细胞之间(例如,健康的、非癌细胞之间)存在的细胞-细胞连接相比,无组织的组织中的细胞之间或癌细胞之间的细胞-细胞连接被扰乱。在进一步的实施方案中,细胞-细胞连接受损,诸如当在无组织的组织之内的细胞之间、癌细胞之间或癌细胞与健康的、非癌细胞之间时,细胞-细胞连接受损。因此,应当理解,术语“受损”和“被扰乱”在本文中可以互换地使用,并且包括其中细胞-细胞连接被物理地扰乱,诸如其结构被改变,和/或其中细胞-细胞连接在功能上受损,例如,具有增加的泄漏。在又一个进一步的实施方案中,当包含在细胞-细胞连接之内的蛋白质错误定位时,所述连接受损和/或被扰乱。在另一个实施方案中,当细胞-细胞连接受损和/或被扰乱时,包含在所述连接之内的蛋白质错误定位。
66、不希望受任何特定理论的束缚,假设结构被扰乱的细胞-细胞连接可以导致(例如,暴露出)通常“隐藏”在未被扰乱的细胞-细胞连接中的表位变得可接近/可用于结合(例如,变得空间上可接近/可用于结合),和/或功能受损(例如,具有增加的“泄漏”)的细胞-细胞连接可以允许增加淋巴细胞穿过所述细胞-细胞连接的侵袭/通过,从而导致某些表位可(例如,被抗原结合蛋白,包括并入car的抗原结合蛋白)接近/可(例如,被抗原结合蛋白,包括并入car的抗原结合蛋白)用于结合。
67、在一个实施方案中,当细胞-细胞连接未被扰乱时,诸如当细胞-细胞连接在健康的、非癌细胞之间,或在有组织的组织之内的细胞之间时,一个或多个表位不可被car胞外域接近/不可被car胞外域用于结合(参见图1,左图)。在另一个实施方案中,当细胞-细胞连接被扰乱时,诸如当细胞-细胞连接在癌细胞或肿瘤细胞之间,或细胞-细胞连接在健康的、非癌细胞和癌细胞之间或在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合(参见图1,右图)。在进一步的实施方案中,仅当细胞-细胞连接被扰乱时,诸如仅当细胞-细胞连接在癌细胞或肿瘤细胞之间,或细胞-细胞连接在健康的、非癌细胞和癌细胞或肿瘤细胞之间或在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。
68、在进一步的实施方案中,当细胞-细胞连接未受损时,诸如当细胞-细胞连接在健康的、非癌细胞之间,或在有组织的组织之内的细胞之间时,一个或多个表位无法被car胞外域接近/无法被car胞外域用于结合。在另一个实施方案中,当细胞-细胞连接受损时,诸如当细胞-细胞连接在癌细胞或肿瘤细胞之间,细胞-细胞连接在健康的、非癌细胞和癌细胞之间,或细胞-细胞连接在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。在进一步的实施方案中,仅当细胞-细胞连接受损时,诸如仅当细胞-细胞连接在癌细胞或肿瘤细胞之间,细胞-细胞连接在健康的、非癌细胞和癌细胞之间,或细胞-细胞连接在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。
69、仅在癌症的情况下才可被接近和/或可用于结合的表位的进一步实例包括存在于与健康的、非癌细胞相比,在癌细胞中错误定位的细胞组分(例如,细胞连接蛋白)中的表位。此类错误定位可以是细胞组分的过表达或上调、突变、蛋白质翻译后修饰的变化、细胞极化的变化和/或组织无组织化的结果。因此,在一些实施方案中,当细胞-细胞连接包含含有不是错误定位的靶表位的细胞连接蛋白时,诸如当细胞-细胞连接在健康的、非癌细胞之间,或在有组织的组织之内的细胞之间时,一个或多个表位无法被car胞外域接近/无法被car胞外域用于结合。在进一步的实施方案中,当细胞-细胞连接包含含有错误定位的靶表位的细胞连接蛋白时,诸如当细胞-细胞连接在癌细胞或肿瘤细胞之间,细胞-细胞连接在健康的、非癌细胞和癌细胞或肿瘤细胞之间,或细胞-细胞连接在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。在其他的实施方案中,仅当细胞-细胞连接包含含有错误定位的靶表位的细胞连接蛋白时,诸如仅当细胞-细胞连接在癌细胞或肿瘤细胞之间,细胞-细胞连接在健康的、非癌细胞和癌细胞之间,或细胞-细胞连接在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。在又一个进一步的实施方案中,仅当细胞-细胞连接包含含有错误定位于细胞-细胞连接之外的靶表位的细胞连接蛋白时,诸如仅当细胞-细胞连接在癌细胞之间,细胞-细胞连接在健康细胞和癌细胞之间,或当细胞-细胞连接以其他方式受损或被扰乱时,诸如在无组织的组织之内的细胞之间时,一个或多个表位可被car胞外域接近/可被car胞外域用于结合。
70、因此,如将理解的,术语“可接近的”和“可用的”在本文中可互换地使用,并且可以指与健康的、非癌细胞相比,在癌细胞上表位的空间上和/或位置上的可接近性/可用性,或指癌细胞上表位的表达。相似的,术语“不可接近的”和“不可用的”在本文中也可互换地使用。
71、在特定的实施方案中,一个或多个表位存在于位于紧密连接之内的细胞连接蛋白中。
72、紧密连接(也称为封闭连接或封闭小带(zonulae occludente))是上皮细胞之间的多蛋白复合物,其一般功能是防止运输的溶质和水渗漏穿过上皮屏障并密封细胞旁途径。它们还可以通过形成小分子(例如阳离子、阴离子或水)的选择性通道来提供渗漏途径(leaky pathway),并且上皮屏障是否分类为“紧密”或“渗漏”取决于细胞之间紧密连接以防止溶质和水的运动的能力。“紧密”上皮屏障的非限制性实例是血脑屏障,而“渗漏”上皮屏障的非限制性实例是在肾近端小管中。因此,紧密连接不仅发挥将细胞保持在一起以形成上皮屏障的功能,其还防止/控制分子和离子通过相邻细胞的膜之间的空间,以及通过防止细胞膜组分在其顶端和侧/基底表面之间的侧向扩散来维持细胞的极性。
73、紧密连接由封闭索的分支网络组成,而每条封闭索独立于其他封闭索发挥作用。每条封闭索由嵌入上皮细胞的质膜中的一排跨膜蛋白形成,而胞外域彼此直接连接。在紧密连接中发现了至少40种不同的蛋白质,它们包括跨膜蛋白和细胞质蛋白。紧密连接中发现的三种主要跨膜蛋白是闭合蛋白、密蛋白和连接黏附分子(jam)蛋白。它们与不同的外周膜蛋白,诸如位于质膜的胞内侧的将封闭索锚定至细胞骨架的肌动蛋白组分的zo-1相结合。以这种方式,紧密连接将相邻细胞的细胞骨架连接在一起。
74、闭合蛋白是nadh氧化酶,影响细胞代谢的某些方面,诸如葡萄糖摄取、atp产生和基因表达。它还对紧密连接的功能很重要,其中已显示闭合蛋白与密蛋白1、密蛋白2和yes1相互作用,并且虽然不是紧密连接的组装所需要的,但其在维持屏障特性中具有作用。闭合蛋白突变或不存在闭合蛋白增加上皮泄漏,并且已经证明了闭合蛋白的损失或异常表达引起乳腺癌组织中的侵袭增加、黏附减少并显著降低紧密连接功能。
75、密蛋白是在许多生物中发现的小型(20-27kda)跨膜蛋白。密蛋白跨越细胞膜四次(即,具有四个跨膜结构域),具有定位于细胞质中的n端和c端,和显示出最高程度的保守性的两个胞外环。第一个胞外环(ecl1)的长度约为53个氨基酸,第二个胞外环(ecl2)的长度约为24个氨基酸。ecl1控制细胞旁离子选择性,ecl2控制紧密连接之内的相邻密蛋白的同二聚化和异二聚化。n末端端通常较短(例如,4-10个氨基酸),而c末端端较长,并且长度在例如21-63个氨基酸变化,并且对于这些蛋白质定位于紧密连接中是必需的。猜测单个或分隔的密蛋白的半胱氨酸形成二硫键。所有人密蛋白(除了密蛋白12之外)都具有允许它们与支架蛋白的pdz域结合的域。
76、连接黏附分子(jam)蛋白位于高内皮细胞之间的紧密连接中,并且不仅涉及这些连接的形成,而且充当免疫细胞的黏附配体。它们还通过其与par-3和jam3的相互作用涉及内皮细胞极性。
77、在一个实施方案中,细胞连接蛋白是密蛋白家族的成员的蛋白质,例如,选自以下任一项:密蛋白1、密蛋白2、密蛋白3、密蛋白4、密蛋白5、密蛋白6、密蛋白7、密蛋白8、密蛋白9、密蛋白10a、密蛋白10b、密蛋白11、密蛋白12、密蛋白14、密蛋白15、密蛋白16、密蛋白17、密蛋白18、密蛋白19、密蛋白20、密蛋白22、密蛋白23和密蛋白25,或相关的含有密蛋白结构域1(claudin domain containing 1)、含有密蛋白结构域2(claudin domain containing2)、跨膜蛋白204和外周髓鞘蛋白22。
78、在又一个进一步的实施方案中,细胞连接蛋白是密蛋白3。在特定的实施方案中,细胞连接蛋白是人密蛋白3(例如,如seq id no:13所示的人密蛋白3)。
79、密蛋白3(也称为cldn3)在人中由cldn3基因编码,并且是紧密连接的必需组分,还是产气荚膜梭菌(clostridium perfringens)肠毒素的低亲和力受体。已证明其与cldn1和cldn5相互作用,并且人密蛋白3具有以下氨基酸序列:
80、msmgleitgtalavlgwlgtivccalpmwrvsafigsniitsqniweglwmncvvqstgqmqckvydsllalpqdlqaaralivvaillaafgllvalvgaqctncvqddtakakitivagvlfllaalltlvpvswsantiirdfynpvvpeaqkremgaglyvgwaaaalqllggallccscpprekkytatkvvysaprstgpgaslgtgydrkdyv(seq id no:13)。
81、上面粗体加下划线的残基指示n38和e153。在进一步的实施方案中,一个或多个表位存在于细胞连接蛋白的一个或多个胞外环中。在一些实施方案中,所述胞外环包括人密蛋白3的胞外环2(ecl2),其包含以下序列:
82、wsantiirdfynpvvpeaqkrem(seq id no:14)。
83、在一些实施方案中,所述胞外环包括人密蛋白3的胞外环1(ecl1),其包含以下序列:
84、rvsafigsniitsqniweglwmncvvqstgqmqckvydsllalpqdlqaar(seq id no:26)。
85、在又一个进一步的实施方案中,一个或多个表位独特地存在于密蛋白3中。如本文所用,术语“独特的”和“独特地存在”指其中在同一蛋白质家族之内的其他紧密相关的蛋白质中未发现所列举的特征。例如,其中一个或多个表位独特地存在于密蛋白3中,在另一种密蛋白家族蛋白中未发现所述一个或多个表位,诸如紧密相关的蛋白密蛋白4、密蛋白6、密蛋白5、密蛋白9或密蛋白17,特别是在密蛋白4、密蛋白6、密蛋白5或者密蛋白9,诸如已知与密蛋白3最接近的同源物密蛋白4中未发现所述一个或多个表位。此类表位可以很小或可以是短长度的氨基酸,诸如4至10个氨基酸,例如4、5、6、7、8、9或10个氨基酸。因此,在一个实施方案中,一个或多个表位的长度是4个氨基酸。密蛋白3中独特存在的表位可以是线性表位或构象表位。线性表位包含蛋白质一级序列之内的连续残基。例如,包含氨基酸序列pvvp(seq id no:15)的表位是存在于密蛋白3中的线性表位,但其不存在于其他紧密相关的密蛋白家族蛋白中,诸如密蛋白4,并且因此可以被认为是密蛋白3中独特存在的表位。构象表位包含在一级蛋白质序列中不连续但几乎非常接近而在蛋白质/抗原的三维结构上形成抗原表面的残基。密蛋白3中独特存在的表位还可以是构象表位。
86、在一些实施方案中,一个或多个表位是包含密蛋白3的ecl1和ecl2中存在的残基的构象表位。在一些实施方案中,一个或多个表位是构象表位,其包含密蛋白3的ecl1中存在的至少一个残基和密蛋白3的ecl2中存在的至少一个残基。在一些实施方案中,当根据seq id no:13编号时,一个或多个表位是构象表位,其至少包含密蛋白3的ecl1中存在的n38并且至少包含密蛋白3的ecl2中存在的e153。在一些实施方案中,一个或多个表位至少包含seq id no:13的n38和e153。在一些实施方案中,一个或多个表位基本上由seq id no:13的n38和e153组成。
87、在一个实施方案中,本文提供了分离的密蛋白3结合蛋白,其与人密蛋白3上的不连续表位结合,该不连续表位至少包含seq id no:13的n38和e153。在一个实施方案,本文提供了分离的密蛋白3结合蛋白,其与人密蛋白3上的不连续表位结合,该不连续表位基本上由seq id no:13的n38和e153组成。在一个实施方案中,其中密蛋白3结合蛋白是嵌合的或人源化的,和/或其中所述密蛋白3结合蛋白选自由以下组成的组:单克隆抗体、人igg1同种型、骆驼ig、ig nar、fab片段、fab’片段、f(ab)’2片段、f(ab)’3片段、scfv、bis-scfv、(scfv)2、微抗体、双抗体、三抗体、四抗体、二硫键稳定化的fv蛋白(dsfv)和sdab。在又一个实施方案中,本文提供了包含多肽的嵌合抗原受体(car),该多肽包含:a)胞外域,其包含分离的密蛋白3结合蛋白,该分离的密蛋白3结合蛋白与人密蛋白3上的不连续表位结合,该不连续表位至少包含seq id no:13的n38和e153;b)跨膜结构域;以及c)一个或多个胞内信号传导结构域。在另一个实施方案,胞外域包含分离的密蛋白3结合蛋白,其与人密蛋白3上的不连续表位结合,所述不连续表位基本上由seq id no:13的n38和e153组成。
88、如本文所用,术语“特异性结合亲和力”、“特异性结合”、或“特异性靶向”描述抗原/表位结合结构域(或包含其的car)与表位的结合,该表位仅在癌细胞上可接近和/或可用于结合。在某些实施方案中,结合结构域(或包含结合结构域的car或含有结合结构域的融合蛋白)以大于或等于约106m-1、107m-1、108m-1、109m-1、1010m-1、1011m-1或1012m-1的ka与靶标结合。“高亲和力”结合结构域(或其单链融合蛋白)指具有至少107m-1、至少108m-11、至少109m-11、至少1010m-11、至少1011m-1或至少1012m-1或更高的ka的那些结合结构域。如果结合结构域(或包含结合结构域的car或含有结合结构域的融合蛋白)与密蛋白3以例如103m-1至1010m-1的亲和力或ka(即,具有单位为i/m的特定结合相互作用的平衡缔合常数)结合或缔合,则可以考虑其“特异性结合”密蛋白3。
89、或者,亲和力可以定义为具有单位为m(例如,10-5m至10-13m,或更小)的特定结合相互作用的平衡解离常数(kd)。根据本公开的结合结构域多肽和car的亲和力可以使用常规技术容易地确定,例如通过竞争性elisa(酶联免疫吸附测定)、通过结合缔合、使用标记配体的置换测定、使用表面等离子体共振装置,诸如biacore t 100(从biacore,inc.,piscataway,nj获得)或光学生物传感器技术,诸如epic系统或enspire(分别可从corning和perkin elmer获得(还参见,例如,scatchard,ann ny acad sci.1949;51(4):660和美国专利号5,283,173或同族专利)。
90、然而,技术人员应当理解,包含含有本文公开的抗原/表位结合蛋白的胞外域的car可以表现出比包含相同抗原/表位结合结构域的抗体更高的灵敏度和选择性。这意味着虽然不能直接检测(诸如通过使用标记抗体或car来可视化结合)所述结合,但可以间接确定(诸如通过细胞功能测定和测量)结合。例如,可以通过使用标记的抗体或car,例如,荧光标记的可溶性抗体,来可视化结合而直接检测所述结合,或可以通过表达抗体或car的细胞的功能(例如激活)而间接检测所述结合,诸如通过细胞因子释放测定(诸如,测量ifnγ释放),测量细胞杀伤,或通过其他功能性测量/技术,如下面的实施例部分详细描述的。因此,在某些实施方案中,当抗体或抗原/表位结合片段包含在car中并因此由细胞以不可溶的、细胞形式表达时,检测(例如,通过car表达细胞的激活)了结合,但当抗体或抗原/表位结合片段以可溶的非细胞形式(例如,可溶的抗体或其抗原结合片段)被包含时,没有检测结合。技术人员将进一步理解,与其他相关蛋白(诸如其他紧密连接蛋白家族成员蛋白,包括紧密连接蛋白4、紧密连接蛋白-5、紧密连接蛋白-6和/或紧密连接蛋白-9)相比,本文所述的car可以对靶抗原/表位(诸如密蛋白3)具有更强的选择性。
91、在特定的实施方案中,car的胞外结合结构域包含抗原结合蛋白,诸如抗密蛋白3结合蛋白,其中抗原结合蛋白选自抗体或其抗原结合片段。
92、在特定的实施方案中,抗原结合蛋白,诸如抗密蛋白3抗体或其抗原结合片段,包括但不限于骆驼ig(骆驼科抗体(vhh))、ig nar、fab片段、fab’片段、f(ab)’2片段、f(ab)’3片段、fv、scfv、bis-scfv、(scfv)2、微抗体、双抗体、三抗体、四抗体、二硫键稳定化的fv蛋白(“dsfv”)和sdab(也称为纳米抗体)。
93、在一个实施方案中,抗原结合蛋白,诸如抗密蛋白3抗体或其抗原结合片段是scfv。
94、在一些实施方案中,car胞外域包含密蛋白3结合蛋白。示例性密蛋白3结合蛋白是对密蛋白3特异性的免疫球蛋白可变区,其包含至少一个人框架区。“人框架区”指人免疫球蛋白可变区的野生型(即,天然存在的)框架区、在人免疫球蛋白可变区的框架区中具有小于约50%(例如,优选地小于约45%、40%、35%、30%、25%、20%、15%、10%、5%或1%)的氨基酸被删除或取代(例如,在相应位置处具有非人免疫球蛋白框架区的一个或多个残基)的人免疫球蛋白可变区的改变的框架区,或在非人免疫球蛋白可变区的框架区中具有小于约50%(例如,优选地小于约45%、40%、35%、30%、25%、20%、15%、10%、5%或1%)的氨基酸被删除或取代(例如,在暴露出的残基的位置处,和/或在相应位置处具有人免疫球蛋白框架区的一个或多个残基)的非人免疫球蛋白可变区的改变的框架区,使得在一个实施方案中,免疫原性降低。
95、在某些实施方案中,人框架区是人免疫球蛋白可变区的野生型框架区。在某些其他的实施方案中,人框架区是在一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个位置处具有氨基酸缺失或取代的人免疫球蛋白可变区的改变的框架区。在其他的实施方案中,人框架区是在一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个位置处具有氨基酸缺失或取代的非人免疫球蛋白可变区的改变的框架区。
96、在特定的实施方案中,密蛋白3结合蛋白包含至少一个、两个、三个、四个、五个、六个、七个或八个选自人轻链fr1、人重链fr1、人轻链fr2、人重链fr2、人轻链fr3、人重链fr3、人轻链fr4和人重链fr4的人框架区(fr)。
97、可以存在于密蛋白3特异性结合结构域中的人fr还包括本文提供的示例性fr的变体,其中已经取代或缺失了示例性fr的一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或更多个氨基酸。
98、在某些实施方案中,密蛋白3结合蛋白包含:(a)人源化轻链可变区,其包含人轻链fr1、人轻链fr2、人轻链fr3和人轻链fr4;以及(b)人源化重链可变区,其包含人重链fr1、人重链fr2、人重链fr3和人重链fr4。
99、本文提供的密蛋白3结合蛋白还可以包含一个、二个、三个、四个、五个或六个cdr。此类cdr可以是选自重链可变区的cdrh1、cdrh2和cdrh3以及轻链可变区的cdrl1、cdrl2和cdrl3的非人cdr或改变的非人cdr。在某些实施方案中,密蛋白3结合蛋白包含重链可变区,该重链可变区包含重链cdrh1、重链cdrh1和重链cdrh3。在某些实施方案中,密蛋白3结合蛋白包含重链可变区,所述重链可变区包含轻链可变区,所述轻链可变区包含轻链cdrl1、轻链cdrl2和轻链cdrl3。在某些实施方案中,密蛋白3结合蛋白包含(a)重链可变区,其包含重链cdrh1、重链cdrh2和重链cdrh3;以及(b)轻链可变区,其包含轻链cdrl1、轻链cdrl2和轻链cdrl3。
100、因此,在一个实施方案中,密蛋白3结合蛋白包含选自来自seq id no:7的cdrh1、cdrh2和cdrh3和/或来自seq id no:8的cdrl1、cdrl2和cdrl3的cdr中的任一者或组合。在进一步的实施方案中,密蛋白3结合蛋白包含来自seq id no:7和8的所有六个cdr。
101、在一个实施方案中,密蛋白3结合蛋白包含至少一个seq id no:1-3所示的重链cdr序列。在特定的实施方案中,密蛋白3结合蛋白包含至少一个与seq id no:1-3所示的重链cdr序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的重链cdr序列。在进一步的实施方案中,密蛋白3结合蛋白包含至少一个与seq id no:1-3所示的重链cdr序列至少90%相同的重链cdr序列。在特定的实施方案中,密蛋白3结合蛋白包含与seq id no:1至少90%相同的cdrh1、与seq id no:2至少90%相同的cdrh2,和/或与seq id no:3至少90%相同的cdrh3。在其他的实施方案中,密蛋白3结合蛋白包含seq id no:1的cdrh1、seq id no:2的cdrh2,和/或seq id no:3的cdrh3。
102、在一个实施方案中,密蛋白3结合蛋白包含至少一个seq id no:4-6所示的轻链cdr序列。在特定的实施方案中,密蛋白3结合蛋白包含至少一个与seq id no:4-6所示的轻链cdr序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的轻链cdr序列。在进一步的实施方案中,密蛋白3结合蛋白包含至少一个与seq id no:4-6所示的轻链cdr序列至少90%相同的轻链cdr序列。在特定的实施方案中,密蛋白3结合蛋白包含与seq id no:4至少90%相同的cdrl1、与seq id no:5至少90%相同的cdrl2,和/或与seq id no:6至少90%相同的cdrl3。在其他的实施方案中,密蛋白3结合蛋白包含seq id no:4的cdrl1、seq id no:5的cdrl2,和/或seq id no:6的cdrl3。
103、在一些实施方案中,密蛋白3结合蛋白包含与seq id no:1至少90%相同的cdrh1、与seq id no:2至少90%相同的cdrh2、与seq id no:3至少90%相同的cdrh3、与seq idno:4至少90%相同的cdrl1、与seq id no:5至少90%相同的cdrl2、和与seq id no:6至少90%相同的cdrl3。
104、在又一个进一步的实施方案中,密蛋白3结合蛋白包含seq id no:1的cdrh1、seqid no:2的cdrh2、seq id no:3的cdrh3、seq id no:4的cdrl1、seq id no:5的cdrl2和seqid no:6的cdrl3。
105、提及“vh”指免疫球蛋白重链的可变区,包括本文公开的抗体、fv、scfv、dsfv、fab、sdab或其他抗体片段的免疫球蛋白重链的可变区。本文考虑的适合构建密蛋白3结合蛋白的重链可变区的说明性实例,包括但不限于seq id no:7所示的重链可变区序列。
106、提及“vl”指免疫球蛋白轻链的可变区,包括本文公开的抗体、fv、scfv、dsfv、fab或其他抗体片段的免疫球蛋白轻链的可变区。本文考虑的适合构建密蛋白3结合蛋白的轻链可变区的说明性实例,包括但不限于seq id no:8中所示的轻链可变区序列。
107、在一个实施方案中,密蛋白3结合蛋白包含与seq id no:7的序列至少75%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的vh序列。在另一个实施方案中,密蛋白3结合蛋白包含与seq id no:7的序列至少90%相同的vh序列。在替代性的实施方案中,密蛋白3结合蛋白包含seq id no:7的vh序列。
108、在进一步的实施方案中,密蛋白3结合蛋白包含与seq id no:8的序列至少75%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的vl序列。在另一个实施方案中,密蛋白3结合蛋白包含与seq id no:8的序列至少90%相同的vl序列。在替代性的实施方案中,密蛋白3结合蛋白包含seq id no:8的vl序列。
109、因此,在一个实施方案中,密蛋白3结合蛋白包含与seq id no:7的序列至少90%相同的vh序列和与seq id no:8的序列至少90%相同的vl序列。在进一步的实施方案中,密蛋白3结合结构域包含seq id no:7的vh序列和seq id no:8的vl序列。
110、在特定的实施方案中,密蛋白3结合蛋白是包含与seq id no:7的序列至少90%相同的vh序列的sdab。在一个实施方案中,密蛋白3结合蛋白是包含seq id no:7的vh序列的sdab。
111、在特定的实施方案中,密蛋白3结合蛋白包含与seq id no:7的序列至少90%相同的vh序列和与seq id no:8的序列至少90%相同的vl序列的scfv,并且优选地包含seq idno:7的vh序列和seq id no:8的vl序列。
112、在一些实施方案中,密蛋白3结合蛋白是scfv,其从n末端到c末端包含vh序列和vl序列,其中vh和vl序列任选地由接头序列分隔。在特定的实施方案中,密蛋白3结合蛋白是scfv,其从n末端到c末端包含seq id no:7的vh序列和seq id no:8的vl序列。在其他的实施方案中,密蛋白3结合蛋白是scfv,其从n末端到c末端包含vl序列和vh序列,其中vl和vh序列任选地由接头序列分隔。在特定的实施方案中,密蛋白3结合蛋白是scfv,其从n末端到c末端包含seq id no:8的vl序列和seq id no:7的vh序列。
113、在某些实施方案中,密蛋白3结合蛋白包含与seq id no:11的序列至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的序列。在进一步的实施方案中,密蛋白3结合蛋白包含与seq id no:11至少90%相同的序列。在又一个进一步的实施方案中,密蛋白3结合蛋白包含seq id no:11的序列。
114、在某些实施方案中,密蛋白3结合蛋白包含与seq id no:18的序列至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%相同的序列。在进一步的实施方案中,密蛋白3结合蛋白包含与seq id no:18至少90%相同的序列。在又一个进一步的实施方案中,密蛋白3结合蛋白包含seq id no:18的序列。
115、接头
116、在某些实施方案中,car包含在各个结构域之间(例如,在vh结构域和vl结构域之间)为了分子的适当间隔和构象而添加的接头残基。在特定的实施方案中,接头是可变区连接序列。“可变区连接序列”是连接vh结构域和vl结构域并提供与两个亚结合结构域的相互作用相容的间隔功能的氨基酸序列,使得所得多肽保持如包含相同的轻链可变区和重链可变区的抗体的、与相同靶分子的特异性结合亲和力。在特定的实施方案中,接头分隔一个或多个重链可变结构域或轻链可变结构域、铰链结构域、跨膜结构域、共刺激结构域和/或胞内信号传导结构域。car可以包含一个、两个、三个、四个、五个或更多个接头。在特定的实施方案中,接头的长度为约1个至约25个氨基酸、约5个至约20个氨基酸、约10个至约20个氨基酸或任何中间长度的氨基酸。在一些实施方案中,接头是1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25个或更多个氨基酸长。
117、接头的说明性实例包括甘氨酸聚合物(g)n;甘氨酸-丝氨酸聚合物(g1-5s1-5)n,其中n是至少一、二、三、四或五的整数;甘氨酸-丙氨酸聚合物;丙氨酸-丝氨酸聚合物;以及本领域已知的其他柔性接头。示例性接头是如seq id no:9所示的甘氨酸-丝氨酸聚合物。
118、间隔结构域
119、在特定的实施方案中,胞外域,即car的结合结构域后跟一个或多个“间隔结构域”,这指将抗原结合结构域移离效应细胞表面以实现适当的细胞/细胞接触、抗原结合和激活的区域(patel等人,gene therapy,1999;6:412-419)。间隔结构域可以衍生自天然的、合成的、半合成的或者重组的来源。在某些实施方案中,间隔结构域是免疫球蛋白的一部分,包括但不限于一个或多个重链恒定区,例如,ch2和ch3。间隔结构域可以包括天然存在的免疫球蛋白铰链区或改变的免疫球蛋白铰链区的氨基酸序列。
120、在一个实施方案中,间隔结构域包含igg1、igg4或igd的ch2结构域和ch3结构域。
121、铰链结构域
122、car的结合结构域通常后跟一个或多个“铰链结构域”,其在将抗原结合结构域定位远离效应细胞表面以实现适当的细胞/细胞接触、抗原结合和激活中发挥作用。car通常包含在结合结构域和跨膜结构域(tm)之间的一个或多个铰链结构域。铰链结构域可以衍生自天然的、合成的、半合成的或者重组的来源。铰链结构域可以包括天然存在的免疫球蛋白铰链区或改变的免疫球蛋白铰链区的氨基酸序列。
123、适合于用于本文所述的car的说明性铰链结构域包括衍生自i型膜蛋白(诸如cd8α和cd4)的胞外区的铰链区,其可以是来自这些分子的野生型铰链区或可以是改变的。在特定的实施方案中,铰链结构域衍生自或包含cd8α铰链区。
124、跨膜结构域
125、在特定的实施方案中,car进一步包含跨膜结构域。“跨膜结构域”(tm)是car的一部分,其融合胞外结合部分和共刺激结构域/胞内信号传导结构域,并将car锚定至免疫效应细胞的质膜(例如,通过穿过细胞膜)。tm结构域可以衍生自天然的、合成的、半合成的或者重组的来源。tm结构域可以至少衍生自(例如,包含)t细胞受体的α或β链、cd3δ、cd3ε、cd3γ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd80、cd86、cd134、cd137(4-1bb)、cd152、cd154、cd278(icos)和pd1的跨膜区。在特定的实施方案中,tm结构域是合成的并且主要包含疏水性残基,诸如亮氨酸和缬氨酸。
126、在一个实施方案中,car包含衍生自cd8α的tm结构域。在另一个实施方案中,car包含衍生自cd8α的tm结构域以及短寡肽或多肽接头,该接头长度优选在1个、2个、3个、4个、5个、6个、7个、8个、9个或10个氨基酸之间,其连接car的tm结构域和共刺激/胞内信号传导结构域。基于甘氨酸-丝氨酸的接头提供了特别合适的接头。衍生自cd8α的示例性tm结构域显示在seq id no:19中。
127、胞内信号传导结构域
128、在特定的实施方案中,car进一步包含胞内信号传导。“胞内信号传导结构域”(也称为“胞内效应结构域”或“信号传导结构域”)指参与将靶抗原(例如,密蛋白3蛋白)与胞外域有效结合(例如,抗密蛋白3car结合)的消息传导至免疫效应细胞的内部,以引发效应细胞功能的car的部分。胞内信号传导结构域负责活化其中表达car的免疫细胞的至少一种正常效应功能,例如,活化、细胞因子产生、增殖和/或细胞毒活性,包括向结合car的靶细胞释放细胞毒因子,或抗原与胞外car结构域结合引发的其他细胞应答。
129、术语“效应功能”指免疫效应细胞的特化的功能。t细胞的效应功能例如可以是细胞毒活性或辅助活性,包括分泌细胞因子。因此,术语“胞内信号传导结构域”指转导效应功能信号并指导细胞以进行特化功能的蛋白质部分。虽然通常可以利用整个胞内信号传导结构域,但在许多情况下不需要使用整个结构域。就使用胞内信号传导结构域的截短部分而言,只要此类截短部分转导效应功能信号,其可以用于代替整个结构域。
130、术语胞内信号传导结构域意指包括足以转导效应功能信号的胞内信号传导结构域的任何截短部分。
131、众所周知,单独通过t细胞受体(tcr)生成的信号不足以完全活化t细胞,并且还需要次级信号或共刺激信号。因此,t细胞活化可以说是由以下两种不同类的信号传导结构域介导的:胞内信号传导结构域,其通过tcr(例如,tcr/cd3复合物)启动抗原依赖性初级活化,以及共刺激信号传导结构域,其以抗原非依赖性的方式作用以提供次级信号或共刺激信号。在一些实施方案中,car包含至少一个“共刺激信号传导结构域”和至少一个“胞内信号传导结构域”。
132、胞内信号传导结构域以刺激方式或以抑制方式调控tcr复合物的初级活化。以刺激方式作用的胞内信号传导结构域可以含有信号传导基序,其被称为基于免疫受体酪氨酸的激活基序或itam。
133、适合于用于本文所述的car的特定的实施方案的含有胞内信号传导结构域的itam的说明性实例包括衍生自fcrγ、fcrβ、cd3γ、cd3ε、cd3δ、cd3ζ、cd22、cd66d、cd79a和cd79b的那些。在一个实施方案中,一个或多个胞内信号传导结构域是cd3ζ。示例性cd3ζ胞内信号传导结构域显示在seq id no:21中。在特别优选的实施方案中,car包含cd3ζ胞内信号传导结构域和一个或多个共刺激信号传导结构域。胞内信号传导结构域和共刺激信号传导结构域可以以任何顺序以串联连接至跨膜结构域的羧基末端。
134、共刺激结构域
135、在特定的实施方案中,car进一步包含一个或多个共刺激信号传导结构域以增强表达car的t细胞的疗效和扩增。如本文所用,术语“共刺激信号传导结构域”或“共刺激结构域”指共刺激分子的胞内信号传导结构域。共刺激分子是除抗原受体或fc受体以外的细胞表面分子,其在与抗原结合后提供t淋巴细胞的有效活化和功能所需要的第二信号。此类共刺激分子的说明性实例包括card11、cd2、cd7、cd27、cd28、cd30、cd40、cd54(icam)、cd83、cd134(ox40)、cd137(4-1bb)、cd278(icos)、dap10、lat、nkd2c、slp76、tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、trim和zap70。
136、在一个实施方案中,car包含选自由cd28、cd134(ox40)和cd137(4-1bb)组成的组的一个或多个共刺激信号传导结构域。在进一步的实施方案中,一个或多个共刺激结构域是cd137(4-1bb)。示例性cd137(4-1bb)共刺激结构域显示在seq id no:20中。
137、在另一个实施方案中,car包含cd137(4-1bb)共刺激信号传导结构域和cd3ζ胞内信号传导结构域。
138、在某些实施方案中,car进一步包含前导序列。在特定的实施方案中,前导序列是cd8前导序列。示例性cd8前导序列如seq id no:10中所示。
139、因此,在某些实施方案中,本文考虑的car包含与seq id no:12、34、35、36、37、38或39的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq idno:12、34、35、36、37、38或39的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:12、34、35、36、37、38或39的序列。
140、在某些实施方案中,本文考虑的car包含与seq id no:25的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq id no:25的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:25的序列。
141、在某些实施方案中,本文考虑的car包含与seq id no:27的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq id no:27的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:27的序列。
142、在某些实施方案中,本文考虑的car包含与seq id no:28的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq id no:28的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:28的序列。
143、在某些实施方案中,本文考虑的car包含与seq id no:29的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq id no:29的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:29的序列。
144、在某些实施方案中,本文考虑的car包含与seq id no:30的序列具有至少85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%氨基酸同一性的序列。在进一步的实施方案中,car包含与seq id no:30的序列至少90%相同的序列。在又进一步的实施方案中,car包含seq id no:30的序列。
145、在特定的实施方案中,提供了嵌合抗原受体(car),其包含:
146、a)包含根据本文公开的任一个实施方案的密蛋白3结合蛋白的胞外域;
147、b)衍生自cd8α的跨膜结构域;和
148、c)衍生自cd3ζ的胞内信号传导结构域。
149、在另一个特定的实施方案中,提供了嵌合抗原受体(car),其包含:
150、a)包含密蛋白3结合蛋白的胞外域,所述密蛋白3结合蛋白包含seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列;seq id no:4的cdrl1序列;seq id no:5的cdrl2序列;和seq id no:6的cdrl3序列;
151、b)衍生自cd8α的跨膜结构域;
152、c)衍生自cd3ζ的胞内信号传导结构域;和
153、d)衍生自cd137(4-1bb)的共刺激结构域。
154、在一些实施方案中,胞外域的密蛋白3结合蛋白是sdab。在其他的实施方案中,胞外域的密蛋白3结合蛋白是包含以下的sdab:seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列。在一些实施方案中,胞外域的密蛋白3结合蛋白是scfv。在其他实施方案中,胞外域的密蛋白3结合蛋白是包含以下的scfv:seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列;seq id no:4的cdrl1序列;seq id no:5的cdrl2序列;和seq id no:6的cdrl3序列。在又一个其他的实施方案中,胞外域的密蛋白3结合蛋白是包含以下的scfv:seq id no:7的vh序列和seq id no:8的vl序列。
155、本文还提供了与包含胞外域的car竞争结合的密蛋白3结合蛋白或嵌合抗原受体(car),该胞外域包含密蛋白3结合蛋白,该密蛋白3结合蛋白包含seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列;seq id no:4的cdrl1序列;seqid no:5的cdrl2序列;和seq id no:6的cdrl3序列。在某些实施方案中,本文考虑的car与包含胞外域的car竞争结合,该胞外域包含密蛋白3结合蛋白,该密蛋白3结合蛋白包含seqid no:7的vh序列和seq id no:8的vl序列。合适地,所述car包含密蛋白3结合蛋白,其是scfv。
156、多肽
157、本文考虑了各种多肽,包括但不限于car多肽及其片段、包含car多肽及其片段的细胞和组合物、表达多肽的抗体和载体。在优选的实施方案中,提供了包含一个或多个car的多肽。在特定的实施方案中,car是密蛋白3结合car,其包含与seq id no:11至少90%相同的氨基酸序列,优选地包含与seq id no:12、34、35、36、37、38或39至少90%相同的序列。
158、除非另有相反说明,否则“多肽”、“多肽片段”、“肽”和“蛋白质”可互换地使用,并且根据常规含义,即,作为氨基酸序列。多肽可以是合成的或重组地产生的。多肽不限于特定长度,例如它们可以包含全长蛋白质序列或全长蛋白质的片段,并且可以包括多肽的翻译后修饰,例如糖基化、乙酰化、磷酸化等等,以及本领域已知的天然存在的和非天然存在的其他修饰。在各种实施方案中,car多肽在蛋白质的n末端处包含信号(或前导)序列,其共翻译地或翻译后地指导蛋白质的转移。可用于本文考虑的car的合适的信号序列的说明性实例,包括但不限于iggl重链信号多肽、cd8α信号多肽、或人gm-csf受体α信号多肽。多肽可以使用多种众所周知的重组和/或合成技术中的任何一种来制备。本文考虑的多肽具体涵盖本公开的car,或具有如本文考虑的car的一个或多个氨基酸的缺失、添加和/或取代的序列。
159、如本文所用,“分离的肽”或“分离的多肽”等等,指从细胞环境中以及从与细胞的其他组分的缔合中体外分离和/或纯化肽或多肽分子,即,其与体内物质没有显著缔合。相似的,“分离的细胞”指从体内组织或器官中获得的细胞,并且基本上不含胞外基质。
160、多肽包括“多肽变体”。多肽变体可以在一个或多个取代、缺失、添加和/或插入上不同于天然存在的多肽。此类变体可以是天然存在的或可以是合成生成的,例如通过修饰一个或多个的上述多肽序列。
161、应当理解,如本文所提供的包含car的多肽可以包含进一步的和/或额外的多肽序列或元件,car诸如包含seq id no:11的氨基酸序列或seq id no:12、34、35、36、37、38或39的car。此类额外的元件包括但不限于消融或控制元件,此类元件可以用于控制细胞中多肽序列的表达或靶向含有多肽的细胞。控制表达的元件或多肽序列可以包含内部核糖体进入位点(ires)、翻译起始序列和/或在翻译之后允许多肽序列的元件分离的切割位点。
162、因此,在一个实施方案中,本文考虑的多肽进一步包含消融元件。如本文所用,“消融元件”指在细胞表面上表达的多肽序列和/或蛋白质,并且其可以用于靶向或检测所述细胞(也称为“消除标志物”)。例如,消融元件可以是细胞表面蛋白的多肽序列,其包含抗体或其抗原结合片段的胞外表位或结合区。因此,在一个实施方案中,消融元件是细胞表面蛋白,其使用对细胞表面蛋白特异的抗体或其抗原结合片段来靶向抗体依赖性细胞毒性(adcc)和/或补体依赖性细胞毒性(cdc)。因此,通过利用此类机制,应当理解,可以特异性地标记/检测表达本文考虑的多肽的细胞,并且可以将其从例如转导的细胞和未转导的细胞的混合群体中特异性地选择或分离。此外,表达包含消融元件的多肽的细胞可以特异性地和选择性地消除,诸如从治疗的受试者的循环中消除/去除。
163、合适的消融元件的实例包括但不限于截短的人egfr多肽(huegfrt)和cd20,它们可以分别被西妥昔单抗和利妥昔单抗识别(wang等人,blood,2011;118(5):1255-1263,paszkiewicz等人,j clin invest,2016;126(11):4262-4272,vogler等人,mol ther j amsoc gene ther,2010;18:1330-8,griffioen等人,haematologica,2009;94:1316-20,以及philip等人,blood,2014;124:1277-87)。合适的消融元件的另一个例子是并入至car胞外域中的短多肽表位标签(也称“e-标签”),然后可以生成抗表位标签car(koristka等人,cancer immunol immunother cii,2019;68:1401-15)。
164、因此,在一个实施方案中,消融元件选自由以下组成的组:截短的人egfr多肽(huegfrt)和cd20。在特定的实施方案中,消融元件是cd20。
165、在一些实施方案中,消融元件切割自car多肽序列。因此,在一个实施方案中,本文考虑的多肽包含切割位点,诸如p2a切割位点。
166、在某些实施方案中,多肽包含seq id no:24所示的序列。
167、多核苷酸
168、在另一个方面,提供了编码如本文所述的一个或多个car的多核苷酸。如本文所用,术语“多核苷酸”或“核酸”指信使rna(mrna)、rna、基因组rna(grna)、正链rna(rna(+))、负链rna(rna(-))、基因组dna(gdna)、互补dna(cdna)或重组dna。多核苷酸包括单链多核苷酸和双链多核苷酸。
169、在各种说明性实施方案中,多核苷酸包括载体、病毒载体和转移质粒,以及包含其的组合物和细胞。在各种说明性实施方案中,多核苷酸编码本文考虑的car或多肽,包括但不限于具有seq id no:12、34、35、36、37、38或39的序列的car,或编码seq id no:12、34、35、36、37、38或39的多核苷酸序列,或seq id no:16和17所示的多核苷酸序列。
170、因此,还提供了编码本文公开的抗原结合蛋白的多核苷酸,包括包含与seq idno:16和/或17至少75%、85%、86%、87%、88%、89%、90%、91%、92%、93%94%、95%、96%、97%、98%或99%相同的序列的多核苷酸。在一个实施方案中,多核苷酸包含seq idno:16和/或17的序列。
171、如本文所用,“分离的多核苷酸”指已经从天然存在状态下位于其两侧的序列中纯化的多核苷酸,例如,已经从通常与该片段相邻的序列中去除的dna片段。“分离的多核苷酸”还指互补dna(cdna)、重组dna或自然界中不存在且已经由人工制备的其他多核苷酸。
172、可以使用本领域已知和可获得的多种成熟技术中的任何一种来制备、操作和/或表达多核苷酸。为了表达期望的多肽,可以将编码该多肽的核苷酸序列插入至适当的载体中。
173、载体
174、在另一个方面,本发明提供了包含编码本文所述的一种或多种car和/或多肽的多核苷酸的载体。
175、本文所用的术语“载体”,指能够转移或运输另一个核酸分子的核酸分子。转移的核酸通常连接至,例如插入至载体核酸分子中。载体可以包括指导细胞中自主复制的序列或可以包括足以允许整合到宿主细胞dna中的序列。有用的载体包括,例如,质粒(例如,dna质粒或rna质粒)、转座子、黏粒(cosmid)、细菌人工染色体和病毒载体。有用的病毒载体包括,例如,复制缺陷型逆转录病毒和慢病毒。
176、在特定的实施方案中,载体是表达载体。表达载体可以用于产生本文考虑的car和多肽。另外,表达载体可以包括允许产生病毒载体的额外的组分,反过来包含本文所考虑的多核苷酸。病毒载体可用于将本文考虑的多核苷酸递送至受试者或受试者的细胞。表达载体的实例包括但不限于质粒、自主复制序列和转座元件。额外的示例性载体包括但不限于质粒、噬菌粒、黏粒、转座子、人工染色体(诸如酵母人工染色体(yac)、细菌人工染色体(bac)或pi衍生的人工染色体(pac))、噬菌体(诸如λ噬菌体或ml3噬菌体)和动物病毒。
177、表达载体的额外的实例是用于在哺乳动物细胞中的表达的pclneo载体(promega);用于慢病毒介导的基因转移和哺乳动物细胞中的表达的plenti4/v5-desttmplenti6/v5-desttm和plenti6.2/v5-gw/lacz(invitrogen)。在特定的实施方案中,本文公开的car和多肽的编码序列可以连接到此类表达载体中,以用于在哺乳动物细胞中表达car和/或多肽。
178、在特定的实施方案中,本文提供的表达载体是包含本文所述的多核苷酸的bac。在特定的实施方案中,bac额外包含一种或多种多核苷酸,该多核苷酸编码当在生产细胞系或包装细胞系中表达时,允许产生病毒载体所必需的蛋白质。举例而言,pct申请wo2017/089307和wo2017/089308描述了用于产生逆转录病毒载体、特别是慢病毒载体的表达载体。在特定的实施方案中,提供了wo2017/089307和wo2017/089308中描述的表达载体,其包含如本文中描述的多核苷酸。
179、表达载体中存在的“控制元件”或“调控序列”是载体复制起点的非翻译区、选择盒、启动子、增强子、翻译起始信号(shine dalgarno序列或科扎克序列)、内含子、多腺苷酸化序列、5’和3’非翻译区-其与宿主细胞蛋白质相互作用以进行转录和翻译。这些元件的强度和特异性可以有所不同。取决于所使用的载体系统和宿主,可以使用任何数量的合适的转录和翻译元件,包括普遍存在的(ubiquitous)启动子和诱导型启动子。
180、用于递送的载体
181、还提供了用于将本文所述的多核苷酸递送至受试者和/或受试者的细胞的载体。此类载体的实例包括但不限于质粒、自主复制序列、转座元件、噬菌粒、黏粒、人工染色体(诸如酵母人工染色体(yac)、细菌人工染色体(bac)或pi衍生的人工染色体(pac))、噬菌体(诸如λ噬菌体或ml3噬菌体)和病毒载体。
182、用作病毒载体的动物病毒的类别的实例包括但不限于逆转录病毒(包括慢病毒)、腺病毒、腺相关病毒(aav)、疱疹病毒(例如,单纯疱疹病毒)、痘病毒、杆状病毒、乳头瘤病毒和乳多空病毒(papovavirus)(例如,sv40)。这些载体在本文中称为“病毒载体”。
183、如技术人员将理解的,术语“病毒载体”广泛用于指核酸分子(例如,转移质粒),其包含病毒衍生的核酸元件,其通常促进该核酸分子的转移或整合至细胞基因组中或整合到介导核酸转移的病毒颗粒中。
184、逆转录病毒是基因递送的常见工具(miller,2000,nature.357:00:00 455-460)。在特定的实施方案中,逆转录病毒用于将编码本文所述的car的多核苷酸递送至细胞。如本文所用,术语“逆转录病毒”指将其基因组rna逆转录成线性双链dna拷贝,并随后将其基因组dna共价整合至宿主基因组中的rna病毒。一旦病毒整合至宿主基因组中,其就称为“原病毒”。原病毒充当rna聚合酶ii的模板,并指导编码产生新病毒颗粒所需的结构蛋白和酶的rna分子的表达。
185、适合于用于特定的实施方案的示例性逆转录病毒包括但不限于:moloney鼠白血病病毒(m-mulv)、moloney鼠肉瘤病毒(momsv)、harvey鼠肉瘤病毒(hamusv)、鼠乳腺肿瘤病毒(mumtv)、长臂猿白血病病毒(galv)、猫白血病病毒(flv)、泡沫病毒(spumavirus)、friend鼠白血病病毒、鼠干细胞病毒(mscv)和劳斯肉瘤病毒(rsv)和慢病毒。
186、如本文所用,术语“慢病毒”指一组(或属)复合逆转录病毒。说明性的慢病毒包括但不限于:hiv(人免疫缺陷病毒;包括hiv 1型和hiv 2型);维斯-纳梅迪病毒(visna-maedivirus)(vmv);山羊(caprine)关节炎脑炎病毒(caev);马感染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv);和猿猴免疫缺陷病毒(siv)。在一个实施方案中,基于hiv的载体骨架(即,hiv顺式作用序列元件)是优选的。
187、逆转录病毒载体并且更特定地慢病毒载体可以用于实践特定的实施方案。因此,本文使用的术语“逆转录病毒”或“逆转录病毒载体”分别意在包括“慢病毒”和“慢病毒载体”。
188、除了核酸以外,病毒颗粒通常还包括各种病毒组分,并且有时还包括宿主细胞组分。
189、术语病毒载体可以指能够将核酸转移至细胞中的病毒或病毒颗粒,或者指转移的核酸本身。病毒载体和转移质粒含有主要衍生自病毒的结构和/或功能遗传元件。术语“逆转录病毒载体”指含有主要衍生自逆转录病毒的结构和功能遗传元件或其部分的病毒载体或质粒。术语“慢病毒载体”指含有结构和功能遗传元件或其部分的病毒载体或质粒,包括主要衍生自慢病毒的ltr。术语“杂合载体”指含有逆转录病毒(例如,慢病毒)序列和非慢病毒序列两者的载体、ltr或其他核酸。在一个实施方案中,杂合载体指包含用于逆转录、复制、整合和/或包装的逆转录病毒(例如,慢病毒)序列的载体或转移质粒。
190、在特定的实施方案中,术语“慢病毒载体”和“慢病毒表达载体”可以用于指慢病毒转移质粒和/或感染性慢病毒颗粒。应当理解,在本文提及元件诸如克隆位点、启动子、调控元件、异源核酸等之处,这些元件的序列在慢病毒颗粒中以rna形式存在,并且在dna质粒中以dna形式存在。
191、原病毒的每一端是称为“长末端重复序列”或“ltr”的结构。术语“长末端重复(ltr)”指位于逆转录病毒dna末端的碱基对结构域,其在其天然序列背景下是直接重复并包含u3、r和u5区。ltr通常提供对逆转录病毒基因表达(例如,基因转录物的启动、起始和聚腺苷酸化)以及病毒复制至关重要的功能。ltr含有许多调节信号,包括转录控制元件、多聚腺苷酸化信号以及病毒基因组复制和整合所需的序列。病毒ltr分为三个区,称为u3、r和u5。u3区含有增强子和启动子元件。u5区是引物结合位点和r区之间的序列,并且含有聚腺苷酸化序列。u3和u5区位于r(重复)区两侧。ltr包含u3、r和u5区,并出现在病毒基因组的5’和3’端两端。与5’ltr相邻的是基因组逆转录(trna引物结合位点)和将病毒rna有效包装到颗粒中(psi位点)所必需的序列。
192、如本文所用,术语“包装信号”或“包装序列”指位于逆转录病毒基因组之内的序列,其是将病毒rna插入至病毒衣壳或病毒颗粒中所需要的,参见例如,clever等人,jvirol.1995;69(4):2101-9。一些逆转录病毒载体使用病毒基因组衣壳化所需的最小包装信号(也称为psi[w]序列)。因此,如本文所用,术语“包装序列”、“包装信号”、“psi”和符号“w”用于指在病毒颗粒形成期间逆转录病毒rna链的衣壳化所需要的非编码序列。
193、在各种实施方案中,载体包含修饰的5’ltr和/或3’ltr。ltr中任一个或两个可以包含一个或多个修饰,包括但不限于一个或多个缺失、插入或取代。通常对3’ltr进行修饰以通过导致病毒复制缺陷来提高慢病毒或逆转录病毒系统的安全性。如本文所用,术语“复制缺陷型”指病毒不能够完全、有效复制,使得不能产生感染性病毒粒子(virion)(例如,复制缺陷型慢病毒后代)。术语“复制活性的”指能够复制的野生型病毒或突变病毒,使得病毒的病毒复制能够产生感染性病毒颗粒(例如,复制活性的慢病毒后代)。
194、“自失活”(sin)载体指复制缺陷型载体(例如,逆转录病毒或慢病毒载体),其中已经对右侧(3’)ltr增强子-启动子区(称为u3区)进行修饰(例如,通过缺失或替换)以防止病毒转录超出第一轮的病毒复制。这是因为在病毒复制过程中,右侧(3’)ltr u3区被用作左侧(5’)ltr u3区的模板,并且因此,在没有u3增强子-启动子的情况下,无法制备病毒转录本。在进一步的实施方案中,修饰了3’ltr,使得u5区用例如理想的poly(a)序列替换。应当注意,还包括对ltr的修饰,诸如对3’ltr、5’ltr或3’ltr与5’ltr两者的修饰。
195、通过用异源启动子替换5’ltr的u3区来驱动产生病毒颗粒期间的病毒基因组的转录,这提供了额外的安全性增强。可以使用的异源启动子的实例包括例如病毒猿病毒40(sv40)(例如,早期或晚期)、巨细胞病毒(cmv)(例如,立即早期)、moloney鼠白血病病毒(momlv)、劳斯肉瘤病毒(rsv)和单纯疱疹病毒(hsv)(胸苷激酶)启动子。典型的启动子能够以不依赖tat的方式驱动高水平的转录。这种替换降低了重组以生成复制活性的病毒的可能性,因为病毒产生系统中没有完整的u3序列。在某些实施方案中,异源启动子在控制病毒基因组转录的方式中具有额外的优势。例如,异源启动子可以是诱导型的,使得仅当存在诱导因子时,才会发生全部或部分病毒基因组的转录。诱导因素包括但不限于一种或多种化学化合物或培养宿主细胞的生理条件,诸如温度或ph。
196、根据某些具体实施方案,大部分或全部病毒载骨架序列衍生自慢病毒,例如,hiv-i。然而,应当理解,可以使用或组合许多不同来源的逆转录病毒和/或慢病毒序列,并且可以容纳某些慢病毒序列中的大量取代和改变,而不损害转移载体发挥本文所述的功能的能力。此外,多种慢病毒载体是本领域已知的,参见naldini等人,(science.1996;272(5259):263-7;proc natl acad sci usa.1996;93(21):11382-8;curr opin biotechnol.1998;9(5):457-63);zufferey等人,nat biotechnol.1997;15(9):871-5;dull等人,jvirol.1998;72(11):8463-71;美国专利号6,013,516;和5,994,136,其中许多可适合于产生病毒载体或转移质粒。
197、在各种实施方案中,载体包含可操作地连接至编码本文所述的car或多肽的多核苷酸的启动子。
198、在特定的实施方案中,载体是非整合载体,包括但不限于附加体载体或在染色体外维持的载体。如本文所用,术语“附加体”指在不整合到宿主的染色体dna中并且不会从分裂性宿主细胞中逐渐丢失的情况下,能够进行复制的载体,也意指所述载体在染色体外或附加体上复制。
199、在一些实施方案中,本文所述的载体是病毒载体。
200、在一些实施方案中,本文所述的病毒载体是逆转录病毒载体。
201、在一些实施方案中,本文所述的逆转录病毒载体是慢病毒载体。
202、在一些实施方案中,本文所述的逆转录病毒载体选自由以下组成的组:人免疫缺陷病毒i(hiv-i);人免疫缺陷病毒2(hiv-2)、维斯纳-梅迪病毒(vmv)病毒;山羊关节炎脑炎病毒(caev);马感染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv);和猿猴免疫缺陷病毒。
203、在一些实施方案中,载体包含含有seq id no:17的序列的核酸。在一些实施方案中,载体是包含核酸序列的病毒载体,该核酸序列包含seq id no:17的序列。在一些实施方案中,病毒载体是包含核酸序列的逆转录病毒载体,该核酸序列包含seq id no:17的序列。在一些实施方案中,逆转录病毒载体是包含核酸的慢病毒载体,该核酸包含seq id no:17的序列。在一些实施方案中,包含含有seq id no:17的序列的核酸的逆转录病毒载体,是选自由以下组成的组的逆转录病毒载体:人免疫缺陷病毒i(hiv-i);人免疫缺陷病毒2(hiv-2)、维斯纳-梅迪病毒(vmv)病毒;山羊关节炎脑炎病毒(caev);马感染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv);和猿猴免疫缺陷病毒。
204、控制元件
205、在特定的实施方案中,载体,包括但不限于表达载体和病毒载体,将包括外源控制序列、内源控制序列或异源控制序列,诸如启动子和/或增强子。“内源”控制序列是与基因组中给定基因天然连接的控制序列。“外源”控制序列是通过遗传操作方式(即,分子生物学技术)与基因并置放置的序列,使得该基因的转录由连接的增强子/启动子指导。“异源”控制序列是来自与被遗传操作的细胞不同的物种的外源序列。
206、如本文所用,术语“启动子”指rna聚合酶与之结合的多核苷酸(dna或rna)的识别位点。rna聚合酶启动并转录可操作地连接至启动子的多核苷酸。在特定的实施方案中,在哺乳动物细胞中起作用的启动子包含位于转录起始位点上游大约25至30个碱基处的at富集区和/或转录起点上游70至80个碱基处发现的另一个序列cncaat区,其中n可以是任何核苷酸。
207、术语“增强子”指含有能够提供增强转录的序列的dna片段,并且在一些情况下可以独立于它们相对于另一个控制序列的方向而发挥功能。增强子可以与启动子和/或其他增强子元件合作或附加地发挥功能。术语“启动子/增强子”指含有能够提供启动子功能和增强子功能两者的序列的dna片段。
208、术语“可操作地连接”指并置,其中所描述的组件处于允许它们以其预期方式发挥功能的关系中。在一个实施方案中,该术语指核酸表达控制序列(诸如启动子和/或增强子)和第二多核苷酸序列(例如,感兴趣的多核苷酸)之间的功能性连接,其中表达控制序列指导对应于第二序列的核酸的转录。
209、如本文所用,术语“组成型表达控制序列”指持续地或连续地允许可操作地连接的序列转录的启动子、增强子或启动子/增强子。组成型表达控制序列可以是“普遍存在的”启动子、增强子或启动子/增强子,其允许在多种细胞和组织类型中表达,或者是“细胞特异性的”、“细胞类型特异性的”、“细胞谱系特异性的”或“组织特异性的”启动子、增强子或启动子/增强子,其分别允许在有限的多种细胞和组织类型中表达。
210、适合于用于特定的实施方案的说明性普遍存在的表达控制序列包括但不限于巨细胞病毒(cmv)立即早期启动子、病毒猿病毒40(sv40)(例如,早期或晚期)、moloney鼠白血病病毒(mon4lv)ltr启动子、劳斯肉瘤病毒(rsv)ltr、单纯疱疹病毒(hsv)(胸苷激酶)启动子、来自痘苗病毒的h5、p7.5和p11启动子、延伸因子1-α(ef1a)启动子、早期生长反应1(egr1)、铁蛋白h(ferh)、铁蛋白l(ferl)、3-磷酸甘油醛脱氢酶(gapdh)、真核翻译起始因子4a1(eif4a1)、热休克蛋白70kda蛋白5(hspa5)、热休克蛋白90kdaβ成员1(hsp90b1)、热休克蛋白70kda(hsp70)、β-驱动蛋白(βkin)、人rosa 26基因座(irions等人,naturebiotechnology 25,1477-1482(2007))、泛素c启动子(ubc)、磷酸甘油酸激酶1(pgk)启动子、巨细胞病毒增强子/鸡β-肌动蛋白(cag)启动子、β-肌动蛋白启动子和骨髓增殖性肉瘤病毒增强子、阴性对照区缺失的d1587rev引物结合位点取代(mnd)启动子(challita等人,jvirol.69(2)·748-55(1995))。
211、在一个实施方案中,载体包含pgk启动子。
212、在特定的实施方案中,从t细胞特异性启动子表达包含car的多核苷酸可以是期望的。
213、如本文所用,“条件表达”可以指任何类型的条件表达,包括但不限于诱导型表达;可阻遏的表达;在具有特定生理、生物或疾病状态等的细胞或组织中表达。该定义并不旨在排除细胞类型特异性表达或组织特异性表达。某些实施方案提供了感兴趣的多核苷酸的条件表达,例如,表达是通过使细胞、组织、生物等经受引起多核苷酸表达或引起由感兴趣的多核苷酸编码的多核苷酸表达增加或减少的处理或条件来控制的。
214、诱导型启动子/系统的说明性实例包括但不限于类固醇诱导型启动子,诸如编码糖皮质激素受体或雌激素受体的基因的启动子(通过用相应激素处理可诱导)、金属硫蛋白启动子(通过用各种重金属处理可诱导)、mx-i启动子(通过干扰素可诱导)、“geneswitch”米非司酮可调节系统(sirin等人,2003,gene,323:67)、cumate诱导型基因开关(wo 2002/088346)、四环素依赖性调控系统等。
215、在一些实施方案中,多核苷酸或包含多核苷酸的细胞利用自杀基因(包括诱导型自杀基因)来降低直接毒性和/或不受控制的增殖的风险。在具体实施方案中,自杀基因对于包含多核苷酸或细胞的宿主不是免疫原性的。可以使用的自杀基因的某些实例是caspase-9或caspase-8或胞嘧啶脱氨酶。caspase-9可以使用特定的二聚化化学诱导剂(cid)活化。
216、在某些实施方案中,载体包含引起免疫效应细胞(例如,t细胞)易受到体内阴性选择的影响的基因片段。通过“阴性选择”意指输注的细胞可以由于个体的体内条件的变化而被消除。可阴性选择的表型可以由赋予对施用的药剂例如化合物的敏感性的基因的插入而引起。
217、可阴性选择的基因是本领域已知的,并且尤其包括以下基因:单纯疱疹病毒i型胸苷激酶(hsv-itk)基因(wigler等人,cell i:223,1977),其赋予更昔洛韦敏感性;细胞次黄嘌呤磷酸核糖转移酶(hprt)基因、细胞腺嘌呤磷酸核糖转移酶(aprt)基因和细菌胞嘧啶脱氨酶(mullen等人,proc.natl.acad.sci.usa,1992;89(33))。
218、在一些实施方案中,遗传修饰的免疫效应细胞,诸如t细胞包含多核苷酸,所述多核苷酸进一步包含使得能够体外选择可阴性选择的表型的细胞的阳性标志物。可阳性选择的标志物可以是基因,该基因在被引入宿主细胞中之后表达显性表型,而允许对携带该基因的细胞进行阳性选择。这种类型的基因是本领域已知的,并且尤其包括赋予潮霉素b抗性的潮霉素-b磷酸转移酶基因(hph)、来自tn5的编码抗生素g418抗性的氨基糖苷磷酸转移酶基因(neo或aph)、二氢叶酸还原酶(dhfr)基因、腺苷脱氨酶基因(ada)和多药耐药性(multi-drug resistance)(mdr)基因。
219、优选地,可阳性选择的标志物和可阴性选择的元件相连,使得可阴性选择的元件的丢失也必然伴随着可阳性选择的标志物的丢失。甚至更优选地,将可阳性选择标志物和可阴性选择标志物融合,使得一个的丢失强制性地导致另一个的丢失。产生为赋予上述期望的阳性选择特征和阴性选择特征两者的表达产物多肽的融合多核苷酸的实例,是潮霉素磷酸转移酶胸苷激酶融合基因(hytk)。该基因的表达产生多肽,该多肽赋予潮霉素b抗性以进行体外阳性选择,并且赋予更昔洛韦敏感性以进行体内阴性选择。参见lupton s.d.,等人,mol.and cell.biology,1991;11:3374-3378。此外,在优选的实施方案中,编码car的多核苷酸位于含有融合基因的逆转录病毒载体中,特别是那些赋予潮霉素b抗性以进行体外阳性选择,并且赋予昔洛韦敏感性以进行体内阴性选择的逆转录病毒载体,例如lupton,s.d.等人(1991),同上中描述的hytk逆转录病毒载体。
220、载体产生
221、在特定的实施方案中,细胞(例如,免疫效应细胞)用编码car的逆转录病毒载体(例如,慢病毒载体)转导。例如,用编码本文所述的car的载体转导免疫效应细胞。这些转导的细胞可以引发car介导的细胞毒性应答。
222、“宿主细胞”包括用载体或多核苷酸体内、离体或体外电穿孔的、转染的、感染的或转导的细胞。宿主细胞可以包括用病毒载体转导的包装细胞、生产细胞和细胞。在特定的实施方案中,将用病毒载体转导的宿主细胞施用于需要疗法的受试者。在某些实施方案中,术语“靶细胞”与宿主细胞可互换地使用,并且指期望细胞类型的转染的、感染的或转导的细胞。在优选的实施方案中,靶细胞是t细胞。
223、为了达到合适的病毒滴度,大规模的病毒载体产生通常是必需的。可以通过将转移载体转染至包含例如以下的病毒结构基因和/或附加基因(accessory gene)的包装细胞系中来产生病毒颗粒:gag、poi、env、tat、rev、vif、vpr、vpu、vpx或nef基因或其他逆转录病毒基因。
224、如本文所用,术语“包装载体”指缺乏包装信号并包含编码一个、两个、三个、四个或更多个病毒结构基因和/或附加基因的多核苷酸的表达载体或病毒载体。通常,包装载体包含在包装细胞中,并经由转染、转导或感染引入细胞中。用于转染、转导或感染的方法是本领域技术人员众所周知的。在特定的实施方案中,经由转染、转导或感染将逆转录病毒/慢病毒转移载体引入到包装细胞系中,以生成生产细胞或生产细胞系。在特定的实施方案中,通过包括例如以下的标准方法将包装载体引入到人细胞或人细胞系中:磷酸钙转染法、脂质体转染法或电穿孔法。在一些实施方案中,将包装载体与显性可选择的标志物一起引入细胞中,显性可选择标志物诸如新霉素、潮霉素、嘌呤霉素、杀稻瘟菌素、博莱霉素(zeocin)、胸苷激酶、dhfr、gln合成酶或ada,随后在适当的药物和克隆的分离存在下进行选择。可选择的标志物基因可以与由包装载体编码的基因物理连接,例如,通过ires或自切割病毒肽。
225、如本文所用,术语“包装细胞系”用于指不含有包装信号但的确稳定或瞬时表达正确包装病毒颗粒所必需的病毒结构蛋白和复制酶(例如,gag、pol和env)的细胞系。可以利用任何合适的细胞系来制备包装细胞。通常,细胞是哺乳动物细胞。在特定的实施方案中,用于产生包装细胞系的细胞是人细胞。可以使用的合适的细胞系包括例如cho细胞、bhk细胞、nock细胞、c3h iot1/2细胞、fly细胞、psi2细胞、bosc 23细胞、pa317细胞、wehi细胞、cos细胞、bsc 1细胞、bsc 40细胞、bmt 10细胞、vero细胞、w 138细胞、mrc5细胞、a549细胞、ht1080细胞、hek293细胞、hek293t细胞、b-50细胞、3t3细胞、nih3t3细胞、hepg2细胞、saos-2细胞、huh7细胞、hela细胞、w 163细胞、211细胞和21ia细胞。在优选的实施方案中,包装细胞是hekk293细胞或hek293 t细胞。在另一个优选实施方案中,细胞是hek293 t细胞。
226、如本文所用,术语“生产细胞系”指能够产生重组逆转录病毒颗粒的细胞系,其包含包装细胞系和包含包装信号的转移载体构建体。感染性病毒颗粒和病毒原液的生产可以使用常规技术进行。生产细胞系包括例如,wo2017/089307和wo2017/089308中描述的那些细胞系,其在宿主细胞基因组的单个基因座中包含产生逆转录病毒载体所必需的所有元件。
227、制备病毒原液的方法是本领域已知的并且通过以下说明:例如,y.soneoka等人,(1995)nucl.acids res.23:628-633和n.r.landau等人,(1992)j.virol.66:5110-5113。可以使用常规技术从包装细胞收集感染性病毒颗粒。例如,如本领域已知的,可以通过细胞裂解或收集细胞培养物的上清液来收集感染性颗粒。任选地,如果期望,可以纯化收集的病毒颗粒。合适的纯化技术是本领域技术人员众所周知的。
228、病毒包膜蛋白(env)决定了最终可以被从细胞系生成的重组逆转录病毒感染和转换的宿主细胞的范围。在慢病毒诸如hiv-1、hiv-2、siv、fiv和eiv的情况下,env蛋白包括gp41和gp120。
229、如本文所用,术语“假型”或“假型化”指其病毒包膜蛋白已用具有优选特征的另一种病毒的病毒包膜蛋白取代的病毒。例如,hiv可以用水疱性口炎病毒g蛋白(vsv-g)包膜蛋白假型化,这允许hiv感染更广泛的细胞,因为hiv包膜蛋白(由env基因编码)通常将病毒靶向至cd4+呈递细胞。在优选的实施方案中,慢病毒包膜蛋白用vsv-g假型化。在一个实施方案中,包装细胞产生用vsv-g包膜糖蛋白假型化的重组逆转录病毒,例如,慢病毒。
230、在其他实施方案中,病毒载体可以用来自另一种逆转录病毒或不相关的病毒的包膜蛋白进行假型化。技术人员将理解,本文所述的病毒载体可以用任何合适的包膜蛋白假型化。
231、使用逆转录病毒载体或慢病毒载体通过病毒感染而非通过转染的基因或其他多核苷酸序列的递送被称为“转导”。在一个实施方案中,逆转录病毒载体通过感染和原病毒整合转导至细胞中。在某些实施方案中,如果靶细胞,例如t细胞包含通过使用病毒载体或逆转录病毒载体感染而递送至细胞的基因或其他多核苷酸序列,则该靶细胞,例如该t细胞是“转导的”。在特定的实施方案中,转导的细胞在其细胞基因组中包含由逆转录病毒载体或慢病毒载体递送的一个或多个基因或其他多核苷酸序列。
232、免疫效应细胞
233、在另一个方面,提供了免疫效应细胞,其包含如本文所述的car、多肽、多核苷酸和/或载体。在各种实施方案中,提供了经遗传修饰以表达本文考虑的car的细胞,用于癌症治疗。如本文所用,术语“遗传工程化的”或“遗传修饰的”指将dna或rna形式的额外的遗传物质添加到细胞中的总遗传物质中。术语“遗传修饰的细胞”、“修饰细胞”和“重定向细胞”可互换地使用。如本文所用,术语“基因疗法”指将dna或rna形式的额外的遗传物质引入至细胞中的总遗传物质中,以恢复、纠正或修饰基因的表达,或用于表达治疗性多肽的目的,例如,car。
234、在特定的实施方案中,将本文考虑的car引入并表达于免疫效应细胞中,从而将免疫效应细胞的特异性重定向至感兴趣的靶抗原,例如,位于细胞-细胞连接之内的细胞连接蛋白,诸如密蛋白家族的成员,特别是密蛋白3。
235、“免疫效应细胞”是具有一种或多种效应功能(例如,细胞毒性细胞杀伤活性、分泌细胞因子、诱导adcc和/或cdc)的免疫系统的任何细胞。本文考虑的示例性免疫效应细胞是t淋巴细胞,特别是细胞毒性t细胞(ctl;cd8+t细胞)、肿瘤浸润淋巴细胞(til)和辅助t细胞(htl;cd4+ t细胞)。在一个实施方式中,免疫效应细胞包括自然杀伤(nk)细胞。在一个实施方式中,免疫效应细胞包括自然杀伤t细胞。在另一个实施方案中,免疫效应细胞包括巨噬细胞。免疫效应细胞可以是自体的/自生的(autologous/autogeneic)(“自身的”)或非自体的(“非自身的”),例如,同种异体的、同基因的或异种的。
236、如本文所用,“自体的”指来自相同受试者的细胞。
237、如本文所用,“同种异体的”指与比较中的细胞在遗传上不同的相同物种的细胞。
238、如本文所用,“同基因的”指与比较中的细胞在遗传上相同的不同受试者的细胞。
239、如本文所用,“异种的”指与比较中的细胞不同物种的细胞。
240、在优选的实施方案中,细胞,例如,免疫效应细胞,是同种异体的。
241、与本文考虑的car使用的说明性的免疫效应细胞包括t淋巴细胞。术语“t细胞”或“t淋巴细胞”是本领域公认的并且旨在包括胸腺细胞、未成熟t淋巴细胞、成熟t淋巴细胞、静息t淋巴细胞或活化t淋巴细胞。t细胞可以是辅助t(th)细胞,例如辅助t细胞i(th1)或辅助t细胞2(th2)。t细胞可以是辅助t细胞(htl;cd4+ t细胞)、细胞毒性t细胞(ctl;cd8+ t细胞)、cd4+cd8+ t细胞、cd4-cd8-t细胞或任何其他t细胞亚群。适合于用于特定实施方案的其他示例性t细胞群体包括初始t细胞和记忆t细胞。
242、在一些实施方案中,免疫效应细胞选自由t淋巴细胞、自然杀伤t淋巴细胞(nkt)细胞、巨噬细胞和自然杀伤(nk)细胞组成的组。
243、在一个实施方案中,免疫效应细胞是细胞毒性t淋巴细胞(cd8+)。
244、如技术人员将理解的,其他细胞也可以与本文所述的car用作免疫效应细胞。特别地,免疫效应细胞还包括nk细胞、nkt细胞、中性粒细胞和巨噬细胞。免疫效应细胞还包括效应细胞的祖细胞,其中此类祖细胞可被体内或体外诱导而分化成免疫效应细胞。因此,在特定的实施方案中,免疫效应细胞包括免疫效应细胞的祖细胞,诸如衍生自脐带血、骨髓或动员的外周血的cd34细胞群体之内含有的造血干细胞(hsc),其在受试者中施用后分化成成熟免疫效应细胞,或可以被体外诱导而分化成成熟免疫效应细胞。
245、如本文所用,经遗传工程化以包含例如密蛋白3特异性car的免疫效应细胞可以称为“抗原特异性重定向的免疫效应细胞”或“ag特异性重定向的免疫效应细胞”。
246、在特定的实施方案中,提供了用于制备或生成表达本文所述的car的免疫效应细胞的方法。在各种实施方案中,此类方法包括将如本文所述的多核苷酸和/或载体引入至免疫效应细胞中。在一个实施方案中,该方法包括转染或转导分离自个体的免疫效应细胞,使得免疫效应细胞表达本文考虑的一种或多种car。在某些实施方案中,免疫效应细胞分离自个体,并在没有进一步体外操作的情况下进行遗传修饰。然后可以将此类细胞直接重新施用至个体中。在进一步的实施方案中,首先活化免疫效应细胞并刺激其以体外增殖,然后进行遗传修饰以表达car。在这方面,可以在遗传修饰(即,转导或转染以表达本文考虑的car)之前和/或之后培养免疫效应细胞。因此,在某些实施方案中,可以通过使细胞与结合cd3的抗体或抗原结合片段和/或结合cd28的抗体或抗原结合片段接触,来刺激和诱导免疫效应细胞以进行增殖;从而生成免疫效应细胞群体。在进一步的实施方案中,生成本文考虑的免疫效应细胞的方法包括通过使细胞与结合cd3的抗体或抗原结合片段以及结合cd28的抗体或抗原结合片段接触,来刺激免疫效应细胞和诱导细胞以进行增殖;从而生成免疫效应细胞群体。
247、在特定的实施方案中,在对本文所述的免疫效应细胞进行体外操作或遗传修饰之前,从受试者获得免疫效应细胞。在特定的实施方案中,car修饰的免疫效应细胞包含t细胞。
248、在特定的实施方案中,可以使用本文考虑的方法直接对外周血单核细胞(pbmc)进行遗传修饰以表达car。在某些实施方案中,在分离pbmc之后,进一步分离t淋巴细胞,并且在某些实施方案中,在遗传修饰和/或扩增之前或之后,细胞毒性t淋巴细胞和辅助t淋巴细胞都可以被分选成初始t细胞亚群、记忆t细胞亚群和效应t细胞亚群。
249、免疫效应细胞,诸如t细胞,可以在使用已知方法分离后进行遗传修饰,或可以体外活化和扩增(或在祖细胞的情况下,分化)免疫效应细胞,然后进行遗传修饰。在特定的实施方案中,免疫效应细胞,诸如t细胞,用本文考虑的car进行遗传修饰(例如,用包含编码car的核酸的病毒载体转导),然后进行体外活化和扩增。在各种实施方案中,可以在遗传修饰之前或之后活化和扩增t细胞以表达car。
250、在特定的实施方案中,用于治疗癌症的修饰的免疫效应细胞群体包含如本文公开的car。例如,从被诊断患有癌症的患者(自体供体)获得的外周血单核细胞(pbmc)制备修饰的免疫效应细胞群体。pbmc形成异质t淋巴细胞群体,其可以是cd4+、cd8+、或cd4+和cd8+。
251、pbmc还可以包括其他细胞毒性淋巴细胞,诸如nk细胞或nkt细胞。可以将携带本文所述的car的编码序列的载体引入至人供体t细胞群体、nk细胞群体或nkt细胞群体中。在特定的实施方案中,除了使用抗cd3抗体和/或抗cd28抗体和il-2或如本文别处所述的本领域已知的任何其他方法进行细胞活化之外,还可以使用流式细胞术对携带表达载体的成功转导的t细胞进行分选,以分离cd3阳性t细胞,然后进行进一步增殖以增加这些表达car蛋白的t细胞的数量。
252、为了用于人受试者的储存和/或制备,使用标准程序用于冷冻保存表达car蛋白的t细胞。
253、在进一步的实施方案中,例如一种、两种、三种、四种、五种或更多种不同的载体的混合物可用于对免疫效应细胞的供体群体进行遗传修饰,其中每种载体编码如本文考虑的不同的嵌合抗原受体蛋白。所得的修饰的免疫效应细胞形成修饰的细胞的混合群体,其中一部分修饰的细胞表达一种以上不同的car蛋白。
254、t细胞制备方法
255、制备用于人疗法的t细胞的方法是本领域已知的。在优选的实施方案中,通过本文考虑的方法制备的t细胞提供改进的过继免疫疗法组合物。不希望受任何特定理论的束缚,据信通过本文考虑的特定的实施方案中的方法制备的t细胞组合物具有优异的特性,包括增加的存活、在相对不存在分化的情况下的扩增、体内持久性和优异的抗耗竭特性。例如,经过修饰以表达抗密蛋白3car的t细胞对可接近的密蛋白3展示出较低的结合动力学,并且在存在可接近的密蛋白3靶标的情况下,具有较低的体内耗竭潜力。抗密蛋白3car-t细胞的低耗竭的倾向保留了其效应功能,导致抑制性受体的低持续表达,并保持功能性效应细胞或记忆t细胞的转录状态。耗竭不是car-t疗法期望的特征,因为它会防止对感染和肿瘤的最佳控制。
256、在一个实施方案中,通过用包含本文考虑的抗密蛋白3car的病毒载体转导t细胞来修饰t细胞。在没有抗原的情况下,抗密蛋白3car-t细胞显示处低水平的基础car活化和干扰素-γ(ifnγ)分泌,这是car-t疗法的期望的属性。car对抗原非依赖性(基底)信号传导的倾向可能表明自我聚集导致抗原非依赖性car活化,反过来可能引起导致治疗效力丧失的早期car耗竭(ajina和maher,2018以及long等人,2015a)。car-t细胞的基底活化可以通过活化标志物cd69、耗竭标志物pd1和tim3的水平、cd3ζ胞内信号传导结构域的磷酸化、以及car-t细胞在不存在抗原的情况下分泌ifnγ的能力来确定。人源化抗密蛋白3car-t细胞在体外显示出与未转导细胞相似的ifnγ分泌水平、活化标志物和耗竭标志物的表达水平以及强直性cd3ζ信号传导的水平,以及显示出与用阳性对照car转导的car-t细胞相比较低的水平。
257、在一个实施方案中,通过用包含本文考虑的抗密蛋白3car的病毒载体转导t细胞来修饰t细胞,其需要更高的靶阈值来活化使其成为“更安全”的car。已经表明,具有高亲和力的car可以导致并行的健康组织靶向,引起中靶/脱靶、脱肿瘤毒性(johnson等人,2015;park等人,2017;watanabe等人,2018)。
258、药物组合物
259、本文所述的免疫效应细胞可以并入到用于治疗本文所述的人疾病的药物组合物中。在一个实施方案中,药物组合物包含免疫效应细胞,其任选地与一种或多种药学上可接受的载剂和/或赋形剂组合。
260、此类组合物包含可接受的药物实践已知的和所要求的药学上可接受的载剂,参见例如,remington’s pharmaceutical sciences,第16版(1980)mack出版公司。
261、药物组合物可以通过注射或连续输注(实例包括但不限于静脉内、腹膜内、皮内、皮下、肌肉内、眼内和门静脉内)进行施用。在一个实施方案中,该组合物适合于用于静脉内施用。
262、遗传修饰的治疗性细胞的“治疗有效量”可以根据诸如以下的因素而变化:个体的疾病状态、年龄、性别和体重,以及干细胞和祖细胞在个体中引发期望应答的能力。治疗有效量还是一种量,其中病毒或转导的治疗性细胞的任何毒性效应或有害效应被治疗有益效应所超过。术语“治疗有效量”包括对“治疗”受试者(例如,患者)有效的量。当表明治疗量时,待施用的组合物的精确量可以由医生考虑到患者(受试者)的年龄、体重、肿瘤大小、感染或转移程度以及病况中的个体差异来确定。一般而言,包含本文所述的t细胞的药物组合物可以以102至1010个细胞/kg体重,优选地105至106个细胞/kg体重,包括这些范围之内的所有整数值的剂量施用。细胞的数量将取决于该组合物打算用于的最终用途以及其中包含的细胞的类型。对于本文提供的用途,细胞的体积通常为一升或更少,可以是500ml或更少,甚至250ml或100ml或更少。因此,期望细胞的密度通常大于106个细胞/ml,例如,大于106、107、108或109个细胞/ml。
263、临床相关的免疫细胞数量可以分配到多次输注中,累计等于或超过105、106、107、108、109、1010、1011或1012个细胞。在一些实施方案中,特别是因为所有输注的细胞将被重定向至特定的靶抗原,可以施用在106个/千克(106至1011每个患者)范围内的较少数量的细胞。在特定的实施方案中,可以施用1x 107和9x 107个之间的car-t细胞。表达car的细胞组合物可以以这些范围之内的剂量多次施用。例如,表达car的细胞组合物可以每7天施用一次。替代性地,表达car的细胞组合物可以作为单剂量进行施用。对于进行疗法的患者,细胞可以是同种异体的、同基因的、异种的或自体的。如果期望,治疗还可以包括施用如本文所述的有丝分裂原(mitogen)(例如,pha)或淋巴因子、细胞因子和/或趋化因子(例如,ifnγil-2、il-12、tnfα、il-18和tnfβ、gm-csf、il-4、il-13、flt3-l、rantes、mip1α等)以增强诱导免疫应答。
264、通常,包含如本文所述活化和扩增的细胞的组合物可以用于治疗和预防免疫受损个体中出现的疾病。特别地,包含本文考虑的car修饰的t细胞的组合物用于治疗癌症。在特定的实施方案中,car修饰的t细胞可以单独施用,或者作为与载剂、稀释剂、赋形剂和/或其他组分(诸如il-2或其他细胞因子)或细胞群体组合的药物组合物施用。在特定的实施方案中,药物组合物包含一定量的遗传修饰的t细胞,这些t细胞与一种或多种药学上或生理学上可接受的载剂、稀释剂或赋形剂组合。
265、包含表达car的免疫效应细胞群体诸如t细胞的药物组合物,可以包含缓冲剂,诸如中性缓冲盐水、磷酸盐缓冲盐水等等;碳水化合物,诸如葡萄糖、甘露糖、蔗糖或右旋糖酐(dextran)、甘露醇;蛋白质;多肽或氨基酸,诸如甘氨酸;抗氧化剂;螯合剂,诸如edta或谷胱甘肽;佐剂(例如,氢氧化铝);和防腐剂。在特定的实施方案中,组合物优选配制用于肠胃外施用,例如,血管内(静脉内或动脉内)、腹膜内或肌内施用。
266、液体药物组合物,无论其是溶液、混悬液或其他类似形式,可以包括以下一种或多种:无菌稀释剂,诸如注射用水、盐水溶液,优选生理盐水、林格氏溶液、等渗氯化钠,固定油,诸如充当溶剂或悬浮介质的合成甘油单酯或甘油二酯、聚乙二醇、甘油、丙二醇或其他溶剂;抗菌剂,诸如苯甲醇或对羟基苯甲酸甲酯;抗氧化剂,诸如抗坏血酸或亚硫酸氢钠;螯合剂,诸如乙二胺四乙酸;缓冲剂,诸如乙酸盐、柠檬酸盐或磷酸盐以及用于调整张力的药剂诸如氯化钠或右旋糖。肠胃外制剂可以封装在由玻璃或塑料制成的安瓿、一次性注射器或多剂量小瓶中。可注射药物组合物优选是无菌的。
267、在一个实施方案中,本文考虑的t细胞组合物配制于药学上可接受的细胞培养基中。此类组合物适合用于施用至人受试者。在特定的实施方案中,药学上可接受的细胞培养基是无血清培养基。
268、在另一个优选的实施方案中,将本文考虑的包含t细胞的组合物配制在包含冷冻保存介质的溶液中。例如,具有冷冻保存剂的冷冻保存介质可以用于维持解冻后的高细胞活力结果。在特定的组合物中使用的冷冻保存介质的说明性实例包括但不限于cryostorcs10、cryostor cs5和cryostor cs2。
269、在特定的实施方案中,组合物包含有效量的单独的或与一种或多种治疗剂组合的表达car的免疫效应细胞。因此,表达car的免疫效应细胞组合物可以单独施用或与其他已知的癌症治疗组合施用,其他已知的癌症治疗诸如放射疗法、化学疗法、移植、免疫疗法、激素疗法、光动力疗法等。该组合物还可以与抗生素组合施用。在本领域中,此类治疗剂可以被接受作为用于本文所述的特定疾病状态,诸如特定癌症的标准治疗。考虑的示例性治疗剂包括细胞因子、生长因子、类固醇、nsaid、dmard、抗炎药、化疗药物、放射治疗剂、治疗抗体或其他活性剂和辅助剂。
270、在某些实施方案中,包含本文公开的表达car的免疫效应细胞的组合物可以与本领域已知的任何数量的化疗剂结合施用。
271、多种其他治疗剂可以与本文所述的组合物结合使用。在一个实施方案中,包含表达car的免疫效应细胞的组合物与抗炎剂一起施用。抗炎剂或药物是本领域已知的。
272、在某些实施方案中,本文所述的组合物与细胞因子结合施用。如本文所用,“细胞因子”意指由一个细胞群体释放的蛋白质的通用术语,其作为细胞间介质作用于另一细胞。此类细胞因子的实例是本领域已知的。
273、在进一步的实施方案中,本文考虑的组合物和car与其他car或表达car的细胞和/或组合物结合施用。例如,抗密蛋白3car或组合物可以与抗细胞表面相关粘蛋白1(muc1)car或表达car的细胞组合物一起施用。在一个实施方案中,抗muc1 car靶向异常糖基化的muc1蛋白(“ag-muc1”;例如,tnmuc1、stnmuc1等),诸如癌细胞表达的异常糖基化的muc1蛋白。替代性地,本文考虑的抗密蛋白3car或组合物可以与抗纽约食管鳞状细胞癌1(ny-eso-1)t细胞受体(tcr)或表达tcr的细胞组合物一起施用。
274、药物组合物可以包含在试剂盒中,其含有表达car的免疫效应细胞以及其他药物,任选地和/或以及使用说明书。为了方便起见,试剂盒可以包含预定量的试剂以及使用说明书。试剂盒还可以包括用于施用该药物组合物的装置。
275、术语“个体”、“受试者”和“患者”在本文中可互换地使用,并且是指展示出可以用本文别处考虑的car、基因治疗载体、基于细胞的疗法以及方法来治疗的疾病、病症或病况的症状的任何动物。在优选的实施方案中,受试者包括展示出可以用本文别处考虑的car、基因治疗载体、基于细胞的治疗剂和方法来治疗的与癌症相关的疾病、病症或病况的症状的任何动物。合适的受试者(例如,患者)包括实验动物(诸如小鼠、大鼠、兔或豚鼠)、农场动物以及家养动物或宠物(诸如猫或狗)。包括了非人灵长类,并且优选地包括了人患者。典型的受试者包括已被诊断患有或在患有表达可接近的密蛋白3蛋白的癌的风险下的人患者。因此,在一个实施方案中,受试者是哺乳动物,诸如灵长类,例如狨猴或猴。在另一个实施方案中,受试者是人。在进一步的实施方案中,受试者是小鼠。
276、如本文所用,术语“患者”指已被诊断患有可以用本文别处公开的car、基因治疗载体、基于细胞的治疗剂和方法治疗的特定的疾病、病症或病况的受试者。
277、如本文所用,“治疗(treatment)”或“治疗(treating)”包括对疾病或病理病况的症状或病理学的任何有益或期望的效果,并且可以包括所治疗的疾病或病况的一种或多种可测量标志物的甚至最小程度的减少。治疗可以任选地包括减轻疾病或病况,或者延迟疾病或病况的进展,例如,延缓肿瘤长出。“治疗”不是必定表明疾病或病况或其相关联的症状的完全根除或治愈。
278、如本文所用,“预防(prevent)”和相似的词语诸如“预防(prevented)”、“预防(preventing)”等表明用于预防、抑制疾病或病况或减少疾病或病况发生或复发的可能性的方法。它还指延迟疾病或病况的起始或复发,或延迟疾病或病况的症状的发生或复发。如本文所用,“预防(prevention)”和相似的词语还包括在疾病或病况起始或复发之前降低疾病或病况的强度、效应、症状和/或负担。
279、癌
280、如本文所用,术语“癌”、“赘生物”和“肿瘤”可互换地使用并且以单数或者复数形式使用,指已经进行恶性转化或已经进行了导致异常或不受调节的生长或过度增殖的细胞变化的细胞。此类变化或恶性转化通常使此类细胞对于宿主生物体是病理性的,因此也旨在包括处于或可以变为病理性并且需要或可以从干预中受益的初癌(precancer)或癌前期(pre-cancerous)细胞。原发性癌细胞(即从恶性转化部位附近获得的细胞)可以通过成熟的技术(诸如组织学检查)容易地与非癌细胞区分开来。例如,此类组织学检查可以通过鉴定被破坏的或受损的细胞-细胞连接(诸如紧密连接)来区分癌细胞与非癌细胞。
281、因此,在特定的实施方案中,癌细胞包含被破坏的或受损的细胞-细胞连接。在进一步的实施方案中,癌细胞包含被破坏的或受损的紧密连接。在此类实施方案中,位于细胞-细胞连接(诸如紧密连接)之内的细胞连接蛋白错误定位并且变得可被本文所述的car和表达car的细胞接近而结合和/或可被本文所述的car和表达car的细胞用于结合。在其他实施方案中,癌细胞在表面上包含错误定位的细胞连接蛋白,诸如位于细胞-细胞连接中的那些。因此,在一些实施方案中,癌细胞包含暴露于表面的错误定位的细胞连接蛋白。
282、如本文所用,癌细胞的定义不仅包括原发性癌细胞,还包括衍生自癌细胞祖先的任何细胞。这包括转移的癌细胞,以及衍生自癌细胞的体外培养物和细胞系。当提及通常表现为实体瘤的癌时,“临床上可检测的”肿瘤指基于肿瘤团块可检测到的肿瘤;例如通过程序,诸如cat扫描、mr成像、x射线、超声或触诊,和/或因为从患者获得的样品中的一种或多种癌特异性抗原的表达而可检测到的肿瘤。换句话说,本文的术语包括任何阶段的细胞、赘生物、癌和肿瘤,包括临床医生称为初癌、肿瘤、原位生长以及晚期转移性生长的那些。
283、如本文所用,术语“治疗(treating)”、“治疗(treatment)”及其派生词意指治疗性疗法。就特定的病况而言,治疗指:(1)改善病况或病况的一种或多种生物学临床表现;(2)干扰(a)生物级联中导致或负责该病况的一个或多个点,或(b)该病况的一种或多种生物学表现;(3)减轻与病况相关联的一种或多种症状、效应或副作用,或与病况或其治疗相关联的一种或多种症状、效应或副作用;或(4)减缓病况或病况的一种或多种生物学临床表现的进展。
284、如本文所用,“预防”意指预防性施用药物(诸如药剂),以基本上减弱病况或其生物学临床表现的可能性或严重性,或延迟此类病况或其生物学临床表现的起始。本领域技术人员将理解,“预防”不是绝对的术语。例如,当受试者被认为在发展癌症的高风险下时,诸如当受试者具有强癌症家族史时,或当受试者已经暴露于致癌物时,预防性治疗是适当的。
285、如本文所用,术语“恶性”指其中一组肿瘤细胞表展示出不受控制的生长(例如,超出正常范围的分裂)、侵袭(例如,侵入和破坏相邻组织)和转移(例如,通过淋巴或血液扩散到身体的其他位置)中的一种或多种的癌症。
286、“癌细胞”指癌性生长或癌性组织的单个细胞。癌细胞包括固体癌和液体癌两者。“肿瘤”或“肿瘤细胞”通常指由细胞异常生长形成的肿胀或病变,其可以是良性的、恶性前的或恶性的。大多数癌形成肿瘤,但液体癌例如白血病,不必然形成肿瘤。对于那些形成肿瘤的癌,术语“癌(细胞)”和“肿瘤(细胞)”可互换地使用。个体中肿瘤的数量就是“肿瘤负荷”,可以测量为肿瘤的数量、体积或重量。
287、在一个实施方案中,靶细胞(例如,癌细胞)表达包含抗原或表位的细胞连接蛋白,该抗原或表位还在健康的、非癌性细胞上表达,并且在一些情况下以与健康的、非癌性细胞相同的水平表达。在进一步的实施方案中,所述细胞连接蛋白的抗原或表位仅当由癌细胞表达时才可用和/或可接近。因此,在特定的实施方案中,当由健康的、非癌性细胞表达时,所述细胞连接蛋白的抗原或表位不可用或不可接近(例如,其是“隐藏的”)。
288、在特定的实施方案中,癌包含或特征在于密蛋白3在紧密连接外部的错误定位和/或使得密蛋白3可被本文所述的car接近而结合的紧密连接的破坏。
289、在一个实施方案中,靶细胞是骨的细胞、骨细胞、成骨细胞、脂肪细胞、软骨细胞、成软骨细胞、肌肉细胞、骨骼肌细胞、成肌细胞、肌细胞、平滑肌细胞、膀胱细胞、骨髓细胞、中枢神经系统(cns))细胞、周围神经系统(pns)细胞、神经胶质细胞、星形胶质细胞、神经元、色素细胞、上皮细胞、皮肤细胞、内皮细胞、血管内皮细胞、乳腺细胞、结肠细胞、食道细胞、胃肠道细胞、胃细胞、结肠细胞、头细胞、颈细胞、牙龈细胞、舌细胞、肾细胞、肝细胞、肺细胞、鼻咽细胞、卵巢细胞、滤泡细胞、宫颈细胞、阴道细胞、子宫细胞、胰腺细胞、胰腺实质细胞、胰腺导管细胞、胰岛细胞、前列腺细胞、阴茎细胞、性腺细胞、睾丸细胞、造血细胞、淋巴细胞或髓系细胞。
290、在一个实施方案中,靶细胞表达密蛋白3蛋白。在一个实施方案中,靶细胞是表达密蛋白3蛋白的造血细胞、食道细胞、肺细胞、卵巢细胞、子宫颈细胞、胰腺细胞、胆囊或胆管的细胞、胃细胞、结肠细胞、乳腺细胞、杯状细胞、肠上皮细胞、干细胞、内皮细胞、上皮细胞或任何细胞。在特定的实施方案中,靶细胞是内皮细胞或上皮细胞。
291、可以通过特定的实施方案中考虑的组合物和方法靶向的细胞的示例性实例包括但不限于以下实体癌的细胞:肾上腺癌、肾上腺皮质癌、肛门癌、阑尾癌、星形细胞瘤、非典型畸胎瘤/横纹肌样瘤、基底细胞癌、胆管癌、膀胱癌、骨癌、脑/cns癌、乳腺癌、支气管肿瘤、心脏肿瘤、宫颈癌、胆管癌、软骨肉瘤、脊索瘤、结肠癌、结直肠癌、颅咽管瘤、导管原位癌(dcis)、子宫内膜癌、室管膜瘤、食道癌、鼻腔神经胶质瘤(esthesioneuroblastoma)、尤文氏肉瘤、颅外生殖细胞肿瘤、性腺外生殖细胞肿瘤、眼癌、输卵管癌、纤维组织肉瘤(fibroushistiosarcoma)、纤维肉瘤、胆囊癌、胃癌、胃肠道类癌肿瘤、胃肠道间质瘤(gist)、生殖细胞肿瘤、神经胶质瘤、胶质母细胞瘤、头颈癌、血管母细胞瘤、肝细胞癌、下咽癌、眼内黑色素瘤、卡波西肉瘤、肾癌、喉癌、平滑肌肉瘤、唇癌、脂肪肉瘤、肝癌、肺癌、非小细胞肺癌、肺类癌、恶性间皮瘤、髓样癌、髓母细胞瘤、脑膜瘤(menangioma)、黑色素瘤、梅克尔细胞癌、中线束癌、口腔癌、粘液肉瘤、骨髓增生异常综合征、骨髓增生性肿瘤、鼻腔和鼻窦癌、鼻咽癌、神经母细胞瘤、少突神经胶质瘤、口癌(oral cancer)、口腔癌(oral cavity cancer)、口咽癌、骨肉瘤、卵巢癌、胰腺癌、胰岛细胞肿瘤、乳头状癌、副神经节瘤、甲状旁腺癌、阴茎癌、咽癌、嗜铬细胞瘤、松果体瘤、垂体瘤、胸膜肺母细胞瘤、原发性腹膜癌、前列腺癌、直肠癌、视网膜母细胞瘤、肾细胞癌、肾盂和输尿管癌、横纹肌肉瘤、唾液腺癌、皮脂腺癌、皮肤癌、软组织肉瘤、鳞状细胞癌、小细胞肺癌、小肠癌、胃癌、汗腺癌、滑膜瘤、睾丸癌、喉癌、胸腺癌、甲状腺癌、尿道癌、子宫癌、子宫肉瘤、阴道癌、血管癌、外阴癌和肾母细胞瘤。
292、在另一个实施方案中,细胞是表达可接近的密蛋白3蛋白的实体癌细胞。在又一个实施方案中,癌是实体癌。可以用本文所述的car、表达car的细胞和组合物来预防、治疗或改善的表达可接近的密蛋白3蛋白的示例性实体癌细胞包括但不限于:食道癌细胞、肺癌(例如,非小细胞肺癌(nsclc))细胞、卵巢癌细胞、宫颈癌细胞、胰腺癌细胞、胆管癌细胞、胃癌细胞、结肠癌细胞、结直肠癌细胞、膀胱癌细胞、肾癌细胞和乳腺癌(例如,三阴性乳腺癌(tnbc))细胞。
293、在某些实施方案中,癌细胞是结直肠癌、胰腺癌、乳腺癌、卵巢癌或肺癌。在一些实施方案中,乳腺癌是三阴性乳腺癌(tnbc)。在一些实施方案中,肺癌是非小细胞肺癌(nsclc)。因此,在进一步的实施方案中,癌选自结肠直肠癌、胰腺癌、三阴性乳腺癌(tnbc)、卵巢癌和非小细胞肺癌(nsclc)。
294、在其他实施方案中,细胞是上皮细胞。在又一个其他的实施方案中,癌是上皮癌。示例性上皮癌包括但不限于实体癌,诸如上文描述的那些。
295、可以用本文考虑的car、表达car的细胞和组合物预防、治疗或改善的液体癌或血液癌的说明性实例包括但不限于:白血病、淋巴瘤和多发性骨髓瘤。可以被本文考虑的car和组合物靶向的细胞的示例性实例包括但不限于以下白血病的细胞:急性淋巴细胞白血病(all)、t细胞急性淋巴细胞白血病、急性髓性白血病(aml)、成髓细胞白血病、早幼粒细胞白血病、粒单核细胞白血病、单核细胞白血病、红白血病、毛细胞白血病(hcl)、慢性淋巴细胞白血病(cll)、慢性髓性白血病(cml)、慢性粒单核细胞白血病(cnnl)和真性红细胞增多症。
296、治疗方法和增加细胞毒性
297、本文考虑的car分子旨在用于本文所述的治疗癌症的组合物、细胞和方法中,从而预防、治疗或改善与所述癌症相关联的至少一种症状。在特定的实施方案中,本发明涉及使用遗传修饰的免疫效应细胞的癌的改进的细胞疗法,该癌表达仅在所述癌中是可接近而结合car和/或可用于结合car的表位。
298、本文考虑的过继细胞疗法的改进的组合物和方法提供了可以容易地扩增、展示出长期体内持久性、并表现出对表达本文所述表位的癌细胞的抗原依赖性细胞毒性的遗传修饰的免疫效应细胞。
299、术语“个体”、“受试者”和“患者”在本文中可互换地使用。在一个实施方案中,受试者是动物。在另一个实施方案中,受试者是哺乳动物,诸如灵长类,例如狨猴或猴。在另一个实施方案中,受试者是人。
300、因此,在其他方面,提供了用本文所述的car、多肽、载体、免疫效应细胞和组合物治疗癌症的方法。本文考虑的遗传修饰的免疫效应细胞提供了过继免疫疗法的改进方法,其用于预防、治疗和改善表达可接近的密蛋白3蛋白的癌,或用于预防、治疗或改善与表达可接近的密蛋白3蛋白质的癌相关联的至少一种症状。
301、在各种实施方案中,本文考虑的遗传修饰的免疫效应细胞提供了改进的过继免疫疗法,其用于在患有癌症的受试者中增加对癌细胞的细胞毒性,或用于在患有癌症的受试者中减少癌细胞数量。在一些实施方案中,癌或癌细胞表达密蛋白3蛋白,其可被本文所述的car和表达car的细胞接近而结合和/或可被本文所述的car和表达car的细胞用于结合。
302、在特定的实施方案中,通过用本文考虑的car对原代免疫效应细胞进行遗传修饰,将原代免疫效应细胞的特异性重定向至表达可接近的密蛋白3蛋白的细胞,例如癌细胞。在各种实施方案中,病毒载体用于用编码包含密蛋白3结合蛋白的car的特定多核苷酸对免疫效应细胞进行遗传修饰,该密蛋白3结合蛋白例如,抗密蛋白3抗体或抗原结合结构域域;铰链结构域;跨膜(tm)结构域;一个或多个共刺激结构域;以及一个或多个胞内信号传导结构域。
303、在一个实施方案中,提供了一种细胞疗法,其中对t细胞进行遗传修饰以表达本文所述的car,从而提供car-t细胞,其中将car-t细胞输注至有此需要的接受者或受试者。输注的细胞能够杀伤接受者体内的导致疾病的细胞。与抗体疗法不同,car-t细胞能够体内复制,这导致可以导致持续的癌症疗法的长期持久性。此外,与如上文所述的抗体疗法相比,本文考虑的car-t细胞疗法可以表现出增加的敏感性和选择性。例如,包含含有包含本文所述的抗原/表位结合结构域的胞外结构域的car可以表现出比包含相同抗原/表位结合结构域的抗体更高的敏感性和选择性,使得能够检测到表达car的细胞的活化(即,当抗体或抗原/表位结合结构域包含在car中并因此由细胞以不可溶的细胞形式表达时),而通过直接可视化方法没有检测到可溶性抗体的结合。
304、在一个实施方案中,car-t细胞可以进行稳健的体内t细胞扩增并且可以持续延长量的时间。在另一个实施方案中,car-t细胞演变成特异性记忆t细胞,其可以被重新活化以抑制任何额外的肿瘤形成或生长。
305、在一些实施方案中,包含含有本文所考虑的car的免疫效应细胞的组合物,用于治疗与表达可接近的密蛋白3蛋白的癌细胞或癌干细胞相关联的病况。
306、如本文所用,短语“改善至少一种症状”指减轻受试者正在治疗的疾病或病况的一种或多种症状。在特定的实施方案中,该正在治疗的疾病或病况是癌症,其中改善的一种或多种症状包括但不限于虚弱、疲劳、气短、容易擦伤和出血、频繁感染、淋巴结肿大、肿胀、或腹部疼痛(由于增大的腹部器官)、骨或关节疼痛、骨折、意外体重减轻、食欲不振、盗汗、持续轻度发烧和排尿减少(由于受损的肾功能)。
307、本文所用的术语“增强”、“促进”、“增加”或“扩大”通常指本文考虑的组合物(例如,编码car的遗传修饰的t细胞或载体),与由对照分子/组合物引起的或在对照条件下的响应相比,产生、引发或引起更大的生理响应(即,下游效应)的能力。可测量的生理响应可包括t细胞扩增、活化、持久性的增加和/或癌细胞杀伤能力的增加,以及从本领域的理解和本文的描述显而易见的其他。“增加”或“增强”量通常是“统计学显著”的量,并且可以包括由对照组合物产生的或对对照细胞谱系的响应的1.1、1.2、1.5、2、3、4、5、6、7、8、9、10、15、20、30、50、100、200、500或更多倍的增加。例如,此类增加或增强的量可以与以下进行比较:观察到的对表达不可接近/不可用的密蛋白3蛋白和/或包含完整或未受损的(例如,未被破坏的)细胞与细胞的连接的健康、非癌性细胞的响应。因此,在一些实施方案中,观察到此类增加或增强的响应是针对表达可接近的密蛋白3蛋白和/或包含受损/被破坏的细胞-细胞连接的癌细胞。
308、术语“减少”、“变少”、“减轻”、“降低”、或“减弱”通常指与对照分子/组合物引起的或在对照条件下的响应相比,本文考虑的组合物产生、引起或导致较小的生理响应(即下游效应)的能力。“减少”或“降低”量通常是“统计学显著”的量,并且可以包括由对照组合物产生的响应(参考响应)或特定细胞谱系中的响应的1.1、1.2、1.5、2、3、4、5、6、7、8、9、10、15、20、30、50、100、200、500或更多倍的减少。
309、在一方面,提供了本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物,其用于疗法,诸如用于癌症的疗法和/或治疗。在进一步的方面,提供了本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物,其用作药物,诸如抗癌药物。在一些实施方案中,本文考虑的用于疗法的car、多肽、多核苷酸、载体、免疫效应细胞或组合物用于疗法的方法和/或治疗的方法,诸如癌症疗法的方法和/或治疗癌症的方法。
310、在一方面,提供了本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物,其用于治疗癌症,其中所述癌症包含细胞-细胞连接的破坏和/或受损的细胞-细胞连接。在另一个方面,提供了治疗患有癌症的受试者的方法,所述方法包括向受试者施用治疗有效量的本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物,其中所述癌症包含细胞-细胞连接的破坏和/或受损的细胞-细胞连接。因此,在一些实施方案中,用于在有此需要的受试者中治疗癌症的方法包括施用有效量的,例如治疗有效量的包含本文考虑的遗传修饰的免疫效应细胞的组合物。施用的量和频率将由如患者的病况以及患者的疾病的类型和严重性的因素来确定,但是适当的剂量可以通过临床试验来确定。
311、本领域普通技术人员将认识到,为影响期望的疗法,可能需要多次施用本文所考虑的组合物。例如,组合物可以在1周、2周、3周、1个月、2个月、3个月、4个月、5个月、6个月、1年、2年、5年、10年或更长的跨度内施用1次、2次、3次、4次、5次、6次、7次、8次、9次或10次或更多次。替代性地,可能仅需要施用一次本文所考虑的组合物。
312、在一个实施方案中,向有此需要的受试者施用有效量的组合物以增强受试者中对癌症的细胞免疫应答。因此,在进一步的方面,提供了用于在有此需要的受试者(诸如患有癌症的受试者)中增加对包含被破坏的细胞-细胞连接的癌细胞的细胞毒性的方法,所述方法包括向受试者施用一定量的本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物。
313、免疫应答可包括由能够杀伤感染细胞的细胞毒性t细胞介导的细胞免疫应答、调节性t细胞应答和辅助t细胞应答。还可以诱导体液免疫应答,其主要由能够活化b细胞因此导致抗体产生的辅助t细胞介导。可以使用多种技术来分析由组合物诱导的免疫应答的类型,这些技术在本领域中有充分描述;例如,current protocols in immunology,由johne.coligan,ada m.kruisbeek,david h.margulies,ethan m.shevach,warren strober编辑(2001)john wiley&sons,ny,n.y。
314、在t细胞介导的杀伤情况下,car配体结合起始car信号传导至t细胞,导致诱导t细胞产生或释放能够通过各种机制诱导靶细胞凋亡的蛋白质的多种t细胞信号传导途径的激活。这些t细胞介导的机制包括(但不限于)将胞内细胞毒性颗粒从t细胞转移到靶细胞中、t细胞分泌促炎细胞因子(细胞因子可以直接(或经由招募其他杀伤效应细胞间接)诱导靶细胞杀伤)、以及上调位于t细胞表面的死亡受体配体(例如,fasl)(死亡受体配体在与靶细胞上的其同源死亡受体(例如,fas)结合后诱导靶细胞凋亡)。因此,一方面,提供了用于在患有癌症的受试者中减少包含被破坏的细胞-细胞连接的癌细胞数量的方法,所述方法包括向受试者施用治疗有效量的本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物。在一个实施方案中,减少包含被破坏的细胞-细胞连接的癌细胞的数量包括t细胞介导的杀伤。
315、在一个实施方案中,与施用前的对包含被破坏的细胞-细胞连接和/或受损的细胞-细胞连接的癌细胞的细胞毒性相比,“有效量”(其可以包括治疗有效量)足以增加对癌细胞(如包含被破坏的细胞-细胞连接和/或受损的细胞-细胞连接的癌细胞)的细胞毒性。在另一个实施方案中,与施用前的包含被破坏的细胞-细胞连接和/或受损的细胞-细胞连接的癌细胞的数量相比,“有效量”足以减少癌细胞(如包含被破坏的细胞-细胞连接和/或受损的细胞-细胞连接的癌细胞)的数量。
316、在某些实施方案中,本文考虑的方法进一步包括施用消融元件的活化剂或结合剂。此类活化剂或结合剂包括但不限于抗体(例如,临床批准的抗体),诸如识别并结合huegfrt或cd20的抗体(即分别是西妥昔单抗或利妥昔单抗)、cd20的小分子拮抗剂等。一旦认为受试者的治疗完成,诸如在受试者或癌症完全响应之后,就可以施用消融元件的活化剂或结合剂。因此,应当理解,施用消融元件活化剂或结合剂将防止受试者中任何慢性的表达car的t细胞活性。在进一步的实施方案中,本文考虑的方法还包括利用消融元件来靶向用于抗体依赖性细胞毒性(adcc)和/或补体依赖性细胞毒性(cdc)的表达car的细胞。因此,在某些实施方案中,本文考虑的方法进一步包括消除表达car的细胞,诸如表达car的t细胞。在其他实施方案中,诸如通过施用类固醇以抑制受试者中任何急性的表达car的t细胞活性,例如以治疗细胞因子风暴是期望的。
317、在进一步的方面,提供了本文考虑的car、多肽、多核苷酸、载体、免疫效应细胞或组合物在制备药物(诸如抗癌药物)中的用途。在一个实施方案中,本文考虑的在制备药物中的用途是制备用于治疗癌症的药物。
318、在一个实施方案中,嵌合抗原受体(car),其包含:a)胞外域,其包含结合细胞连接蛋白的至少一种表位的抗原结合蛋白,其中所述细胞连接蛋白位于细胞-细胞连接之内,并且在癌细胞中,其中所述细胞连接蛋白的至少一种表位仅可被所述car胞外域接近而结合;b)跨膜结构域;c)一个或多个胞内信号传导结构域。在一个实施方案中,car进一步包含一个或多个共刺激结构域。在一个实施方案中,根据本文公开的实施方案中任一项的car,其中细胞连接蛋白是紧密连接蛋白,和/或其中当细胞-细胞连接位于有组织的组织内的细胞之间时;和/或当细胞与细胞的连接未受损时,该至少一种表位不可被car胞外域接近而结合;和/或其中当细胞-细胞连接位于癌细胞之间、癌细胞与非癌性细胞之间时,当细胞-细胞连接受损时,和/或当细胞连接蛋白错误定位与细胞-细胞连接之外时,该至少一种表位可被car的胞外域接近而结合。
319、在一个实施方案中,根据前述实施方案中任一项的car,其中细胞连接蛋白是密蛋白家族的成员;和/或其中至少一种表位存在于细胞连接蛋白的一个或多个胞外环中;和/或其中细胞连接蛋白是密蛋白3;和/或其中密蛋白3暴露于具有被破坏的或紊乱的紧密连接的实体癌中的细胞表面;和/或其中密蛋白3不暴露于细胞表面并且位于正常或非癌性细胞的细胞-细胞连接中。
320、在一个实施方案中,根据前述实施方案中任一项的car,其中所述至少一种表位独特地存在于密蛋白3中;和/或其中该至少一种表位的长度是4个氨基酸;和/或其中该至少一种表位是不连续表位。
321、在一个实施方案中,根据前述实施方案中任一项的car,其中抗原结合蛋白选自抗体或其抗原结合片段;和/或其中抗原结合蛋白选自由以下组成的组:单克隆抗体、骆驼ig、ig nar、fab片段、fab’片段、f(ab)’2片段、f(ab)’3片段、scfv、双scfv、(scfv)2、微抗体、双抗体、三抗体、四抗体、二硫键稳定化的fv蛋白(dsfv)和sdab;和/或其中抗原结合蛋白是scfv。
322、在一个实施方案中,根据前述实施方案中任一项所述的car,其中所述抗原结合蛋白包含选自以下的cdr中任一个或其组合:来自seq id no:7的cdrh1、cdrh2和cdrh3和/或来自seq id no:8的cdrl1、cdrl2和cdrl3;或抗原结合蛋白包含来自seq id no:7和8的所有六个cdr;或抗原结合蛋白包含:seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列;seq id no:4的cdrl1序列;seq id no:5的cdrl2序列;以及seqid no:6的cdrl3序列。与这些实施方案一致,抗原结合蛋白包含与seq id no:7的序列至少90%相同的可变重链(vh)序列,和与seq id no:8的序列至少90%相同的可变轻链(vl)序列;或者其中抗原结合蛋白包含seq id no:7的可变重链(vh)序列,和seq id no:8的可变轻链(vl)序列;或其中抗原结合蛋白从n末端至c末端包含seq id no:7的vh序列和seq idno:8的vl序列;或其中抗原结合蛋白从n末端至c末端包含seq id no:8的vl序列和seq idno:7的vh序列。
323、在一个实施方案中,根据上述实施方案中任一项的car,其中所述跨膜结构域衍生自选自由以下组成的组的多肽:t细胞受体的α链或β链、cd3δ、cd3ε、cd3γ、cd3ζ、cd4、cd5、cd8α、cd9、cd16、cd22、cd27、cd28、cd33、cd37、cd45、cd64、cd80、cd86、cd134、cd137(4-1bb)、cd152、cd154、cd278(icos)和pd1;或其中跨膜结构域衍生自cd8α。在一个实施方案中,根据前述实施方案中任一项的car,根据前述实施方案中任一项的car,其中一个或多个胞内信号传导结构域衍生自选自由以下组成的组的胞内信号传导分子:fcrγ、fcrβ、cd3γ、cd3ε、cd3δ、cd3ζ、cd22、cd66d、cd79a和cd79b,或其中一个或多个胞内信号传导结构域是cd3ζ。在一个实施方案中,根据前述实施方案中任一项的car,该car进一步包含衍生自选自由以下组成的组的共刺激分子的一个或多个共刺激结构域:card11、cd2、cd7、cd27、cd28、cd30、cd40、cd54(icam)、cd83、cd134(ox40)、cd137(4-1bb)、cd278(icos)、dap10、lat、nkd2c、slp76、tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、trim和zap70;或其中一个或多个共刺激结构域是cd137(4-1bb)。
324、在一个实施方案中,根据前述实施方案中任一项的car,胞外域包含与seq id no:11具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性的氨基酸;或其中car包含seq id no:11的氨基酸序列。在一个实施方案中,根据前述实施方案中任一项的car,胞外域包含与seq id no:18具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性的氨基酸;或其中car包含seq id no:18的氨基酸序列。
325、在一个实施方案中,根据前述实施方案中任一项的car,该car包含与seq id no:12、24、25、27、28、29或30具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性的氨基酸序列;或其中car包含seq id no:12、24、25、27、28、29或30的氨基酸序列;或其中car包含不具有seq id no:10的cd8前导序列的与seq id no:12、24、25、27、28、29或30具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性的氨基酸序列。本领域普通技术人员将理解,在不影响car的功能的条件下,可以使用本领域已知的标准技术来修饰或缺失引入根据前述实施方案中任一项的car中的seq id no:10的cd8前导序列。与这些实施方案一致,根据前述实施方案中任一项的car,该car包含与seq id no:34、35、36、37、38或39具有至少90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的序列同一性的氨基酸序列。
326、在一个实施方案中,根据前述实施方案中任一项的car,该car包含a)包含密蛋白3结合蛋白的胞外域,所述密蛋白3结合蛋白包含seq id no:1的cdrh1序列;seq id no:2的cdrh2序列;seq id no:3的cdrh3序列;seq id no:4的cdrl1序列;seq id no:5的cdrl2序列;和seq id no:6的cdrl3序列;b)衍生自cd8α的跨膜结构域;c)衍生自cd137(4-1bb)的共刺激结构域;以及d)衍生自cd3ζ的胞内信号传导结构域。在一个实施方案中,提供了与根据前述实施方案中任一项的car竞争结合的car。
327、在一个实施方案中,提供了多肽,其包含前述实施方案中任一项的car的氨基酸序列。在又一个实施方案中,其中多肽进一步包含消融元件。与这些实施方案一致,其中消融元件是细胞表面蛋白,其使用抗体或抗原结合片段靶向抗体依赖性细胞毒性(adcc)和/或补体依赖性细胞毒性(cdc);和/或其中该消融元件衍生自选自由以下组成的组的多肽:截短的人egfr多肽(huegfrt)和cd20,或其中该消融元件是cd20。在一个实施方案中,提供了载体,其包含根据前述实施方案中任一项的多核苷酸。在又一个实施方案中,其中载体是病毒载体;和/或其中载体是逆转录病毒载体,诸如慢病毒载体;和/或其中逆转录病毒载体选自由以下组成的组:人免疫缺陷病毒i(hiv-i);人免疫缺陷病毒2(hiv-2)、维斯纳-梅迪病毒(vmv)病毒;山羊关节炎脑炎病毒(caev);马感染性贫血病毒(eiav);猫免疫缺陷病毒(fiv);牛免疫缺陷病毒(biv)和猿猴免疫缺陷病毒。在一个实施方案中,提供了载体生产细胞,其包含根据本文公开的实施方案中任一项的多核苷酸序列和/或根据前述实施方案中任一项的载体。
328、在一个实施方案中,提供了免疫效应细胞,其包含根据前述实施方案中任一项的car、多肽、多核苷酸和/或载体。与这些实施方案一致,免疫效应细胞选自由以下组成的组:t淋巴细胞、自然杀伤t淋巴细胞(nkt)细胞、巨噬细胞、和自然杀伤(nk)细胞;或其中免疫效应细胞是细胞毒性t淋巴细胞(cd8+)。在一个实施方案中,提供了药物组合物,其包含根据前述实施方案中任一项的免疫效应细胞和药学上可接受的赋形剂。还提供了包括生成包含根据前述实施方案中任一项的car的免疫效应细胞的方法,所述方法包括将根据前述实施方案中任一项的多核苷酸和/或载体引入免疫效应细胞中。与这些实施方案一致,所述方法进一步包括通过使细胞与结合cd3的抗体或其抗原结合片段以及结合cd28的抗体或其抗原结合片段接触,来刺激免疫效应细胞并诱导细胞进行增殖;从而生成免疫效应细胞群体。在一个实施方案中,其中刺激免疫效应细胞是在将根据前述实施方案中任一项的载体引入该细胞之前进行的;和/或其中免疫效应细胞包含t淋巴细胞。
329、在一个实施方案中,提供了根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物用于治疗癌症。在一个实施方案中,提供了在有此需要的受试者中治疗癌症的方法,所述方法包括向受试者施用治疗有效量的根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞、或药物组合物。又在其他的实施方案中,提供了在患有癌症的受试者中增加对癌细胞的细胞毒性的方法,所述方法包括向受试者施用有效量的根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。在一个实施方案中,提供了在患有癌症的受试者中增加对癌细胞的细胞毒性的方法,所述方法包括向受试者施用有效量的根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。在其他的实施方案中,提供了在患有癌症的受试者中减少癌细胞的数量的方法,所述方法包括向受试者施用有效量的根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物。与这些实施方案一致,其中癌症的特征在于密蛋白3在紧密连接外部的错误定位和/或紧密连接的破坏,使得密蛋白3可接近而结合;或者其中癌症的特征在于紧密连接蛋白-3由于紧密连接的破坏而暴露于细胞表面。在一个实施方案中,其中癌症是实体癌;或其中实体癌是结直肠癌、胰腺癌、乳腺癌(例如,三阴性乳腺癌(tnbc))、卵巢癌、肺癌(例如,非小细胞肺癌(nsclc))或前列腺癌;或者其中癌症是上皮癌。
330、在一个实施方案中,提供了根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物在制备用于治疗癌症的药物中的用途。又在其他实施方案中,提供了根据前述实施方案中任一项的car、多肽、多核苷酸、载体、免疫效应细胞或药物组合物,其用于疗法。
331、尽管出于理解清楚的目的,已经通过说明和实例的方式详细描述了前述实施方案,但是本领域普通技术人员基于本文所考虑的教导,在不脱离所附权利要求的精神或范围的条件下,可以进行对其进行某些变化和修改是显而易见的。以下实施例仅通过说明的方式,而非通过限制的方式提供。本领域技术人员将容易地到,可以变化或修改各种非关键参数以产生基本上相似的结果。
332、实施例
333、实施例1–car-t细胞的生成
334、分离来自健康人外周血的cd4+和cd8+ t细胞,随后用编码抗-密蛋白-3或对照car构建体(对照car是抗cd19 car)的慢病毒载体转导。从健康供体分离的cd4+和cd8+ t细胞均成功转导了编码抗-密蛋白-3car或对照抗-cd19 car的慢病毒载体。car t细胞是从多个供体分离的细胞中生成的,并根据后续体外和体内功能测定的需要进行扩增和冷冻。
335、材料和方法
336、cd4+和cd8+ t细胞的分离以及t细胞的激活
337、根据制造商的说明,如下使用histopaque(sigma,目录号10771)从全外周血和nhs血液和移植(nhsbt)锥体中分离外周血单核细胞(pbmc)。将细胞重悬于automacs运行缓冲液中,并每107个细胞添加fcr封闭试剂、cd4微珠和cd8微珠(均为miltenyi biotec)。将细胞混合并在4℃下孵育15分钟。然后,洗涤、离心细胞并且每108个细胞重悬于冷automacs运行缓冲液中。使用possel_s分离方案在automacs pro-separator(miltenyi biotec)上运行细胞溶液。将含有磁性标记的cd4+和cd8+ t细胞的阳性级分用pbs洗涤三次,以确保细胞溶液中edta的量减少至少200倍,因为edta可能影响t细胞激活。最后一次pbs洗涤后,将细胞沉淀物重悬于适当体积的texmacs培养基(miltenyi biotec)中,并取出样品用于在nc-250nucleocounter(chemometec)上计数。
338、将细胞重悬于texmacs培养基中。将transact t细胞激活试剂(miltenyi biotec)以及il-7和il-15添加到细胞中,以达到每种细胞因子10ng/ml的终浓度。将细胞溶液(1x106个细胞/ml)铺板到细胞培养板中,随后将细胞在37℃、5%co2的加湿培养箱中孵育24小时。
339、用慢病毒载体转导t细胞并扩增car-t细胞
340、用编码抗-密蛋白-3car(906_009)和报告基因(lngfr)的慢病毒载体(称为906_009-lngfr)或抗cd19 car载体(对照)以moi为3转导细胞。car构建体包含lngfr标志物,能够检测和/或富集表达car-t细胞的t细胞。lngfr标志物系统使用瞬时表达的截短的人低亲和力神经生长因子受体(lngfr)分子作为表面标志物来检测和/或选择转染细胞。细胞在37℃、5%co2的加湿培养箱中孵育。在整个培养期间,细胞维持在texmac培养基以及il-17和il-15中,每种细胞因子的浓度为10ng/ml。对于某些批次,细胞在il-2而不是il-7和il-15上培养。如果使用il-2,则遵循相同的培养程序,但添加100国际单位(iu)/ml的il-2,而不是il-7和il-15。转导后12天收获t细胞,并以1x107-1x108个细胞/ml的细胞密度冷冻在cs5冷冻介质(sigma,#c2999)中。
341、通过使用流式细胞术(macsquant analyzer 10)检测截短的人低亲和力神经生长因子受体(lngfr;cd271)与pe缀合的抗lngfr抗体(ab)的表达来确定转导效率。数据使用flowjo v10.1分析。
342、对于某些car-t批次,需要将所有car-t群体相对于最低转导效率归一化。为了准确归一化car-t细胞群,分析了lngfr+细胞的频率并对细胞进行计数。随后,计算将lngfr+细胞的频率降低至规定水平所需的未转导t细胞的体积,并酌情添加到每个细胞群中。
343、制备了两种用抗-密蛋白-3car载体(906_009-lngfr)转导的细胞制备物,一种为悬浮细胞(称为“载体1”),一种为贴壁细胞(称为“载体3”)。除了两种不同的细胞制备物之间的转导效率存在差异(参见下面的讨论)之外,两种不同的细胞制备方法之间没有观察到显著差异。
344、用于生成纯car-t细胞群体的t细胞富集
345、对于一些car-t批次,t细胞在诱导后第12天通过使用automacs pro-separator富集或easysep富集的阳性选择进行富集,以生成纯car-t细胞群,如下所述。
346、对于automacs pro-separator富集,每107个细胞添加lngfr微珠(miltenyibiotec),并将细胞充分混合,然后在4℃下孵育15分钟。洗涤细胞,并使用possel_s分离方案在automacs pro-separator上运行细胞溶液。将含有磁性标记的lngfr+ t细胞的阳性级分用pbs洗涤三次,以确保细胞溶液中edta的量减少至少200倍,因为edta可能影响t细胞激活。
347、easysep富集在转导后第9天或转导后第12天进行,这取决于测定的要求和培养物中的细胞总数。使用easysep人cd271阳性选择试剂盒ii(stemcell technologies uk ltd)和easysep rapidshere珠(stemcell technologies)对具有用lngfr标签化的不同car的转导t细胞进行阳性选择。根据待富集的转导t细胞的数量,使用easyplate磁体(stemcelltechnologies)或easyeight磁体(stemcell technologies)。将新鲜解冻或培养的转导t细胞以1x107至2x107之间的密度重悬于补充有easysep人fcr阻断剂(25μl/ml)和easysep人cd271阳性选择混合物(50μl/ml)的texmacs培养基中,并在rt下孵育15分钟。
348、为了获得更高的细胞密度,将1x108至2x108个细胞重悬于补充有指示浓度的easysep人fcr阻断剂和easysep人cd271阳性选择混合物的texmacs培养基中。将50μl/ml的easysep rapidshere珠添加到每个样品中,并将细胞在rt下孵育15分钟。孵育后,将样品加入洗涤缓冲液(含有2%胎牛血清(fbs)和2mm edta的pbs),移至easyplate或easyeighteasysep磁体上并孵育10分钟。小心除去上清液,避免干扰附着至珠的阳性选择细胞。再进行3次洗涤后,将细胞重悬于texmacs培养基中,并移出样品以在nc-250nucleocounter上计数,并进行富集后lngfr分析,以确认富集成功。
349、如果在转导后第9天进行富集,则将富集的car-t细胞重新铺板到含有浓度为10ng/ml的il-7和il-15的texmacs培养基中。将细胞在37℃、5%co2的加湿培养箱中孵育72小时,并在转导后第12天如上所述进行冷冻。
350、如果在转导后第12天进行富集,则将富集的细胞立即用于功能测定或冷冻。
351、结果
352、t细胞的扩增、转导效率以及car-t细胞群的富集和归一化
353、所有t细胞群均成功扩增,扩增倍数范围在14至178倍之间,具体取决于特定的供体。所有t细胞群的平均扩增倍数为76。
354、用抗-密蛋白-3car载体1以moi为3转导的car-t细胞在多个供体和载体批次间具有在41%-60%之间的转导效率(基于lngfr阳性细胞的频率)。用抗-密蛋白-3car载体3以moi为3转导的car-t细胞在所用的三个供体中实现了29%-37%的较低转导效率。所有对照car t细胞(抗cd19car)在多个供体和载体批次间使用moi为3实现了48%-75%的转导效率。
355、通过automacs pro-separator富集(数据未显示)和easysep lngfr富集()两者,富集lngfr+car-t细胞以提供100%lngfr+car-t细胞群是成功的,如图2a中针对所有产生的car-t细胞批次所示。
356、将car-t细胞群相对于表达lngfr的t细胞的所需频率的归一化是成功的,如图2b中针对所产生的car-t批次所示。
357、使用automacs pro-separator的cd4和cd8阳性选择能够使>95%的cd3+细胞群在第0天被转导。这使得载体能够高效地仅转导期望的细胞类型。cd4/cd8阳性选择后单核细胞污染极少(<5%),其中剩余的单核细胞在培养期间死亡,导致转导后第12天出现纯cd3+细胞群。
358、从健康供体分离的cd4+和cd8+ t细胞均成功转导有编码抗-密蛋白-3car或对照抗-cd19 car的慢病毒载体。在慢病毒载体1和3之间观察到转导效率的差异。所有t细胞群均成功扩增,其中在某些car构建体的供体中观察到一些异常扩增。
359、使用automacs pro-separator和easysep lngfr微珠两者富集car-t细胞是成功的,并能够提供100%lngfr+car-t群体用于后续功能测定。除此之外,car-t细胞群相对于lngfr+细胞的所需频率的归一化是成功的。
360、产生的所有car-t细胞均能够用于功能测定,以测试抗-密蛋白-3car载体1。悬浮细胞中产生的car-t细胞用于后续实验。
361、实施例2–car表达和t细胞表型的影响
362、本研究的目的是评估强直信号传导(抗原非依赖性信号传导)在体外对抗-密蛋白-3car-t细胞的影响。表现出强直信号传导的car-t细胞会导致体外t细胞功能受损和耗竭以及体内功效低下。强直信号传导受car结构、接头或铰链、信号传导结构域、表面表达位置和水平等特征的组合影响。通过测量细胞上清液中分泌的细胞因子(ifnγ)的基础水平来评估强直信号传导,通过测量激活(cd69)和耗竭(pd-1和tim-3)标志物来区分连续t细胞表型,以及测量增强的抗原非依赖性信号传导(pcd3ζ)。响应与分别表现出低水平和高水平的强直信号传导的阴性对照抗cd19 car和阳性对照(gd2-28ζ)car进行基准比较。
363、结果表明,与阳性对照(gd2-28ζ)car-t细胞相比,抗cd19 car阴性对照和抗-密蛋白-3car均赋予低水平的强直信号传导,表明密蛋白-3car构建体的体外抗原非依赖性激活水平较低。
364、材料和方法
365、阴性和阳性对照car的生成
366、阴性对照抗cd19 car使用具有4-1bb-cd3ζ胞质信号传导结构域的fmc62 scfv生成,并在本文中用作对照,以对低水平的强直信号传导响应进行基准测试。阳性对照car(gd2-28ζ)使用具有ch2-ch3 igg1接头以及cd28-cd3ζ跨膜和胞质跨越结构域的14g2a scfv生成。此处,ef1a启动子用于增强car的转导效率,并应导致驱动强直信号传导响应的倾向增加。与4-1bbζ胞质结构域相比,cd28ζ跨膜和胞质结构域应增加强直信号传导水平,而与所使用的慢载体转导启动子无关。此外,14g2a抗gd2 scfv克隆具有寡聚倾向,这一特征以gd2-28ζcar结构为特征,导致car依赖性信号传导的内在激活。阳性对照car中使用的igg1ch2-ch3细胞外接头也可能有助于观察到的强直信号传导水平。
367、cart-细胞解冻和培养
368、将car-t细胞(从低温冷冻细胞或新鲜细胞中解冻)重悬于texmacs培养基中,并在含有10ng/ml il-7/il-15的texmacs培养基中将细胞密度调整为2×106个细胞/ml。在lngfr富集之前,将重悬的细胞置于37℃、5%co2的加湿培养箱中24小时。
369、解冻后car-t细胞的lngfr富集
370、使用easysep人cd271阳性选择试剂盒和easysep右旋糖酐rapidspheres阳性选择表达lngfr的car-t孔。收获car-t细胞,并在经过非组织培养物处理的96孔板中,在补充有easysep人fcr阻断剂和easysep人cd271阳性选择混合物的texmacs培养基中重悬至10至20×106个细胞的密度,并在rt下孵育15分钟。将easysep右旋糖酐rapidspheres添加到细胞悬浮物中,并在rt下孵育15分钟。此后,使用easyplate easysep磁体选择表达lngfr的细胞,重悬于补充有10ng/ml人il-7/il-15的texmacs培养基中,并在随后的测定或冷冻保存之前在37℃与5%co2下置于加湿培养箱中72小时。将冷冻保存的lngfr富集细胞解冻,并以2.5×106/孔的密度接种在补充有10u/ml il-2的texmacs培养基中,并在37℃与5%co2下置于加湿培养箱中24小时。提供上清液和细胞用于后续测定。
371、裂解物生成和蛋白质定量
372、从培养物中收获car-t和未转导的t细胞,并将2×106个细胞重悬于冷dpbs(含钙和镁)中,离心,并通过重复移液冷裂解缓冲液来裂解所得细胞沉淀物。将裂解物离心、等分、快速冷冻并储存在-80℃下以便长期储存。使用二喹啉甲酸(bca)测定法对裂解物中的蛋白质水平进行定量。
373、car-t细胞上清液中ifnγ细胞因子分泌的测定
374、人ifnγ中观尺度发现(meso scalediscovery,msd)板加载有测试样品。然后将板密封并在室温下在板摇床上孵育90分钟。洗涤板并将检测抗体添加到每个孔中。将板密封并在室温下在板摇床上孵育2小时。此后,洗涤板并在msd sector 600成像仪上读取。计算6名供体间的测试car t细胞分泌的ifnγ水平的平均值和标准误差,并使用graphpad prism(bonferroni oneway anova)绘制数据。
375、car-t细胞表型(cd69、tim-3、pd-1)的测定
376、将未转导的t细胞和car-t细胞解冻并计数。将2.5x105个细胞/孔等分到96孔板中。然后洗涤细胞,并将适当的抗体混合物(含有针对cd3、cd8、cd69、tim3、pd1的抗体)添加到每个孔中。将细胞在室温、黑暗中孵育15分钟,然后以1μg/ml的终浓度重悬于含有dapi活/死染料的培养基中。通过流式细胞术分析样品并使用flowjo v10软件分析流式细胞术数据。
377、激活/耗竭标志物cd69、pd-1和tim-3的表达和共表达通过按cd4+和cd8+群体对单个活细胞进行分层而生成。一旦门控为cd4+或cd8+细胞群,激活/耗竭标志物仅通过单一阳性进行鉴定。然后应用随后的布尔门控逻辑来表征三个激活/耗竭标志物的单、双和三阳性/阴性细胞群。
378、对于数据分析,对阴性对照(抗cd19 car)、阳性对照(gd2-28ζcar)和抗-密蛋白-3car计算了六个pbmc供体间的三阳性(pd-1、tim-3和cd69)、双阳性(cd69和tim-3或cd69和pd-1或tim-3和pd-1)和单阳性(pd-1或tim-3或cd69)的平均百分比。使用graphpad prism(bonferroni oneway anova)分析数据。
379、经由car特异性cd3ζ磷酸化确定下游信号传导
380、从2×106car-t细胞中获得裂解物,并且将浓度归一化至300μg/ml并加热。上样前将抗-pcd3ζ、抗-cd3ζ、gapdh和二抗添加到裂解物中。使用peggy-sue高通量毛细管western技术评估蛋白质水平。根据最多6个供体的总cd3ζ和gapdh加载对照计算磷酸化cd3ζ(pcd3ζ)的归一化水平。
381、使用compass for sw软件(peggy-sue)进行抗原非依赖性信号传导数据分析,产生主要指标。在此处,使用软件确定各个染色剂的峰下面积(aup),并根据gapdh(总蛋白质加载)水平的aup对响应进行归一化。将测试car-t细胞(阳性对照(gd2-28ζ)和抗-密蛋白-3car-t细胞)的归一化pcd3ζ水平除以针对阴性对照car-t细胞(抗cd19 car)检测到的归一化pcd3ζ水平。计算了6名供体间测试car t细胞的car特异性磷酸化水平(pcd3ζ)的平均值和标准误差。使用graphpad prism(bonferroni oneway anova)绘制数据。
382、结果
383、来自car t细胞的基础水平ifnγ分泌
384、t细胞的ifnγ分泌是t细胞激活的关键测量指标,并且抗原非依赖性信号传导可以部分地通过该细胞因子的分泌来评估。图3a中呈现的数据显示,与阳性对照(gd2-28z)car-t细胞(22557±12903pg/ml)相比,来自抗-密蛋白-3car t细胞的ifnγ分泌显著减少(611.8±755.1pg/ml)。在未转导的t细胞(123.7±103.0pg/ml)、阴性对照(抗cd19 car;666.4±725.1pg/ml)和抗-密蛋白-3car-t细胞之间没有观察到显著差异(图3a)。
385、基础t细胞激活(cd69+)和耗竭(tim-3+和pd-1+)表型
386、显示出激活(cd69+)和耗竭标志物(tim-3+和pd-1+)增加的t细胞基础连续表型的分化可以补充用于检测强直信号传导的测定的子集。图3b中显示的数据显示,与阴性对照(抗cd19 car)和抗-密蛋白-3car-t细胞相比,阳性对照(gd2-28ζcar)的激活和耗竭表型显著增加。对于阳性对照(gd2-28ζcar),与cd8+ t细胞(三阳性:0.42±0.4%,双阳性:3.9±2.31%,单阳性:14.18±4.75%)相比,cd4+ t细胞(三阳性:2.05±1.57%,双阳性:6.89±3.61%,单阳性:14.59±7.36%)显示出激活和耗竭表型的更高增加。对于抗-密蛋白-3car-t细胞,与显著更低的cd8+ t细胞(三阳性:0.54±0.5%,双阳性:0.61±0.25%,单阳性:3.51±1.37%)相比,cd4+ t细胞(三阳性:0.06±0.06%,双阳性:0.71±0.44%,单阳性:2.99±0.96%)表现出激活和耗竭表型的更高增加(图3b)。
387、car特异性cd3ζ的磷酸化
388、从结果分析来看,抗-密蛋白-3car的car pcd3ζ归一化水平(0.68±0.39)与阳性对照(gd2-28ζ)car(7.32±3.84)相比显著更低,并且相比阴性对照(抗-cd19)car pcd3ζ没有显著差异(图3c)。
389、从ifnγ分泌、激活(cd69+)和耗竭(tim3+和pd-1+)表型以及car pcd3ζ水平获得的结果来看,与阳性对照(gd2-28ζ)car-t细胞相比,抗-cd19 car和抗-密蛋白-3car均赋予低水平的强直信号传导。根据总cd3ζ染色估计的t细胞上的car转导水平显示出基于所使用的启动子的差异。与使用pgk启动子表达的抗-cd19 car和抗-密蛋白-3car相比,使用ef1a启动子转导的阳性对照(gd2-28ζ)car-t细胞赋予更高水平的car特异性总cd3ζ。因此,抗-cd19 car和抗-密蛋白-3car也表现出较低水平的磷酸化cd3ζ、细胞因子释放以及激活和耗竭表型的分化。这再次证实了载体的效率可能是诱导强直信号传导的促成因素。
390、除启动子外,与阳性对照(gd2-28ζ)car-t细胞不同,抗-cd19 car和抗-密蛋白-3car-t细胞是使用没有igg1 ch2-ch3接头的4-1bbζ胞质结构域生成的,这改善任何强直信号传导效应。该数据再次证实,抗-密蛋白-3car-t细胞表现出低水平的强直信号传导和抗原非依赖性激活,这将以其他方式对体外car-t细胞功能产生不利影响。
391、实施例3–抗-密蛋白-3car-t细胞对表达密蛋白的细胞系的特异性
392、这些研究的目的是生成表达密蛋白-3的细胞系,用于抗-密蛋白-3car-t细胞的特异性的验证和功能活性的评估。具体而言,使用cytotox red测定和靶细胞的汇合度来测量抗-密蛋白-3car-t细胞的细胞毒性。此外,在与表达密蛋白-3的细胞共培养24小时后,使用中观尺度发现(msd)测定法测量ifnγ释放来评估car-t细胞的激活。结果表明,抗-密蛋白-3car-t细胞主要响应于hcldn3进行杀伤,并且与其他人密蛋白几乎没有细胞毒性交叉反应。
393、材料和方法
394、rko-ko细胞系、rko-ko人cldn3 gfp和小鼠cldn3 gfp细胞系的生成和表征
395、rko-ko细胞系是通过使用crispr-cas编辑技术敲除结直肠癌(rko)细胞系中的cldn3基因而制成的。
396、使用抗cldn3抗体通过流式细胞术进一步测试选定的rko-ko克隆,以确认没有检测到细胞外cldn3表达。选择rko-ko克隆26.1作为亲本细胞系的初级克隆,用于进一步生成过表达hcldn3、mcldn3和其他人密蛋白细胞系。
397、过表达人cldn3和小鼠cldn3的rko-ko细胞系是通过用含有(i)表达为具有c端单体gfp标签的标签化蛋白的人cldn3基因或(ii)表达为具有c端单体gfp标签的标签化蛋白的小鼠cldn3基因以及嘌呤霉素选择标记的商业慢病毒载体(lv)以moi为5转导rko-ko克隆26.1细胞系而生成的。使用流式细胞术评估转导效率(gfp表达)。
398、单克隆细胞系是通过从异质群体中进行单细胞分选来选择表达高、中和低水平gfp的细胞而开发的。
399、表达人cldn家族成员cldn4、cldn5、cldn6、cldn8、cldn9和cldn17细胞系的多克隆rko-ko细胞系使用如上所述的类似方法,通过用编码表达为具有c端单体gfp标签的标签化蛋白的cldn4、cldn5、cldn6、cldn8、cldn9或cldn17基因以及嘌呤霉素选择标记的商业慢病毒转导rko-ko克隆26.1细胞系来生成。
400、通过qpcr表征rko-ko和rko-ko转导的细胞系
401、在rko-ko非转导细胞以及分别过表达cldn3、4、6、9、17和mcldn3的rko-ko细胞中,相对于管家基因actb评估人密蛋白3、4、5、6、9和17以及小鼠cldn3基因的mrna表达。通过实时定量pcr(rt-qpcr)检测mrna表达。rt-qpcr结果显示转导的cldn在各自的rko-ko细胞系中过表达(数据未显示)。
402、car-t细胞解冻和培养
403、当使用冷冻car-t细胞时,将细胞解冻并用texmacs重悬。在一些实验中,如本文别处所述富集car-t细胞。
404、incucyte杀伤测定的共培养设置
405、靶细胞以2×105个细胞/ml的密度重悬于细胞培养基中,然后转移至测定板的相应孔中,使得每孔有2x104个细胞。然后将测定培养板转移至36.5℃/5%co2的加湿incucytes3中24小时,然后进行car-t细胞共培养。
406、从各自的测定孔中取出细胞上清液,并用含有500nm cytotox red试剂的新鲜细胞培养基替换,然后将板转移到36.5℃/5%co2的加湿incucyte s3中,然后添加效应细胞(car-t细胞)。将car-t细胞和未转导的t细胞重悬于细胞培养基中至密度为2×105个细胞/ml,然后添加到孔中。将测定板置于37℃/5%co2的加湿incucyte s3中。图像采集安排在6天的时间跨度内以2小时的间隔进行。进行图像分析以确保对描述靶细胞杀伤的总红色面积的增加和生成的总红色面积掩蔽的具体可视化以确定总面积(μm2/图像)。在每个供体中进行归一化。
407、使用msd的细胞因子浓度测量
408、将归一化或富集的t细胞与靶细胞以1:1e:t(效应细胞:靶细胞,其中“效应细胞”是转导的car-t细胞)比例混合,并在37℃、5%co2下共培养。24小时后,将板离心并收集上清液,以便使用与上文实施例2中描述的方法类似的方法,使用适当的检测抗体(sulfo-tag抗hifnγ、sulfo-tag抗htnfa和sulfo-tag抗hil2抗体)来定量细胞因子分泌。
409、结果
410、cart细胞对表达密蛋白的rkoko的激活响应
411、未转导的或抗cd19(对照)和抗-密蛋白-3car-t细胞与表达与密蛋白3密切相关的密蛋白的rko ko细胞系共培养。然后收集这些共培养物的上清液并对感兴趣的细胞因子进行定量。这些实验的数据如图4a-4d和表3所示。
412、最初,研究了car-t细胞响应于整个细胞系组的il-2、ifnγ和tnfα分泌。除了抗-密蛋白-3car-t细胞对hcldn3的显著响应之外,图4a中显示的该数据显示出所有三种细胞因子响应于hcldn4的分泌的小幅增加。
413、然后,注意力集中在实验中的核心细胞系组(hcldn4、hcldn6和hcldn9)上,该实验观察了6个供体中的ifnγ响应(如图4b和4c所示)。抗-密蛋白-3car-t细胞再次对hcldn4产生响应,并且在该实验中还观察到对hcldn9的响应。抗-密蛋白-3car-t细胞与抗cd19对照car-t细胞响应于hcldn4和hcldn9分泌的ifnγ的倍数变化分别为25和14.3。尽管这种响应很显著,但在与hcldn3共培养物中高出2495倍的响应相比时,它是值得考虑的。
414、图4d中呈现的信息进一步支持了这两个实验的数据,显示了另外七个供体的细胞因子分泌。这些供体中只有一个对hcldn9表现出响应,但对hcldn4表现出更一致的响应(这同样是最小的)。该图中呈现的一些供体随后被再次使用(12031、92024和c1700657)。在这些情况中的每一种中,数据都支持之前的结果。
415、除了抗-密蛋白-3car-t细胞对hcldn3的强烈响应外,最一致的响应是对于mcldn3。这不仅可以从ifnγ上调的形式看出,还可以从il-2和tnfα上调的形式看出(图4a、4b和4c)。这种响应的重要性也在图4b和4c以及表3中得到了证明,其中抗-密蛋白-3car-t细胞的ifnγ响应比抗cd19对照car-t细胞高439倍。
416、表3-与对照(抗-cd19car-t细胞)相比,抗-密蛋白-3cart细胞的ifng分泌倍数变化的统计显著性。cl=置信区间。
417、
418、1ut=未转导
419、car-t细胞的rko细胞杀伤
420、为了专门研究与car-t细胞一起培养时的靶细胞活力,进行了许多杀伤测定,以确定t细胞激活(通过细胞因子响应测量)如何转化为细胞毒性和随后的靶细胞凋亡。
421、从这一系列实验收集的数据汇总在表4中(报告为测定终点的活细胞%)。没有实验导致hcldn4、hcldn6或hcldn9活力丧失,但偶尔观察到对mcldn3的响应。这在96小时时最为明显,此时rko ko mcldn3在与来自2个供体的抗-密蛋白-3car-t细胞一起培养时达到71%和86%或最大响应。
422、在6个供体和核心细胞系组中进行了实验,以确认抗-密蛋白-3car-t细胞的cldn3特异性细胞毒性响应。使用两个读数,汇合%(图5a和5b)和cytotox显色,或活细胞%(图6a-6c)。其中第一个,汇合%表明通过特定共培养物特有的靶细胞数量的变化来杀伤细胞。第二个读数量化了当活力丧失导致cytotox染料流入时发生的红色显色。当细胞死亡增加时,cytotox红色反应较高,转化为低%活细胞。用于收集该数据的图像示例如图5a所示。
423、当抗-密蛋白-3car-t细胞与表达hcldn3或mcldn3的rko ko一起培养时,特别观察到汇合%的变化,尽管与ifnγ分泌一样,对hcldn3的响应幅度要大得多。活细胞%读数证实了这一点,与对照相比,当抗-密蛋白-3car-t细胞与rko ko mcldn3或rko ko hcldn3共培养时,观察到显著的细胞毒性作用。
424、表4-多克隆细胞系测定终点的活细胞%
425、
426、*与rko ko hcldn3 l14共培养
427、抗-密蛋白-3car-t细胞与表达mcldn3的细胞发生交叉反应
428、可以使用小鼠组织进行许多相关实验,因此了解抗-密蛋白-3car-t细胞如何与mcldn3反应是有用的。本文进行的实验一致表明,抗-密蛋白-3car-t细胞被mcldn3表达激活,导致ifnγ、tnfα和il-2的分泌。虽然不如对hcldn3的响应那么高,但激活的t细胞确实表现出显著的细胞毒性反应,表现为靶细胞的损失。
429、大多数数据是使用表达不同水平mcldn3表达的细胞系进行的,然而,为了进一步了解响应,还使用了表达高水平或低水平mcldn3的一些细胞系。在这些条件下,只有当抗-密蛋白-3car-t细胞与表达高mcldn3的rko ko细胞一起培养时,才能观察到激活响应。
430、抗-密蛋白-3car-t细胞不响应于其他人密蛋白而进行杀伤
431、在本文提出的任何实验中,没有观察到抗-密蛋白-3car-t细胞响应于hclnd6、hcldn5、hcldn8或hcldn17的激活。然而,细胞因子的分泌显示出对hcldn4和hcldn9的一些反应性。尽管图4a描述了显著的激活响应,但它无法与抗-密蛋白-3car-t细胞对hcldn3和mcldn3的响应进行比较。值得注意的是,这并不转化为任何杀伤响应,这表明抗-密蛋白-3car-t细胞不响应于除hcldn3之外的任何人密蛋白而进行显著杀伤。
432、本文提供的数据显示抗-密蛋白-3car-t细胞至少部分地被hcldn4和hcldn9激活。该响应明显低于对hcldn3的响应,并且不会转化为细胞毒性作用或细胞死亡。然而,抗-密蛋白-3car-t细胞确实与mcldn3发生交叉反应,并且已经描述了靶细胞的部分杀伤的情况。该数据表明,抗-密蛋白-3car-t细胞主要响应于hcldn3进行杀伤,并且与其他人密蛋白几乎没有细胞毒性交叉反应。
433、实施例4–抗-密蛋白-3car-t细胞对密蛋白-3阳性肿瘤细胞系的细胞毒性
434、本研究的目的是基于表达该构建体的t细胞特异性杀伤表达人密蛋白-3(hcldn3)的靶细胞的倾向,展示抗-密蛋白-3car的表达和细胞毒性效力。这些数据表明,抗-密蛋白-3car-t细胞能够分泌ifnγ并杀伤衍生自结直肠癌、乳腺癌和胰腺癌的表达hcldn3的癌细胞系。
435、材料和方法
436、通过macsquant tyto分选富集lngfr阳性car-t细胞
437、将细胞在缓冲液中洗涤,用稀释度为1:50的lngfr pe抗体在4℃下染色30分钟,然后根据制造商的说明使用macsquant tyto分选进行分选。本文所述实验中使用的所有car-t细胞具有至少90%lngfr阳性的纯度。
438、量化t细胞表面的car分子
439、将1x105个细胞和50μl bangs labs quantum simply cellular珠重悬于1:20稀释的抗lngfr pe或1:50稀释的抗hcldn3 pe中,并在4℃下孵育30分钟。将细胞和珠洗涤两次,然后在cytoflex s机器上测量细胞和珠的pe信号。
440、细胞杀伤测定的共培养设置
441、如上文实施例3中所述设置用于incucyte杀伤测定的共培养物,不同之处在于使用incucyte zoom而不是incucyte s3。
442、xcelligence杀伤测定的共培养物通过以25,000个细胞/孔的密度将靶细胞接种到细胞培养板中建立,并在xcelligence实时细胞分析(rtca)仪器的细胞培养箱中培养。接种后约20小时,将效应细胞以0.5:1或1:1car-t细胞与靶细胞的比例添加,并放回细胞培养箱中。使用的靶细胞是下表5中所示的癌细胞系。
443、表5-癌细胞系:
444、
445、
446、使用msd的细胞因子浓度测量
447、将靶细胞系重悬,然后将2x104或2.5x104个细胞接种到96孔板中。然后将归一化或富集的t细胞以1:1e:t(效应细胞:靶细胞,其中“效应细胞”是转导的car-t细胞)比例添加到板中,并在37℃、5%co2下共培养24-48小时。共培养后将板离心,并收集上清液,以便使用适当的检测抗体定量细胞因子分泌,如上文实施例2中所述。
448、结果
449、car表达和hcldn3表达的定量
450、car分子在t细胞表面的表达是car功能的必要条件。测量lngfr表达作为car表达的替代。lngfr和car分子应按1:1的比例转化,但由于蛋白质稳定性的潜在差异,因此量化的lngfr仅是car分子数量的估计。
451、未转导的细胞(ut)仅显示出非常低的lngfr表达信号;在10,000到20,000之间(图7a),这被认为是背景信号。
452、供体12031和92024表面上平均有190,000和166,000个lngfr分子,供体d5表面上有301,000个分子。这种差异可能是由于t细胞生成的差异造成的。
453、如本文先前所述,生成hcldn3敲除rko细胞系(rko-ko)并用作功能测定的阴性对照。对以不同水平表达hcldn3的rko-ko细胞(多克隆rko-ko hcldn3细胞系;非单细胞分选)或针对高表达(rko-ko hcldn3h12)或低表达(rko-ko hcldn3 l14)分选的rko-ko细胞的杀伤是car效力的指示。通过使用quantum simply cellular珠和抗cldn3 pe定量表达来确认hcldn3表达的差异(图7b)。rko-ko细胞显示低于珠水平的信号,因此它们的hcldn3水平被视为0。rko-ko hcldn3 l14 low细胞表面上平均有80,000个hcldn3分子,而rko-ko hcldn3h12 high细胞表面上平均有800,000个hcldn3分子。因此,这两个细胞系的hcldn3表达存在10倍的差异。
454、car-t细胞的细胞毒性
455、图8a-8d显示了孵育90小时的示例incucyte杀伤测定。显示了与低水平表达hcldn3的rko-ko细胞或rko-ko细胞一起孵育的富含lngfr的抗cd19对照car-t细胞(图8a)或抗-密蛋白-3car-t细胞(图8b)的示例图像,并且相应的杀伤曲线显示抗-密蛋白-3car-t细胞具有细胞毒性,但对照细胞没有细胞毒性(图8c)。当抗-密蛋白-3car-t细胞与靶细胞系一起孵育时,通过红色染料的面积测量的信号显色是可见的。定量和归一化数据如图8c所示,其显示与靶标阴性细胞一起孵育的抗-密蛋白-3car-t细胞不会导致细胞裂解,但与表达hcldn3的rko细胞一起孵育的抗-密蛋白-3car-t细胞导致完全靶细胞杀伤,而抗-cd19对照则没有。
456、表6显示了达到最大响应50%(表明靶细胞被杀伤50%)所需的时间。这些值揭示了测定之间的差异,这可以通过hcldn3表达的差异来解释,但这在不同实验中并不一致。虽然在一些实验中,50%的最大响应是在24至41小时后实现的,但其他实验显示50%的最大响应是在51小时至最多74小时后实现的。其他数据(未显示)对所有6个供体的t细胞和靶细胞进行同等处理,显示6个供体中有4个在80至86小时之间传播减少,一个供体在68小时内传播减少,一个供体在实验后96小时内未达到50%细胞毒性。杀伤动力学的差异无法解释,但重要的是,所有实验都导致靶细胞完全裂解。
457、使用xcelligence方法在表达密蛋白-3的细胞系ht-29-luc上获得了类似的细胞毒性结果(图8d)。以1:1的比例对三个供体观察到100%细胞毒性,并在80小时、30小时和50小时后达到100%细胞毒性。40小时和60小时后,以1:2的比例(效应细胞:靶细胞)实现100%细胞毒性。通过msd分析以与xcelligence实验相同的方式进行的共培养物的细胞因子分泌(数据未显示)。当t细胞与ht-29-luc共培养时,在冷冻和解冻的供体以及新鲜使用的供体中检测到干扰素γ(ifnγ),但在没有细胞系的情况下孵育时未检测到。
458、未转导的细胞或抗-cd19对照car-t细胞响应于表达密蛋白-3的细胞的ifnγ分泌与响应于不表达密蛋白-3的细胞出于相同水平。这些结果表明没有观察到非特异性细胞因子分泌。抗-密蛋白-3car-t细胞响应于不表达密蛋白-3的靶细胞而分泌,导致与阴性对照相似的背景细胞因子分泌,表明抗-密蛋白-3car不识别靶细胞上的其他分子。
459、在所有8个进行的实验中,将抗-密蛋白-3car-t细胞与表达密蛋白-3的靶细胞一起培养,均导致ifnγ分泌。不同实验之间测量的实际细胞因子量有所不同,但在所有情况下,与抗-密蛋白-3car-t细胞响应于靶标阴性细胞相比,抗-密蛋白-3car-t细胞响应于其靶标的特异性细胞因子分泌增加了至少100倍。
460、表6-表达cldn3的rko细胞达到最大响应(完全靶细胞杀伤)50%的时间
461、
462、
463、*这些值通过3次重复测定
464、表达rko-ko cldn3的靶细胞的滴定
465、最大响应(完全靶细胞杀伤)在细胞系之间有所不同,但也可以指示部分靶细胞杀伤。这可能是由于细胞毒性效应物功能不足或在并非所有肿瘤细胞都表达靶标时发生。为了确定最大响应的差异并确认incucyte测定中可以实现部分杀伤,对靶细胞进行了滴定。rko-ko和rko-ko hcldn3多克隆细胞以不同比例混合,并与抗-密蛋白-3car-t细胞一起孵育。当只有2%的rko-ko细胞表达hcldn3时,信号不可见,但当hcldn3表达细胞比例较高时,可见信号增加(图9)。这些结果表明部分杀伤可以实现,如果比较相同的靶细胞系,则这在最大响应存在差异时是可见的。
466、hcldn3表达与car-t激活的关系
467、了解car-t细胞如何响应于靶标密度有助于预测靶标表达在替代环境中的效果。进行实验来研究t细胞激活和靶标表达之间的关系。
468、通过使用hcldn3 mrna(使用mmessage mmachine t7 ultra试剂盒从线性化质粒在体外产生)对hcldn3敲除(ko)细胞系(rko-ko)进行核转染来严格控制hcldn3表达,以创建hcldn3表达梯度(图10a)。这使得研究能够在明确的系统中进行,该系统独立于可能影响t细胞对hcldn3响应的可变因素(例如其他生物标志物)。确认hcldn3的表达后,将靶细胞与car-t细胞一起培养,并通过cd69表达(通过流式细胞术测量,如前面实施例中所述)或细胞因子分泌(ifnγ/颗粒酶b)评估激活响应。
469、在每个实验中,观察到抗-密蛋白-3car-t细胞的特异性激活和hcldn3表达。这种hcldn3依赖性激活呈现出靶标表达与ifnγ和颗粒酶b的t分泌之间的相关性(图10c和10d以及表7)。尽管没有进行统计分析,但hcldn3阳性群体的大小与稳定在100%靶标表达的cd69表达之间也存在明显的关系(图10b)。总体而言,这显示了靶标表达和car-t激活之间的关系。
470、在上述实验中,rko-ko采用梯度优化进行核转染,该梯度优化创建了随着hcldn3阳性群体减少而产生的靶标梯度。在另一项实验中,研究了降低整个细胞群中hcldn3表达的影响(表8)。在这种情况下,数据表明,随着hcldn3表达的增加,t细胞激活减少(如ifnγ分泌所示)。cd69表达在每个表达水平之间保持一致。
471、表7-不同靶标表达水平下细胞因子分泌的显著性
472、
473、
474、估计值报告为抗-密蛋白-3和抗-cd19对照car-t细胞之间ifnγ水平的倍数变化。cl=置信区间。
475、表8-研究t细胞响应于靶标表达梯度的数据的汇总
476、
477、根据hcldn3表达和t细胞激活的三种不同适应症筛选癌细胞系
478、在上述研究中,研究了抗-密蛋白-3car-t细胞仅对一种表达不同水平的外源hcldn3的结直肠癌细胞系的响应。在此,评估了抗-密蛋白-3car-t细胞对表达内源性hcldn3的三种主要适应症(结直肠癌、胰腺癌和乳腺癌)的31种癌细胞系组的响应,包括ht-29-luc和rko-ko细胞系分别作为阳性和阴性对照。首先通过流式细胞术和实时定量pcr(rt-qpcr)筛选来自结直肠癌(图11a)、胰腺癌(图11b)和乳腺癌(图11c)的细胞系的hcldn3表达。在所有细胞系上检测到不同水平的hcldn3表达(图11a-11c,左侧),范围从0%到100%。有趣的是,在部分阳性细胞系(例如sw403或sw480)中,当细胞与hcldn3抗体一起孵育时,观察到总群体而不是明确定义的阳性和阴性群体发生变化。在同一组细胞系中通过rt-qpcr对hcldn3基因的表达水平进行定量(图11a-11c,中间),并且在cldn3 mrna的量中观察到类似的模式。由于crispr方法,即使在阴性细胞系对照(rko-ko)中也可以检测到少量hcldn3 mrna。比较rt-qpcr和流式细胞术数据时,观察到ht-29-luc、t84和sw403是两种测定中最高的密蛋白3表达者,而rko-ko和colo320-dm是最低的表达者。
479、使用抗cd19作为阴性car对照,与选定的癌细胞系共培养后,还研究了抗-密蛋白-3car-t细胞的激活(图11a-11c,右侧)。重要的是,所有表达hcldn3的细胞系都激活了抗-密蛋白-3car-t细胞,如高水平的ifnγ所示,而与rko-ko共培养的抗-密蛋白-3car-t细胞没有观察到任何响应。然而,一些通过流式检测未检测到hcldn3表达的细胞系colo320-dm(0.068%)、dld-1(0.347%)、hc1954(0.55%)和bxpc3(1.95%)也能够激活抗-密蛋白-3car-t细胞。一种可能的解释是所用商业抗体的检测极限。
480、所有hcldn3阳性细胞系都能激活抗-密蛋白-3car-t细胞,但不能激活抗-cd19对照car-t细胞。然而,无论是通过流式细胞术还是rt-qpcr,都没有发现抗-密蛋白-3car-t激活与hcldn3表达水平之间存在明显的相关性。
481、来自三种适应症的癌细胞系的杀伤
482、为了研究抗-密蛋白-3car-t细胞针对更广泛肿瘤的功能,选择了具有不同hcldn3表达水平的几种癌细胞系来进行杀伤测定。表9显示了三个incucyte实验的总结,每个实验均使用三个供体。由于供体之间的结果非常一致,表9总结了每个实验的三个供体。来自三种适应症的细胞系被抗-密蛋白-3car-t细胞杀伤,表明该car有潜力用于多种适应症。也可见ht-29-luc完全杀伤(数据未显示)。只有一种结直肠癌株colo-320dm没有被抗-密蛋白-3car-t细胞杀伤。三种细胞系hcc1954、bxpc3和hpac被部分杀伤。部分杀伤在显微术图像中可见,作为凋亡细胞或细胞层中的孔洞,而获得的信号非常低或不存在,如原始数据中可见(图12)。
483、表9-抗-密蛋白-3car-t细胞对衍生自结直肠癌、乳腺癌或胰腺癌的靶细胞的细胞毒性
484、
485、n无杀伤
486、p部分杀伤(图像中可见但不可量化的杀伤)
487、c完全杀伤
488、n/a未获得数据
489、lngfr分子定量表明稳健car表达
490、检测到的lngfr数量在166,000至301,000之间。假设car表达和lngfr表达相当,并且考虑到平均cd8+ t细胞表面有50,000个t细胞受体,估计t细胞表面上的hcldn3 car丰度足以激活t细胞。
491、抗-密蛋白-3car-t细胞杀伤动力学因实验而异
492、确定car-t细胞效力的一方面是诱导细胞毒性的速度。通过确定多少小时后达到最大响应的50%来对此进行分析。这些结果因实验而异,因此很难得出结论。然而可以说,在所有情况下,都实现了完全的靶细胞杀伤,这是确定car效力的一个重要方面。
493、抗-密蛋白-3car-t细胞特异性杀伤表达cldn3的细胞
494、抗-密蛋白-3car-t细胞对表达hcldn3的靶细胞具有特异性。这方面的证据源于实验,其中内源性hcldn3被敲除的rko细胞(rko-ko)不会被抗-密蛋白-3car-t细胞杀伤。相比之下,表达hcldn3的细胞系被抗-密蛋白-3car-t细胞杀伤。此外,如果将rko-ko细胞和过表达外源hcldn3的rko-ko细胞混合,则仅检测到部分细胞毒性,这表明即使t细胞也仅被表达hcldn3的靶细胞特异性激活。这些结果表明抗-密蛋白-3car-t细胞活性对hcldn3具有特异性。
495、抗-密蛋白-3car-t细胞激活的增加与密蛋白3表达的增加相关
496、为了调查哪些患者群体可能对抗-密蛋白-3car-t细胞治疗有响应,了解car的激活阈值很有帮助。如上所述,使用受控模型专门研究靶标表达与t细胞激活之间的关系。通过将靶标的表达降低至流式细胞术无法再检测到的程度,目的是确定激活抗-密蛋白-3car-t细胞所需的靶标表达水平。
497、ifnγ分泌是t细胞激活响应的关键测量指标,cd69是常用的激活标记。颗粒酶b(靶细胞凋亡的整体诱导剂)的定量也被用来为靶标表达与car-t细胞毒性之间的关系提供明确的证据。当rko-ko用1ng密蛋白3mrna核转染时,这些指标上调,导致5%的阳性群体,清楚地显示了抗-密蛋白-3car-t细胞的敏感性。即使抗原可用性较低,car-t细胞响应也是有效的。培养基中颗粒酶b的存在表明发生了靶细胞凋亡,但在不研究靶细胞本身的情况下,这无法明确说明。
498、由于抗体的检测限,很难说明观察到的表达是一小群密蛋白3表达细胞还是低表达的100%靶标阳性细胞群。观察到的任何靶细胞凋亡都无法与密蛋白阳性群体的准确定量相关。
499、尽管观察到抗原表达与抗-密蛋白-3car-t细胞激活之间存在明确的关系,但主要由于抗原检测的局限性而无法建立激活阈值。然而重要的是,在这个人工系统中,抗-密蛋白-3car-t细胞对密蛋白3的表达存在剂量响应。
500、与来自不同适应症的细胞系组共培养时,观察到抗-密蛋白-3car-t细胞激活
501、为了研究抗-密蛋白-3car-t细胞与更广泛的靶细胞的功效,针对mrna和蛋白质水平上的密蛋白3表达筛选了31种癌细胞系(包括结直肠癌、胰腺癌和乳腺癌)。值得注意的是,所有表达hcldn3的细胞系都可以激活抗-密蛋白-3car-t细胞,从而将这种car的功效扩展到更广泛的癌症适应症。
502、抗-密蛋白-3car-t细胞具有杀伤衍生自不同适应症的肿瘤细胞的潜力
503、抗-密蛋白-3car-t细胞的激活可能不会导致靶细胞杀伤,因此针对三种肿瘤适应症测试了细胞毒性。对于大多数测试的靶细胞系可见完全或部分杀伤,这与car-t细胞的ifnγ释放一致(图11a-11c)。只有结直肠癌细胞系colo-320dm没有被抗-密蛋白-3car-t细胞杀伤,很可能是因为其没有表现出hcldn3表达,尽管其能够部分激活car-t细胞。
504、抗-密蛋白-3car在t细胞上的表达水平表明其可以将t细胞活性重定向到表达hcldn3的肿瘤细胞。其特异性杀伤具有hcldn3外源性表达的靶细胞,同时不伤害经由crispr/cas9技术去除抗原的细胞。抗-密蛋白-3car-t细胞能够分泌ifnγ并杀伤衍生自结直肠癌、乳腺癌和胰腺癌的表达hcldn3的癌细胞系,尽管由于检测试剂的限制无法确定激活阈值。这表明car能够将t细胞重定向到若干类型的癌症。最后,在这些细胞系中的hcldn3表达与ifnγ释放水平之间没有发现明显的相关性,这可能是由于这些细胞系的不同生物学特性所致。
505、实施例5-重复的抗原依赖性刺激以评价抗-密蛋白-3car-t细胞的体外长期抗肿瘤活性
506、本研究的目的是分析基于相同scfv变体的六种抗-密蛋白-3car构建体的表达、细胞因子分泌和细胞毒性效力。此外,通过重复的抗原刺激评估了抗-密蛋白-3car-t细胞的长期功能。
507、材料和方法
508、将针对密蛋白-3的scfv克隆到miltenyi biotec car间隔区文库的三个主链(l、s、xs)中
509、编码scfv变体的质粒以两种不同的方向制备:重-轻(vh-vl)和轻-重(vl-vh)。scfv被克隆到miltenyi biotec car间隔区文库的三个主链中,间隔区长度不同,长间隔区(l,higg4 h-ch2-ch3)、短间隔区(s,hcd8)和极短间隔区(xs,higg4铰链)导致6种不同的结构:
510、 <![cdata[间隔区<sup>1</sup>]]> scfv方向h-l scfv方向l-h 长(l) 906_002 906_007 短(s) 906_004 906_009 极短(xs) 906_005 906_010
511、1间隔区(或铰链结构域):细胞外结构域和跨膜结构域之间的结构域。
512、pbmc制备和泛t细胞的分离
513、pbmc是从两个健康供体的血沉棕黄层中分离出来的。使用泛t细胞人分离试剂盒无接触分离t细胞。根据制造商的方案,使用2x108个白细胞进行泛t细胞的分离。将t细胞重悬于含有il-7(10ng/ml)、il-15(10ng/ml)和t细胞transact人(1:100)的texmacs培养基中,并调整浓度为1x106个细胞/ml。
514、car-t细胞的生成和扩增
515、泛t细胞以1x106个细胞/ml的浓度和每孔2ml接种到24孔板中(见上文)。用transact激活t细胞一天后,进行转导。将慢病毒载体以5的感染复数(moi)添加到t细胞中。转导后24至48小时,除去每孔的上清液并添加含有il-7和il-15的新鲜texmacs。根据t细胞密度,每2至3天将t细胞培养物按1:2或1:3进行分裂,以将细胞浓度保持在0.5x106至2x106个细胞/ml之间。
516、转导效率(通过lngfr)和car表达的确定
517、生成的car构建体包含lngfr作为标记基因,因此如前所述,经由使用抗lngfr-pe的抗lngfr染色通过流式细胞术(macsquant analyzer 10)分析转导效率。
518、为了分析car表达,使用蛋白质l经由可变轻链(κ链)对car进行染色。将细胞重悬于含有l-生物素蛋白(5μg/1000μl)的缓冲液中,在4℃下孵育45分钟后,洗涤细胞并重悬于含有抗生物素-pe的缓冲液中。然后洗涤细胞并通过流式细胞术(macsquant analyzer 10)进行分析。
519、长期共培养:incucyte
520、靶细胞rko-ko cldn3 h1(人密蛋白-3敲除+人密蛋白-3和经由慢病毒转导引入gfp标志物)用于该测定。在进行测定前72小时解冻t细胞(见上文),并在含有il-7和il-15的texmacs中恢复。测定当天,将t细胞充分重悬,并对相同条件(相同供体并表达相同car构建体)进行汇集,并考虑到lngfr阳性t细胞的细胞浓度和频率,调整t细胞的转导效率并且共培养设置为对于4x104和3x104的靶细胞,效应细胞:靶细胞2.5:1。添加t细胞悬浮物,并在incucyte中孵育共培养物,以经由绿色汇合来监测靶细胞的生长。第3天,添加新鲜的靶细胞培养基。第4天,在添加t细胞之前大约4至5小时,将新鲜靶细胞以与第一轮相同的浓度接种到新的细胞培养板中。汇集来自相同条件的t细胞,并将调整后的t细胞以2.5:1的e:t添加到新鲜接种的靶细胞中。将细胞培养板在incucyte中孵育,以经由绿色汇合来监测靶细胞的生长。第7天,在添加t细胞之前大约4至5小时,将新鲜靶细胞以3x104靶细胞的浓度接种到新的细胞培养板中。汇集来自相同条件的所有t细胞。
521、重复的抗原刺激:抗原spike-in
522、将靶细胞rko-ko cldn3 h1(人密蛋白-3敲除+人密蛋白-3和标记gfp)与t细胞共培养。来自供体h5和p的t细胞在建立共培养物之前解冻96小时,并在含有il-7和il-15的texmacs中恢复。
523、为了对耗竭标志物、转导效率、cd4和cd8进行染色,使用了以下缀合物:lag3(cd223)-vioblue、pd-1(cd279)-pe-vio770、tim3(cd366)-apc、cd8-apc-vio770、cd4-viogreen、lngfr-pe和7-aad。制备这些缀合物的主混合物。将细胞重悬于主混合物中,然后在4℃(黑暗中)下孵育10分钟。将细胞重悬于peb(含0.5%bsa的clinimacs)中,并在macsquant analyzer 10上测量样品。将基于转导的t细胞达到2:1的e:t的所需体积的t细胞悬浮物重悬于适当体积的靶细胞培养基中,将t细胞悬浮物添加到靶细胞中,将共培养物在加湿培养箱(37℃和5%co2)中孵育。每24小时对t细胞进行一次耗竭标志物染色,并将新鲜的靶细胞添加到共培养物中。在第3天最后一次添加新鲜靶细胞。
524、结果
525、t细胞染色以分析转导效率(经由lngfr)和car表达
526、为了分析从供体d5生成的car t细胞的转导效率(见上文),在第7天通过流式细胞术测量了lngfr标记基因表达。从染色获得的数据表明转导是成功的并且实现了39%至50%的lngfr阳性t细胞的频率(参见图13)。此外,在第15天,再次分析lngfr表达(参见图13),以调整t细胞至用于功能测试的其转导效率。car分子在t细胞表面的表达是car功能的必要条件。因此,car表达经由protein l染色来确定(见上文)。获得的数据显示所有生成的car变体均得到表达,并且car阳性t细胞群的频率达到了范围为35%至43%之间(参见图13)。此外,还包括表达针对密蛋白-3的不同scfv的car-t细胞作为阳性对照。
527、萤光素酶杀伤测定
528、为了评价抗-密蛋白-3car-t细胞的细胞毒性,进行了基于萤光素酶的杀伤测定。使用乳腺癌细胞系t-47d进行共培养。该靶细胞系被工程化以在用编码两种标志物的慢病毒载体转导后表达萤光素酶和egfp,然后再转导细胞。制备并扩增表达各种抗-密蛋白-3car的t细胞或未转导的t细胞,并在共培养前在没有细胞因子的情况下培养48小时。然后将t细胞以根据最低转导效率(lngfr阳性细胞的频率)调整的3种不同的效应细胞与靶细胞(e:t)比率(即5:1、1:1和0.2:1)添加到靶细胞系中,并且孵育共培养物(加湿,37℃,5%co2)。建立共培养后20小时取出上清液并保存直至经由macsplex测定测量细胞因子。将d-萤光素溶液添加至细胞中,并在孵育后5分钟,用发光计(victor,perkinelmer)读取发光。
529、表达针对密蛋白-3的不同scfv的cart细胞用作阳性对照。该图(图14)显示共培养20小时后被杀伤的靶细胞的频率。当与未转导的t细胞共培养时,未观察到被杀伤的靶细胞频率的增加。表达各种抗-密蛋白-3car构建体的t细胞与表达人密蛋白-3的t-47d共培养,显示出取决于e:t比率的被杀伤的靶细胞频率和细胞毒性的增加。当e:t为5:1时,被杀伤的靶细胞的频率为96%-99.7%,并且发现被杀伤的靶细胞的频率随着e:t比率的降低而降低。此外,7个测试的car构建体之间被杀伤的靶细胞的频率相似。
530、经由macsplex测定确定上清液中的细胞因子分泌
531、使用macsplex测定分析共培养上清液(见上文)的细胞因子il-2、ifnγ和tnf-α浓度。仅分析e:t比例为1:1的共培养样品。样品和macsplex测定是根据macsplex cytokine12试剂盒(人)制造商的方案制备的,并在macsquant analyzer 10上进行分析。所得浓度以pg/ml描绘(图15a-15c)。用于分析的上清液未稀释。在未转导的t细胞与癌细胞系t-47d共培养的条件下,上清液中未检测到il-2、ifnγ和tnf-α水平升高。此外,在来自“仅靶细胞”条件的样品中也未检测到细胞因子。与模拟t细胞相比,在其中表达基于906变体的各种抗-密蛋白-3car的car t细胞与t-47d细胞共培养的所有条件下,显示出il-2和ifnγ的水平升高。在t-47d存在的情况下,906_004、906_009和阳性对照密蛋白-3car分泌最高量的il-2。包括906_005的这些构建体也显示出最高的ifnγ分泌。仅检测到低水平的tnf-α,其中在样品906_009和阳性对照密蛋白-3car中检测到最高浓度。
532、t细胞与重复抗原刺激的长期共培养
533、通过incucyte监测与表达906_002(长间隔区)、906_004(短间隔区)或906_005(极短间隔区)car变体的t细胞共培养的靶细胞的生长。结果表明,对于在第一轮靶细胞暴露中的两个供体(g5和h5),靶细胞被所有三种car构建体高效清除(图16a和16d)。而在单独培养靶细胞rko-ko cldn3 h1的对照中,观察到增殖。将car t细胞转移到新鲜靶细胞上进行第二轮和第三轮靶细胞遭遇后,car变体之间的差异变得可见。与表达具有短间隔区和极短间隔区变体的抗-密蛋白-3car的t细胞相比,表达具有长间隔区的car变体的t细胞控制靶细胞生长的效率较低(图16c和16e)。对于供体h5,第2轮后没有获得足够的lngfr阳性t细胞,因此未进行第3轮。
534、重复的抗原刺激:抗原spike-in
535、在第0、1、2、3和6天通过流式细胞术分析耗竭标志物(tim3、pd-1、lag3)的表达。双阳性(tim3、pd-1)和三阳性(tim3、pd-1、lag3)t细胞分析中仅包括lngfr阳性t细胞。
536、图17a-17d中描绘的结果显示,在第一次添加靶细胞之前的第0天,双阳性和三阳性转导的t细胞的频率低于5%。然而,对于两个供体来说,从第一天到第三天,双阳性和三阳性t细胞的频率随着靶细胞遭遇而增加。与供体h5相比,供体p显示出耗竭标志物表达更高的增加(图17b)。两天(第4天和第5天)未添加新鲜靶细胞后,第6天的染色表明双阳性和三阳性转导t细胞的频率下降,这对于供体p比对于供体h5更为明显。
537、表达基于906scfv变体的各种抗-密蛋白-3car构建体的t细胞与表达人密蛋白-3的t-47d共培养,显示出取决于e:t比率的被杀伤靶细胞的频率增加。当癌细胞系与未转导的t细胞共培养时,没有观察到这一点。这表明当与抗人-密蛋白-3car-t细胞共培养时,表达人密蛋白-3的靶细胞发生特异性裂解。此外,所有表达抗-密蛋白-3car构建体的t细胞(其scfv方向和间隔区长度(l、s和xs)不同)对测试的靶细胞显示出相当的裂解能力。总体而言,抗-密蛋白-3car在裂解表达人密蛋白-3的靶细胞方面的功能与表达阳性对照密蛋白-3构建体的car-t细胞相当。
538、与未转导的t细胞相比,与t-47d共培养的抗-密蛋白-3car-t细胞上清液中分泌的细胞因子il-2和ifnγ浓度增加。这表明在表达人密蛋白-3的靶细胞存在的情况下,基于906变体的抗-密蛋白-3car-t细胞具有特异性细胞因子分泌。构建体906_009和906_004显示出最高浓度的分泌细胞因子,它们都具有共同的短间隔区。对于这些构建体,分泌的细胞因子水平与表达阳性对照密蛋白-3构建体的car-t细胞相当甚至更高。
539、为了进一步评价基于906scfv表达不同car变体的t细胞的性能,进行更具挑战性的测定。因此,进行了长期共培养,其中添加了三轮新鲜靶细胞。表达具有3个不同间隔区(l、s和xs)的906变体的car-t细胞在第一轮靶细胞遭遇中表现同样出色。然而,表达短间隔区和极短间隔区的变体能够在所有三轮共培养期间清除新鲜添加的rko-ko cldn3 h1细胞。对于基于长间隔区变体的car,来自一个供体(h5)的car-t细胞仅在第一轮中清除靶细胞,而来自第二个供体(g5)的car-t细胞仅在前两轮靶细胞暴露期间清除靶细胞。预计scfv的方向不会影响这些结果。
540、在经由抗原spike-in进行重复抗原刺激的测定中,在重复抗原遭遇后lngfr阳性t细胞的耗竭标记物的表达增加是明显的(图17a-17e),然而两个测试的供体之间的差异比表达基于906scfv的各种car构建体的t细胞更明显。因此,在该测定中,无法就特定car构建体变体的功能差异得出结论。此外,第6天的数据表明,在第4天和第5天没有添加新鲜靶细胞后,耗竭标志物双阳性和三阳性car t细胞的频率下降。目前还不确定频率的降低是否是由于lngfr阳性t细胞上这些标志物的实际减少所致,或者可能归因于其他原因例如未耗竭的t细胞的扩增,并且这可能导致未耗竭的t细胞的总体频率降低。
541、抗-密蛋白-3car在原代t细胞上的表达水平表明它们可以将t细胞活性重定向到表达密蛋白-3的肿瘤细胞。这些抗-密蛋白-3car-t细胞能够裂解表达密蛋白-3的靶细胞,并在靶标存在的情况下选择性分泌il-2和ifnγ。此外,抗-密蛋白-3car-t细胞能够在若干轮靶细胞暴露期间清除表达密蛋白-3的肿瘤细胞。
542、实施例6-抗-密蛋白-3car-t细胞对cldn3阳性肿瘤细胞的增殖响应
543、本研究的目的是评估抗-密蛋白-3car-t细胞响应于密蛋白-3阳性靶细胞的抗原刺激而增殖的能力。
544、材料和方法
545、实验准备
546、通过培养效应细胞和靶细胞72小时来评估car t细胞的增殖。
547、对于这些实验,在2个独立实验中用4个基于相同scfv变体的构建体(906-002、906-004、906-007和906-009;参见实施例5)慢病毒转导来自6个供体的t细胞。工程改造t细胞,将低亲和力神经生长因子受体(lngfr)标记基因直接插入car序列中,以便通过靶向car分子的细胞外部分上表达的lngfr标记基因的免疫磁珠进行分选来分离car阳性细胞。
548、与密蛋白-3阳性(rko)和密蛋白-3阴性(rko-ko)细胞系按1:1共培养72小时后,通过掺入[3h]胸苷来测量car-t细胞增殖。胸苷掺入测定采用如下策略,其中放射性核苷3h-胸苷在有丝分裂细胞分裂期间掺入染色体dna的新链中。
549、实验方案
550、通过以1:1的比率共培养效应细胞和靶细胞来测量car-t细胞增殖。1×105的富集的car-t细胞与1×105的cldn-3阳性rko或cldn-3阴性(rko hucldn-3ko)细胞系共培养。48小时后,用1μci(37bq)的[3h]-胸苷(perkinelmer)脉冲细胞并再孵育21小时,以使t细胞将放射性掺入分裂细胞的新合成的dna中。使用细胞收集器(micro 96收集器-skatroninstruments)将细胞收集到过滤垫上。为了确定响应于[3h]胸苷掺入而发生的细胞分裂程度,使用wallac 1450microbeta trilux液体闪烁和发光β计数器(perkin elmer)测量掺入dna的放射性,并将其表示为每分钟计数(cpm)。数据分析在graphpad prism版本5.0.4中进行。数据表示为平均值±标准误差,并通过双尾学生t检验进行分析,如图图例所示。研究结果的显著性定义如下:ns,不显著;*p<0.05;**p<0.01;***p<0.001;****p<0.0001。
551、结果
552、比较了用以两种不同方向(vh-vl和vl-vh)和两种间隔区长度编码抗-密蛋白-3scfv的4种慢病毒构建体(906-002、906-004、906-007和906-009)转导的car-t细胞的增殖能力。
553、结果表明,与用针对密蛋白-3表达细胞系(rko)的其他构建体906-002、906-004、906-007car转导的t细胞相比,906-009抗-密蛋白-3car t细胞在体外表现出显著更强的抗原特异性增殖(图18)。
554、当与rko-密蛋白-3ko细胞系一起培养时,抗-密蛋白-3car-t细胞均未表现出任何增殖。
555、抗cd19 car-t细胞与密蛋白-3rko细胞一起培养时没有表现出增殖。
556、这些数据预测906-009抗-密蛋白-3car-t细胞可以具有更大的体内增殖能力,从而可能产生更大的抗肿瘤临床活性。这些发现表明,使用抗-密蛋白-3car-t细胞作为结肠癌的癌症免疫疗法将维持针对肿瘤抗原的增殖和细胞毒性响应。
557、实施例7-cdx nsg模型中抗-密蛋白-3car-t细胞活性的体内评估和针对人crcpdx样品的体外评估
558、本研究的目的是评估用抗-密蛋白-3car转导的t细胞在小鼠模型中的体内功效及其在患者衍生的人异种移植(pdx)模型中的体外功能。结果表明,抗-密蛋白-3car-t细胞延长了小鼠的存活并控制了肿瘤的生长。
559、材料和方法
560、为了评估抗-密蛋白-3car-t细胞在体内杀伤肿瘤细胞的功效,使用表达cldn3的结肠癌细胞系ht-29luc。该研究的主要读数是(1)对小鼠肿瘤生长和存活的影响。次要读数包括(2)血清细胞因子释放以评估t细胞激活,(3)通过组织病理学检测肿瘤和小鼠组织中t细胞的分布,以及(4)血液中car t的检测。
561、在患者衍生的人异种移植(pdx)模型中进一步评估了抗-密蛋白-3car-t细胞的功能性。在第0天(d0),解冻pdx细胞,通过流式细胞术表征并接种。第1天(d1),将t细胞解冻并以1:1的比率接种在pdx细胞顶部。第2天(d2),收集上清液并经由msd测定评估细胞因子水平。收获pdx和t细胞,并经由流式细胞术针对cldn3、pd-l1、epcam(肿瘤细胞)和cd69(t细胞)表达进行表征。
562、nsg小鼠
563、在研究启动之前,对用于接种的ht-29luc细胞进行了全面的人和鼠病原体(charles river)筛查,所有结果均为阴性。与此同时,供体的血液经检测对乙型肝炎、丙型肝炎和艾滋病毒i/ii呈阴性。
564、在研究过程中测试了小鼠粪便中是否存在其他病原体。研究中的小鼠以及另一项研究中同一供应商的小鼠的粪便对星状病毒-1和分段丝状细菌(sfb)检测呈阳性。与兽医协商后,认为这两种生物体不具有临床健康影响。据报道,sfb和星状病毒-1都对免疫系统的发育有影响,并且sfb还在炎症调节中发挥作用。
565、肿瘤细胞制备和对nsg小鼠的接种
566、收获ht-29luc细胞并收集上清液用于人和鼠病原体测试,以确认细胞的无病原体状态。对收获的细胞进行计数,随后将0.5x106 ht-29luc细胞皮下(s/c)接种到每只nsg小鼠的右胁腹。
567、肿瘤生长、安乐死和组织收获
568、密切监测小鼠直至研究结束。通过触诊/卡尺测量来测量所有小鼠的肿瘤大小,并每周记录三次,然后每周记录两次体重。
569、根据终点标准诸如肿瘤体积,在各个终点处宰杀小鼠并收获组织。将肿瘤和脾脏(整个组织/器官完整)收集在冰上的pbs中。一半用于组织处理,另一半用10%中性缓冲福尔马林(nbf)固定长达48小时以进行组织病理学检查。收集心脏、肺、结肠、肾、肝、卵巢和脑并直接用10%nbf固定。所有固定组织均供应给gsk tmcp uk histology,ware。
570、t细胞解冻、培养和给药
571、为了确保肿瘤大小在各组之间均匀分布,根据肿瘤体积将小鼠随机分为7-8只小鼠的组。当肿瘤可触及时(约100mm3),car-t细胞经由尾静脉注射以每只小鼠1x107个细胞的剂量给药,如下表10所示。
572、表10:小鼠研究中car-t细胞的给药
573、 组 t细胞 剂量 小鼠/组 a 无t细胞(pbs) na 8 b 对照(抗-cd19)car <![cdata[1x10<sup>7</sup>]]> 7 c 抗-密蛋白-3car(906-009) <![cdata[1x10<sup>7</sup>]]> 8
574、血液中的血清细胞因子测定和car-t细胞检测
575、在t细胞给药前和给药后7天收集所有研究小鼠的血液样品,以评估血清细胞因子的释放,并在给药后第28天收集血液样品,以评估血液中的car-t细胞。
576、通过msd使用以下检测抗体检测收集的小鼠血清样品中的细胞因子:sulfo-tag抗-hu ifn抗体、sulfo-tag抗-hu il-1β抗体、sulfo-tag抗-hu il-2抗体、sulfo-tag抗-huil-4抗体、sulfo-tag抗-hu il-6抗体、sulfo-tag抗-hu il-8抗体、sulfo-tag抗-hu il-10抗体、sulfo-tag抗-hu il-12p70抗体、sulfo-tag抗-hu il-13抗体和sulfo-tag抗hu tnfα抗体。
577、收集给药后第28天仍在研究的每只小鼠的全血并用以下抗体染色:cd45-fitc(1/100稀释);cd3-buv395(1/50稀释);cd8-apcvio770(1/200稀释);cd4-percpvio770(1/50稀释);和lngfr-pevio770(1/600稀释)。
578、pdx共培养和流式细胞术
579、使用五种结直肠癌模型和一种卵巢癌模型建立患者衍生的人异种移植(pdx)模型。pdx结直肠癌细胞模型(cr5052、cr5080、cr5089、cr5030、cr5087)和pdx卵巢癌细胞模型(ov5287)获自crown biosciences。
580、第0天:将pdx细胞悬浮物解冻、计数并以50,000-100,000个细胞/孔接种。
581、使用以下抗体组通过流式细胞术分析来表征剩余的pdx细胞:epcam-bv650(1/600稀释);cldn3-pe(1/10稀释);pdl1-bv421(1/100稀释);cd45-fitc(1/100稀释);lngfr-pevio770(1/100稀释);和cd69-bv786(1/100稀释)。
582、第1天:将t细胞解冻并以1:1car-t细胞与pdx细胞的比率添加到pdx细胞中。使用含有单独pdx细胞和单独t细胞的附加孔。
583、第2天:收集上清液并经受细胞因子测定。此外,收获共培养的细胞并使用与对d0所用相同的组通过流式细胞术进行评估。
584、收集上清液并如上所述进行细胞因子测定。
585、结果
586、肿瘤生长迟缓和存活
587、体内研究的主要目的是评估抗-密蛋白-3car-t细胞在ht-29luc结肠癌体内模型中的功效。
588、在体内给药的同一天,对人t细胞进行了转导效率、记忆和耗竭表型的表型分析。细胞表现出高活力(87%-92%),并通过lngfr染色确定抗cd19car的转导效率为32%,抗-密蛋白-3car的转导效率为35.8%。这与冷冻前t细胞归一化至30%转导效率时获得的转导效率和活力一致。此外,更复杂的t细胞表型分析证实30%的细胞表达lngfr(对于cd19为27%,对于抗-密蛋白-3car为32.7%),并表明两种car的cd8 t细胞比cd4 t细胞更丰富。cd4 t细胞的lngfr表达百分比高于cd8 t细胞。cd3 t细胞的tim3和pdl-1表达率分别为97%和86%-88%。
589、抗-密蛋白-3car-t细胞控制肿瘤生长(图19a-19b)。对来自肿瘤接种位点的组织进行离体组织学分析。没有检测到肿瘤细胞,因此抗-密蛋白-3car-t细胞确实完全摧毁了肿瘤。本研究中的存活时间被定义为“小鼠肿瘤达到1000mm3所需的时间”。每组中肿瘤小于1000mm3的小鼠比例如图19a所示,证实了抗cd19 car-t细胞和抗-密蛋白-3car-t细胞之间的存活时间存在显著差异。
590、从t细胞接种后第30天开始,一些小鼠表现出姿势低下、眯眼、脱发、呼吸困难、步态异常、立毛和体重减轻的迹象。根据动物福利规定,这些小鼠在出现这些症状的最初迹象时就被宰杀。考虑到发病时间,这些症状可能与肿瘤破坏或移植物抗宿主病(gvhd)相关的细胞因子释放综合征(crs)有关。这些临床症状仅在抗-密蛋白-3car-t细胞治疗组中观察到,因为抗cd19 car治疗对照组的所有小鼠由于肿瘤体积较大而在较早的时间点被处死。
591、抗-密蛋白-3 car-t细胞在肿瘤和健康组织中的分布(ihc)
592、通过组织病理学评估抗-密蛋白-3car-t细胞的组织分布和潜在的小鼠组织损伤。本研究的评价表明,两个t细胞给药组的鼠组织中血管周围人t细胞广泛积累。由于抗-密蛋白-3car可以识别小鼠cldn3,因此需要考虑潜在的毒性作用。在给予抗cd19或抗-密蛋白-3car-t细胞的动物中,肝细胞和上皮细胞更新出现非常轻微的增加。此外,没有观察到结肠或肺的上皮损伤。因此,没有发现抗-密蛋白-3car-t细胞相关的组织损伤或鼠内源性靶标破坏的组织学证据。
593、外周血中的car t细胞
594、给药后第28天,对仍在研究中的所有小鼠进行血液的流式细胞术分析,以确定car-t细胞的存在。这些细胞的检测范围为25至4438个car-t细胞计数/ul全血。通过t细胞上的lngfr表达测量的car-t细胞百分比维持在30%-40%左右,并且与给药当天测试的表达相当(图20)。研究组之间没有重大差异。在抗-cd19 car组和抗-密蛋白-3car组中,cd4 t细胞上的lngfr表达频率均高于cd8 t细胞。
595、血清细胞因子水平
596、为了评估血清中的细胞因子水平,在t细胞给药前和d7后从所有小鼠收集样品。如图21a-21b所示,抗-密蛋白3car-t细胞给药的小鼠在治疗后7天显示出增加的ifnγ水平(中位数为225pg/ml,相比之下cd19为32pg/ml)。其他测试的细胞因子没有显示出明显的趋势或测量值低于检测水平。
597、患者衍生的异种移植物(pdx)表征和共培养建立
598、抗-密蛋白-3car-t细胞的功能在患者衍生的人异种移植(pdx)模型中进行了测试。这些模型允许重现人肿瘤中肿瘤细胞的异质性。根据cldn3表达、组织病理学肿瘤特征和体外培养细胞存活,选择了五种结直肠癌模型。此外,选择一种卵巢癌模型作为cldn3低表达者。
599、然后使用pdx样品与抗-密蛋白-3car与抗-cd19 car(阴性对照)t细胞建立共培养。主要读数为:(1)使用肿瘤标志物epcam、pdl-1和cldn3经由流式细胞术表征解冻后的pdx样品(d0),以及(2)通过细胞因子释放测量t细胞激活(对来自24小时共培养物的上清液进行msd测定)。次要读数为:(3)使用肿瘤标志物epcam、pdl-1和cldn3以及t细胞标志物cd45、lngfr(表示car t细胞)和cd69(激活标志物)经由流式细胞术表征共培养样品。这些实验使用ht-29细胞作为cldn3阳性对照,使用rko-ko细胞作为cldn3阴性对照。
600、从pdx模型供应商获得的rnaseq数据表明,epcam将是结直肠(cr)pdx模型的合适肿瘤细胞标志物,但不适用于卵巢(ov)pdx模型。cr模型中epcam阳性细胞群的百分比范围为41%至65%,但在ov pdx样品中仅检测到14%至17%。cr pdx样品的表征表明epcam阳性肿瘤细胞上的cldn3表达为26%至55%(图22)。经由流式细胞术在ov模型中未检测到cldn3(0.29%)。此外,正如预期的那样,在任何实验中的rko-ko细胞(阴性对照)中均未检测到cldn3。d0时pdx样品中表达pdl-1的靶细胞(epcam+cldn3+pdl-1+群体)的百分比低于2%,但在共培养后有所增加,并且在d2时与抗cd19 car-t细胞共培养物相比在抗-密蛋白-3car-t细胞共培养物中升高。
601、如msd测定所测量,在此试点共培养实验中测试的所有pdx模型(cr5030、cr5080、cr5052、cr5087、cr5089、ov5287)和阳性对照(ht-29)诱导抗-密蛋白-3car-t细胞细胞因子释放(ifnγ、il-2和tnf-α),而阴性对照(rko-ko、单独的t细胞以及所有与抗cd19 car t细胞的共培养物)没有诱导t细胞响应(图23)。
602、当将抗-密蛋白-3car-t细胞共培养物与抗cd19 car-t细胞共培养物进行比较时,t细胞的表征显示早期t细胞激活标志物cd69的表达升高(抗-密蛋白-3car-t细胞共培养物中cd45+lngfr+cd69+群体范围为69%至82%,而抗-cd19 t细胞共培养物中为11%至22%)。
603、具有可触知的ht-29luc肿瘤的nsg小鼠接种抗-密蛋白-3car-t细胞或抗cd19car-t细胞,剂量为1x107细胞总数或pbs(无t细胞)。抗-密蛋白-3car-t细胞延长了小鼠的存活时间并控制了肿瘤的生长,这通过肿瘤块的完全破坏(组织学)得到证实。这些数据得到了t细胞给药后d7时血清ifnγ水平升高的支持。因此,抗-密蛋白-3car-t细胞在体内肿瘤杀伤方面表现出高功效。
604、小鼠组织的组织病理学分析表明,两个t细胞给药组的血管周围人t细胞广泛积累。没有观察到抗-密蛋白-3car-t细胞相关组织损伤的证据。这支持了这样的假设:限于健康组织中的紧密连接(tj)的cldn3是抗-密蛋白-3car-t细胞无法进入的。然而,当cldn3错误定位在tj之外时,会被肿瘤中的抗-密蛋白-3car-t细胞识别。
605、总之,抗-密蛋白-3car-t细胞被证明是高效的体内抗癌疗法。
606、为了评价car-t细胞在另一种模型中的功效,使用了衍生自患者的人异种移植(pdx)模型,该模型能够模拟人肿瘤细胞的异质性。它们用于在体外评估抗-密蛋白-3car-t细胞的功能。五种结直肠pdx模型和cldn3阳性对照细胞(ht-29)的实验显示了升高的抗-密蛋白-3car-t细胞细胞因子释放(ifnγ、il-2和tnf-α),而阴性对照(rko-ko共培养物、单独的t细胞以及所有与抗-cd19 car-t细胞的共培养物)都不会诱导t细胞响应。与在相同实验和可比的tnf-α测量中运行的两个cr模型相比,通过rnaseq的cldn3表达非常低的ov模型也诱导了抗-密蛋白-3car-t细胞响应,且ifnγ和il-2水平较低。
607、经由流式细胞术的下游pdx细胞表征表明卵巢模型中没有cldn3表达。由于已证明抗-密蛋白-3car-t细胞对其他密蛋白家族成员没有表现出细胞毒性交叉反应性(见上文),并且在筛选中未观察到脱靶结合效应(见下文),因此卵巢细胞可能表达低于流式细胞术检测水平的低cldn3水平。这与之前使用抗-密蛋白-3car-t细胞的共培养实验一致,该实验显示在cldn3表达非常低的细胞系存在的情况下细胞因子水平增加。正如预期的那样,在任何实验的rko-ko细胞(阴性对照)中均未检测到cldn3。共培养后,与抗cd19对照组相比,抗-密蛋白-3car-t细胞组中靶标表达肿瘤细胞中的pdl-1水平升高。此外,与抗-cd19 car-t细胞相比,抗-密蛋白-3car-t细胞显示出更高的cd69水平,进一步证实了对共培养物的响应。
608、实施例8-抗-密蛋白-3car载体中包含cd20提供了受控抗-密蛋白-3car-t细胞缺失的机制,而不改变抗-密蛋白-3car-t细胞靶向细胞毒活性
609、密蛋白-3的出现伴随着相关风险,即非肿瘤相关的异常密蛋白-3表达可能会重新激活car-t细胞并重新引导细胞毒性t细胞攻击正常细胞上的癌症抗原。为了提高靶向car-t细胞的密蛋白-3的安全性,可以在治疗载体中引入t细胞缺失技术形式的预编程控制安全措施,使t细胞产物对t细胞缺失敏感。
610、细胞表面b细胞抗原cd20是多种治疗抗体的靶标,也即fda批准的利妥昔单抗(rituximab),这是一种i型抗体,可与cd20主要细胞外环的二硫键限制部分结合,并经由补体依赖性细胞毒性(cdc)和抗体依赖性细胞毒性(adcc;golay et al.,2013mabs 5:826-837)诱导细胞凋亡。
611、该研究的目的是i)评价cd20作为有效的car-t细胞缺失技术,ii)评估906_009治疗载体中包含cd20是否会改变906_009car-t细胞对表达密蛋白3的靶细胞的细胞毒性响应,iii)观察表达cd20的car-t细胞中钙通量的任何变化,和iv)预测cd20_906_009_so(抗-密蛋白-3car,剪接位点优化(so)载体)的免疫原性。结果表明,将cd20纳入抗-密蛋白-3car-t细胞治疗策略中可以用作car-t细胞缺失技术。
612、材料和方法
613、为了评估cd20的活性,对用包含cd20消融元件(cd20_906_009)或缺乏cd20消融元件(906_009)的密蛋白-3car载体转导的car-t细胞进行了比较。未转导的t细胞和cd20_zsgreen(表达cd20和zsgreen荧光蛋白的载体)或cd20_cd19(表达cd20和cd19的载体)转导的t细胞被纳入对照。通过cdc和adcc测定评估cd20的靶向t细胞缺失。通过xcelligence细胞毒性测定评估906_009上游包含cd20引起的car-t细胞细胞毒性活性的任何变化。
614、慢病毒转移载体的设计和生成
615、设计编码906_009car上游cd20细胞消融基因的慢病毒(pg3)转移构建体以生成cd20_906_009。除此之外,还设计了具有上游cd20和短间隔cd8α铰链的抗cd19 car分子(镜像906_009car中存在的两种结构),即cd20_cd19_gsk。对序列进行密码子优化并进一步修饰以从序列中去除任何潜在的剪接位点。所得转基因质粒cd20_906_009_so和906_009_so分别具有与其前身cd20_906_009和906_009相同的蛋白质序列。
616、car t细胞的富集
617、转导后第13天,如上文实施例2中所述,使用rapidspheres通过car表达来选择car-t细胞,不同之处在于将细胞重悬于山羊抗小鼠f(ab)2-生物素而不是抗lngfr/cd271ab中。
618、cdc和adcc测定
619、将car-t细胞和对照细胞重悬于染色溶液中。特别是,cd20_906_009car-t细胞用cell trace violet(ctv)染色,906_009car t细胞用cell trace far red(ctfr)染色(ctfr用于对未转导的细胞或仅表达抗-密蛋白-3car的细胞进行染色,并且ctv用于对表达cd20的细胞进行染色)。ctv和ctfr染色细胞由供体以1:1的比例配对。
620、对于cdc测定,然后用利妥昔单抗(mabthera)或抗rsv同种型对照和兔补体(rab)或热灭活的兔补体(hi)处理这些对(图25)。将来自13个供体的总细胞池中的ctv比例针对cd20表达细胞作图,如图26所示。
621、对于adcc测定,从献血单位(gsk-stevenage)获取新鲜血液。如上文所述分离pbmc。然后使用nk细胞生物素抗体和微珠对细胞进行nk细胞阴性选择。然后细胞在ls柱上进行磁力分离,收集未标记的细胞并添加到染色和配对的t细胞中。将共培养物在37℃下孵育20小时。
622、xcelligence细胞毒性测定
623、如上文实施例4中所述建立用于xcelligence杀伤测定的共培养物,其中靶细胞k562和rko-ko与效应细胞(car-t和对照t细胞)以效应细胞与靶细胞1:1的比率共培养。存在的对照是仅靶细胞、仅效应细胞和靶细胞加100%裂解(0.5%triton x)。
624、钙通量分析
625、将car-t细胞和未转导的对照以每孔5x104个细胞接种在细胞培养板中,并在37℃、5%co2下孵育,然后添加含有以下的测定缓冲液:1)毒胡萝卜素(5xfac=18μm,3.6μmfac)和dmso(5xfac=0.6%v/v,0.12%v/vfac);和2)离子霉素(6xfac=4μm,0.67μm fac)。然后通过flipr分析处理过的细胞。
626、cd20由利妥昔单抗根据补体依赖性细胞毒性(cdc)和抗体依赖性细胞毒性(adcc)两者进行靶向
627、为了确认抗-密蛋白-3car-t细胞中包含cd20是否可以通过利妥昔单抗标记疗法细胞以用于缺失,进行了cdc和adcc测定。
628、将治疗性抗-密蛋白-3car-t细胞上的cd20表达水平与成熟的利妥昔单抗靶标b细胞进行比较(图24)。通过使用具有已知人fc结合位点的珠和针对cd20的人mab(分别为抗人quantum simply cellular珠和抗cd20-pe-vio770),使用cd20的中值荧光强度计算潜在cd20结合位点的数量。数据显示,3个供体间cd20_906_009car-t细胞上的cd20结合位点数量的范围为5.16至5.24个,相比之下供体匹配的b细胞范围为5.75至5.9个。cd20_906_009car-t细胞内的cd20+群体范围在35%-41%之间。本文提供的整个cdc和adcc数据中使用的cd20_906_009car-t细胞中cd20+表达的范围为35%-74%,因此该测定中的细胞代表较低的转导率,从而导致以下结论:cd20_906_009car-t细胞的cd20表达与b细胞相当。
629、进行了cdc测定,以确认用利妥昔单抗和补体处理时,表达cd20的抗-密蛋白-3car-t细胞可以缺失。该数据表明,当用兔补体(rab)加利妥昔单抗处理时,ctv染色细胞中发生缺失,而同种型和hi处理的ctv染色细胞(对照)未缺失(图25和26)。缺失的效果还取决于ctv染色细胞内的cd20表达%,其中随着cd20+群体的增加,观察到更多的细胞缺失。进一步分析比较了rab与hi处理条件下的ctv细胞(pctv)比例。
630、由于利妥昔单抗使cd20+细胞缺失的机制尚不完全清楚,并且可能是由cdc和/或adcc实现的,并且因为使用兔补体代替人补体可能无法准确预测人的cdc,因此进行了adcc测定以确认当用利妥昔单抗加nk细胞处理时,表达cd20的抗-密蛋白-3car-t细胞可以缺失。将使用原始cd20_906_009和906_009载体生成的抗-密蛋白-3car-t细胞与剪接位点优化(so)载体cd20_906_009_so和906_009_so进行比较。本文提供的adcc数据集来自3个供体。
631、图27显示针对同种型或利妥昔单抗条件绘制的nk处理与培养基对照相比的pctv比率。重复对供体62的测定,第一次和第二次实验的数据分别标记为1和2。结果表明,原始cd20_906_009和cd20_906_009_socar-t细胞的细胞数量均减少。在供体62中,每个独立测定的原始变体和so变体之间的缺失事件相似,但cd20表达分别相差54%和76%。第二次测定是用新鲜解冻的细胞进行的,这可能会影响结果。还使用新鲜解冻的细胞对供体79进行adcc,这对于cd20_906_009或cd20_906_009_socar-t细胞再次没有显示出惊人的结果。对于cd20_906_009_so,供体87中的car-t细胞缺失比cd20_906_009car-t细胞更大,这可能是由于cd20表达分别为83%和62%。为了增强adcc的效果,通过906_009car表达富集来自供体62和87的cd20_906_009和906_009非冷冻保存car-t细胞。观察到pctv比率存在差异,这可能是由于ctv染色条件下cd20+群体增加所致。
632、cd20不改变906_009 car t细胞对密蛋白-3靶细胞的细胞毒性
633、通过xcelligence测定实时测量具有和不具有cd20的抗-密蛋白-3car-t细胞的细胞毒性,其中使用阻抗测量来追踪细胞生长随时间的变化。来自13个供体的906_009和cd20_906_009car-t细胞靶向表达密蛋白3的细胞系ht-29-luc。未转导的cd20-zsgreen t细胞和cd20_cd19_gsk car-t细胞被纳入对照。每30分钟测量一次细胞毒性,其中缺乏阻抗与肿瘤细胞杀伤相关。由于对照靶细胞的过度汇合,细胞毒性分析仅在最多24小时内有效。图28显示,在20小时时存活的细胞%在cd20_906_009和906_009car-t细胞之间没有显著差异,其中两个值均接近0%,而对照细胞更接近100%存活。图29中的kt50值表明杀伤50%靶细胞所花费的时间在cd20_906_009和906_009car-t细胞之间没有显著差异。
634、图30显示了来自4个供体的so细胞和原始car-t细胞在20小时时存活的细胞%。所有条件在20小时时都处于或接近0%存活细胞,但是cd20_906_009与cd20_906_009_so相比20小时存活细胞%显著较低,并且提示906_009与906_009_so相比较低。此外,cd20_906_009与cd20_906_009_so相比kt50值显著较低,并且提示906_009与906_009_so相比较低(图31)。
635、具有和不具有cd20的car-t细胞中钙通量没有变化
636、为了确定cd20是否影响car-t细胞的钙通量,首先将来自4个供体的未转导t细胞、cd20_906_009_so和906_009car-t细胞暴露于毒胡萝卜素,毒胡萝卜素抑制内质网ca2+依赖性atp酶,导致胞质钙水平增加,这随后通过添加离子霉素来刺激钙流入。dmso被纳入对照,并通过flipr分析处理的细胞。供体99 906_009_socar-t细胞的dmso条件从板上分离,因此生成异常阴性值。图32中的结果表明,未转导的细胞或具有或不具有cd20的car-t细胞之间的钙通量没有差异。
637、本文提供的数据支持在抗-密蛋白-3car-t细胞治疗策略中使用cd20作为car-t细胞缺失技术。
638、cdc数据表明,表达cd20的抗-密蛋白-3car-t细胞被利妥昔单抗标记为缺失。初步adcc数据还表明,使用利妥昔单抗的缺失也适用于nk细胞。cdc和adcc测定两者中car-t细胞缺失的性能取决于cd20+群体,这可能表明在这些体外方法中完全清除cd20+car-t细胞的潜力。在转基因载体中的906_009car上游编码cd20不会影响抗-密蛋白-3car-t细胞的细胞毒性。
639、cd20被认为是b细胞中的钙通道,但与未转导的或906_009car-t细胞相比,cd20似乎不会改变用cd20_906_009_so生成的抗-密蛋白-3car-t细胞的钙通量。
640、实施例9–使用质膜蛋白阵列评估抗-密蛋白-3car-t细胞与预期靶标以外的蛋白质的结合(脱靶结合)
641、本研究的目的是鉴定转导的t细胞的任何脱靶活性。使用一组表达载体通过质膜蛋白阵列评估抗-密蛋白-3car-t细胞与预期靶标以外的蛋白质的结合,该阵列由超过5000个全长克隆组成,覆盖超过3500个不同的质膜蛋白质,其中许多蛋白质由多种变体代表。bcmacar-t细胞作为阳性对照纳入该研究。
642、材料和方法
643、生成car-t细胞以支持预筛选、初步筛选和验证性筛选
644、如实施例1所述,用moi为2.4的bcma-car慢病毒载体(bcma-030)或moi为5的密蛋白3car慢病毒载体(906-009)转导从分离自人血液的pbmc纯化的t细胞。细胞在37℃、5%co2下孵育,并在整个培养期间维持在texmacs培养基和100iu/ml il-2中。转导后12天收获细胞,并以1x108个细胞/ml冷冻在crystor cs5冷冻培养基中。生成未转导的t细胞作为阴性对照。t细胞由一个供体90928生成。
645、bcmacar-t细胞的转导效率通过使用流式细胞仪(macsquant analyzer 10)测量与bcma-af647的结合来确定。抗-密蛋白-3car-t细胞的转导效率通过使用pe缀合的抗lngfr ab和流式细胞术(macsquant analyzer 10)测量lngfr表达来确定。数据使用flowjov10.1分析。
646、质膜蛋白阵列
647、预筛选研究:将未转导的和car转导的t细胞(供体90928)添加到固定的未转染hek293细胞和过表达bcma、密蛋白3、已知t细胞相互作用因子和对照蛋白的hek293细胞的载玻片中,以在初步筛选之前研究背景染色水平。
648、初步筛选:对于初步筛选,使用反向转染在人hek293细胞中单独表达编码全长人质膜蛋白的4070种蛋白质。将细胞在13个微阵列载玻片上一式两份排列并固定。来自供体90928的未转导的和car转导的t细胞用细胞示踪剂红色染料标记,并以预先优化的t细胞与hek293细胞的比例应用于质膜蛋白阵列。
649、验证性筛选:以一式两份点样编码初步筛选中鉴定的命中的载体,并用于反向转染人hek293细胞。设置了重复的载玻片。将来自供体90928的未转导的t细胞和转导的t细胞(每张载玻片3.2x107个细胞)应用于质膜蛋白阵列。
650、通过荧光成像评估结合,并使用imagequant软件(ge)对转导效率进行定量。蛋白质“命中”被定义为相较于背景水平显示出升高信号的重复点。这是通过使用imagequant软件上网格化的图像进行目视检查来实现的。根据重复点的强度,命中被分类为“强”、“中”、“弱”或“非常弱”。
651、结果
652、生成car-t细胞以支持初步筛选和验证性筛选
653、转导后12天测定转导效率。bcmacar-t细胞的转导效率为63.1%,906-009car-t细胞的转导效率为50%。
654、质膜蛋白阵列:预筛选
655、选择供体90928进行初步筛选。hek转导的细胞的点样图如图33a所示。观察到未转导的t细胞与已知t细胞相互作用物(pvr、cd244、tnfsf4、icoslg、cd86)的结合(图33b)。观察到bcma转导的t细胞与bcma转染的hek293细胞的结合(图33c)以及906-009car-t细胞与密蛋白3转染的hek293细胞的结合(图33d)。
656、质膜蛋白阵列:初步筛选
657、通过在imagequant上分析荧光,总共鉴定了28个命中。染色的强度范围为从非常弱到强。
658、质膜蛋白阵列:验证性筛选
659、28个命中的点样图如图34a所示。观察到未转导的t细胞与已知t细胞相互作用物的结合。鉴定了bcmacar-t细胞与表达bcma的hek细胞以强强度的一种特异性相互作用。鉴定了906-009car-t细胞与表达密蛋白3的hek细胞的一种car特异性相互作用(图34d和表11)。在验证性筛选中观察到表达slc6a6的hek细胞与906-009car-t细胞的非常弱的强度结合不一致,但在初步筛选中没有观察到(数据未显示)。
660、表11-car的汇总-特异性命中
661、
662、在对针对过表达4070种人蛋白质的文库的人hek293的结合筛选car-t细胞后,未转导的t细胞显示出与许多已知的t细胞相互作用物的结合。用作阳性对照的bcmacar-t细胞显示出与bcma的强强度单一特异性相互作用。906-009car-t细胞显示出与表达密蛋白3的hek细胞的弱强度结合。
663、实施例10-细胞因子峰体内研究
664、car是可以重新编程t细胞的特异性、功能和持久性的合成抗原受体。它们通常由与t细胞激活结构域(cd3复合物的zeta链)和共刺激结构域(通常为cd28或4-1bb)融合的scfv或sdab组成。与特定配体的接合将促进装备car的t细胞的激活并增强对靶肿瘤细胞的杀伤(june and sadelain2018)。近十年来,嵌合抗原受体(car)-t疗法已成为免疫疗法中一个充满前景的领域,在血液肿瘤中取得了巨大成功,并显示出治疗实体瘤的潜力(jackson,rafiq,and brentjens 2016;fucàet al.,2020)。
665、cldn3属于整合膜蛋白大家族,对于上皮细胞之间紧密连接(tj)的形成至关重要(itallie and anderson 2004)。正常组织结构的破坏是癌症的标志,cldn3表达改变与各种上皮癌的进展有关,包括那些具有高度未满足需求的癌症,如结直肠癌、乳腺癌、胰腺癌和卵巢癌(singh,sharma,and dhawan2010)。据报道,cldn3错误定位在肿瘤tj之外,但不在健康组织中(corsini et al.,2018),这种机制将cldn3转变为car-t细胞靶标,选择性杀伤肿瘤细胞,同时不损害隐藏在紧密连接中的正常细胞。
666、“so-cd20-906_009”是特异性靶向cldn3抗原的人源化car t,由人源化scfv以及cd8铰链、cd3信号传导结构域和4-1bb共刺激结构域组成。“902_007-lngfr”是scfv car-t对照,对人和小鼠cldn3具有相似的亲和力。“cd20-cd19”是具有cd20消融组分的非cldn3car-t对照。
667、炎症引起的组织损伤(即细胞因子释放增加)可能会由于紧密连接的丧失而导致cldn3暴露在健康组织上,从而使其能够接触到cldn3 car t细胞,从而构成潜在的安全风险。本研究的主要目的是评估cldn3 car t/肿瘤细胞接合诱导的细胞因子分泌的潜在增加是否可能由于紧密连接的潜在破坏而导致健康组织的毒性。朝着这个方向,选择了若干时间点,对来自用902_007-lngfr、so-cd20-906_009或cd20-cd19给药的cdx小鼠模型的血清样品中的细胞因子释放进行离体测量。选择时间点是为了确保可以鉴定细胞因子分泌峰值,并随后可以在细胞因子分泌峰值时评估正常组织。msd多重测定用于检测以下细胞因子:ifnγ、il-10、il-12p70、il-13、il-1β、il-2、il-4、il-6、il-8、tnf-α随时间变化。在各个终点对正常组织和肿瘤进行组织病理学评估。
668、材料和方法
669、为了评估cldn3 car t/肿瘤细胞接合诱导的细胞因子分泌增加是否可能因紧密连接的潜在破坏而导致健康组织产生毒性,我们使用了ht-29luc人结直肠癌模型。当肿瘤平均肿瘤体积达到320mm3时,对ht29-luc荷瘤nsg小鼠给药cldn3 car t细胞(so-cd20-906_009、902_007-lngfr)或非靶向对照cd19 car t细胞(cd20-cd19)。进行了细胞因子分泌谱的时程分析。同时还对肿瘤和器官(肺、肝、脾、心脏、结肠、肾、卵巢、脑、眼睛、视神经)进行组织病理学评估。具体而言,有以下研究读数:a)t细胞给药后第3、4、5、7和14天通过msd测量的血清样品中细胞因子的释放(ifn、il-10、il-12p70、il-13、il-1β、il-2、il-4、il-6、il-8、tnf-α),以及b)t细胞给药后第3、4、7和14天肿瘤和器官(肺、肝、脾、心脏、结肠、肾、卵巢、脑)以及t细胞给药后第14天眼睛和视神经的组织病理学评估。时间点“t细胞给药后第5天”仅作为早期时间点(第3天、第4天)、第7天(在之前的体内功效研究中历史上选择的)和晚期时间点(第14天)之间的中间点在血液/血清采集中包含。
670、nod scid γ (nsg)小鼠的采购
671、96只雌性8-9周龄nsg小鼠购自charles river,uk。
672、肿瘤细胞接种(研究第0天)
673、在研究开始之前,将ht29-luc细胞的上清液(3x 200μl)提交用于小鼠/大鼠病原体(charles river)的综合pcr组测试和无菌测试。所有样品均检测为阴性。ht29-luc细胞在接种小鼠之前在mccoy's、10%fbs培养基、5%co2、37℃培养箱中扩增两周。接种前,收获ht29-luc细胞并收集上清液(3x 200μl)用于小鼠/大鼠病原体(charles river)测试和无菌测试以确认细胞的无病原体状态。对收获的ht29-luc细胞进行计数,并于冰上在预冷的pbs:基质胶(1:1)中重悬,至每只小鼠100μl中的终浓度为0.5x 106个细胞。对于总共95只小鼠,细胞需求如下:95x 0.5x 106细胞(细胞剂量/小鼠)x 2(注射器死体积)=9.5x107细胞。因此,总共10x107个细胞重悬于20ml预冷的pbs:基质胶(1:1)中。将细胞保存在冰上并转移至ivsd(8f,动物单元)以将细胞皮下(s/c)接种到每只nsg小鼠的右胁腹。
674、t细胞给药(研究第23天)
675、在转导后第12天和t细胞冷冻之前,提交来自car t细胞(so-cd20-906_009、902_007-lngfr和cd20-cd19)的上清液(3x 200μl)用于小鼠/大鼠病原体(charles river)的综合pcr组测试和无菌测试。所有样品均检测为阴性。所有细胞在转导后第12天被冷冻并保持冷冻状态(-150℃)。预先计算t细胞给药所需的小瓶数量,并在同一天解冻细胞以供t细胞给药使用,如下所述。
676、t细胞给药当天,将car t细胞(so-cd20-906_009、902_007-lngfr和cd20-cd19)在水浴(37℃)中解冻,并转移至含有冷texmacs培养基的50ml试管中,并轻轻地用移液器上下吸取以继续解冻过程。将冷texmacs添加到每个管中以达到50ml的最终体积。rt下300xg离心10分钟后,将细胞沉淀物重悬于冷texmacs中。将细胞在rt下以300xg离心10分钟,然后重悬于温热的texmacs中并计数。然后,将细胞在rt下以300xg离心10分钟,重悬于预冷的pbs中,最终浓度为每只小鼠100μl中1x107个细胞。将细胞保存在冰上并转移至ivsd至动物单元(8f),用于对携带ht29-luc肿瘤的nsg小鼠进行静脉(i.v)注射。详细计算如下:
677、·so-cd20-906_009:交付:5.5x108细胞
678、·902_007-lngfr:交付:6.47x108细胞
679、·cd20-cd19:交付:6.4x108细胞
680、研究设计
681、图39说明了研究设计。简而言之,雌性nsg小鼠在研究第0天(sd)接种ht-29luc。在sd23,小鼠给药car t细胞(当肿瘤达到约320mm3时)。在sd5、sd26、sd27、sd28、sd30和sd37收集血液样品。在sd26、sd27、sd30和sd37收集组织和肿瘤。
682、稳健的研究设计考虑
683、与uk srf一致,研究统计学家和稳健的研究设计指南、随机化和盲法策略如下:
684、随机化:动物在到达时被随机化。此外,在t细胞给药之前,在咨询研究统计学家jack euesden后,根据基于肿瘤体积扩散的正式随机化计划将动物分配到治疗组。当肿瘤达到平均体积约320mm3时,根据肿瘤体积分布对动物进行随机化(基于t细胞给药前一天的肿瘤测量,以便有时间进行随机化决策)。具体而言,计算每笼的平均log10肿瘤体积,并将笼分为两部分——“低”肿瘤体积(低于或等于总体中位数)或“高”肿瘤体积(高于总体中位数)。使用jmp v14进行了具有两个治疗因素(天数和治疗)的随机完整区组设计。对所有12x组进行随机化(不同的治疗和不同的终点/血液采样/肿瘤采集)。此外,离体msd读数也进行了随机化。
685、盲法:研究人员在整个研究过程中均处于盲态。具体而言,ivsd对细胞剂量和治疗是不知情的,科学家支持的t细胞制剂用于给药。此外,msd和组织病理学读数都是盲法。
686、肿瘤细胞接种(研究第0天)
687、s/c肿瘤植入在ii级无菌柜中进行。所有使用的设备在使用前均经过消毒。通过异氟醚-氧气混合物在室中将动物短暂麻醉并移至面对锥体。右胁腹剃毛,然后用酒精擦拭。将细胞重悬于pbs中,然后在冰上与基质胶(1:1pbs/细胞:基质胶)充分混合。每只小鼠皮下注射总体积为100μl的基质胶和含有细胞的pbs溶液。动物被转移到恢复区进行监测直到完全康复,然后再放回笼子中进行监测。
688、t细胞给药(研究第23天)
689、当肿瘤平均体积达到320mm3时,经由尾静脉注射car t细胞,剂量为每只小鼠1x107个细胞。疗法的静脉(i.v.)给药在ii级无菌柜中进行。
690、肿瘤测量、研究计划和个体终点
691、通过卡尺测量所有小鼠的肿瘤大小并每周记录三次。从研究第-21天(小鼠分娩后7天)开始测量所有小鼠的体重。在研究第-16天测量体重后,以2天的间隔记录所有后续测量。使用excel计算肿瘤体积,如下所示:
692、肿瘤体积=肿瘤长度*(肿瘤宽度^2)*0.5
693、本研究中有单独的终点(t细胞给药后第3、4、7和14天)。
694、血液收集
695、在研究第5天(t细胞给药前23天)收集所有小鼠的血液样品,但由于体重较低,#43小鼠(“第3天”终点,组:902_007-lngfr)排除在外。根据正式随机化计划,根据笼id在研究第26、27、28、30和37天(分别是t细胞给药后第3、4、5、7和14天)对小鼠进行后续抽血,如上所述。值得注意的是,血液样品是在所有时间点从所有car t组中收集的。每只小鼠收集大约100μl血液,其中每个样品另外收集5μl血液用于损耗。对于血清样品,将全血收集到serum microtainer管中,并在室温(rt)下凝结至少30分钟。一旦凝结,将血液以14840x g离心3分钟,并将血清转移至micronics管中。将血清冷冻在-80℃直至用于msd测定。根据许可证,每只小鼠在28个滚动天内的最大采血量为小鼠体重的10%。
696、血清细胞因子测定msd
697、按照制造商说明使用10重板进行msd测定:
698、试剂和样品制备:将冷冻小鼠血清样品、商业小鼠血清和v-plex稀释剂解冻并在rt下平衡。根据制造商的说明重构测定校准品。实验期间不使用时,所有试剂和抗体均保存在冰上。
699、校准品和样品稀释:将msd试剂盒提供的校准品1重悬于1ml稀释剂2中,颠倒3次,在rt下平衡15分钟,然后使用短脉冲短暂涡旋。对于连续稀释以生成细胞因子标准品校准曲线:通过将300μl重构的校准品1溶液转移到新鲜的eppendorf管中来制备最高的校准品1浓度。然后,通过将100μl最高的校准品转移至300μl稀释剂2中进行下一次校准品稀释,并通过涡旋充分混合。这种4倍连续稀释再进行5次,以生成7个校准品。第8个小瓶仅填充稀释剂2。纳入额外的校准组(血清标准品)市售小鼠血清以确认回收率:用20%市售小鼠血清在稀释剂2中制备校准品稀释物,如上所述(4倍连续稀释)。最后一瓶(第8瓶)仅在稀释剂2中含有20%小鼠血清。对于样品稀释:所有小鼠血清样品均通过将25μl血清添加到100μl稀释剂2(1比5稀释)中并适当混合来制备。对于检测抗体溶液制备:msd以50x储备溶液单独提供每种检测抗体。工作溶液为1x。然后,在使用前立即检测检测抗体溶液:将每种抗体60μl(总共10个)混合并添加到2.40ml稀释剂3中。对于读取缓冲液制备:msd以4x储备溶液提供了读取缓冲液t。工作溶液为2x。于1个板,将10ml读取缓冲液t(4x)与10ml去离子水混合。
700、测定方案:将板用150μl/孔的洗涤缓冲液洗涤3次。根据板布局,每孔添加50μl校准品或制备的血清样品。接下来,将板在rt下以750rpm摇动孵育2小时。孵育后,用150μl/孔的洗涤缓冲液洗涤板3次,然后添加检测抗体溶液(25μl/孔),并将板在rt下以750rpm摇动孵育2小时。孵育后,将板用150μl/孔的洗涤缓冲液洗涤3次。接下来,将150μl 2x读取缓冲液t添加到每个孔中,然后立即在msd sector 600imager上读取板。
701、肿瘤生长
702、肿瘤体积数据(mm3)在graphpad prism上绘制。使用单因素anova和tukey多重比较检验来比较car t组的各个时间点。使用双因素anova和bonferroni多重比较来比较cart组随时间变化的“t细胞给药后第14天”终点。
703、血清细胞因子测定
704、研究统计学家使用r版本3.6.1内的lme4包中实现的线性混合模型对msd原始数据进行了分析。每种细胞因子均单独建模。完整的数据集可以在elnb:n74766-9中查看。细胞因子释放转化为log10以确保同方差性。固定效应用于car t组和时间(及其相互作用)。使用具有4个自由度的自然样条(由aic确定)对时间进行建模。对板和小鼠使用随机截距,其中每只小鼠具有随机斜率。线性对比用于比较结构/时间点之间的边际平均值,并使用1,000次迭代的多重插补来处理低于量化下限的值,并进行适当的自由度校正(barnard andrubin 1999)。
705、结果
706、雌性nsg小鼠在sd0接种结直肠癌细胞系ht-29luc(0.5x106个细胞/小鼠)。当肿瘤达到约320mm3(sd23)时,小鼠给药car t细胞(so-cd20-906_009、902_007-lngfr或cd20-cd19);(1x107细胞/小鼠)。在sd5(t细胞给药前23天)从所有小鼠中获取血清样品,但由于体重较低,#43小鼠(“第3天”终点,组:902_007-lngfr)排除在外。接下来,在t细胞给药后的以下几天从相应的笼(基于随机化计划)收集血清样品:第3、4、5、7和14天(分别为sd26、sd27、sd28、sd30和sd37)。时间点:3、4、7、14为终点;在安乐死之前进行抽血以进行随后的血清分离。来自终点“第14天”的小鼠也被用于在“第5天”时间点收集血清。对于所有单独的终点,收集肿瘤和组织(肺、肝、脾、心脏、结肠、肾、卵巢、脑)并提交用于组织病理学评估。特别是对于“第14天”终点,还收集了眼睛和视神经。
707、给药so-cd20-906_009、902_007-lngfr或cd20-cd19的cdx小鼠模型中细胞因子随时间的释放
708、按照正式的随机化计划,使用msd 10重测定在随后的3轮中运行所有时间点的所有小鼠的血清样品。为了避免逐轮变异并遵守稳健的研究设计原则,msd测定的随机板布局包括来自所有时间点的样品。ifnγ、il-2和tnf-α分泌的一些关键观察结果(图35)总结如下:
709、ifnγ:
710、·与cd20-cd19对照组相比,902_007-lngfr在第3天、第4天、第5天和第7天时间点与基线显著不同(全部p<0.0001)(图35a-图35b)。
711、·与cd20-cd19对照组相比,so-cd20-906_009在第3天、第4天、第5天和第7天时间点与基线显著不同(全部p<0.0001)(图35a-图35b)。
712、·与第3天、第4天、第5天和第7天时间点相比,902_007-lngfr组在第14天存在统计学显著下降(所有时间点p<0.0001,第3天与第14天相比:p=0.0079)(图35a-图35b)。
713、·与第3天、第4天、第5天和第7天时间点相比,so-cd20-906_009组在第14天存在统计学显著下降(全部p<0.0001)(图35a-图35b)。
714、·902_007-lngfr和so-cd20-906_009组似乎具有不同的动力学;so-cd20-906_009组有从第3天开始较早增加的趋势(图35a)。
715、·在第7天,902_007-lngfr和so-cd20-906_009组均可观察到分泌“峰值”(图35b)。
716、il-2:
717、·与cd20-cd19对照组相比,902_007-lngfr在第4天(p=0.0331)和第5天(p=0.0098)时间点与基线显著不同(图35c-图35d)。
718、·与cd20-cd19对照组相比,so-cd20-906_009在第4天(p=0.0022)和第5天(p=0.0031)时间点与基线显著不同(图35c-图35d)。
719、·与第4天(p=0.582)和第5天(p=0.8862)时间点相比,902_007-lngfr在第14天没有统计学上显著的下降(图35c-图35d)。
720、·与第4天(p=0.0963)和第5天(p=0.0518)时间点相比,so-cd20-906_009在第14天没有统计学上显著的下降(图35c-图35d)。
721、tnf-α
722、·与cd20-cd19对照组相比,902_007-lngfr在第4天(p=0.0377)、第5天(p=0.0094)和第7天(p=0.0291)时间点与基线显著不同(图35e-图35f)。
723、·与cd20-cd19对照组相比,so-cd20-906_009在第3天(p=0.003)、第4天(p<0.0001)、第5天(p<0.0001)和第7天(p=0.0126)时间点与基线显著不同(图35e-图35f)。
724、·与第7天(p=0.0317)相比,902_007-lngfr组在第14天存在统计学显著下降(图35e-图35f)。
725、·与第3天(p=0.0011)、第4天(p<0.0001)、第5天(p<0.0001)和第7天(p=0.0002)相比,so-cd20-906_009组在第14天存在统计学显著下降(图35e-图35f)。
726、总体而言,与cd20-cd19对照组相比,902_007-lngfr和so-cd20-906_009组中t细胞给药后所有细胞因子的细胞因子分泌均增加(图36)。值得一提的是,对于所有细胞因子,so-cd20-906_009在第14天时细胞因子分泌均下降(图36)。
727、902_007-lngfr和so-cd20-906_009对cdx小鼠模型中肿瘤生长的影响
728、在用于本研究之前,两种cldn3 car t细胞(902_007-lngfr或so-cd20-906_009)均经过体外qc测试。简而言之,通过msd测量的细胞因子(ifnγ、il-2和tnf-α)释放来评估902_007-lngfr或so-cd20-906_009的功能活性。具体而言,将902_007-lngfr、so-cd20-906_009、cd20-cd19或未转导的(“ut”)细胞与一组结直肠癌细胞系(包括ht-29luc细胞)共培养约22小时。选择该组以包括表达cldn3靶标的癌细胞系(ht-29luc、rko ko人cldn3)和cldn3表达低/不存在的rko ko细胞系。总体而言,cldn3 car t细胞在体内之前成功通过了qc,并且表明cldn3 car t细胞响应于表达cldn3的结直肠肿瘤细胞而分泌ifnγ、il-2和tnf-α,正如预期的那样。
729、功能评估表明902_007-lngfr和so-cd20-906_009对小鼠cldn3具有交叉反应性。902_007-lngfr和so-cd20-906_009对人cldn3表现出相似水平的细胞毒性(通过细胞面积以相似速率减少显示)。so-cd20-906_009还响应于小鼠cldn3靶细胞和部分杀伤的小鼠cldn3细胞系分泌细胞因子(通过与对照相比细胞面积减少以及测定结束时图像中活细胞和死细胞的混合物显示)。so-cd20-906_009对小鼠cldn3的杀伤响应显著小于902_007-lngfr对小鼠cldn3的杀伤响应。当比较902_007-lngfr对小鼠cldn3和人cldn3的响应时,小鼠cldn3和902_007-lngfr共培养物中死细胞面积的百分比较小。
730、从“第14天”终点开始评估各组小鼠的肿瘤生长动力学(图37)。在sd35(t细胞给药后12天),与给药cd20-cd19的小鼠相比,给药so-cd20-906_009的小鼠肿瘤体积有统计学上显著的减小(p<0.01);效果一直持续到终点(sd37;t细胞给药后14天)(p<0.0001)。值得注意的是,在给小鼠给药之前,将so-cd20-906_009和cd20-cd19的转导效率(t.e.)归一化为63%,以便进行此类比较。总体而言,so-cd20-906_009具有有效的抗肿瘤作用,显示出肿瘤体积的急剧减小。
731、另一方面,从sd33开始,902_007-lngfr有控制肿瘤生长的趋势,尽管与其他car t组相比没有统计学上的显著差异(图37)。这表明902_007-lngfr在体内主动控制肿瘤生长,并且考虑到细胞因子分泌谱,902_007-lngfr似乎在此肿瘤模型中有效。值得注意的是,与其他car分子相比,902_007-lngfr的t.e.较低。具体而言,与cd20-cd19和so-cd20-906_009相比,902_007-lngfr细胞具有几乎一半的t.e.。902_007-lngfr在给小鼠给药之前未归一化。因此,对于902_007-lngfr和其他car t组之间肿瘤生长影响的差异,无法得出任何假设或结论。值得注意的是,本研究并非旨在比较或评估cldn3 car t细胞治疗的肿瘤的肿瘤生长动力学,因为它不是标准疗效研究,而是有一个明确的终点。
732、最后,值得一提的是,在“第4天”或“第7天”终点处,给药cd20-cd19与so-cd20-906_009或902_007-lngfr的小鼠的肿瘤体积没有统计学上的显著差异(图38)。
733、给药902_007-lngfr、so-cd20-906_009或cd20-cd19的cdx小鼠模型中的毒性评估
734、在ht-29luc人结直肠癌nsg小鼠模型中对902_007-lngfr或so-cd20-906_009的毒性进行了2周的研究。对包括肿瘤在内的选定组织进行显微镜检查。组织病理学评估是一项调查的一部分,旨在确定cldn3 car t细胞在稳健的肿瘤接合后可能释放到血液循环中的高循环水平的促炎细胞因子是否可能通过破坏正常组织上皮细胞中的紧密连接导致cldn3暴露来诱导随后的中靶脱肿瘤毒性。
735、902_007-lngfr和so-cd20-906_009均不会在表达鼠cldn3的正常非炎性(无固有或诱导炎症)组织(即肺、肝、脾、心脏、结肠、肾、卵巢和脑)中引起毒性或累积。然而,这两种cldn3 car t产品都能消除人cldn3阳性结直肠癌肿瘤。
736、cldn3在肿瘤组织中的错误定位使得car t细胞疗法可以利用该靶标来选择性杀伤肿瘤细胞。另一方面,炎症引起的组织损伤(即细胞因子释放增加)可能导致健康组织上的cldn3暴露或/和紧密连接的丧失,使其可接近cldn3 car-t细胞,从而构成潜在风险。促炎细胞因子(例如ifnγ和tnf-α)对tj和上皮通透性的影响已有描述(coyneet al.,2002;prasad et al.,2005;capaldo and nusrat 2009)。
737、先前对nsg小鼠进行的体内研究报告称,对已知cldn3定位的正常组织不存在任何car t细胞相关的影响。这一发现令人鼓舞,但就人临床安全性而言并不确定。因此,需要进行体内研究来评估cldn3 car t细胞在稳健的肿瘤接合后是否会释放高水平的促炎细胞因子到血液循环中。此外,还评估了这种细胞因子分泌是否可能通过破坏正常组织上皮细胞中的紧密连接导致cldn3暴露而诱导随后的中靶脱肿瘤毒性。之前使用ht-29luc肿瘤模型和cldn3 car t细胞(各种构建体)进行的体内功效研究评估了t细胞给药前(基线)和t细胞给药后7天的细胞因子分泌。据报道,与基线相比,t细胞给药后7天,与给药非靶向对照cart细胞的小鼠相比,给药cldn3car t细胞的小鼠的ifnγ分泌有所增加。然而,与基线相比,t细胞给药后7天,与给药非靶向对照car t细胞的小鼠相比,给药cldn3 car t细胞的小鼠中观察到tnf-α和il-2的分泌量最少/可忽略不计。尽管这些发现为cldn3 car t细胞在体内的功效提供了关键证据,但细胞因子分泌动力学尚未得到探索。同时,在上述研究中仅在终点时对正常组织和肿瘤进行组织病理学评估。同样,由于在这些研究终点时完成的快速组织恢复,可能错过了评估潜在的中靶脱肿瘤毒性的“窗口”。因此,决定在接近细胞因子分泌峰值的时间点评估毒性。为此,在存在细胞因子分泌升高的情况下,在频繁的时间点研究了细胞因子分泌动力学和cldn3 car t/肿瘤细胞接合效应导致的潜在毒性。
738、朝着这个方向,对带有ht-29luc肿瘤的nsg小鼠中已建立的肿瘤给药cldn3 car t细胞(so-cd20-906_009或902_007-lngfr)或非靶向对照car t细胞(cd20-cd19)。值得注意的是,与之前的体内功效研究相比,t细胞剂量保持不变。为了“拉伸”体内模型以触发高细胞因子分泌水平,t细胞给药时的肿瘤体积比之前的体内功效研究更高。两个cldn3 car t组都显示出ifnγ的分泌“峰值”。尽管早期时间点(第3天、第4天或第5天)和第7天之间没有统计学上的显著差异,但此处并未严格定义分泌“峰值”。值得强调的是,与第3天、第4天、第5天和第7天时间点相比,第14天的ifnγ分泌量出现统计学显著下降。此外,第7天可以被视为ifnγ分泌水平显著较高的最后一个时间点,然后在第14天下降。考虑到这一点,可以表明ifnγ释放在体内系统性达到最大水平,在cldn3 car t细胞给药后第7天达到“峰”。据报道,给药后第7天是kte-x19的分泌“峰”,kte-x19是一种针对复发性或难治性套细胞淋巴瘤患者的抗cd19 car t细胞疗法(wanget al.,2020)。
739、值得注意的是,so-cd20-906_009中的ifnγ分泌水平从早期时间点(第3天)开始升高,并保持这种分布直至第7天。然而,t细胞给药后7天,在所有car t组间,对肿瘤生长没有差异影响。相比之下,so-cd20-906_009在给药12天后显著减少体内肿瘤体积。这表明cldn3 car-t/肿瘤细胞接合后细胞因子的分泌先于体内肿瘤生长控制。
740、重要的是,在这项研究中,so-cd20-906_009和902_007-lngfr在表达鼠cldn3的正常非炎性(无固有或诱导炎症)组织(即肺、肝、脾、心脏、结肠、肾、卵巢和脑)中没有显示出毒性或累积。
741、值得一提的是,组织病理学读数补充了我们通过卡尺测量肿瘤生长的结论,并且与组织病理学相比,卡尺测量的灵敏度可能稍低且发病较晚,因为肿瘤在消融后不会立即内爆。so-cd20-906_009有效地控制肿瘤生长,这与组织病理学读数一致,组织病理学读数显示so-cd20-906_009消融人cldn3阳性结直肠癌肿瘤。然而,组织病理学读数使我们得出结论,902_007-lngfr具有控制肿瘤生长的效力/能力,但该研究终止得太早,无法通过卡尺测量来证明这一点(不是本研究的主要目标)。应该强调的是,本体内研究中,与cd20-cd19和so-cd20-906_009相比,902_007-lngfr具有几乎一半的t.e.。因此,902_007-lngfr需要更多时间来影响肿瘤生长。
742、总之,本研究表明,so-cd20-906_009或902_007-lngfr/肿瘤细胞体内接合诱导的细胞因子分泌增加不会在表达鼠cldn3的正常非炎性(无固有或诱导炎症)组织中引起毒性或累积。
743、实施例11-体内消融实验
744、car是重编程t细胞特异性、功能和持久性的合成抗原受体。“so-cd20-906_009”是特异性靶向cldn3抗原的人源化car-t细胞,由人源化scfv以及cd8铰链、cd3ζ信号传导结构域和4-1bb共刺激结构域组成。
745、据报道,cldn3在肿瘤中错误定位于紧密连接(tj)之外,但在健康组织中不是(corsini等人,2018),这种机制将cldn3转变为car-t细胞靶标,用于选择性杀伤肿瘤细胞,同时不伤害隐藏在紧密连接中的正常细胞。然而,cldn3可能携带中靶脱肿瘤毒性的风险。为了控制这种潜在风险,研究人员研究了能够长期靶向耗竭不适当激活的car t细胞的“消融技术”。这是通过car-t细胞的cd20共表达和抗cd20抗体的应用来实现的。
746、本研究的目的是为通过施用抗cd20 mab利妥昔单抗进行so-cd20-906_009(cd20共表达car)t细胞的体内消融提供原理证明。通过ddpcr、流式细胞术和免疫组织化学(ihc)研究mab施用后血液和组织(脾脏、骨髓、肺和肝脏)中car t细胞的存在。
747、利妥昔单抗(rituxan,在本报告中缩写为rtx)是小鼠-人嵌合抗cd20mab,经fda批准用于治疗b细胞淋巴瘤。rtx在人体中的作用模式(moa)主要由巨噬细胞和自然杀伤(nk)细胞介导(marshall等人,2017)。在小鼠中,它被认为是由骨髓细胞特别是巨噬细胞介导的,而其他报告证明了nk细胞的重要影响(经marshall等人(2017)和其中的参考文献、uchida 2004、shiokawa等人(2010)综述)。在这项研究中,使用了缺乏t、b和nk细胞的nsg-sgm3小鼠系。然而,该品系经由小鼠巨噬细胞保留了吞噬细胞效应功能,并转基因表达人il3、gm-csf和scf,这被证明可以增加小鼠巨噬细胞的存在(nicolini等人,2004)。此外,还向这些小鼠注射了人类pbmc(hpbmc),其中包括nk细胞和单核细胞。该系统促进了rtx的抗体依赖性细胞吞噬作用(adcp)以及抗体依赖性细胞介导的细胞毒性(adcc)机制的使用。在小鼠环境中,经由补体系统的直接细胞死亡和补体依赖性细胞毒性(cdc)对于rtx moa来说非常微不足道,并且根据环境的不同,后者被认为是有利的或不利的(marshall等人,2017)。发现所使用的小鼠模型适合原理证明,但与每个小鼠模型一样,在向患者转化方面存在局限性。在本研究中评估了以下参数:
748、1)流式细胞术分析,以评估最终血样中so-cd20-906_009car-t细胞的数量。
749、2)ddpcr分析,以通过测量研究过程中(前、24小时、72小时和最终)和组织(骨髓、肝脏、肺、脾脏)中最终时间点hiv载体整合到dna中的情况评估小鼠血液中so-cd20-906_009car-t细胞的存在。
750、4)免疫组织化学(ihc)和原位杂交(ish)分析,以鉴定cd3+ t细胞的一般植入和分布、rtx靶细胞的cd20表达、最终时间点组织(骨髓、肝脏、肺、脾脏)中作为so-cd20-906_009载体rna的wpre-04的表达。
751、5)生物分析,以评估最终血清rtx浓度。这是为了确认成功的rtx应用并评估最终水平作为该模型中缺少so-cd20-906_009car-t细胞消融的情况下的潜在解释。这尤其重要,因为据报道,免疫缺陷小鼠品系表现出更高的mab清除率(oldham等人,2020)。
752、6)对组织(心脏、结肠、肾脏、脑、卵巢、肺、肝脏、脾脏)进行组织病理学分析,以进一步了解最终时间点在这种新型nsg-sgm3小鼠品系中car-t细胞对正常健康组织的潜在毒性。
753、尽管没有提出具体权利要求,但这项研究是根据此类研究公认的科学实践进行的。
754、材料和方法
755、小鼠品系:nod.cg-prkdcscid il2rgtm1wjltg(cmvil3,csf2,kitlg)1eav/mloyszj(缩写:nsg-sgm3),10-12周龄雌性。运送后,让小鼠适应10天。
756、随机化:在研究开始前对小鼠进行称重,并根据它们的体重随机分到治疗组(a-d)和最终采样日。
757、样本量基于统计学家的建议,每组十只小鼠,两个笼子,每笼五只小鼠。表12:治疗组以及给药方案和样本量。x表示应用各自的标题。n/a表示不应用(没有细胞)。媒介物表示没有施用mab而是施用了媒介物。
758、
759、研究第-1天:将来自同一供体的hpbmc和so-cd20-906_009car-t细胞在texmacs培养基中解冻、计数、以1:1比例混合、用磷酸盐缓冲盐水(pbs)洗涤一次并在无菌pbs中制备用于给药。t细胞剂量基于之前使用cldn3 car-t细胞的体内功效研究,hpbmc剂量基于内部研究。so-cd20-906_009构建体的转导效率(te)在注射前测量为37.8%,同时检测到32.4%cd20+细胞(n74546-5)。so-cd20-906_009t细胞产物的载体拷贝数(vcn)为每个细胞0.93个拷贝。按照上表12中的方案,将1x107 so-cd20-906_009t细胞或1x107 hpbmc或1x107 t细胞加1x107 hpbmc经由尾静脉(i.v.)在200μl pbs中注射至小鼠中。在整个过程中轻轻搅拌细胞悬浮液,以防止细胞在注射器中沉淀。剩余的细胞用于流式细胞术分析以确认te、cd20表达并评估细胞组成。
760、研究第0天:最终抗体浓度在早晨新鲜制备并按照上表12中的方案通过腹膜内(i.p.)途径以每只小鼠250μg/100μl施用。rtx剂量基于文献(bonifant等人,2016以及valton等人,2018)和该领域专家的咨询意见。使用抗呼吸道合胞病毒(rsv)mab synagis作为同种型对照。这是fda批准用于预防rsv疾病高危儿童因呼吸道合胞病毒(rsv)引起的需要住院治疗的严重下呼吸道疾病的治疗。synagis剂量基于rtx剂量,类似或更高的剂量之前在小鼠模型中使用过但没有任何毒性报告(mejias等人,2004)。使用5%葡萄糖作为媒介物对照。
761、采样:采样时间点基于文献和专家建议(tasian等人,2017,bonifant等人,2016,valton等人,2018,与该领域专家的交流)。在生存期,在mab给药前(mab前)d0以及mab或同种型或媒介物给药后24和72小时,从每只小鼠收集65μl血液进行pcr分析。为了采集血液,将动物放入无菌转移容器中,并在尾部放血前在环境温度为39℃的保温柜中加热约10分钟。最终采样错开于两个最终日(分别为mab后第7天和第8天),以确保可行性和高样品质量。每个最终采样日,每组人道处死五只小鼠并收集样品。如上所述,在研究开始之前,每天每组处死的小鼠是随机化的。
762、将每只小鼠用异氟醚深度麻醉,并经由心脏穿刺采集终末血用于流式细胞术、pcr和血清rtx浓度测定。通过颈部脱臼对小鼠实施安乐死,然后经由摘除心脏停止循环来确认死亡。在一些记录的情况中,血液在最终采血期间凝结成块。这导致so-cd20-906_009中的一只小鼠没有血清样品,并且没有mab ctrl组。
763、随后,采集骨髓、脾脏、肝脏和肺进行pcr和组织学分析。此外,还收集了心脏、结肠、肾脏、大脑和卵巢,用于小鼠品系的一般组织病理学评估。
764、盲法:对主要和次要读数的评估和分析是完全盲法的。本研究中的主要和次要读数是ddpcr、流式细胞术和ihc、ish,用于检测so-cd20-906_009和cd20细胞。第三读数是rtx浓度和一般组织病理学评估。
765、流式细胞术分析
766、接种前接种的so-cd20-906_009和人pbmc成分的表征
767、每孔添加1-2x105个细胞至96孔v底聚丙烯板中进行抗体染色。首先将板离心(300x g)5分钟,弃去上清液并重悬于200μl facs缓冲液中来洗涤样品。重复离心并弃去上清液。然后将样品重悬于100μl fc阻断剂中,并在室温下孵育10分钟。然后加入100μl facs缓冲液洗涤样品,然后离心5分钟,弃去上清液。然后用100μl抗f(ab’)2-生物素对样品进行染色,并在黑暗中于4℃下孵育30分钟。随后进行两次洗涤-首先加入100μl facs缓冲液,离心5分钟并弃去上清液;然后用200μl facs缓冲液重复。然后用100μl抗体混合物(含有hpbmc特异性抗体和链霉亲和素-apc二抗)对样品进行染色,并在4℃下避光孵育30分钟。如上所述再进行两次洗涤,然后将样品重悬于100μl含有dapi的facs缓冲液中。室温避光孵育10分钟后,在bd lsrfortessa x-20流式细胞仪上采集样品。
768、补偿对照的制备:使用ultra comp ebeads制备补偿对照。简而言之,将1滴ultracomp ebeads添加到96孔v形底板的孔中,并按原液浓度添加0.5μl每种抗体缀合物。对于抗f(ab’2)-生物素+链霉亲和素-apc补偿对照,将0.5μl每种试剂添加到珠中。对于dapi补偿对照,将100μl细胞铺板,并添加原液浓度的0.5μl dapi。在黑暗中室温下孵育15分钟后,在bd lsrfortessa x-20上采集补偿对照,并在采集血样之前计算补偿矩阵。
769、小鼠终末血中so-cd20-906_009和人pbmc的表征和计数(流式细胞术)
770、rbc裂解:rbc裂解液按照制造商的说明书制备。收到小鼠全血后,将每只小鼠的大约400μl血液从含有edta的真空采血管转移至含有10ml rbc裂解液的15ml falcon管中。将样品短暂涡旋,然后在室温下孵育10分钟。然后将样品离心(300x g)7分钟,并小心去除上清液。然后将样品重悬在另外的1-5ml rbc裂解液中,并再孵育5分钟以裂解任何剩余的rbc。随后,添加5ml facs缓冲液(dpbs+2%fbs(hi)+0.05%叠氮化钠+2mm edta),然后将样品离心5分钟。除去上清液后,将样品重悬于剩余的上清液中(管中剩余约100-200μl),然后转移至96孔v形底聚丙烯板中进行抗体染色。
771、抗体染色:在准备抗体染色时,首先通过将板离心(300x g)5分钟来洗涤样品,弃去上清液并重悬于200μl facs缓冲液中。重复离心并弃去上清液。然后将样品重悬于100μlfc阻断剂中,并在室温下孵育10分钟。然后加入100μl facs缓冲液洗涤样品,然后离心5分钟,弃去上清液。然后用100μl抗f(ab’)2-生物素对样品进行染色,并在黑暗中于4℃下孵育30分钟。随后进行两次洗涤-首先加入100μl facs缓冲液,离心5分钟并弃去上清液;然后用200μlfacs缓冲液重复。然后用100μl抗体混合物(含有hpbmc特异性抗体和链霉亲和素-apc二抗)对样品进行染色,并在4℃下避光孵育30分钟。如上所述再进行两次洗涤,然后将样品重悬于100-200μl含有dapi的facs缓冲液中。此外,每个样品中还添加了10μlcountbright珠。室温避光孵育10分钟后,在bd lsrfortessa x-20流式细胞仪上采集样品。
772、补偿对照的制备:使用ultra comp ebeads制备补偿对照。简而言之,将1滴ultracomp ebeads添加到96孔v形底板的孔中,并按原液浓度添加0.5μl每种抗体缀合物。对于抗f(ab’2)-生物素+链霉亲和素-apc补偿对照,将0.5μl每种试剂添加到珠中。对于dapi补偿对照,将100μl细胞铺板,并添加原液浓度的0.5μl dapi。在黑暗中室温下孵育15分钟后,在bd lsrfortessa x-20上采集补偿对照,并在采集血样之前计算补偿矩阵。
773、使用ddpcr测量小鼠血液和组织中的so-cd20-906_009 car-t细胞dna从小鼠血液中提取dna
774、根据制造商的说明,使用qiaamp dna micro试剂盒从小鼠血液中提取dna。简而言之,将35μl缓冲液atl添加到65μl血样中,使总体积为100μl,并向其中添加10μl蛋白酶k和100μl缓冲液al。通过涡旋充分混合样品,并在56℃下振荡孵育10分钟。将样品短暂离心以从盖子收集液滴,并添加50μl乙醇。将样品彻底涡旋并在室温下孵育3分钟。将全部裂解物转移至qiaamp minelut柱,盖上盖子,将柱在6000g下离心1分钟,并弃去流出液。添加500μl缓冲液aw2,将样品以6,000x g离心1分钟,并弃去流出液。然后将柱以20,000x g离心3分钟,以使膜完全干燥。然后将qiaamp minelut柱放入干净的1.5ml微量离心管中,向膜中添加20μl无核酸酶水,并在室温下孵育10分钟。通过以20,000x g离心1分钟来洗脱dna。使用nanodrop 2000测量dna浓度。
775、从小鼠组织中提取dna
776、将小鼠器官(肝脏、肺和脾脏)收集到2ml eppendorf safe-lock管中,向其中添加te缓冲液和1个不锈钢珠(直径5mm)。将骨髓沉淀重悬于te缓冲液中,并转移至带有1个不锈钢珠(直径5mm)的2ml eppendorf safe-lock管中。将管放入tissuelyser适配器中并以15hz均质化20秒。重复该均质化步骤直至没有可见的团块残留。对于骨髓样品,两个样品需要额外20秒均质化。对于其他器官,重复均质化三次,导致总均质化时间为80秒。根据制造商的说明,使用promega maxwell rsc组织dna试剂盒从均质化样品中提取dna。将卡盒装入塔盘板中,并将均质化样品添加到卡盒的孔1中。将柱塞放入卡盒的孔8中,并将含有100μl洗脱缓冲液的空洗脱管放入架子的洗脱管区域,然后开始运行。使用nanodrop 2000测量dna浓度。
777、ddpcr
778、使用mlui消化提取的dna,生成适合ddpcr的片段,并在96孔板中制备。对于血液样品,在20μl反应液中消化500ng dna;对于组织样品,在40μl反应中消化1μg dna。按下表所述制备反应并在37℃下孵育15分钟,然后在80℃下孵育5分钟。制备了22μl ddpcr反应,其中含有50ng mlui消化的dna和ddpcr超混合液用于最终浓度为1x的探针。使用的引物的最终浓度为900nm,对于cdkn1a使用的探针的最终浓度为125nm,对于hiv使用的探针的最终浓度为250nm。在22μl反应中,20μl用于液滴生成。样品一式两份运行。使用px1 pcr板密封机在180℃下密封板5秒,并将反应混合物短暂涡旋并离心。使用qx200自动液滴发生器生成液滴,该发生器将样品分成纳升大小的液滴,每个液滴都用作单独的反应。液滴生成后,使用px1 pcr板密封机在180℃下密封板5秒。将板插入pcr热循环仪中并在95℃下孵育10分钟,然后进行40个循环(95℃ 30秒和60℃ 1分钟)。酶在98℃下灭活10分钟,并在液滴读数之前将板冷却至4℃。在液滴读取器上读取液滴,在通道1中测量hiv(fam),在通道2中测量cdkn1a(vic)。
779、血清利妥昔单抗浓度
780、使用基于样品稀释(1比10mrd,最大回收稀释剂)和抗独特型(id)捕获和抗人抗体检测的经过验证的gyrolab免疫测定方法,对小鼠血清样品中的利妥昔单抗进行分析。使用1μl等份血清时,定量下限(llq)为0.3μg/ml。定量上限(hlq)为100μg/ml。含有以3种不同分析物浓度制备并与研究样品一起储存的利妥昔单抗的质量控制样品(qc),根据单独制备的校准标准对每批样品进行分析。为了使分析可接受,不超过总qc结果的三分之一和不超过每个浓度水平结果的二分之一与标称浓度的偏差不超过25%。适用的分析运行满足所有预定义的运行验收标准。简而言之,rexxip f中的生物素化抗利妥昔单抗rexxip a和alexa标记的抗人igg被稀释。制备小鼠血清中的工作溶液。将工作溶液添加至384ldv板上的stock_solution。将对照基质添加到对照孔中。将血清样品添加至stock_solution 384ldv板中并以1,500x g离心5分钟。利用labcyte echo 525将校准品和质量对照添加到pcr板中。将捕获抗体、检测抗体和洗涤缓冲液添加到pcr板中,并将板以3,000x g离心5分钟。最后,将板密封并使用gyrolab xpand运行。
781、结果
782、本研究中使用的so-cd20-906_009car-t细胞产品在初始评估预冻时的te为37.8%。该细胞批次经过adcc和cdc测定,以确认细胞可以在体内研究开始之前在体外被消融。
783、与接种到小鼠中平行,经由流式细胞术评估接种的细胞的细胞组成、te和cd20表达(图42a-42c)。该分析表明,hpbmc中的大多数细胞(51%)是t细胞,其次是单核细胞(21%)和b细胞(21%),只有一小部分是nk细胞(4%)。正如预期的那样,单独的t细胞被证实具有99%的cd3+ t细胞纯度。接受两者的组的hpbmc和t细胞混合物代表1:1的混合比例,其中74%t细胞,其次是11%单核细胞和11%b细胞和仅2%nk细胞。接种当天(解冻后)检测到35%的te(单独使用t细胞的b组为33+2%f(ab’)2+),而38%的t细胞为cd20+。在pbmc和t细胞混合物中,由于同时存在b细胞,cd20+f(ab’)2细胞的百分比略高于接种的t细胞。单独的hpbmc具有占b细胞13%的cd20+f(ab’)2细胞。
784、mab治疗后7或8天的小鼠终末血中的so-cd20-906_009计数和hpbmc组成(流式细胞术)
785、so-cd20-906_009经由f(ab’)2抗体检测。在淘汰当天,从so-cd20-906_009和无mab ctrl小鼠的约400μl血液中回收平均2,293个f(ab’)2阳性细胞(95%ci:1,484-3,544)(图43a-43b,表12-13)。这比在无so-cd20-906_009ctrl小鼠中观察到的平均高17倍,其中平均回收了135个f(ab’)2阳性细胞(95%ci:87-210)–反映了在此测定中观察到的f(ab’)2检测(抗f(ab)2’与t细胞结合)的背景水平。无mab ctrl小鼠和无so-cd20-906_009ctrl小鼠分别代表本研究中用于血液f(ab’)2计数的阳性对照组和阴性对照组。在so-cd20-906_009和mab治疗的小鼠中,与so-cd20-906_009和同种型mab ctrl小鼠相比,mab治疗后7和8天的f(ab’)2计数显著降低。平均而言,mab治疗小鼠的血液中检测到413个f(ab’)2阳性细胞(95%ci:267-639),相比之下同种型mab ctrl小鼠的血液中检测到2,527个(95%ci:1,635-3,906)。此外,同种型mab ctrl小鼠与无mab ctrl小鼠中回收的f(ab’)2计数没有差异,两者均接受相同剂量的t细胞。尽管与同种型mab ctrl小鼠相比,mab处理的小鼠中的f(ab’)2计数显著减少,但f(ab’)2计数仍然高于无so-cd20-906_009ctrl小鼠中的f(ab’)2计数(p值<0.001)。mab治疗的小鼠中的f(ab’)2计数比无so-cd20-906_009ctrl小鼠平均高3倍(平均差异278个计数),相比之下,同种型mab ctrl小鼠的f(ab’)2计数平均高18.6倍(平均差异2,392个计数)。因此,这表明,根据绝对计数,在mab治疗后7和8天,小鼠中f(ab’)阳性细胞显著但不完全消融。
786、表13.来自小鼠终末血的衍生计数(流式细胞术):
787、
788、
789、std=标准。df=自由度。cl=置信区间。
790、表14.小鼠终末血衍生计数的统计分析(流式细胞术)
791、
792、
793、std=标准。df=自由度。cl=置信区间。
794、在回收的f(ab’)2计数中,观察到小鼠之间存在相当大的变异性。这反映在小鼠中回收的总体人类细胞数量中,包括总t细胞计数(图43c)。在无so-cd20-906_009ctrl小鼠中,平均而言,由于接种方案,t细胞计数低于无mab ctrl小鼠或同种型mab ctrl小鼠中的t细胞计数。此外,在小鼠中回收的t细胞计数数量与回收的f(ab’)2计数数量之间观察到正相关-即使在不含so-cd20-906_009t细胞的无so-cd20-906_009ctrl小鼠中也是如此。因此,f(ab’)2计数也被认为是每只小鼠内回收的t细胞计数的一部分,以解释这一点(图43d)。在无mab ctrl小鼠中,淘汰当天f(ab’)2阳性t细胞的比例为平均0.34(95%ci:0.32-0.37)。与注射时观察到的情况相比,这没有变化(图43a)。相比之下,在无so-cd20-906_009ctrl小鼠中,f(ab’)2阳性t细胞的比例显著较低,平均为0.049(95%ci:0.043-0.055)。这反映了在该测定中观察到的f(ab’)2检测的背景水平。同样,在mab治疗的小鼠中,f(ab’)2阳性t细胞的比例也较低,平均为0.055(95%ci:0.047-0.059);这明显低于同种型mabctrl小鼠中f(ab’)2阳性细胞的比例,平均为0.26(95%ci:0.24-0.28)(p值>0.0001)。然而,最重要的是,mab治疗的小鼠中f(ab’)2阳性t细胞的比例与无so-cd20-906_009ctrl小鼠相当(p值为0.35)。因此,这表明基于so-cd20-906_009t细胞的比例,mab治疗后7天和8天小鼠血液中的so-cd20-906_009car-t细胞被高效消融。
795、尽管与无mab ctrl小鼠相比,在同种型mab ctrl小鼠中观察到t细胞内f(ab’)2阳性细胞的比例有所下降(分别为0.26与0.34),但绝对f(ab’)2计数是相当的。此外,在淘汰时在同种型mab ctrl小鼠中观察到的f(ab’)2比例与注射时观察到的比例没有变化。t细胞内f(ab’)2比例的差异是由于所用接种物的成分所致-与不含额外hpbmc的无mab ctrl小鼠相比,同种型mab ctrl小鼠含有更高量的未转导t细胞(由hpbmc贡献)。如前所述,当比较接种前和终末血时,无mab ctrl小鼠和同种型mab ctrl小鼠中t细胞内f(ab’)2阳性细胞的比例保持相等。此外,f(ab’)2上cd20的表达也得以维持,因为在淘汰时血液中共表达car和cd20的so-cd20-906_009的比例与细胞接种时相当(图44)。
796、除了f(ab’)2计数之外,还在淘汰时评估了小鼠血液中的hpbmc组成。在小鼠中回收的hcd45+细胞(代表所有hpbmc和so-cd20-906_009细胞)中,大多数在淘汰时是t细胞(数据未显示)。平均而言,t细胞占同种型mab ctrl小鼠中所有hcd45+细胞的98.44%,而占无so-cd20-906_009ctrl小鼠中所有hcd45+细胞的94.69%。这显著高于注射时-其中t细胞分别占同种型mab ctrl小鼠和无so-cd20-906_009ctrl小鼠中hcd45+细胞的74.03%和51.3%(图42a-42c)。尽管在小鼠血液中可检测到一些b、nk和单核细胞,但它们普遍低于检测灵敏度水平。
797、总之,如通过流式细胞术(f(ab’)2)检测的,mab治疗后7天和8天,小鼠血液中的so-cd20-906_009car-t细胞被有效消除。
798、使用ddpcr检测小鼠样品中的so-cd20-906_009
799、小鼠血液随时间变化
800、在施用mab之前,接受so-cd20-906_009的所有组之间的血液中存在相当的hiv拷贝数(图45a)。正如预期的那样,无so-cd20-906_009组的hiv拷贝水平无法检测到,并且由于大多数值为零而被排除在hiv拷贝分析之外。对于接受so-cd20-906_009的所有组,每组内测得的hiv拷贝数存在相当大的差异。在研究的最终时间点,将小鼠根据mab后第7天和第8天的采样日期进行分组。在这两个最终日,hiv拷贝数没有显著差异。在整个研究过程中,在接受so-cd20-906_009的所有组中观察到总hiv拷贝数稳步下降,这在mab后72小时和最终时间点最为显著。在mab施用后,在mab施用后24小时观察到与同种型mab组相比,mab治疗组中的hiv拷贝显著减少(p<0.0001,图45b)。这对应于mab治疗组的hiv拷贝数减少了85.11%。在mab后72小时和最终时间点也观察到hiv拷贝数减少,其中观察到百分比减少了70.44%和61.56%。
801、mab治疗后7或8天的小鼠组织
802、与血液样品一样,无so-cd20-906_009ctrl组被排除在hiv拷贝分析之外,因为大多数值为零。在研究的最终时间点,将小鼠分为两个淘汰日期(mab后第7天和第8天)。淘汰日期对组织中测量的hiv拷贝有显著影响(f检验,p=0.001),因此该术语包含在统计分析模型中。在所有四种测试组织(骨髓、肝脏、肺和脾脏)中,与同种型mab治疗组相比,mab治疗组的hiv拷贝显著减少(p<0.0001,图46a-46b)。与同种型mab组相比,mab组的hiv拷贝数在骨髓中减少了95.75%、在肝脏中减少了88.05%、在肺中减少了95.75%和在脾脏中减少了98.66%。还值得注意的是,与同种型mab ctrl组相比,无mab ctrl组中测得的hiv拷贝数存在显著差异,这在骨髓、肝脏、肺和脾脏中观察到(p<0.0001)。
803、组织学
804、获得的强有力的证据表明,腹膜内施用后7/8天,rtx消除了so-cd20-906_009,特别是在脾脏中消除,但也在肝脏和肺中消除,达到70%至98%(95%置信区间为30%至100%)。so-cd20-906_009在正常非发炎小鼠组织中不会引起任何毒性,这有助于确定候选药物潜在的中靶脱肿瘤毒性的危险。
805、血清利妥昔单抗浓度
806、测量所有利妥昔单抗治疗小鼠的最终血清利妥昔单抗浓度(μg/ml)(表17)。无so-cd20-906_009ctrl组显示浓度范围为18.038至39.862μg/ml,平均值为28.672μg/ml。mab组显示范围为18.657至38.646μg/ml,平均值为27.372μg/ml。
807、与之前有关hpbmc在免疫功能低下的小鼠品系中植入的报道一致(schultz等人,2012),在细胞输注后8或9天(mab后第7/8天),t细胞代表了血液中的大部分细胞,仅少量植入b细胞或骨髓细胞(数据未显示)。此外,可以在血液和组织中检测到t细胞(图43a-43d、44、45a-45b和46a-46b),如先前在输注后6至7天后的其他研究中所示(valton等人,2018,king等人,2008,bonifant等人,2016,tasian等人,2014)。
808、通过流式细胞术测定的小鼠血液中的绝对f(ab’)2计数表明mab治疗后so-cd20-906_009消融。正如我们观察到的,即使没有接种so-cd20-906_009细胞,血液中总体t细胞较高的小鼠也具有较高的f(ab’)2计数,绝对f(ab’)2计数并不能解释总t细胞植入。当比较无so-cd20-906_009ctrl小鼠和mab小鼠之间的f(ab’)2计数时,这一点尤其重要,因为与mab小鼠相比,无so-cd20-906_009ctrl小鼠接种的总体t细胞较少。同样,考虑到血液中观察到的t细胞计数的小鼠间差异也很重要。因此,f(ab’)2计数是相对于总t细胞计数进行评估的,这样可以更准确地比较小鼠血液中的f(ab’)2计数,不仅可以在小鼠之间进行比较,更重要的是在治疗组之间进行比较。
809、通过流式细胞术在无so-cd20-906_009ctrl小鼠中观察到f(ab’)2的一些背景检测。这是基于一小部分具有观察到的抗f(ab’)2染色的t细胞。根据测定开发工作和每个实验当天运行的已知计数参考对照,预计会出现一些背景f(ab’)2检测,结果表明,在1,000个细胞下,f(ab’)2检测的灵敏度降低(数据未显示)。然而,这不仅限于f(ab’)2阳性细胞,因为所有pbmc群体的检测灵敏度也降低到了1,000个计数以下(数据未显示)。因此,通过流式细胞术不太能确定小鼠血液中低于1,000的精确f(ab’)2计数,其中包括所有so-cd20-906_009和mab小鼠,以及无so-cd20 -906_009ctrl小鼠。尽管如此,它还是能够表明,在mab小鼠(用rtx治疗)的血液中,未检测到高于背景(无so-cd20-906_009ctrl小鼠血液中的f(ab’)2计数)的f(ab’)2计数,因此这表明用mab治疗的小鼠血液中so-cd20-906_009t细胞被高效消融。
810、此外,我们观察到,在同种型mab ctrl小鼠以及无mab ctrl小鼠中,终末血中存在的so-cd20-906_009car-t细胞保留了与接种前水平相当的car和cd20表达。这表明转导的细胞确实在体内细胞表面维持了cd20和car两者的表达。
811、该研究的一个关键终点是比较so-cd20-906_009和mab组与so-cd20-906_009和同种型mab组在血液和组织中的hiv拷贝数,因此计算下降百分比以比较mab和同种型治疗组。通过使用ddpcr,本研究表明,与同种型mab ctrl组相比,mab组血液中的hiv拷贝数有效减少了最高达85.11%,组织中的hiv拷贝数有效减少了最高达98.66%。当比较血液中的hiv计数时,随着时间的推移,所有so-cd20-906_009植入组的hiv总拷贝数稳步下降。这在mab后72小时和研究的最终时间点最为显著。因此,两组(mab和同种型mab ctrl)之间的百分比差异随着时间的推移而减小(mab后24小时为85.11%,最终时间点为61.56%)。因此,百分比变化数据应与mab治疗组中的hiv总拷贝数一起解释,其表明hiv拷贝数持续下降,直到研究的最终时间点。
812、在研究的最终时间点(mab后第7/8天)采集骨髓、肝脏、肺和脾脏,接受同种型mab的所有组织都具有可检测到的hiv拷贝。这证实了组织中存在so-cd20-906_009,并表明so-cd20-906_009从血液重新分布到组织,这可能部分导致随后研究时间点血液中测得的hiv拷贝数下降。在所有研究的组织中,与同种型mab组相比,mab组的hiv拷贝数显著减少。这进一步证实了mab治疗组中so-cd20-906_009t细胞的成功消融。
813、解释此数据时需要注意的一点是,从血液或组织中测量的hiv(或在研究中用作对照的人类参考基因cdkn1a,此处未报告)的拷贝中准确量化so-cd20-906_009细胞数量是不可能的。理论上,可以根据pcr反应中测得的基因拷贝数来估计细胞数量。然而,这将假设在提取过程中完全回收所有dna并在pcr中完全扩增。此外,为了比较样品之间的细胞计数,需要假设所有样品的dna提取效率相同。对血液中已知数量的car-t细胞进行测试并提取的初步实验发现,与加标细胞相比,dna拷贝的回收率较低,并且样品间总dna产量存在差异。通过在所有pcr反应中加载等体积的dna,对样本进行归一化。因此,pcr不应被视为估计总细胞数的准确定量方法,而是使用hiv拷贝数得出任何结论。
814、为了确认rtx的成功应用并评估在不存在so-cd20-906_009car-t细胞消融的情况下的最终水平,测量了最终血清样品中的rtx浓度。我们的结果证实,rtx治疗组中的所有小鼠均接受了rtx给药,并在最终采样时显示出高于10μg/ml的水平。这尤其重要,因为据报道,免疫缺陷小鼠品系表现出更高的mab清除率(oldham等人,2020)。
815、总之,本研究表明,在给定的小鼠模型中,单次rtx剂量即可有效消除so-cd20-906_009car-t细胞。血液中的消融(24小时内)得到了证明,并且能够证明在临床环境中,组织中的消融与血液相比难以接近且具有更低的rtx效率(ema,2005)。
816、表15-用so-cd20-906_009和mab治疗的小鼠与用so-cd20-906_009和同种型mab ctrl治疗的小鼠之间血液hiv拷贝数的百分比变化总结。
817、
818、cl=置信区间
819、表16–用so-cd20-906_009和mab治疗的小鼠以及用so-cd20-906_009和同种型mab ctrl治疗的小鼠组织中hiv拷贝数的百分比变化总结。
820、 组织 hiv拷贝数变化% 较低cl 较高cl p值 肝脏 -88.05 -92.12 -81.87 p<0.0001 肺 -95.75 -97.2 -93.56 p<0.0001 脾脏 -98.66 -99.12 -97.97 p<0.0001 骨髓 -95.75 -97.2 -93.55 p<0.0001
821、cl=置信区间
822、表17-利妥昔单抗治疗小鼠的最终血清利妥昔单抗浓度(μg/ml)。无so-cd20-906_009 ctrl组显示浓度范围为18.038至39.862μg/ml,平均值为28.672μg/ml。so-cd20-906_009和mab组显示范围为18.657至38.646μg/ml,平均值为27.372μg/ml。
823、
824、
825、实施例12–在肺癌中的作用
826、非小细胞肺癌具有高的未满足的患者需求,该需求可以通过car-t细胞疗法来满足。此研究的目的是探究cldn3 car-t细胞在体外对于非小细胞肺癌(nsclc)细胞系的功效。“906-009_lngfr”含有与“so-cd20-906_009”cldn3 car-t细胞相同的scfv、铰链、信号传导部分和共刺激结构域,然而其不含cd20结构域并且含有lngfr标签。
827、首先,研究了大范围nsclc细胞系的cldn3表达并且选择了一组细胞系。随后,进行功能性实验以探究906-009_lngfr car-t细胞(“906-009_lngfr”)对nsclc细胞系的应答。选择用于功能性实验的一组细胞系以覆盖大范围的cldn3表达水平(mrna和蛋白质),感兴趣的疾病亚型(鳞状或腺癌)以及转移性和原发性病理学。将活化和细胞毒性用作为906-009_lngfr对nsclc细胞系的功能性应答的指示器,并且分别通过量化活化因子(ifnγ和颗粒酶b)和膜联蛋白v(annexin v)的表达来进行体外探究。
828、所有表达cldn3的nsclc细胞系均活化906-009_lngfr,导致与ut(“未转导的”)和cd19 mb car-t细胞(“cd19_lngfr”)相比,ifnγ和颗粒酶b的分泌增加。在对表达cldn3的nsclc的应答中也观察到强效的细胞毒性。在除了具有最低水平的cldn3表达的细胞系中的两个(nci-h1650和colo320dm)之外的所有细胞系中均观察到完全杀伤。这与颗粒酶b的水平相关;在其中观察到完全杀伤的所有共培养物都具有1998pg/ml(3个供体的平均值)以上的颗粒酶b水平。在仅观察到部分的、供体特异性的杀伤的nci-h1650和colo320dm共培养物中,量化了显著更低的颗粒酶b水平。
829、在完全杀伤的细胞系中,最低cldn3mrna的细胞系(nci-h1651)和最高cldn3表达的细胞系(ht-29)(9.55和93.93(fpkm),相对cldn为0.004和0.13)两者都能够通过906-009_lngfr诱导相似水平的ifnγ分泌(分别为40,534pg/ml和31,138pg/ml),表明低水平的cldn3能够活化906-009_lngfr。活化的t细胞还与cd19和ut相比分泌更高的颗粒酶b水平,间接地表明906-009_lngfr对于nsclc细胞系的细胞毒性活性。
830、总之,此研究中的数据表明,906-009_lngfr的活化和细胞毒性应答将由表达高至低水平的cldn3的nsclc细胞系诱导。处于流式细胞术检测极限的细胞系也诱导了强烈的应答,显示了car的敏感性。疾病亚型分析和病理学证明,906-009_lngfr car-t细胞将对表达cldn3的nsclc细胞系应答,而与疾病亚型(鳞状或腺癌)和病理学(转移性或原发性)无关。总之,此报告提供了表明nsclc可以是适合于cldn3 car-t细胞的患者群体的体外证据。
831、材料和方法
832、此研究的目的是通过证实在nsclc细胞系中强大的cldn3表达和cldn3 car-t细胞的功能性应答,理解是否可以用cldn3car-t细胞治疗nsclc患者。
833、最初,rnaseq数据用于从三个主要疾病亚群中选择具有不同cldn3水平的细胞系。随后,通过流式细胞术和qrt-pcr分别评估cldn3蛋白和cldn3mrna的表达。基于收集的数据,选择表达高到低水平的靶表达的一系列细胞系用于功能性实验。为了说明nsclc患者群体的多样性,从两种最常见的亚型(腺癌和鳞状细胞癌)转移性和原发性病理学两者中选择细胞系。
834、使用两个关键的读出,活化因子分泌(颗粒酶b和ifnγ)和杀伤(通过膜联蛋白v的表达证实)来评估906-009_lngfr car-t细胞的功能性应答。t细胞活化和靶细胞死亡的组合证实了细胞毒性应答,而单独的活化因子水平可以用于指示细胞毒性应答或在浓度低时提示应答降低。还评估了cldn3的表达以比较在靶细胞铺板(plating)当天对靶标表达的应答。由于crc是ftih研究中的主要适应症,该组中包含在先前的效力测定中使用的大量crc细胞系作为906-009_lngfr的基准。虽然没有提出具体的声明,但此研究是根据此类型研究公认的科学实践进行的。
835、细胞系培养。在共培养之前一至两周,使用补充有10%fbs和1%glutamax的rpmi解冻细胞系。每3-4天分裂细胞,并在用于共培养的接种当天:用tryple收集细胞,并在nucleocounter 202上计数。
836、t细胞解冻。来自供体pr19k133900、pr19c133904和pr19w133916的906-009_lngfr、cd19 mb(cd19 car阴性对照“,cd19_lngfr”)和ut(未转导的)t细胞(在2021n467314中描述的生产)在共培养当天解冻。将t细胞在手中解冻并重悬于10ml的冷texmacs中。将细胞在300xg减速旋转10分钟(rt),并再次重悬浮于冷texmacs中。将细胞悬浮液再次以300xg旋转20分钟,并重悬于5ml冷texmacs中。然后将细胞在nucleocounter 202上计数并等分用于进一步测定。
837、qpcr。rna提取:使用promega maxwell rsc simplyrna cells试剂盒并按照制造商的方案从细胞系沉淀中提取rna。简言之,将细胞沉淀重悬于200μl含有硫代甘油的均化溶液中。然后加入200μl裂解缓冲液后裂解均质化的细胞。然后将裂解的细胞加入到maxwell cartridge的孔1,并将5μl重构的dna酶1加入到孔5。将柱塞加入到孔8并在rsc 48机器上运行cartridge。在50μl无核酸酶的水中洗脱rna,并在cdna合成前储存于-80℃。cdna合成:使用nanodrop 2000测量rna。然后使用4μlsuperscript ivvilotmmaster mix和每个样品1μg的rna按照制造商的方案进行反转录。对于四个样品,产生无rt对照,其含有1μg rna和4μl的无rt master mix。使用c1000触摸热循环仪(touchthermal cycler)将反应物在25℃孵育10分钟,然后在50℃孵育10分钟,接着在85℃孵育5分钟。rt-qpcr:使用taqman基因表达测定(gene expression assays)对人cldn3以及内源参照基因肌动蛋白b(actb)和泛素c(ubc)的cdna进行rt-qpcr。简而言之,用无核酸酶的水将样品cdna预稀释1/5。创建1/5 7点gdna系列稀释。根据制造商的方案,通过混合5μltaqman fast advanced master mix、0.5μltaqman基因表达测定、2.5μl无核酸酶的水和2μl的cdna/gdna(如上制备),建立每个pcr反应物。使用quantstudio 6flex实时pcr系统在microamp光学384孔反应板中进行pcr。
838、初始运行具有gdna污染,因此使用ip08和ubc进行故障排除运行以确定失败原因。iv vilo no rt master mix的污染是运行失败的原因,因此用新鲜的iv vilo cdna合成试剂盒重复上述方法。
839、流式细胞术。通过流式细胞术分析靶细胞系以确定cldn3表达。将细胞悬浮液在facs缓冲液(d-pbs+2%fbs)中洗涤两次,在40μl人trustain fcx fc阻断剂中重悬并在室温孵育10分钟。然后用40μl 2x pe密蛋白-3抗体或pe rea igg1同种型对照抗体(工作浓度为5μg/ml)将细胞染色并在黑暗中室温孵育30分钟。然后将细胞在facs缓冲液中洗涤三次,然后重悬于dapi溶液(1μg/ml dapi在d-pbs中)中。立即使用cytoflex流式细胞仪分析细胞。
840、用于细胞因子检测的共培养设置。在与t细胞共培养的前一天,将靶细胞系分离并计数。洗涤细胞,在300xg离心,以对于每个实验的正确密度重悬于培养基中。然后将2.5×104个细胞接种到96孔板中。第二天,将新鲜解冻并标准化的t细胞以1:1e:t(效应细胞:靶细胞,其中“效应细胞”是经转导的car-t细胞)的比例加入到板,并在37℃、5%co2共培养。每种共培养条件重复三次。24小时后,将板离心,收集上清液并储存于-80℃以量化细胞因子分泌。
841、人ifnγ-细胞因子u-plex msd测定。按照制造商的说明,使用2个细胞因子u-plex板进行msd测定。
842、板制备。通过加入3:2比例的接头:抗体,将生物素化的抗体偶联至接头(ifnγ偶联至接头1,颗粒酶b偶联至接头10)。将混合物涡旋并在室温孵育30分钟。加入终止溶液,接头:抗体:终止溶液为3:2:2,将混合物涡旋,然后在室温孵育30分钟。通过合并并且在终止溶液中稀释接头偶联的抗体1/10来制备包被溶液。将包被溶液涡旋并通过向每个孔加入50μl来包被板。将板密封并在室温振荡孵育1小时。
843、试剂和样品制备。将冷冻样品和稀释液3和2解冻,并平衡至室温。然后将样品板在2000xg旋转3分钟。将测定校准品1在250μl稀释液2中重构并在室温孵育30分钟,并将测定校准品23在冰上解冻。
844、校准品和样品稀释。对于生成细胞因子标准品校准曲线的系列稀释:通过在稀释液2中以1/10稀释校准品1和校准品23来制备第一标准品。然后用4倍系列稀释来制备标准品2至7。样品也在稀释液2中稀释,以使其符合标准曲线的顶部和底部。
845、测定方案。用150μl/孔的洗涤缓冲液(pbs+0.05%吐温)洗涤板3次,并将50μl的校准品或稀释的上清液样品铺板。将平板在室温以至少750rpm振荡孵育2小时。孵育后,用150μl/孔的洗涤缓冲液洗涤板3次,然后向每个孔加入50μl的检测抗体溶液(在稀释剂3中以1/100稀释的ifnγ和颗粒酶b的抗体)。在室温下孵育板,以至少750rpm振荡1小时。孵育后,用150μl/孔的洗涤缓冲液洗涤板3次。接下来,向每个孔加入150μl的msd gold read buffer,并然后立即在msd sector 600成像仪上读板。
846、基于incucyte的杀伤测定
847、板包被。向nunclon delta surface 96孔板的每个孔加入50μl的0.01%多聚-l-鸟氨酸,并将板在4℃孵育过夜。第二天,用150μl pbs洗涤板三次,并在生物安全柜中风干1小时。
848、靶细胞铺板。按上述将靶细胞系分离和计数并且以适当的浓度重悬,以每孔15,000或25,000个细胞接种在50μl体积的共培养基(无酚rpmi+10%fbs+1%glutamax+1%丙酮酸钠+1%neaa)中。单独地确定每个细胞系的接种密度。将平板在37℃用5%co2孵育过夜。
849、t细胞铺板。第二天,将50μl的用于细胞凋亡的膜联蛋白v染料(在共培养培养基中稀释以在150μl总孔体积中达到1:500的终浓度)加入到含有靶细胞的板。板在37℃用5%co2孵育同时制备t细胞。将按上述制备的t细胞以适当的浓度重悬,以在50μl的共培养培养基中达到1:1的靶细胞:t细胞比例。然后将板转移到ncucyte sx5,并在整个实验过程中在37℃用5%co2孵育。
850、图像采集。使用incucyte sx5用10倍放大率的黏附的逐个细胞扫描(adherentcell-by-cell scan)类型获取图像。在phase和nir通道中收集数据。以3小时的间隔每孔获取4个图像持续7天的时间段。
851、结果
852、nsclc细胞系的cldn3表达。
853、评估24个nsclc细胞系以及阳性(ht-29)和阴性(rko ko)crc对照的cldn3 mrna和蛋白的表达。将细胞系培养6周的时间段,并收集样品用于三个不同的流式细胞术和qpcr实验(图47a-47b和表18)。
854、如通过流式细胞术分析所确定的,大多数(16个)的nsclc细胞系由同质的cldn3阳性群体组成,具有反映不同细胞系的细胞表面上各种水平的cldn3的不同mfi(1.2(rko ko)至738(ht-29)标准化mfi)。基于荧光中的群体切换(shift)而非不同群体,在细胞系中,剩下的8个细胞系对cldn3部分阳性,并且一个细胞系为cldn3阴性(nci-h1703)。蛋白质水平的增加主要反映了mrna的增加,尽管有一些异常值,例如nci-h1650。
855、基于表达数据选择了一系列细胞系,目的是在一系列表达水平上显示对nsclc表达cldn3的细胞系的功能性应答,独立于病理学(转移性或原发性两者)和两个主要疾病亚群(腺癌和鳞状)(表19)。选择具有宽范围的cldn3表达水平(基于相对cldn3和%膜结合cldn3群体)的一组12个细胞系来探究906-009_lngfr对低水平以及高水平靶标表达的应答。选择具有部分阳性群体的三个细胞系以及nsclc细胞系nci-h1703,其基于低相对cldn3mrna、0%膜结合的cldn3群体和类似于rko ko(用作阴性对照的cldn3 ko细胞系)的标准化mfi被推定为阴性(表18)。
856、该研究中也包括在本技术中已被表征的几种crc细胞系。选择下列细胞系;具有非常低的cldn3 mrna表达的crc细胞系(colo320dm),以及具有与中等和高cldn3表达的nsclc细胞系相当的cdln3表达水平的三种另外的细胞系(dld1、hct15和ht-29)。已经存在研究cldn3 car-t细胞对细胞系的应答的大量数据,并且在此研究中将这些crc细胞系用作基准。
857、在共培养的接种日(加入t细胞的前一天)再次确认靶细胞中的cldn3表达。注意到实验中cldn3蛋白表达水平的差异(分析为图47b和表18中的标准化mfi)。具体地,在最初的细胞系筛选阶段,一致证明nci-h1650含有部分阳性的低cldn3群体(35%,n=3),标准化的cldn3 mfi大于rko ko(2.7vs 1.4,n=3)。在用于功能性实验的靶细胞接种当天,nci-h1650表达的cldn3水平低于在rko ko中观察到的背景(1.55vs 1.8标准化mfi),并且仅2.28%的cldn3阳性(图54a-54j)。值得注意的是,在显示nci-h1650为35%cldn3阳性的实验中,nci-h1650始终具有低于nci-h 1703的相对cldn3mrna水平(表18)。
858、表18-nsclc细胞系的cldn3表达。在三个实验中通过qpcr(2-δct)和流式细胞术(标准化pe mfi)评估cldn3表达。
859、
860、表18-续
861、
862、
863、表19-用于进一步实验选择的细胞系及其在功能性测定中的用途
864、
865、
866、表20-在限定的相对cldn3水平下评估ifnγ倍数变化(906-009_lngfrvs cd19_lngfr)表达。cl=置信区间。
867、 对比 估计 下cl 上cl p值 0.00037 10.37 4.16 25.86 p<0.001 0.001 227.07 129.2 399.08 p<0.001 0.003 2963.58 1367.58 6422.18 p<0.001 0.01 8076.66 4132.53 15785.1 p<0.001 0.03 14593.88 8859.49 24039.91 p<0.001 0.1 4887.35 2536.91 9415.47 p<0.001
868、表21-在选定的相对cldn3水平下评估颗粒酶b倍数变化(906-009_lngfr vs cd19_lngfr)表达。cl=置信区间。
869、 对比 估计 下cl 上cl p值 0.00037 3.63 2.1 6.25 p<0.001 0.001 36.46 26.05 51.02 p<0.001 0.003 263.98 166.49 418.54 p<0.001 0.01 622.32 417.42 927.79 p<0.001 0.03 534.92 397.29 720.23 p<0.001 0.1 446.28 301.92 659.66 p<0.001
870、表22-906-009_lngfr共培养物中靶细胞杀伤应答的定性总结
871、 细胞系 适应症 供体1 供体2 供体3 ht-29 结肠直肠 是 是 是 rko-ko 结肠直肠 否 否 否 colo 320 结肠直肠 部分 否 否 dld1 结肠直肠 是 是 是 nci-h1650 nsclc 部分 部分 否 nci-h1703 nsclc 否 否 否 nci-h520 nsclc 是 是 是 nci-h2170 nsclc 是 是 是 nci-h1651 nsclc 是 是 是 hcc15 nsclc 是 是 是
872、
873、nsclc细胞系对906-009_lngfr的活化
874、为了探究906-009_lngfr对nsclc细胞系的功效,在906-009_lngfr和靶细胞共培养24小时后,量化活化因子ifnγ和颗粒酶b。由此得到的数据在图49a-49b中呈现为三个供体的平均值。
875、相对cldn3mrna表达高于0.001dct的所有细胞系(高达最高cldn3表达的细胞系ht-29,0.13dct)都使906-009_lngfr car-t细胞活化,导致高于对照水平(ut/cd19_lngfr共培养物)的强健ifnγ和颗粒酶b分泌。在除两种细胞系(一种crc和一种nsclc)以外的所有细胞系中,颗粒酶b的水平都高于800pg/ml。具有较低水平的颗粒酶b的两种细胞系也分泌较低水平的ifnγ,并且显示表达低于0.001的cldn3mrna和处于背景水平的cldn3蛋白。
876、在共培养中包含在已经先前效力测定中使用的具有相似的cldn3水平(低、中和高)的crc细胞系。由906-009_lngfr响应于crc细胞系而分泌的ifnγ和颗粒酶b的水平不高于响应于nsclc细胞系的水平。具有最高cldn3mrna水平的crc细胞系ht-29具有与最高cldn3mrna表达的nsclc细胞系hcc0827(65,415pg/ml ifnγ和3,678pg/ml颗粒酶b)相似的ifnγ和颗粒酶b水平(31,139pg/ml和4,357pg/ml)(表23)。
877、906-009_lngfr的这些应答对表达靶标的细胞是特异性的。cd19_lngfr不分泌高于ut水平的ifnγ和颗粒酶b,并且906-009_lngfr响应于cldn3阴性细胞系nci-h1703和rkoko不分泌这些因子。
878、表达与应答之间的关系。
879、图3所呈现的数据表明,低水平的cldn3可以诱导显著的906-009_lngfr活化应答(通过ifnγ和颗粒酶b分泌来量化)。为了理解处于何种水平的cldn3mrna的激活应答可以达到峰值和稳定期,对表达与应答之间的关系进行了建模(图50a-50b)。然后使用该曲线来估计在特定cldn3表达水平下相对于cd19 mb的倍数变化(表20和表21)。
880、这些模型表明,在低cldn3水平,预期活化因子的统计学显著增加。即使在相对cldn3为0.00037时,估计ifnγ的显著倍数变化(相对于cd19_lngfr)为10.37,颗粒酶b的显著倍数变化为3.63。模型中使用的最高cldn3 mrna水平为0.099(hcc0827 nsclc)细胞系。由于只有少数细胞系显示非常低的cldn3水平,在低表达水平估计相对于cd19_lngfr的倍数变化的统计功效更低;即使如此,显然906-009_lngfr对nsclc细胞系的低水平cldn3表达是有反应的。
881、基于图50a中的曲线,在相对cldn 3mrna表达为~0.02时,ifnγ浓度表现为稳定期。在相对cldn3mrna为0.03时,估计的ifnγ分泌倍数变化比cd19_lngfr高14594倍,显示出对nsclc细胞系的强效活化应答。基于图4b,在较低水平的cldn3表达时在约0.005的相对cldn3mrna的相对cldn3表达时颗粒酶b应答达到稳定。
882、906-009_lngfr诱导nsclc细胞系中靶细胞死亡的效力
883、此工作旨在评估906-009_lngfr在一系列nsclc靶细胞中诱导细胞死亡的能力。在凋亡细胞死亡期间,磷脂酰丝氨酸被外化,这可以通过膜联蛋白v染色可见。为了评估此研究中的靶细胞死亡,在靶细胞与906-009_lngfr共培养的整个持续期间量化膜联蛋白v染色。与906-009_lngfr共培养后,将膜联蛋白v染色的总面积与相位图像共同解释,以评估靶细胞的存在。
884、在几个测试的nsclc细胞系中观察到由906-009_lngfr诱导的靶细胞的完全死亡,这是通过存在表达膜联蛋白v细胞簇和没有可见的膜联蛋白v阴性靶细胞来确定的(图51为crc细胞系和图52为nsclc细胞系)。当在与906-009_lngfr的共培养中观察到靶细胞死亡时,这发生在短的时间范围内(加入car-t细胞后最多4天)。在对于cldn3表达为阴性的nci-h1703细胞系中,在与906-009_lngfr共培养期间没有观察到靶细胞死亡。
885、为了评估906-009_lngfr在表达低水平cldn3的细胞系中诱导靶细胞死亡的能力,将crc细胞系colo320dm和nsclc细胞系nci-h1650与906-009_lngfr一起培养。在两种细胞系中,观察到部分靶细胞死亡,这定义为与cd19_lngfr共培养物相比,906-009_lngfr共培养物中的膜联蛋白v染色增加,以及靶细胞数量减少或完整性降低(图53a-53b)。对于crc细胞系colo320dm,在测试的三个供体中只有一个供体中观察到杀伤,伴随着膜联蛋白v染色的增加和靶细胞数量的减少。在nsclc细胞系nci-h1650中,在所有三个测试的供体中,906-009_lngfr共培养物中的膜联蛋白v染色增加早于cd19_lngfr共培养物,然而,仅在三个测试的供体中的两个供体中观察到靶细胞完整性降低。
886、此研究证明906-009_lngfr cldn3 car-t细胞针对一系列衍生自鳞状细胞癌和腺癌nsclc亚型两者的表达cldn3的nsclc细胞系诱导靶细胞死亡的能力(表22以及图51、52和53a-53b)。
887、为了扩大受益于cldn3 car t细胞疗法的潜在适应症,重要的是要证明对源自感兴趣疾病的一系列细胞系具有强大的功能性应答。此研究旨在通过使用906-009_lngfr与nsclc细胞系的共培养物并确定是否有证据表明cldn3 car-t细胞可以用作对于nsclc的疗法来证明这一点。因此,在此工作中,从具有不同cldn3水平的鳞状和腺癌亚型以及转移性和原发性病理学中选择一组细胞系。
888、有证据表明,通过流式细胞术检测cldn3蛋白是受限的。首先,在部分阳性细胞系中没有观察到有差异的cldn3阳性和阴性群体,与阴性对照相比仅有荧光切换(图54a、54c、54e、54g、54i)。其次,基于功能性实验当天进行的流式细胞术,一些对于cldn3仅部分阳性(dld1-36%和nci-h1651-75%)的细胞系被100%杀伤。
889、此研究中的数据显示906-009_lngfr对一系列nsclc细胞系的效力。在具有高于5.82的cldn3 fpkm的所有细胞系中观察到完全的靶细胞死亡(所有剩余靶细胞的膜联蛋白v表达)(表23)。在所有这些条件下,还存在高于800pg/ml的颗粒酶b分泌。在nci-h520与供体pr19w133916 906-009_lngfr的共培养物中观察到最低水平的颗粒酶b(其中在等同实验中完全杀伤是明显的)(969pg/ml)。这表明此颗粒酶b的水平指示在所有靶细胞中会导致细胞凋亡的应答。因此,所有具有高于此水平的颗粒酶b的细胞系(除非本质上能够通过颗粒酶b逃避t细胞杀伤)都可能被906-009_lngfr杀伤。与靶细胞共培养后,高于969pg/ml的颗粒酶b水平,可以独立于适应症、疾病亚型和病理学而观察到,因此可能与相对cldn3的水平有关。
890、还研究了ifnγ/颗粒酶b与cldn3表达之间的关系,使用此研究中收集的数据以模仿在变化的cldn3水平下活化因子的预期水平。值得注意的是活化应答在低水平的cldn3表达时达到峰值;(对于ifnγ相对cldn3为~0.02,对于颗粒酶b相对cldn3为~0.005)。这种在较低水平cldn3mrna的情况下颗粒酶b分泌的稳定期与完全杀伤相关,进一步表明这种颗粒酶b分泌差异化模式指示杀伤。
891、该组细胞系中包含的四种cldn3阳性crc细胞系通过906-009_lngfr诱导相似水平的ifnγ和颗粒酶b分泌。ht-29(其表达的相对cldn3为0.12,相比之下最高cldn3表达的nsclc细胞系hcc0827的相对cldn3为0.099)没有分泌更高水平的ifnγ(31,138pg/ml,相比于65,414pg/ml),并且分泌相似水平的颗粒酶b(4,357pg/ml,相比于3,678pg/ml),表明无论cldn3阳性细胞中的抗原水平如何,都达到了最高的活化水平。在具有最低水平的cldn3表达(mrna和蛋白)的nsclc和crc细胞系两者中,906-009_lngfr导致的ifnγ分泌也相对较低。总之,这表明nsclc细胞系能够诱导与具有相似表达水平的crc细胞系诱导的应答同样强大的体外活化应答。
892、在906-009_lngfr car-t细胞与nci-h1650的共培养物中观察到ifnγ/颗粒酶b的上调,即使cldn3的基线水平(0.0036相对cldn3和0.61fpkm)。基于来自功能性实验的表达数据,nci-h1650的cldn3蛋白的表达不高于基线水平(1.5标准化的cldn3表达)。然而,在一些共培养中有明显的活化应答(2,525pg/ml ifnγ和220pg/ml颗粒酶b)和部分杀伤。如结果中所示,nci-h1650先前始终显示出比阴性细胞系更高的cldn3蛋白,即使相对cldn3是低的,这表明对于此细胞系,mrna不是蛋白表达的指示。实验之间的差异可能是由于当接近所使用抗体的检测下限时,流式细胞术测定的可靠性降低而导致的。该数据也可能不能代表共培养时的cldn3表达,因为在靶细胞铺板后16小时铺板t细胞。因此,很可能此细胞系表达此研究中使用的流式抗体检测不到的低水平的cldn3,该低水平的cldn3足以诱导活化应答和最小的膜联蛋白v表达。
893、nsclc细胞系nci-h1650的部分杀伤应答通过靶细胞生长的降低控制和部分细胞凋亡(通过膜联蛋白v表达证实)来表征。相比于完全杀伤的细胞系(其中存在969pg/ml或更高的颗粒酶b),这与减少的颗粒酶b分泌(220pg/ml)相关。在流式细胞术的检测极限,这种部分杀伤应答与具有低cldn3蛋白表达的crc细胞系colo320dm相似,但具有比nci-h1703更高的cldn3 mrna。在一个供体(具有最高ifnγ和颗粒酶b浓度)内观察到部分杀伤,并且细胞系继续生长。这表明906-009_lngfr car-t细胞的这种降低的应答是不依赖适应症的。
894、总之,nsclc细胞系诱导了强大的活化应答(估计在低至0.00037的相对cldn的情况下相对于cd19显著的颗粒酶b和ifnγ分泌)和有效的杀伤应答(在相对cldn3高于0.0038的细胞系中100%细胞死亡)。在低水平的cldn3观察到活化和杀伤,而不依赖于病理和疾病亚群。在crc和nsclc细胞系中有相似水平的cldn3表达的情况下,有相似的活化和杀伤应答。这些显示cldn3 car-t细胞的效力的crc细胞系的广泛数据集已经存在,因此对nsclc的相似应答和基准进一步验证了此数据集。在来自两个关键的nsclc亚群(腺癌和鳞状细胞癌)的nsclc细胞系中诱导了靶细胞死亡,表明906-009_lngfr car-t细胞针对来自不同疾病亚型的一系列nsclc细胞系是有效的。
895、还观察到cldn3的表达和活化因子分泌之间的关系对于ifn和颗粒酶b是不同的。这些活化因子的水平在低水平的cldn3表达的情况下达到峰值(在实验当天分别为0.02dct和0.005dct相对cldn3),显示906-009_lngfr car-t细胞对此适应症中表达cldn3的细胞系的敏感性。在相对cldn3mrna为0.0008和更低时也观察到有限的活化和细胞毒性应答,其中仅诱导部分杀伤并且检测到较低水平的ifnγ和颗粒酶b.
896、总之,这证实了表达高和低水平cldn3的一系列nsclc细胞系可以使导致靶细胞死亡的906-009_lngfr car-t细胞活化,表明nsclc可以是对于此疗法感兴趣的适应症。
897、实施例13–cldn3表位定位
898、在本研究中,使用906-009_lngfr评估cldn3 car表位。“906-009_lngfr”含有与“so-cd20-906_009”cldn3 car-t细胞相同的scfv、铰链、信号传导部分和共刺激结构域;然而其不含cd20结构域并且含有lngfr标签。cldn3结合元件保持相同,并且已经证明这两个分子具有相当的功能。产生工具rko靶细胞,其表达用丙氨酸替换野生型残基的不同cldn3突变体。通过与表达突变体的rko靶细胞系共培养后的ifnγ释放来评估906-009_lngfr活化。此外,在流式细胞术中使用906-mab(包含906-009_lngfr中的scfv的单克隆抗体版本)以评估与细胞系的结合。
899、为了鉴定906-009_lngfr的表位,进行在计算机上的(in silico)蛋白质结构分析以预测残基表面可及性。数据用于产生表达不同的用丙氨酸替换候选野生型残基的突变的cldn3版本的工具rko cldn3 ko靶细胞。在cldn3胞外环1和2(ecl-1和ecl-2)两者中产生突变。
900、通过使用流式细胞术测量906-mab与rko ko靶细胞的结合来确定表位。将从3个健康供体产生的906-009_lngfr与rko ko靶细胞共培养之后,通过ifnγ分泌来评估car t活化。如果突变在906-009_lngfr的表位内,则预期结合和活化减少,并且因此与rko kocldn3野生型(wt)细胞相比,906-mab和ifnγ信号减少。
901、与表达wt cldn3的rko细胞相比,906-mab与n38a和e153a突变体靶细胞的结合显著降低。与表达wt cldn3的rko细胞相比,906-009_lngfr与这些突变体的共培养也导致24小时后的ifnγ释放显著减少。数据表明氨基酸n38和e153对于906-009_lngfr的结合和活化是关键的,因此是car结合表位的一部分。数据还显示,906-009_lngfr表位是非线性的,跨越cldn3蛋白(参见例如,seq id no:13)的细胞外环1(n38)和细胞外环2(e153)两者。
902、材料和方法
903、蛋白质结构分析。进行蛋白质结构分析以选择用于细胞系产生的cldn3突变。在ccg(化学计算组)moe(分子操作环境)2018.01或2019.0101中,手动或使用自动moe对齐功能将蛋白质序列对齐。使用ccg moe 2018.01将蛋白质晶体结构相互叠加。将结构中的任何非密蛋白链删除,并且在存在的情况下,在叠加之前将多个密蛋白链分离成离散的标签。使用ccg moe 2018.01或2019.0101中的残基性质功能计算残基表面可及性。在使用多个不同叠加结构的情况下,在microsoft excel中对输出进行分析。将在ccg moe中生成的自动序列对齐用于在excel中手动对齐蛋白质序列,连同相关的表面可及性数据。平均“asa(a^2)”[表面可及面积]和“暴露(%)”[相对于gly-x-gly三肽肽内的残基的表面可及性百分比]值在相关结构中平均化,并且注释为暴露(>36%)或部分暴露(>9%)。使用具有默认参数的ccg moe 2019.0101同源模型函数进行蛋白质同源建模。
904、cldn3突变体靶细胞系的产生。millipore sigma使用15个不同的盒(cassette)的靶向整合产生总共15个单克隆细胞系,每个盒编码驱动cldn3 wt或cldn3单点氨基酸突变体(本文称为“rko ko靶细胞”)表达的ef1α启动子和在rko cldn3 ko细胞(本文称为“rkoko”)中aavs1基因座的gfp。细胞在使用前储存在-150℃。
905、抗cldn 3 906-mab的产生。根据实验n65028-27产生抗cldn3 906-mab,并在biorad与pe外部缀合。
906、906-009_lngfr和ut-t细胞生产。如先前章节所述,生产t细胞并使其标准化。简言之,从人全血中分离cd4/cd8 t细胞,转导并扩增。在低温贮藏和-150℃储存之前,将细胞标准化至30%的转导效率。
907、rko ko靶细胞系的培养。在含有10%fbs、1%glutamax和1%丙酮酸钠的rpmi中培养细胞。在共培养建立的同一天使用流式细胞术分析细胞。
908、用于共培养和流式的rko ko靶细胞系制备。将所有细胞接种于含有10%fbs、1%glutamax和1%丙酮酸钠的rpmi中。将rko ko细胞(cldn3阴性,内部产生)用作阴性对照细胞系,将sigma产生的rko ko cldn3 wt细胞用作阳性对照细胞系。从t75烧瓶中除去培养基,并用pbs洗涤烧瓶,然后向每个烧瓶加入3ml tryple。将细胞放置不超过5分钟并轻敲烧瓶以驱逐(dislodge)细胞。为了使tryplee失活,每个烧瓶加入9ml培养基,并使用nucleocounter nc-250进行细胞计数。将铺板所需的细胞体积转移到falcon管,并在400xg离心5分钟。除去上清液并将细胞重悬于铺板培养基(plating media)中至终浓度为3×105细胞/ml。以100μl中3×104个细胞/孔将细胞一式三份接种到96孔平底板中,并在37℃、5%co2孵育1小时,同时制备用于共培养的t细胞。对于流式细胞术,将1x105个细胞接种到一式两份的96孔v-底板中。
909、t细胞的解冻并与靶细胞共培养。将t细胞(储存于-150℃)解冻至37℃并逐滴转移到10ml温的铺板培养基中。将细胞在400xg离心5分钟,除去上清液并重悬于5ml的铺板培养基中。使用nucleocounter nc-250对细胞进行计数。将细胞以9x104个细胞/孔接种到靶细胞上部,靶细胞:转导的t细胞比例为1:1。在37℃、5%co2将共培养板孵育24小时。
910、流式细胞术。如先前章节所述,接种rko ko靶细胞用于流式细胞术。用流动缓冲液(pbs+2%fbs+2mm edta+0.05%叠氮化钠)加满孔,并将板在300xg离心5分钟。弹掉上清液,将细胞重悬于150μl流式缓冲液中。将板在300xg离心5分钟。弹掉上清液,并在室温将细胞以1:100重悬于50ul igg block中10分钟。孵育后,如上所述将板洗涤两次。将细胞重悬于50ul在流式缓冲液中的稀释的抗体(均为1/300稀释)中或单独的流式缓冲液(未染色的对照)中。细胞在室温下孵育30分钟。孵育后,用150μl流式缓冲液洗涤板两次。然后将细胞以1:200的浓度重悬于100ul含有dapi的流式缓冲液中作为活/死染色。立即在cytoflexs上运行细胞。在快速流速下获取细胞,停止条件为10,000个活细胞(基于总的>单个(singlet)>活的)。
911、msd。共培养板在400xg离心5分钟,并将上清液转移到96孔v底板并在-80℃储存直至msd分析。按照制造商的说明进行msd ifn γ测定。将上清液解冻至室温并在稀释液2中适当稀释。使用板洗涤器用150μl的pbs+0.05%吐温(sodexo)洗涤v-plex msd板三次。将人ifnγ校准品在1000μl的稀释液2中重构,在室温下平衡15分钟并短暂涡旋。使用稀释液2,进行1:4稀释系列以制备8点校准曲线,其包含作为空白的仅稀释液2。每个板装载50μl的校准品和相关样品,密封并在室温振荡孵育2小时。如前所述洗涤板。将检测抗体在稀释液3中稀释(1:50),并向每孔加入25μl。将板密封并在室温振荡孵育2小时。如前所述洗涤板,并向每个孔加入150μl的2x读取缓冲液t,然后在msd sector 600成像仪上读取。
912、数据分析:流式细胞术。使用flowjo分析流式细胞术数据,并在microsoft excel和rstudio中进一步分析。将906-mab的结合确定为pe阳性细胞,其在未染色的对照上被门控(gated),而将gfp表达确定为fitc阳性细胞,其在gfp阴性的rko ko对照细胞系上被门控。门控设置在总细胞>单个(singlet)>活的>906-mab-pe阳性内(图55a)。在flowjo中计算pe阳性细胞百分比(占活细胞的百分比)和中位荧光强度(mfi)的统计学,并将其导出到microsoft excel用于进一步分析。在r版本3.6.3中进行统计分析。简言之,对mfi进行log10转换,并使用细胞系的固定效应和板的随机效应的混合模型,同时在细胞系的固定效应和板的随机效应的混合模型中以线性比例分析%亲本。
913、数据分析:ifnγ释放的msd分析。使用msd workbench软件分析msd数据。将标准品和未知品分配给每个msd板上的相关孔。软件使用来自校准品的原始信号,以使用具有1/y2加权函数的4参数逻辑模型(或s形剂量应答)生成标准曲线。从相对标准曲线内插未知样品,并乘以规定的稀释系数以产生以pg/ml为单位的ifnγ的“计算浓度”。将这些值导出到microsoft excel用于统计分析以及数据绘制以供演示。对细胞因子释放进行log10转换,并使用car、细胞系及其相互作用的固定效应的混合模型。随机效应用于板和供体。
914、结果
915、用于选择突变体细胞系产生的蛋白质结构分析。进行在计算机(in silico)上的蛋白质结构分析以确定氨基酸突变为丙氨酸的优先顺序。氨基酸的优先顺序是基于表面可及性预测,以选择最有可能成为906-009_lngfr结合表位的一部分的氨基酸。依序进行分析,使用初步体外实验以帮助通知每个后续蛋白质分析(数据未显示)。
916、分析1。人cldn4(pdb 5b2g)、小鼠cldn15(pdb 4p79)和小鼠cldn19(pdb 3x29)的蛋白质晶体结构在ccg moe 2018.01中进行了比对和叠加,并计算了仅涵盖cldn4链或涵盖所有结构的平均asa和表面暴露百分比,并将其映射到对齐的cldn3蛋白质序列上。使用表面可及性预测来选择用于丙氨酸扫描诱变的cldn3残基,最初分类为[1]涵盖cldn4链的“暴露”,[2]来自涵盖所有结构的额外“暴露”残基,[3]涵盖cldn4链的“部分暴露”,以及[4]来自涵盖所有结构的额外“部分暴露”残基。线性肽扫描先前已经鉴定细胞外环2(ecl2)潜在为表位的一部分,并且因此在视觉上使用该信息以进一步确定用于丙氨酸扫描诱变的“暴露”残基的优先顺序,如下所列。
917、1.空间相关的ecl2残基:phe146,tyr147,pro149,leu150,pro152和glu153
918、2.空间相关的ecl1环1残基:ile35,gly36,ser37,asn38,ile40和thr41
919、3.空间相关的ecl1环3残基:asp67,ser68,leu69,leu70,ala71,leu72,pro73和gln74
920、4.ecl1环2,加另外的更少空间相关性的ecl1/2残基:ser57,thr58,gly59,gln60,met61,gln62,cys63,lys64,val65,gln77,ala78,asn140,arg144,lys156和glu158
921、分析2。丙氨酸扫描诱变鉴定了ecl2内的残基glu153可能为表位的一部分。使用人cldn4(pdb 5b2g)作为模板产生人cldn3的同源模型。计算ecl1的两个高度表面暴露区(残基35-42和57-61)的平均asa和暴露百分比,并结合与来自丙氨酸扫描输出的对ecl2的接近度,用于将这些ecl1残基按ser37,asn38,gly36,ile35,ile40,thr41,ser57,thr58,gly59,gln60至met61的顺序优先用于丙氨酸扫描诱变。
922、分析3。额外的丙氨酸扫描诱变进一步鉴定了ecl1内的残基asn 38可能为表位的一部分。将此信息映射到ccg moe 2019.0101中的cldn3同源模型上,并与先前的诱变数据相结合,用于通过视觉地选择用于额外的丙氨酸扫描诱变的进一步的残基,如下所示。
923、1.ecl2:phe146,tyr147和gln155
924、2.ecl1:gln43,ile45,gln56,leu70和ala71
925、分析4。人密蛋白3、4、5、6、8、9和17的蛋白质序列在ccg moe 2019.0101中进行人工对齐。cldn4在car-t ifnγ测定中表现出小的信号,而其余列出的密蛋白没有显示任何ifnγ信号。因此,仅在cldn3和后面的密蛋白家族成员之间不同的残基可能是导致观察到的信号缺乏的原因。将(1)与cldn4或(2)与任何其他cldn序列(但不是cldn4)不同的cldn3的细胞外环内的残基独立地映射到cldn3同源模型上。然而,结合对car-t的结合/效力有影响的先前突变的位置,对这些后面的残基在对齐和结构上的分析不能鉴定用于丙氨酸诱变的任何明显的进一步残基位置。
926、分析5。利用ccg moe 2019.0101映射到cldn3同源模型上的所有丙氨酸扫描诱变数据的进一步目视检查用于选择三个额外的用于诱变的残基:ala154,phe34和arg157。最终的rko ko cldn3突变体细胞是基于此蛋白质结构分析产生的,如先前章节所述。
927、906-mab和抗hcldn3结合的流式细胞术分析。为了评估cldn3突变对car t结合的影响,通过流式细胞术评估包含906-009_lngfr结合结构域的scfv的单克隆抗体版本(称为906-mab)与rko ko靶细胞的结合。用于分析的细胞系包含rko ko、cldn3敲除(作为阴性对照包含)、rko ko cldn3突变体细胞(具有各种单氨基酸cldn突变)和rko ko cldn3 wt细胞(阳性对照)。如先前章节所述的选择并产生rko ko cldn3突变体细胞系。
928、906-mab显示与rko ko cldn3 wt细胞系和所有rko ko cldn3突变体细胞的结合(如pe-mfi所示),n38a和e153a突变体细胞系除外,其显示与wt相比显著降低的906-mab-pemfi和%906-mab-pe阳性群体(图55b、55c、55d;表24、25)。如所预期的,906-mab不与rko ko阴性对照细胞系结合。
929、gfp表达在rko ko cldn3 wt和突变体细胞系之间保持相似(图55b),表明906-mab结合的差异不是总cldn3蛋白表达差异的假象(artefact)。
930、这些数据显示,cldn3蛋白的残基n38和e153中的突变导致对906-mab结合的能力降低,表明这些氨基酸参与906-009_lngfr结合表位。
931、表24-906-mab与rko ko cldn3突变细胞结合相比于rko ko cldn3 wt细胞的比较。估计为相对于cldn3 wt的倍数变化mfi,其中1x为相同。cl=置信区间。
932、 细胞系 估计 下cl 上cl p值 rko ko 0.01 0 0.05 p<0.001 f34a 0.4 0.11 1.51 0.28 n38a 0.01 0 0.04 p<0.001 i39a 0.95 0.25 3.6 1 s42a 3.91 1.04 14.73 0.043 q43a 2.68 0.71 10.12 0.216 i45a 3.17 0.84 11.94 0.109 n148a 2.75 0.73 10.39 0.195 p149a 2.03 0.54 7.66 0.545 v150a 2.98 0.79 11.26 0.141 p152a 5.07 1.34 19.11 0.013 e153a 0.01 0 0.05 p<0.001 q155a 3.4 0.9 12.83 0.08 k156a 0.73 0.19 2.76 0.971 r157a 1.31 0.35 4.93 0.985
933、表25-906-mab与rko ko cldn3突变细胞结合相比于rko ko cldn3 wt细胞的比较。估计为相比于cldn3 wt的%亲本的变化,其中0%为无变化。cl=置信区间。
934、
935、表26-与rko ko cldn3 wt细胞(标准化为未转导的t细胞)相比,906-009_lngfr与rko ko cldn3突变体细胞共培养后的ifnγ释放。估计为ifnγ占cldn3 wt中ifnγ的百分比,其中100%为相同。cl=置信区间。
936、
937、
938、906-009_lngfr与rko靶细胞系共培养后的ifnγ-细胞因子分泌。细胞因子分泌是t细胞对抗原结合应答的一部分,并且ifnγ释放的检测用于确定cldn3突变对car t活化的影响。在906-009_lngfr与rko ko靶细胞共培养24小时后,测量ifnγ细胞因子的释放。如所预期的,906-009_lngfr与rko ko细胞(cldn3阴性)的共培养没有诱导单独t细胞对照中的水平以上的ifnγ(数据未显示)。与野生型相比,906-009_lngfr仅与n38a和e153a突变体细胞系共培养后,ifnγ分泌显著减少(两种突变体的倍数变化均为0.01,p<0.001)。将数据标准化为与来自匹配供体的未转导t细胞共培养的ifnγ分泌(图56;表26)。与野生型相比,与s42a、p152a和q155a突变体细胞系的共培养导致少量但显著增加的ifnγ分泌(p<0.05)(表26)。然而,由于相比于野生型细胞,这些突变体的%906-mab-pe阳性细胞群体没有显著减少,并且在与这些突变体细胞共培养后,906-009_lngfr ifnγ的释放也没有显著减少,因此这些对mfi的观察结果不太可能是生物学相关的。这些数据表明,cldn3(参见例如,seqid no:13)蛋白的残基n38和e153的突变导致906-009_lngfr被靶细胞活化的能力降低。
939、此研究的目的是通过确定906-009_lngfr结合和活化所必需的氨基酸残基来鉴定906-009_lngfr表位。通过在两个cldn3细胞外环中将单个氨基酸突变为丙氨酸来产生工具细胞系。使用流式细胞术鉴定这些改变中的哪个将减少car结合(通过906-mab的结合来测量,906-mab是906-009_lngfr scfv结合结构域的单克隆抗体版本),同时评估car t与突变体细胞系共培养后的ifnγ分泌以确定突变是否降低car t活化。
940、在测试的突变中,cldn3氨基酸残基n38和e153的突变仅引起906-mab结合的显著降低。这些突变也专门导致906-009_lngfr活化显著降低。总之,这些数据表明n38和e153残基是906-009_lngfr(和so-cd20-906_009)结合表位的一部分,并且对于906-009_lngfr靶标结合和随后的活化是关键的。这些数据还显示car表位是非线性和不连续的,跨越cldn3蛋白的ecl-1(n38)和ecl-2(e153)。
941、总之,来自此研究的数据显示,当残基n38和e153突变时,906-009_lngfr(和so-cd20-906_009)的活化和结合均降低,提供了有力证据表明这些氨基酸在cldn3 car表位中是关键的。
942、尽管本文已经显示和描述了本发明的优选实施方案,但是对于本领域技术人员来说显而易见的是,此类实施方案仅作为示例提供。在不脱离本发明的情况下,本领域技术人员现在可以想到许多变化、改变和取代。应当理解,在实践本发明时,可以采用对本文所述的本发明的实施方案的各种替代。
943、序列表
944、seq id no:1:906cdrh1
945、nywvh
946、seq id no:2:906cdrh2
947、riepnssgsqynekfkn
948、seq id no:3:906cdrh3
949、gvmvpldy
950、seq id no:4:906cdrl1
951、kasqdinryia
952、seq id no:5 906cdrl2
953、ytstlqp
954、seq id no:6 906cdrl3
955、lqyetlys
956、seq id no:7:906vh
957、qvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvss
958、seq id no:8:906vl diqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleik
959、seq id no:9:甘氨酸-丝氨酸接头
960、ggggsggggsggggsggggs
961、seq id no:10:cd8前导序列
962、malpvtalllplalllhaarp
963、seq id no:11:906scfv(vl-vh方向)
964、diqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvss
965、seq id no:12:906_009完整car序列
966、malpvtalllplalllhaarpdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssastttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
967、seq id no:13:人密蛋白3
968、msmgleitgtalavlgwlgtivccalpmwrvsafigsniitsqniweglwmncvvqstgqmqckvydsllalpqdlqaaralivvaillaafgllvalvgaqctncvqddtakakitivagvlfllaalltlvpvswsantiirdfynpvvpeaqkremgaglyvgwaaaalqllggallccscpprekkytatkvvysaprstgpgaslgtgydrkdyv
969、seq id no:14:人密蛋白3ecl2
970、wsantiirdfynpvvpeaqkremgagly
971、seq id no:15:pvvp表位
972、pvvp
973、seq id no:16:编码906scfv的nt序列(vl-vh方向)
974、gacatccagatgacccagagccctagcagcctgagcgccagcgtgggagacagggtgaccatcacctgcaaggccagccaggacatcaacaggtacatcgcctggtaccagcagaagcccggcaaggcccccaagctgctgatccactacaccagcaccctgcagcccggcgtgccctctaggtttagcggcagcggcagcggcaccgacttcaccctgaccatcagcagcctccagcccgaggacttcgccacctactactgcctgcagtacgagaccctgtacagcttcggccagggcaccaagctggagattaagggcggaggtgggagcggcggaggaggcagcggcggaggcggtagcgggggcggaggcagccaggtgcagctcgtgcagagcggagccgaggtgaaaaagcccggaagctctgtcaaggtgagctgcaaggccagcggctacaccttcaccaactactgggtgcactgggtgaggcaggctcccggacagggcctggagtggatgggcaggatcgagcccaacagcagcggcagccagtacaacgagaagttcaagaacagggtgaccatcaccgccgacaagagcaccagcaccgcctacatggaactgagcagcctgaggagcgaggacaccgccgtgtattactgcgccaggggcgtgatggtgcccctggactactggggccagggcaccctggtgacagtgagcagc
975、seq id no:17:编码906_009完整car序列的nt seq
976、atgaccacccccaggaactccgtgaacggcaccttccccgccgagccaatgaagggccctatcgctatgcagagcggccccaagcccctgttcaggaggatgtcaagcctcgtgggccctacccagagcttcttcatgagggagagcaagaccctgggcgccgtgcagatcatgaacggcctcttccatatcgccctgggcggcctgctgatgatccccgctggcatttacgcccccatctgcgtgaccgtgtggtatcccctgtggggcggcatcatgtacatcattagcgggagcctgctggccgccaccgagaagaactctcggaagtgcctggtgaagggcaagatgatcatgaacagcctgagcctcttcgccgcca
977、tctccggcatgatcctgagcatcatggacatcctgaacatcaagatcag
978、ccacttcctgaagatggaaagcctcaacttcatcagggcccacacccc
979、ctacatcaacatctacaactgcgagcccgccaatcccagcgagaagaa
980、cagccccagcacccagtactgctacagcatccagagcctgttcctcgg
981、catcctgagcgtgatgctgatcttcgccttcttccaagagctggtgatc
982、gccggcatcgtggagaacgagtggaagaggacctgcagcaggccaaa
983、gagcaacatcgtgctgctgagcgccgaggagaagaaggagcagacta
984、tcgagatcaaggaggaggtggtgggcctgacagagaccagcagccag
985、cccaagaacgaggaggacatcgagatcatccccatccaggaggagga
986、ggaggaggaaaccgagaccaacttccccgagcccccccaggatcagg
987、agtctagccccatcgagaacgacagcagccccggcagcagggccaaa
988、aggagcggcagcggcgcaaccaacttcagcctgctgaagcaggccgg
989、agacgtggaggagaatcccggcccaatggcactgccagtcaccgctct
990、gctgctgcccctggccctgctgctgcacgccgccaggcccgatattca
991、gatgacccagtccccctctagcctgagcgccagcgtgggcgacagggt
992、gaccatcacctgcaaggccagccaggacatcaacagatacatcgcctg
993、gtaccagcagaagcccggcaaggcccccaagctgctgatccactacac
994、cagcaccctgcagcccggcgtgcctagcagatttagcggcagcggcag
995、cggcaccgacttcaccctgactatcagcagcctgcagcccgaggactt
996、cgccacctactactgcctgcagtacgagacactgtacagcttcggcca
997、gggcaccaagctggaaattaaaggcggaggcggcagcggcggcggc
998、ggctcaggcggcggaggcagcggcggcgggggcagccaggtgcagc
999、tggtccagagcggcgccgaggtgaaaaagcccggcagcagcgtgaa
1000、agtgtcctgcaaggccagcggctacaccttcaccaactactgggtgca
1001、ctgggtccggcaggcccccggccagggactggagtggatggggagga
1002、tcgagcctaacagcagcggcagccagtacaacgagaagttcaagaac
1003、agggtgaccatcaccgccgacaagagcaccagcaccgcctacatgga
1004、gctcagcagcctgcgcagcgaagacaccgccgtgtattactgcgccag
1005、gggcgtgatggtgcccctggactactggggacagggcaccctggtga
1006、ccgtgagcagcgcctctaccacaacccccgctcccaggccccccaccc
1007、ctgcccccaccattgcctcacaacccctgagcctgaggcccgaggcct
1008、gtaggcccgccgccggaggcgccgtgcacaccaggggcctggacttc
1009、gcctgcgacatctatatctgggcccccctggccggaacctgtggcgtgc
1010、tgctcctgagcctggtgatcaccctgtactgcaagcggggcaggaaga
1011、agctgctgtacatcttcaagcagcccttcatgaggcccgtccagacca
1012、cccaggaggaggacgggtgcagctgcaggtttcccgaagaggagga
1013、aggcggctgcgagctgagggtcaagtttagcaggagcgccgacgctc
1014、ccgcctaccagcaagggcagaatcagctctacaacgagctgaacctg
1015、ggcaggagggaggagtacgacgtgctggacaaaaggaggggcaggg
1016、accccgagatgggcggcaagcccagaaggaagaacccccaggaggg
1017、cctgtacaacgagctgcagaaggacaaaatggccgaggcctacagcg
1018、agatcggcatgaagggcgagaggaggaggggcaagggccacgacgg
1019、cctgtaccagggcctgagcaccgctaccaaggacacctacgacgccct
1020、gcacatgcaggccctgcctcccagatga
1021、seq id no:18:906scfv(vh-vl方向)
1022、qvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleik
1023、seq id no:19:cd8跨膜结构域
1024、iyiwaplagtcgvlllslvitlyc
1025、seq id no:20:4-1bb共刺激结构域
1026、krgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcel
1027、seq id no:21:cd3z胞内信号传导结构域
1028、rvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1029、seq id no:22:人cd20
1030、mttprnsvngtfpaepmkgpiamqsgpkplfrrmsslvgptqsffmresktlgavqimnglfhialggllmipagiyapicvtvwyplwggimyiisgsllaateknsrkclvkgkmimnslslfaaisgmilsimdilnikishflkmeslnfirahtpyiniyncepanpseknspstqycysiqslflgilsvmlifaffqelviagivenewkrtcsrpksnivllsaeekkeqtieikeevvgltetssqpkneedieiipiqeeeeeetetnfpeppqdqesspiendssp
1031、seq id no:23:p2a切割位点
1032、gsrakrsgsgatnfsllkqagdveenpgp
1033、seq id no:24:包括hcd20和906_009car序列的多肽
1034、mttprnsvngtfpaepmkgpiamqsgpkplfrrmsslvgptqsffmresktlgavqimnglfhialggllmipagiyapicvtvwyplwggimyiisgsllaateknsrkclvkgkmimnslslfaaisgmilsimdilnikishflkmeslnfirahtpyiniyncepanpseknspstqycysiqslflgilsvmlifaffqelviagivenewkrtcsrpksnivllsaeekkeqtieikeevvgltetssqpkneedieiipiqeeeeeetetnfpeppqdqesspiendsspgsrakrsgsgatnfsllkqagdveenpgpmalpvtalllplalllhaarpdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssastttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1035、seq id no:25:906_004完整的car序列
1036、malpvtalllplalllhaarpqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikastttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1037、seq id no:26:人密蛋白3ecl1
1038、rvsafigsniitsqniweglwmncvvqstgqmqckvydsllalpqdl qaar
1039、seq id no:27:906_007完整的car序列
1040、malpvtalllplalllhaarpdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssaseskygppcppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgkiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1041、seq id no:28:906_010完整的car序列
1042、malpvtalllplalllhaarpdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssaseskygppcppcpiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1043、seq id no:29:906_002完整的car序列
1044、malpvtalllplalllhaarpqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikaseskygppcppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgkiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1045、seq id no:30:906_005完整的car序列
1046、malpvtalllplalllhaarpqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikaseskygppcppcpiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1047、seq id no:31:间隔区l
1048、eskygppcppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk
1049、seq id no:32:间隔区s
1050、tttpaprpptpaptiasqp lslrpeacrpaaggavhtrgldfacd
1051、seq id no:33:间隔区xs
1052、eskygppcppcp
1053、seq id no:34:不具有cd8前导序列的906_009完整的car序列
1054、diqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssastttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1055、seq id no:35:不具有cd8前导序列的906_004完整的car序列
1056、qvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikastttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1057、seq id no:36:不具有cd8前导序列的906_007完整的car序列
1058、diqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssaseskygppcppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgkiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1059、seq id no:37:不具有cd8前导序列的906_010完整的car序列
1060、diqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikggggsggggsggggsggggsqvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssaseskygppcppcpiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1061、seq id no:38:不具有cd8前导序列的906_002完整的car序列
1062、qvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikaseskygppcppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfqstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgkiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
1063、seq id no:39:不具有cd8前导序列的906_005完整的car序列
1064、qvqlvqsgaevkkpgssvkvsckasgytftnywvhwvrqapgqglewmgriepnssgsqynekfknrvtitadkststaymelsslrsedtavyycargvmvpldywgqgtlvtvssggggsggggsggggsggggsdiqmtqspsslsasvgdrvtitckasqdinryiawyqqkpgkapkllihytstlqpgvpsrfsgsgsgtdftltisslqpedfatyyclqyetlysfgqgtkleikaseskygppcppcpiyiwaplagtcgvlllslvitlyckrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelrvkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalppr
- 还没有人留言评论。精彩留言会获得点赞!