γδT细胞的工程化及其组合物的制作方法
背景技术:
1、对癌症t细胞免疫疗法日益增长的关注集中在工程化的t细胞作为治疗部分的明显能力上。伽马德尔塔t细胞(γδt细胞)代表在其表面上表达独特、定义性γδt细胞受体(tcr)的t细胞的子集。此tcr由一个伽马(γ)和一个德尔塔(δ)链组成。人γδt细胞可广泛地分类为一种或两种类型:外周血液驻留γδt细胞和非造血组织驻留γδt细胞。大多数血液驻留γδt细胞表达vδ2tcr,而此现象在组织驻留γδt细胞之中不太常见,后者更频繁地使用vδ1和/或其他vδ链。
2、相对于αβt细胞,缺少用于高效转导γδt细胞以表达所需转基因的方法。因此,在此领域中需要用于转导γδt细胞以产生足够品质和数量的γδt细胞群以用作疗法,例如用作过继性t细胞疗法的改进方法。
技术实现思路
1、在一个方面,本发明的特征在于通过用具有β逆转录病毒假型和逆转录病毒科病毒载体骨架的病毒载体转导γδt细胞群来产生工程化的γδt细胞群的方法。β逆转录病毒假型可以是狒狒内源性病毒(baev)。β逆转录病毒假型可以是rd114。
2、在一些实施方案中,逆转录病毒科病毒载体骨架是逆转录病毒载体骨架(例如,慢病毒骨架、γ逆转录病毒骨架,或α逆转录病毒骨架)。
3、工程化的γδt细胞可以是vδ1t细胞。工程化的γδt细胞可以是vδ2t细胞。工程化的γδt细胞可以是非vδ1/vδ2t细胞。
4、在一些实施方案中,病毒载体包括转基因。转基因可编码细胞表面受体(例如,嵌合抗原受体(car))和/或细胞因子(例如,分泌细胞因子或膜结合细胞因子)。在一些实施方案中,转基因编码il-15(例如,分泌il-15或膜结合il-15)。在一些实施方案中,病毒载体包括第一转基因和第二转基因。在一些实施方案中,第一转基因编码car并且第二转基因编码装甲蛋白(例如,细胞因子,例如,il-15,例如,分泌il-15或膜结合il-15)。
5、在一些实施方案中,car靶向cd19、cd20、ror1、cd22、癌胚抗原、甲胎蛋白、ca-125、5t4、muc-1、上皮肿瘤抗原、前列腺特异性抗原、黑色素瘤相关抗原、突变的p53、突变的ras、her2/neu、叶酸结合蛋白、hiv-1包膜糖蛋白gpl20、hiv-1包膜糖蛋白gp41、gd2、cd123、cd33、cd138、cd23、cd30、cd56、c-met、间皮素、gd3、herv-k、il-llrα、κ链、λ链、cspg4、erbb2、egfrviii、vegfr2、组合her2-her3、组合her1-her2、ny-eso-1、滑膜肉瘤x断点2(ssx2)、黑色素瘤抗原(mage)、由t细胞识别的黑色素瘤抗原1(mart-1)、gp100、前列腺特异性抗原(psa)、前列腺特异性膜抗原(psma)、前列腺干细胞抗原(psca)、g9d2,或其组合。
6、在另一个方面,本发明的特征在于产生工程化的γδt细胞群的方法。所述方法包括提供起始γδt细胞群以及在不存在病毒载体的情况下,培养起始γδt细胞群持续第一培养期以产生启动的(primed)γδt细胞群。所述方法还可包括在有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的启动的γδt细胞的量的具有β逆转录病毒假型的病毒载体存在下,培养启动的γδt细胞群持续第二培养期,由此产生工程化的γδt细胞群。
7、在一些实施方案中,病毒载体的量有效转导至少20%的启动的γδt细胞。
8、在一些实施方案中,第一培养期为1天或更长时间(例如,1天、2天、3天、4天、5天、6天、7天、8天、9天、10天,或更长时间,例如,1-3天、3-5天、5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为2天或更长时间(例如,2天、3天、4天、5天、6天、7天、8天、9天、10天,或更长时间,例如,1-3天、3-5天、5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为5天或更长时间(例如,5天、6天、7天、8天、9天、10天,或更长时间,例如,5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为7天或更长时间(例如,7天、8天、9天、10天,或更长时间,例如,7-10天,或更长时间)。
9、在一些实施方案中,第二培养期为2天或更长时间(例如,2天、3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天,或更长时间,例如,2-4天、4-7天、7-10天、10-14天,或更长时间)。在一些实施方案中,第二培养期为7天或更长时间(例如,8天、9天、10天、11天、12天、13天、14天,或更长时间,例如,7-10天、10-14天,或更长时间)。
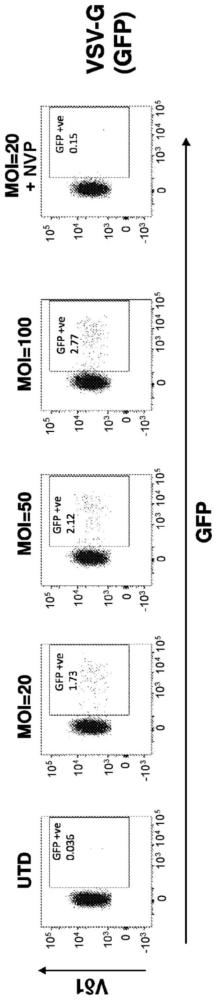
10、在一些实施方案中,启动的γδt细胞群表达asct-1和/或asct-2。在一些实施方案中,启动的γδt细胞群缺少vsv-g进入受体(例如,ldl受体)的功能性表达。
11、在一些实施方案中,病毒载体以不大于10(例如,不大于5,例如,约1至约5)的感染复数(moi)与启动的γδt细胞一起培养。
12、在另一个方面,本发明的特征在于通过以下方式产生工程化的γδt细胞群的方法:提供起始γδt细胞群;以及在il-15和有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的起始γδt细胞群的量的具有β逆转录病毒假型的病毒载体存在下,培养起始γδt细胞群来,由此产生工程化的γδt细胞群。
13、在一些实施方案中,起始γδt细胞群缺少asct-1和/或asct-2的表达。在一些实施方案中,工程化的γδt细胞群表达asct-1和/或asct-2。起始γδt细胞群可缺少vsv-g进入受体(例如,ldl受体)的功能性表达。
14、在一些实施方案中,病毒载体以不大于10(例如,不大于5,例如,约1至约5)的moi与起始γδt细胞群一起培养。
15、在一些实施方案中,病毒载体具有β逆转录病毒假型baev或rd114。
16、在一些实施方案中,病毒载体包括逆转录病毒科病毒载体骨架。逆转录病毒科病毒载体骨架可以是逆转录病毒载体骨架(例如,慢病毒骨架、γ逆转录病毒骨架,或α逆转录病毒骨架)。
17、工程化的γδt细胞可以是vδ1t细胞。工程化的γδt细胞可以是vδ2t细胞。工程化的γδt细胞可以是非vδ1/vδ2t细胞。
18、在一些实施方案中,病毒载体包括转基因。转基因可编码细胞表面受体,例如,嵌合抗原受体(car)和/或细胞因子(例如,分泌细胞因子或膜结合细胞因子)。在一些实施方案中,转基因编码il-15(例如,分泌il-15或膜结合il-15)。在一些实施方案中,病毒载体包括第一转基因和第二转基因。在一些实施方案中,第一转基因编码car并且第二转基因编码装甲蛋白(例如,细胞因子,例如,il-15,例如,分泌il-15或膜结合il-15)。
19、在一些实施方案中,car靶向cd19、cd20、ror1、cd22、癌胚抗原、甲胎蛋白、ca-125、5t4、muc-1、上皮肿瘤抗原、前列腺特异性抗原、黑色素瘤相关抗原、突变的p53、突变的ras、her2/neu、叶酸结合蛋白、hiv-1包膜糖蛋白gpl20、hiv-1包膜糖蛋白gp41、gd2、cd123、cd33、cd138、cd23、cd30、cd56、c-met、间皮素、gd3、herv-k、il-llrα、κ链、λ链、cspg4、erbb2、egfrviii、vegfr2、组合her2-her3、组合her1-her2、ny-eso-1、ssx2、mage、mart-1、gp100、psa、psma、psca、g9d2,或其组合。
20、在另一个方面,本发明的特征在于通过用病毒载体转导γδt细胞群来产生表达car的γδt细胞群的方法,所述病毒载体包括编码car的转基因;β逆转录病毒假型;和逆转录病毒科病毒载体骨架。
21、在另一个方面,本发明的特征在于通过用病毒载体转导γδt细胞群来产生表达car和装甲蛋白的γδt细胞群的方法,所述载体包括编码car的第一转基因;编码装甲蛋白的第二转基因;β逆转录病毒假型;和逆转录病毒科病毒载体骨架。在一些实施方案中,装甲蛋白是细胞因子(例如,膜结合细胞因子或分泌细胞因子(例如,膜结合il-15或分泌il-15)。
22、在一些实施方案中,β逆转录病毒假型是baev。在其他实施方案中,β逆转录病毒假型是rd114。
23、在一些实施方案中,病毒载体包括逆转录病毒科病毒载体骨架。逆转录病毒科病毒载体骨架可以是逆转录病毒载体骨架(例如,慢病毒骨架、γ逆转录病毒骨架,或α逆转录病毒骨架)。
24、γδt细胞可以是vδ1t细胞。γδt细胞可以是vδ2t细胞。γδt细胞可以是非vδ1/vδ2t细胞。
25、在另一个方面,本发明的特征在于通过以下方式产生表达car的γδt细胞群的方法:提供起始γδt细胞群以及在不存在病毒载体的情况下,培养起始γδt细胞群持续第一培养期以产生启动的γδt细胞群。所述方法还可包括在具有β逆转录病毒假型和编码car的转基因的病毒载体存在下,培养启动的γδt细胞群持续第二培养期,其中病毒载体的量有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的启动的γδt细胞,由此产生表达car的γδt细胞群。
26、在另一个方面,本发明的特征在于通过以下方式产生表达car和装甲蛋白的γδt细胞群的方法:提供起始γδt细胞群以及在不存在病毒载体的情况下,培养起始γδt细胞群持续第一培养期以产生启动的γδt细胞群。所述方法还可包括在具有β逆转录病毒假型、编码car的第一转基因,和编码装甲蛋白的第二转基因的病毒载体存在下,培养启动的γδt细胞群持续第二培养期,其中病毒载体的量有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的启动的γδt细胞,由此产生表达car和装甲蛋白的γδt细胞群。在一些实施方案中,转基因编码il-15(例如,分泌il-15或膜结合il-15)。在一些实施方案中,病毒载体包括第一转基因和第二转基因。在一些实施方案中,第一转基因编码car并且第二转基因编码装甲蛋白(例如,细胞因子,例如,il-15,例如,分泌il-15或膜结合il-15)。
27、在一些实施方案中,病毒载体的量有效转导至少20%的启动的γδt细胞。
28、在一些实施方案中,第一培养期为1天或更长时间(例如,1天、2天、3天、4天、5天、6天、7天、8天、9天、10天,或更长时间,例如,1-3天、3-5天、5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为2天或更长时间(例如,2天、3天、4天、5天、6天、7天、8天、9天、10天,或更长时间,例如,1-3天、3-5天、5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为5天或更长时间(例如,5天、6天、7天、8天、9天、10天,或更长时间,例如,5-7天、7-10天,或更长时间)。在一些实施方案中,第一培养期为7天或更长时间(例如,7天、8天、9天、10天,或更长时间,例如,7-10天,或更长时间)。
29、在一些实施方案中,第二培养期为2天或更长时间(例如,2天、3天、4天、5天、6天、7天、8天、9天、10天、11天、12天、13天、14天,或更长时间,例如,2-4天、4-7天、7-10天、10-14天,或更长时间)。在一些实施方案中,第二培养期为7天或更长时间(例如,8天、9天、10天、11天、12天、13天、14天,或更长时间,例如,7-10天、10-14天,或更长时间)。
30、在一些实施方案中,启动的γδt细胞群表达asct-1和/或asct-2。在一些实施方案中,启动的γδt细胞群缺少vsv-g进入受体(例如,ldl受体)的功能性表达。在一些实施方案中,大于95%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于96%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于97%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于98%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于99%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。
31、在一些实施方案中,病毒载体以不大于10(例如,不大于5,例如,约1至约5)的moi与启动的γδt细胞一起培养。
32、在另一个方面,本发明的特征在于通过以下方式产生表达car的γδt细胞群的方法:提供起始γδt细胞群;以及在il-15和具有β逆转录病毒假型和编码car的转基因的病毒载体存在下,培养起始γδt细胞群,其中病毒载体的量有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的起始γδt细胞群,由此产生表达car的工程化的γδt细胞群。
33、在另一个方面,本发明的特征在于通过以下方式产生表达car和装甲蛋白的γδt细胞群的方法:提供起始γδt细胞群;以及在il-15和具有β逆转录病毒假型、编码car的第一转基因,和编码装甲蛋白的第二转基因的病毒载体存在下,培养起始γδt细胞群,其中病毒载体的量有效转导至少3%(例如,至少4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的起始γδt细胞群,由此产生表达car和装甲蛋白的工程化的γδt细胞群。在一些实施方案中,装甲蛋白是细胞因子,例如,il-15,例如,分泌il-15或膜结合il-15。
34、在一些实施方案中,起始γδt细胞群缺少asct-1和/或asct-2的表达。工程化的γδt细胞群可表达asct-1和/或asct-2。起始γδt细胞群可缺少vsv-g进入受体(例如,ldl受体)的功能性表达。在一些实施方案中,大于95%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于96%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于97%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于98%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。在一些实施方案中,大于99%的启动的γδt细胞群缺少足够水平的vsv-g进入受体表达(例如,ldl受体)来介导可检测的vsv-g进入(例如,如通过基于blam-vpr的测定所测量)。
35、在一些实施方案中,病毒载体以不大于10(例如,不大于5,例如,约1至约5)的moi与起始γδt细胞群一起培养。
36、在一些实施方案中,β逆转录病毒假型是baev或rd114。
37、在一些实施方案中,病毒载体包括逆转录病毒科病毒载体骨架。逆转录病毒科病毒载体骨架可以是逆转录病毒载体骨架(例如,慢病毒骨架、γ逆转录病毒骨架,或α逆转录病毒骨架)。
38、工程化的γδt细胞可以是vδ1t细胞。工程化的γδt细胞可以是vδ2t细胞。工程化的γδt细胞可以是非vδ1/vδ2t细胞。
39、在一些实施方案中,car靶向cd19、cd20、ror1、cd22、癌胚抗原、甲胎蛋白、ca-125、5t4、muc-1、上皮肿瘤抗原、前列腺特异性抗原、黑色素瘤相关抗原、突变的p53、突变的ras、her2/neu、叶酸结合蛋白、hiv-1包膜糖蛋白gpl20、hiv-1包膜糖蛋白gp41、gd2、cd123、cd33、cd138、cd23、cd30、cd56、c-met、间皮素、gd3、herv-k、il-llrα、κ链、λ链、cspg4、erbb2、egfrviii、vegfr2、组合her2-her3、组合her1-her2、ny-eso-1、ssx2、mage、mart-1、gp100、psa、psma、psca、g9d2,或其组合。
40、在另一个方面,本发明的特征在于通过如本文所述的方法产生的工程化的γδt细胞群。
41、在一些实施方案中,至少10%(例如,至少11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的群体表达car。在一些实施方案中,至少50%(例如,至少55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的工程化的γδt细胞群表达car。在一些实施方案中,至少10%(例如,至少11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的工程化的γδt细胞群表达装甲蛋白,例如,细胞因子(例如,分泌细胞因子或膜结合细胞因子(例如,il-15,例如,分泌il-15或膜结合il-15)。在一些实施方案中,至少50%(例如,至少55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的工程化的γδt细胞群表达装甲蛋白,例如,细胞因子(例如,分泌细胞因子或膜结合细胞因子(例如,il-15,例如,分泌il-15或膜结合il-15)。在一些实施方案中,至少10%(例如,至少11%、12%、13%、14%、15%、16%、17%、18%、19%、20%、25%、30%、35%、40%、45%、50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的工程化的γδt细胞群表达car和装甲蛋白,例如,细胞因子(例如,分泌细胞因子或膜结合细胞因子(例如,il-15,例如,分泌il-15或膜结合il-15)。在一些实施方案中,至少50%(例如,至少55%、60%、65%、70%、75%、80%、85%、90%、95%、97%、99%,或基本上全部)的工程化的γδt细胞群表达car和装甲蛋白,例如,细胞因子(例如,分泌细胞因子或膜结合细胞因子(例如,il-15,例如,分泌il-15或膜结合il-15)。
42、在另一个方面,本发明的特征在于通过如本文所述的方法产生的表达car的γδt细胞群。
43、在另一个方面,本发明的特征在于通过如本文所述的方法产生的表达car和装甲蛋白的γδt细胞群。在一些实施方案中,装甲蛋白是细胞因子(例如,分泌细胞因子或膜结合细胞因子(例如,il-15,例如,分泌il-15或膜结合il-15)。
44、应理解,本文所述的本发明的方面和实施方案包括“包含方面和实施方案”、“由方面和实施方案组成”和“基本上由方面和实施方案组成”。除非另外指出,否则如本文所用的单数形式“一个/种(a/an)”和“所述(the)”包括复数个参考物。
45、如本文所用的术语“约”是指本技术领域的技术人员容易知晓的相应值的常见误差范围。在本文中提及“约”值或参数包括(并且描述)关于所述值或参数本身的实施方案。在一些情况下,“约”涵盖相对于指定值的+20%,在一些情况下+10%,在一些情况下+5%,在一些情况下+1%,或在一些情况下+0.1%的变化,因为此类变化对于进行所公开的方法而言是适当的。
46、如本文使用,术语“工程化的γδt细胞”是指表达转基因(即,被转导至工程化的γδt细胞或其亲本细胞中的基因)的γδt细胞。
47、如本文使用,术语“启动的γδt细胞”是指受培养条件影响的起始群(例如,内源性γδt细胞群)。在一些情况下,相对于其经历培养条件之前的未启动的对应物,启动的γδt细胞具有不同功能病毒进入受体概况。在一些实施方案中,启动的γδt细胞群是扩增的γδt细胞群。
48、如本文使用,“扩增的γδ细胞群”是指包括γδt细胞的造血细胞群,所述细胞以诱导γδ细胞扩增,即,增加γδ细胞数量的条件和持续时间来培养。同样地,如本文使用,“扩增的vδ1t细胞群”是指包括vδ1t细胞的造血细胞群,所述细胞以诱导vδ1t细胞扩增,即,增加vδ1细胞数量的条件和持续时间来培养。类似地,如本文使用,“扩增的vδ2t细胞群”是指包括vδ2t细胞的造血细胞群,所述细胞以诱导vδ2t细胞扩增,即,增加vδ2细胞数量的条件和持续时间来培养。
49、如本文使用,γδt细胞“群”是指三个或更多个γδt细胞(例如,至少10、至少102、至少103、至少104、至少105、至少106、至少107、至少108、至少109、至少1010、至少1011、至少1012,或至少1013)个γδt细胞(例如,工程化的γδt细胞)的组。特定细胞类型的群体(例如,内源性γδt细胞群、启动的γδt细胞群,或工程化的γδt细胞群)是指所述类型的细胞而并非更广泛群体内的不同类型的细胞。例如,如果108个t细胞的起始群的10%的细胞是γδt细胞,则起始γδt细胞群为107个。
50、如本文使用,“装甲蛋白”是指由转基因编码的蛋白,所述转基因在由γδt细胞(例如,表达car的γδt细胞)表达时,例如通过旁分泌信号传导(例如,细胞因子信号传导)来增加γδt细胞针对靶细胞的持续或增加的免疫原性,以改善例如细胞持久性、细胞活力、活化和其他所需特征。装甲蛋白可以是膜结合蛋白或可溶性蛋白。例如,装甲蛋白包括膜结合蛋白,诸如膜结合受体(例如,αβtcr、天然细胞毒性受体(例如,nkp30、nkp44或nkp46)、细胞因子受体(例如,il-12受体)和/或趋化因子受体(例如,ccr2受体)和/或膜结合配体或细胞因子(例如,膜结合il-15、膜结合il-7、膜结合cd40l、膜结合4-1bb、膜结合4-1bbl、膜结合ccl19)。另外地或可选地,装甲蛋白可以是可溶性蛋白,诸如可溶性配体或细胞因子(例如,可溶性il-15、可溶性il-7、可溶性il-12、可溶性cd40l、可溶性4-1bbl和/或可溶性ccl19)。在一些实施方案中,装甲蛋白不是抗原特异性的。
51、如本文使用,“il-15”是指充当一种或多种il-15受体(il-15r)亚基的激动剂的天然或重组il-15或其变体(例如,其突变体、突变蛋白、类似物、亚基、受体复合物、片段、同工型和拟肽)。如同il-2,il-15是可支持il-2依赖性细胞系ctll-2的增殖的已知t细胞生长因子。il-15首先由grabstein等人(science 264.5161:965-969,1994)报导为114个氨基酸的成熟蛋白。如本文所用,术语“il-15”意指天然或重组il-15和突变蛋白、类似物、其亚基,或其复合物(例如,受体复合物,例如,寿司肽,如pct公布号wo 2007/046006中所述),并且其各自可刺激ctll-2细胞的增殖。在ctll-2增殖测定中,用成熟形式的il-15的重组表达前体和同框融合物转染的细胞的上清液可诱导ctll-2细胞增殖。
52、人il-15可根据grabstein等人(science 264.5161:965-969,1994)描述的程序或常规程序诸如聚合酶链反应(pcr)来获得。人il-15cdna在1993年2月19日寄存于并且被指定登录号69245。
53、人il-15的氨基酸序列(基因id 3600)在登录定位符np000576.1gi:10835153(同工型1)和np_751915.1gi:26787986(同工型2)下发现于genbank中。鼠(小家鼠(musmusculus))il-15氨基酸序列(基因id 16168)在登录定位符np_001241676.1gi:363000984下发现于genbank中。
54、il-15还可以指衍生自各种哺乳动物物种,包括例如人、猿、牛、猪、马和鼠的il-15。如本文所提及,il-15“突变蛋白”或“变体”是基本上与天然哺乳动物il-15的序列同源,但是由于氨基酸缺失、插入或取代而具有不同于天然哺乳动物il-15多肽的氨基酸序列的多肽。变体可包含保守取代序列,意味着给定氨基酸残基通过具有类似生理化学特征的残基来替换。保守取代的实例包括一个脂族残基取代另一个脂族残基,诸如ile、val、leu或ala彼此取代,或一个极性残基取代另一个极性残基,诸如在lys与arg;glu与asp;或gln与asn之间的取代。其他此类保守取代,例如,具有类似疏水性特征的整个区域的取代,是众所周知的。天然存在的il-15变体也由本发明涵盖。此类变体的实例是由替代mrna剪接事件或il-15蛋白的蛋白水解裂解所产生的蛋白质,其中il-15结合特性得以保留。mrna的替代剪接可产生截短但具有生物活性的il-15蛋白。可归因于蛋白水解的变化包括例如,由于蛋白水解从il-15蛋白中去除一个或多个末端氨基酸(通常1-10个氨基酸)所导致的在不同类型宿主细胞中表达后的n或c末端中的差异。在一些实施方案中,蛋白质的末端可例如用化学基团诸如聚乙二醇来修饰以改变其物理特性(yang等人cancer76:687-694,1995)。在一些实施方案中,蛋白质的末端或内部可用额外氨基酸来修饰(clark-lewis等人pnas 90:3574-3577,1993)。
55、如本文所用,“非造血细胞”包括基质细胞和上皮细胞。基质细胞是任何器官的非造血结缔组织细胞并且支持所述器官的实质细胞的功能。基质细胞的实例包括成纤维细胞、周细胞、间充质细胞、角质形成细胞、内皮细胞和非血液学肿瘤细胞。上皮细胞是装衬在整个身体中的血管和器官的腔体和表面的非造血细胞。它们通常在形状上是鳞状、柱状或立方体样并且可被排列成单个细胞层,或两个或更多个细胞层。
56、如本文所用,“非造血组织驻留γδt细胞”、“非造血组织衍生”,和“非造血组织-天然γδt细胞”是指在组织外植时,存在于非造血组织中的γδt细胞。非造血组织驻留γδt细胞可获自任何合适人或非人动物非造血组织。非造血组织是除了血液或骨髓以外的组织。在一些实施方案中,γδt细胞不获自诸如血液或滑液的生物流体的特定类型的样品。此类合适人或非人动物非造血组织的实例包括皮肤或其一部分(例如,真皮或表皮),胃肠道(例如,胃肠上皮、结肠、小肠、胃、阑尾、盲肠或直肠)、乳腺组织、肺(优选地其中组织不通过支气管肺泡灌洗来获得)、前列腺、肝和胰腺。在一些实施方案中,非造血组织驻留γδt细胞可衍生自淋巴组织,诸如胸腺、脾或扁桃体。γδt细胞也可驻留于人癌症组织,例如,乳腺和前列腺中。在一些实施方案中,γδt细胞不获自人癌症组织。非造血组织样品可通过标准技术例如,通过外植(例如,活检)来获得。非造血组织驻留γδt细胞包括例如vδ1t细胞、双阴性(dn)t细胞、vδ2t细胞、vδ3t细胞和vδ5t细胞。
57、如本文所用,短语“以有效……的量”是指诱导可检测结果(例如,相对于其起始群,具有统计上显著增加数量的细胞的数量,例如,p<0.05)的量。
58、如本文所用,“扩增的γδ细胞群”是指包括γδt细胞的造血细胞群,所述细胞以诱导γδ细胞扩增,即,增加γδ细胞数量的条件和持续时间来培养。同样地,如本文所用,“扩增的vδ1t细胞群”是指包括vδ1t细胞的造血细胞群,所述细胞以诱导vδ1t细胞扩增,即,增加vδ1细胞数量的条件和持续时间来培养。类似地,如本文所用,“扩增的vδ2t细胞群”是指包括vδ2t细胞的造血细胞群,所述细胞以诱导vδ2t细胞扩增,即,增加vδ2细胞数量的条件和持续时间来培养
59、术语“标志物”在本文中是指dna、rna、蛋白质、碳水化合物、糖脂,或基于细胞的分子标志物,其在患者样品中的表达或存在可通过标准方法(或本文所公开的方法)来检测。
60、“表达”所关注标志物的细胞或细胞群是如下细胞或细胞群,其中编码蛋白质的mrna或蛋白质本身(包括其片段)被确定为存在于细胞或群体中。标志物的表达可通过各种手段来检测。例如,在一些实施方案中,标志物的表达是指细胞上的标志物的表面密度。例如用作流式细胞术的读出的平均荧光强度(mfi)代表细胞群上的标志物的密度。本领域的技术人员将理解mfi值取决于染色参数(例如,浓度、持续时间和温度)和荧光染料组成。然而,在适当对照的情形中考虑时,mfi可以是定量的。例如,如果在相当条件下染色,标志物的抗体的mfi显著高于相同细胞群上的适当同种型对照抗体的mfi,则可认为细胞群表达所述标志物。另外地或可选地,根据常规流式细胞术分析方法(例如,通过根据同种型或“荧光减一”(fmo)对照来设定门),使用正性和负性门,可在逐个细胞的基础上认为细胞群表达标志物。通过此度量,如果检测到的对标志物阳性的细胞的数量显著高于背景(例如,通过对同种型对照进行门控),可认为群体“表达”标志物。
61、如本文所用,“vsv-g进入受体的功能性表达”是指足以在至少5%的靶细胞群中介导可检测的vsv-g进入的vsv-g进入受体表达水平,如通过基于β内酰胺酶-vpr(blam-vpr)的测定所测量。参见例如cavrois等人nat biotechnol.11:1151-1154,2002。相反地,在“缺少vsv-g进入受体的功能性表达”的细胞群中,大于95%的细胞群缺少足以介导可检测的vsv-g进入的vsv-g进入受体表达水平,如通过基于blam-vpr的测定所测量。
62、如本文所用,当群体的表达以阳性细胞的百分比来陈述并且所述百分比与参考群体的阳性细胞的对应百分比进行比较时,百分比差异是各相应群体的亲本群体的百分比。例如,如果标志物在群体a的10%的细胞上表达并且相同标志物在群体b的1%的细胞上表达,则认为群体a的标志物阳性细胞频率比群体b大9%(即,10%-1%,而不是10%÷1%)。当频率乘以亲本群体中的细胞数量时,计算细胞绝对数量的差。在以上给出的实例中,如果在群体a中有100个细胞并且在群体b中有10个细胞,则相对于群体b,群体a具有100倍细胞数量,即,(10%x 100)÷(1%x 10)。
63、标志物的表达水平可以是核酸表达水平(例如,dna表达水平或rna表达水平,例如,mrna表达水平)。可使用确定核酸表达水平的任何合适方法。在一些实施方案中,核酸表达水平使用qpcr、rtpcr、rna-seq、多重qpcr或rt-qpcr、微阵列分析、基因表达系列分析(sage)、技术、原位杂交(例如,fish),或其组合来确定。
64、如本文所用,细胞的“参考群体”是指对应于所关注细胞的细胞群,相对于所述群体来测量所关注细胞的表型。例如,非造血组织衍生的γδ细胞的分离群体上标志物的表达水平可与造血组织衍生的γδt细胞(例如,血液驻留γδ细胞,例如,衍生自相同供体或不同供体的血液驻留γδ细胞)或在不同条件下(例如,在实质性tcr活化存在下、在外源性tcr活化剂(例如,抗cd3)存在下,或在与基质细胞(例如,成纤维细胞)实质性接触中)扩增的非造血组织衍生的γδt细胞上相同标志物的表达水平进行比较。群体还可与较早状态下的自身进行比较。例如,参考群体可以是在其扩增之前的分离细胞群体。在此情况下,扩增的群体与其在扩增步骤之前的自身组成进行比较,即,在此情况下,其过去组成是参考群体。
65、如本文所用,术语“嵌合抗原受体”或可选地“car”是指重组多肽构建体,其包括胞外抗原结合结构域、跨膜结构域,和任选地传播对细胞进行活化的活化信号和/或共刺激信号的胞内结构域。在一些实施方案中,car包括car融合蛋白的n末端的任选的前导序列。
- 还没有人留言评论。精彩留言会获得点赞!