苯并吡喃酮的制备方法与流程
本发明涉及有机合成领域,具体而言,涉及一种苯并吡喃酮的制备方法。
背景技术:
1、具有苯并吡喃酮骨架并具有负介电各向异性的液晶化合物,因为其满足对热和光的高稳定性、高向列相最高温度、低液晶相最低温度、小粘度、合适的光学各向异性、较大的负介电各向异性、合适的弹性常数以及与其他液晶化合物具有良好的相容性,因而可以广泛地应用于液晶材料制造。
2、目前,苯并吡喃酮类化合物主要通过以下技术路线来制备制备:
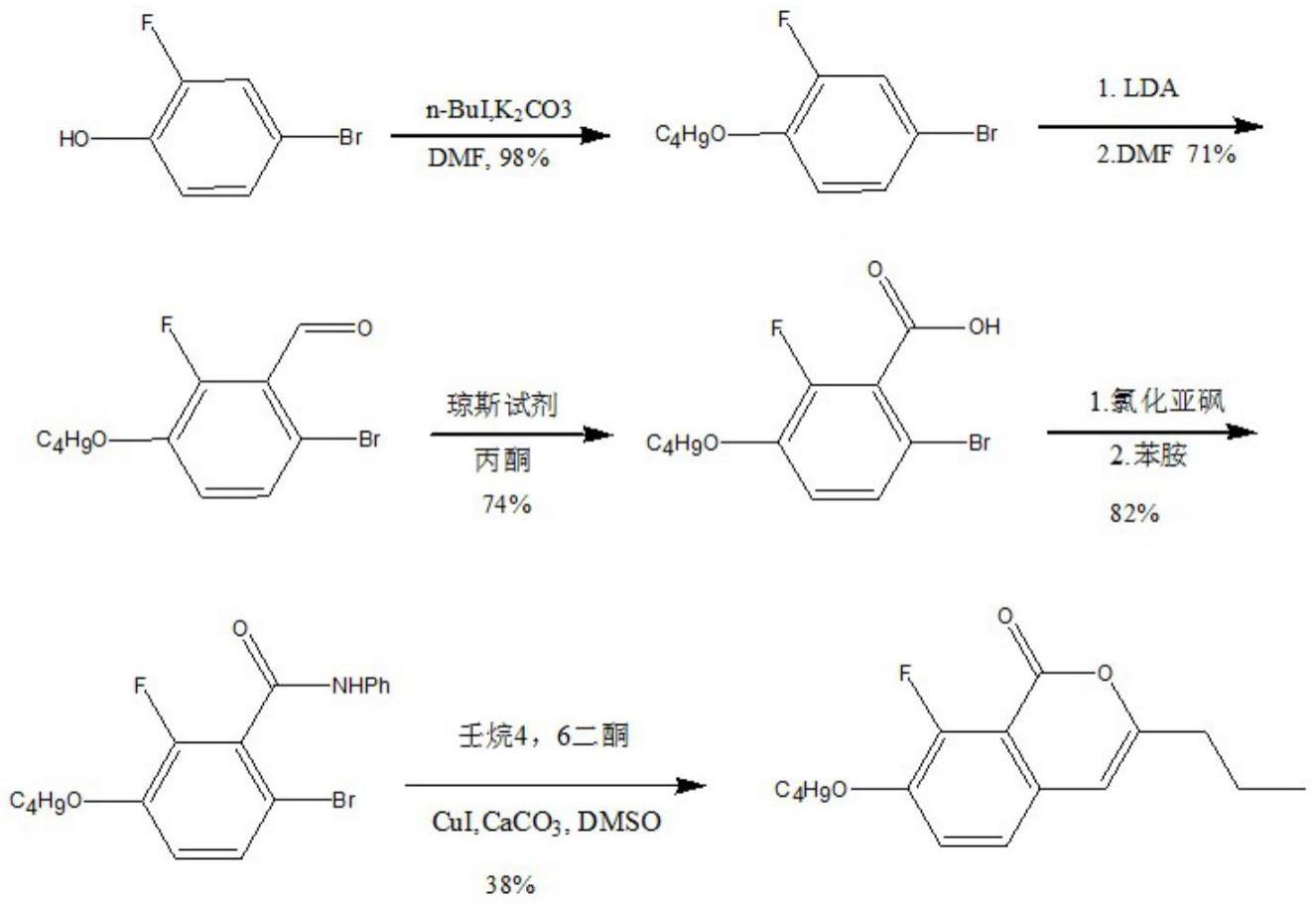
3、路线一
4、
5、路线二
6、
7、
8、其中,路线一以2-氟-4-溴苯酚为原料经醚化,lda成醛,醛基氧化,羧基保护,偶联环化等步骤,仅制备得到烷基取代的苯并吡喃酮衍生物,且原文中烷基取代的苯并吡喃酮总收率约16%,收率较低;路线二以3-氟-4-乙氧基苯乙醛为原料,需要另外制备,过程中需要用到锂试剂,反应条件苛刻,过程中收率大多在30-40%。
9、综上,苯并吡喃酮类化合物合成比较困难,条件较为苛刻,亟需一种更为易于实现的苯并吡喃酮的合成方法。
技术实现思路
1、本发明的主要目的在于提供一种苯并吡喃酮的制备方法,以解决现有技术中苯并吡喃酮制备难度大、收率低的问题。
2、为了实现上述目的,根据本发明的一个方面,提供了一种苯并吡喃酮的制备方法,该制备包括:
3、步骤s1,以三氟硝基苯为第一原料,与硝基甲烷进行邻位取代反应,得到1,2-二氟-4-硝基-3-硝甲基苯,1,2-二氟-4-硝基-3-硝甲基苯与醇盐发生对位取代反应,得到第一中间体,第一中间体的结构如式ⅰ所示,其中,r1选自碳原子数为1~4的烷基;
4、
5、步骤s2,将第一中间体经内夫反应,将硝甲基转化为羧基,得到第二中间体;
6、步骤s3,将第二中间体经还原反应、氧化反应和脱氮重排反应将硝基转化为醛肼,得到醛肼中间体;
7、步骤s4,在催化剂作用下,将醛肼中间体与结构如式ⅰⅰ所示的第二原料进行亲核加成反应生成仲醇中间体,将仲醇中间体进行关环反应,得到结构如式ⅰⅰⅰ所示的目标产物,
8、
9、
10、式ⅰⅰ和式ⅰⅰⅰ中,r2选自取代或者未取代的环己基、苯基或者双环己基烷基,取代基各自独立的为c1~c5烷基中的任意一种;式ⅰⅰⅰ中,r1选自碳原子数为1~4的烷基。
11、进一步地,硝基甲烷的用量为第一原料三氟硝基苯摩尔量的5~20倍;
12、优选的,步骤s1的邻位取代反应中加入有机碱;优选的,有机碱包括三乙胺、三乙烯二胺、四甲基胍、n-甲基吗啉和季铵碱中的任意一种或者多种;优选的,有机碱的用量为第一原料三氟硝基苯摩尔量的1-3倍。
13、进一步地,步骤s1中,邻位取代反应的温度为-10~-30℃,优选的,邻位取代反应在惰性气体氛围中进行;
14、优选的,邻位取代反应包括:在反应容器中加入硝基甲烷和有机碱,在惰性气体氛围内降温至取代反应的反应温度,加入第一原料三氟硝基苯,进行取代反应;优选的,第一原料三氟硝基苯以滴加的方式加入;
15、优选的,邻位取代反应完成后,将反应体系进行水洗,减压浓缩回收硝基甲烷,得到1,2-二氟-4-硝基-3-硝甲基苯。
16、进一步地,步骤s1中,对位取代反应包括包括:将1,2-二氟-4-硝基-3-硝甲基苯与第一溶剂和醇盐混合,加热回流,反应5-10小时,向体系中加入第一酸性水溶液调节ph值,浓缩,打浆水洗,得到第一中间体;
17、优选的,醇盐包括醇钠、醇钾中的任意一种或者多种;优选的,醇盐的用量为1,2-二氟-4-硝基-3-硝甲基苯摩尔量的1~2倍;
18、优选的,第一溶剂包括乙醇、甲醇、丙醇和异丙醇中的任意一种或者多种;
19、优选的,ph值调节至中性;
20、优选的,第一酸性水溶液包括盐酸溶液、硫酸溶液、乙酸溶液、氯化铵水溶液和硫酸铵水溶液中的任意一种或者多种。
21、进一步地,在步骤s2中,内夫反应中加入第一催化剂,第一催化剂包括四丁基碘化铵、醋酸锌、和碘化锌中的任意一种或者多种;
22、优选的,第一催化剂包括四丁基碘化铵和醋酸锌,更优选的,四丁基碘化铵的用量为第一中间体摩尔量的2~10%,醋酸锌的用量为第一中间体摩尔量的5~20%;
23、优选的,内夫反应在第二溶剂中进行,第二溶剂为水;优选的,第二溶剂的用量为第一中间体体积的的1~5倍;
24、优选的,步骤s2包括:将第一中间体与第二溶剂、第一催化剂混合,进行内夫反应,反应完毕进行酸化、第一纯化,得到第二中间体;
25、优选的,内夫反应的温度为80-100℃,反应时间为10-30小时;
26、优选的,第一纯化包括将酸化的产物用甲基叔丁基醚溶解提取、水洗、浓缩,浓缩得到的固体产物使用石油醚洗涤,得到第二中间体。
27、进一步地,步骤s3中,还原反应为在第二催化剂的作用下与氢气反应,第二催化剂包括雷尼镍、钯碳和铂碳中的任意一种或者多种;
28、优选的,氢气的压力为0.2-1mpa;
29、优选的,还原反应在第三溶剂中进行,第三溶剂包括乙醇、甲醇和水中的任意一种或者多种;
30、优选的,还原反应的温度为30~50℃,反应的时间为5~10小时;
31、优选的,还原反应的处理过程包括:将第二中间体与第二催化剂、第三溶剂混合,在反应装置中充入氢气进行反应,反应完毕,经过滤、浓缩、结晶得到还原产物。
32、进一步地,步骤s3中,氧化反应包括将还原反应的产物与三聚甲醛、第四溶剂混合,反应第一时间,加入氧化剂,继续反应第二时间,反应完毕后,经第二纯化,得到氧化反应的产物,其中,第四溶剂为有机溶剂;
33、优选的,氧化剂选自过氧化氢水溶液和叔丁基过氧化氢中的任意一种或者多种;
34、优选的,三聚甲醛中甲醛单体的摩尔量为还原反应的产物的摩尔量的1~3倍;
35、优选的,第四溶剂包括乙腈;
36、优选的,反应的温度为75-85℃,更优选的,氧化剂在60-70℃条件下加入;
37、优选的,第一时间为8-10小时,第二时间为5-8小时;
38、优选的,第二纯化包括通过蒸馏或者减压蒸馏分离出第四溶剂,过滤,水洗除去过氧化氢,烘干得到氧化反应的产物。
39、进一步地,步骤s3中,脱氮重排反应的处理过程包括:将氧化反应的产物用第五溶剂溶解,与水合肼一水合物混合,回流状态下进行反应,经第三纯化,得到醛肼中间体;
40、优选的,第五溶剂包括乙醇;
41、优选的,第三纯化包括:减压浓缩、甲基环戊基醚提取、水洗。
42、进一步地,步骤s4中,亲核加成反应在第二碱试剂和催化剂作用下进行;
43、优选的,第二碱试剂包括碳酸钾、磷酸钾和叔丁醇钾中的任意一种或者多种;更优选的,第二碱试剂的用量为醛肼中间体摩尔量的2~10%;
44、优选的,催化剂包括fe(dmpe)2cl2;
45、可选的,亲核反应中还加入添加剂,添加剂选自氟化钠、氟化钾和氟化铯中的任意一种或者多种,优选的,添加剂的用量为醛肼中间体摩尔量的2~10%;
46、优选的,亲核加成反应在惰性气体氛围中进行。
47、进一步地,关环反应为光延反应;优选的,关环反应的处理过程包括:将仲醇中间体与三苯基膦、第六溶剂混合,滴入偶氮二甲酸二乙酯进行反应,反应结束后,加入水淬灭反应,经过第四纯化,得到目标产物;
48、优选的,关环反应的温度为0-10℃;
49、优选的,上述第六溶剂包括四氢呋喃、2-甲基四氢呋喃、二氯甲烷和甲基环戊醚中的任意一种或者多种;
50、优选的,第四纯化包括减压浓缩,乙醇冷冻洗涤,过滤,烘干。
51、进一步地,r1选自碳原子数为2~4的烷基,r2选自取代或者未取代的环己基、苯基或者双环己基烷基,取代基各自独立的为c1~c5烷基中的任意一种;
52、优选的,r1选自乙基或者正丁基,r2选自取代或者未取代的环己基、苯基或者双环己基烷基,优选的,取代基位于对位,取代基为c1~c4烷基中的任意一种。
53、应用本发明的技术方案,使用三氟硝基苯为起始原料,先与硝基甲烷进行邻位取代,再与醇盐进行对位取代,所得硝基取代物经内夫反应,再经还原、氧化脱氮重排将硝基转化为醛肼,在铁催化剂催化下再与特定结构的醛进行亲核加成生成仲醇中间体,最后经关环即得目标产物。上述制备苯并吡喃酮的方法,原料的来源比较广泛,反应条件比较温和,反应整体收率较高,制备的产物易于分离提纯,能够有效降低苯并吡喃酮类化合物的工艺成本。
- 还没有人留言评论。精彩留言会获得点赞!