全合成酮还原酶及应用该酮还原酶的制备方法与流程
本发明涉及合成,特别是涉及基因工程与酶工程合成,具体而言,涉及全合成酮还原酶及应用该还原酶的制备方法。
背景技术:
1、手性醇化合物作为天然产物和手性药物合成中的重要中间体化合物,其合成一直是本领域技术人员研究的热点。手性化合物合成中手性中心的构建是合成中的关键环节,不同的手性化合物其药理活性、代谢及毒性都有着重大差异。对于手性药物,通常一组对映体中,一个是活性有效的,而另一个是无效,甚至是有毒的。
2、譬如,替格瑞洛合成中的关键中间体化合物(s)-2-氯-1-(3,4-二氟苯基)乙醇和富马酸丙酚替诺福韦合成中的关键中间体化合物(r)-9-(2-羟丙基)腺嘌呤都是手性中间体,其光学纯度在目标药物化合物的制备中起着至关重要的作用。
3、还原酶作为生物催化剂在生物法合成中具有重要作用。但是在还原酶的应用中,能否异源表达,表达效果好坏,以及能否有效、高效催化底物转化为目标光学手性化合物,都需要具体问题具体分析。在现有技术中,还原酶往往只能单一作用在某一底物转化合成中,针对不同的手性化合物的需要,必须要构建不同的催化酶。
技术实现思路
1、本发明所要解决的技术问题是提供一种全合成酮还原酶,并利用该全合成酮还原酶作为生物催化剂,提供一种新的合成替格瑞洛合成关键中间体化合物(s)-2-氯-1-(3,4-二氟苯基)乙醇和合成富马酸丙酚替诺福韦关键中间体化合物(r)-9-(2-羟丙基)腺嘌呤的方法,进而不仅得到高光学纯度的目标化合物,同时能够实现一酶两用。
2、为了解决上述技术问题,本发明公开了一种酮还原酶,所述酮还原酶的氨基酸序列如seq id no:1所示。
3、同时,本发明还公开了该酮还原酶的编码基因,所述编码基因的核苷酸序列如seqid no:2所示。
4、同时,本发明还公开了一种连接有上述编码基因的重组质粒。优选地,该重组质粒为pet-28a(+)。
5、进一步地,在本发明中还公开了重组质粒的构建方法,分别设计如seq id no:3所示的上游引物p1和如seq id no:4所示的下游引物p2,将pet-28a(+)质粒bamh i和xhoi双酶切处理后,将经pcr扩增的含有bamh i和xhoi酶切位点含有如seq id no:2所示的编码基因的目的基因与载体pet-28a(+)连接,所用连接体系为目的基因4μl,载体pet-28a(+)2μl,buffer 2μl,连接酶1μl,16℃过夜。
6、进一步地,本发明还公开了pcr扩增的条件为:98℃3min,98℃30s,55℃90s、72℃90s,35个循环;pcr扩增体系:模板1.5μl,上下游引物各1.5μl,灭菌的双蒸水20.5μl,primerstarmix25μl;其中模板为puc57。
7、同时,本发明还公开了含有上述重组质粒的宿主细胞。优选地,该宿主细胞为大肠杆菌。
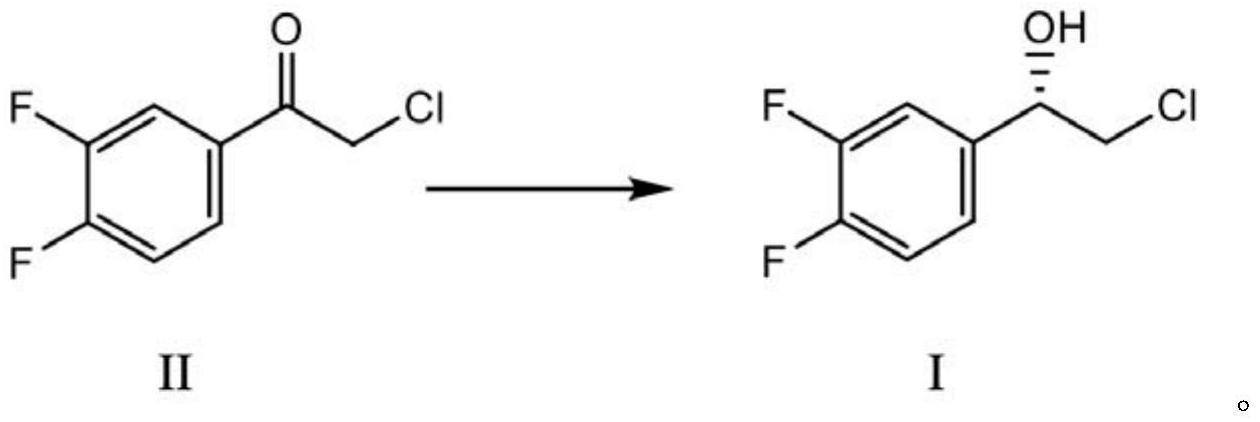
8、另一方面,本发明还公开了应用该酮还原酶的制备化合物(s)-2-氯-1-(3,4-二氟苯基)乙醇的方法,将重组工程菌培养、破碎后添加至含有底物化合物ⅱ、nadp+、异丙醇和异丙醇还原酶酶粉的反应体系中,经反应形成化合物ⅰ,所述重组工程菌是以e.colibl21(de3)为宿主,pet-28a(+)为载体,表达如seq id no:1所示的酮还原酶的大肠杆菌,
9、
10、在另一个发明,本发明还公开了应用该酮还原酶制备化合物(r)-9-(2-羟丙基)腺嘌呤的方法,将重组工程菌培养、破碎后添加至含有底物化合物ⅳ、nadp+、异丙醇和异丙醇还原酶酶粉的反应体系中,经反应形成化合物ⅲ,所述重组工程菌是以e.colibl21(de3)为宿主,pet-28a(+)为载体,表达如seq id no:1所示的酮还原酶,
11、
12、进一步优选地,所述重组工程菌培养方法如下:将重组菌接种于培养基中,37℃震荡培养过夜,按照2%的接种量转接于lb培养基中,37℃培养至od600=0.6时,加入50μl0.5mol/l的诱导剂,16~25℃诱导16h,离心收集菌体。
13、进一步优选地,所述重组工程菌采用超声波破碎的方式,超声功率为260w,超声程序为运行3s,间隔5s,总时长3min。
14、进一步优选地,所述酮还原酶在反应体系中的浓度为0.04g/ml。
15、本发明通过全合成的方法获得了一种新的酮还原酶,该酮还原酶能够稳定异源功能性表达,同时该酮还原酶能够在替格瑞洛合成关键中间体化合物(s)-2-氯-1-(3,4-二氟苯基)乙醇的制备中和富马酸丙酚替诺福韦关键中间体化合物(r)-9-(2-羟丙基)腺嘌呤的制备中均表现出高效地催化活性,具有巨大的工业化应用潜力,有望成为催化不同手性构型的通用酮还原酶。
技术特征:
1.一种酮还原酶,其特征是,所述酮还原酶的氨基酸序列如seq id no:1所示。
2.一种dna分子,其特征是,所述dna分子含有编码权利要求1所述的酮还原酶的编码基因,所述编码基因的核苷酸序列如seq id no:2所示。
3.一种重组质粒,其特征是,所述重组质粒连接有权利要求2所述的dna分子,进一步优选地,该重组质粒为pet-28a(+)。
4.根据权利要求3所述的重组质粒,其特征是,所述重组质粒是通过以下方法构建,分别设计如seq id no:3所示的上游引物p1和如seq id no:4所示的下游引物p2,将pet-28a(+)质粒bamh i和xhoi双酶切处理后,将经pcr扩增的含有bamh i和xhoi酶切位点含有如seq id no:2所示的编码基因的目的基因与载体pet-28a(+)连接,所用连接体系为目的基因4μl,载体pet-28a(+)2μl,buffer 2μl,连接酶1μl,16℃过夜。
5.根据权利要求4所述的重组质粒,其特征是,pcr扩增的条件为:98℃3min,98℃30s,55℃90s、72℃90s,35个循环;pcr扩增体系:模板1.5μl,上下游引物各1.5μl,灭菌的双蒸水20.5μl,primerstarmix25μl;其中模板为puc57。
6.一种宿主细胞,其特征是,所述宿主细胞含有上述重组质粒,优选地,该宿主细胞为大肠杆菌。
7.应用权利要求1所述的酮还原酶制备化合物(s)-2-氯-1-(3,4-二氟苯基)乙醇的方法,其特征是,将重组工程菌培养、破碎后添加至含有底物化合物ⅱ、nadp+、异丙醇和异丙醇还原酶酶粉的反应体系中,经反应形成化合物ⅰ,所述重组工程菌是以e.colibl21(de3)为宿主,pet-28a(+)为载体,表达如seq id no:1所示的酮还原酶的大肠杆菌,
8.应用权利要求1所述的酮还原酶制备在化合物(r)-9-(2-羟丙基)腺嘌呤的方法,将重组工程菌培养、破碎后添加至含有底物化合物ⅳ、nadp+、异丙醇和异丙醇还原酶酶粉的反应体系中,经反应形成化合物ⅲ,所述重组工程菌是以e.colibl21(de3)为宿主,pet-28a(+)为载体,表达如seq id no:1所示的酮还原酶,
9.根据权利要求7或8所述的方法,其特征是,所述重组工程菌培养方法如下:将重组菌接种于培养基中,37℃震荡培养过夜,按照2%的接种量转接于lb培养基中,37℃培养至od600=0.6时,加入50μl0.5mol/l的诱导剂,16~25℃诱导16h,离心收集菌体。
10.根据权利要求7或8所述的方法,其特征是,所述重组工程菌采用超声波破碎的方式,超声功率为260w,超声程序为运行3s,间隔5s,总时长3min。
11.根据权利要求7或8所述的方法,其特征是,所述酮还原酶在反应体系中的浓度为0.04g/ml。
技术总结
本发明涉及合成技术领域,特别是涉及基因工程与酶工程合成技术领域,具体而言,涉及全合成酮还原酶及应用该还原酶的制备方法。通过全合成的方法获得了一种新的酮还原酶,该酮还原酶能够稳定异源功能性表达,同时该酮还原酶能够在替格瑞洛合成关键中间体化合物(S)‑2‑氯‑1‑(3,4‑二氟苯基)乙醇的制备中和富马酸丙酚替诺福韦关键中间体化合物(R)‑9‑(2‑羟丙基)腺嘌呤的制备中均表现出高效地催化活性,具有巨大的工业化应用潜力,有望成为催化不同手性构型的通用酮还原酶。
技术研发人员:戚陈陈,邬小兵,张康,杨柳
受保护的技术使用者:重庆普佑生物医药有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!