引物探针组及其应用的制作方法
本发明涉及生物,特别涉及引物探针组及其应用。
背景技术:
1、致泻大肠杆菌(diarrheagenic escherichia coli,dec),可通过食物引起人类发病,主要包括肠道致病性大肠杆菌(enteropathogenic escherichia coli,epec)、肠毒性大肠杆菌(enterotoxigenic escherichia coli,etec)、肠出血性大肠杆菌(shiga toxin-producing escherichia coli,stec/ehec)、肠道侵袭性大肠杆菌(enteroinvasiveescherichia coli,eiec)、肠道集聚性大肠杆菌(enteroaggregative escherichia coli,eaec)。致泻大肠杆菌属于腹泻病一个重要病原。研究发现,致泻大肠杆菌感染在细菌性感染腹泻发生原因中占首位。因此,临床尽早经有效措施检测致泻大肠杆菌,可进一步了解腹泻人群中感染情况,指导临床诊疗。以往,临床多采用常规方法检测,但也具有操作时间长、检出率低等特点,且致泻大肠杆菌血清分型较多,极易出现交叉凝结现象,增加检测难度。传统的分离
2、培养技术是致泻大肠杆菌鉴定、检测的标准方法,但常规的细菌培养与鉴定方法不足以将各种致泻大肠杆菌分别开。随着分子生物学的发展,普通pcr和荧光pcr也被应用在致泻大肠杆菌的鉴定,但普通pcr操作复杂,需要电泳,容易污染,鉴定准确度不高。因此,需要有既快速又准确的鉴定方法来鉴别致泻大肠杆菌的各个分型。
3、目前对于致泻大肠埃希氏菌的鉴定方法主要有:传统微生物法和血清学分析法、分子生物学检测法。传统微生物分离与鉴定以及血清学方法在鉴定病原微生物难以区分多种致泻大肠埃希氏菌,其检测周期长、操作步骤繁琐、结果易受人为主观因素干扰。特别是致病菌含量低的标本,直接培养很难挑出目标菌,增菌后进行分离易受杂菌影响;由于杂菌增长速度较快,掩盖了目标菌,导致很难挑出可疑目标菌落,具有交叉反应严重、假阳性多、灵敏度低等缺点。分子生物学检测法目前应用最常见的为pcr法,pcr大大弥补了对样本核酸浓度要求高的局限,具有检测灵敏度高、特异性好等特点,但常规的pcr方法通常不能一步得出检测结果,需要凝胶电泳辅助判断,而电泳步骤不仅需要增加人工成本和检测时间,也容易导致污染,产生假阳性结果。
4、因此,提供特异性更好、灵敏度更高的致泻大肠杆菌鉴定方法具有重要的现实意义。
技术实现思路
1、有鉴于此,本发明提供的引物探针组及其应用,采用了多重荧光定量pcr法进行扩增检测,进而使五种致泻大肠杆菌的鉴定具有更好的特异性和更高的灵敏度。
2、为了实现上述发明目的,本发明提供以下技术方案:
3、本发明提供了基因组合在制备致泻大肠杆菌的多重检测试剂或试剂盒中的应用;
4、所述基因组合包括stp、sth、lt、stx1、stx2、ipah、aggr、asta、pic和eaea;
5、所述致泻大肠杆菌包括etec、ehec、eiec、eaec和epec。
6、本发明还提供了引物探针组,包括引物组x和探针x;
7、所述引物组x包括引物(2x-1)和引物2x;
8、所述引物(2x-1)具有:
9、(1)、如seq id no:(3x-2)所示的核苷酸序列;或
10、(2)、如(1)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(1)的相同或相似;或
11、(3)、与如(1)或(2)所示的核苷酸序列至少有75%同源性的核苷酸序列;
12、所述引物2x具有:
13、(4)、如seq id no:(3x-1)所示的核苷酸序列;或
14、(5)、如(4)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(4)的相同或相似;或
15、(6)、与如(4)或(5)所示的核苷酸序列至少有75%同源性的核苷酸序列;
16、所述探针x具有:
17、(7)、如seq id no:3x所示的核苷酸序列;或
18、(8)、如(7)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(7)的相同或相似;或
19、(9)、与如(7)或(8)所示的核苷酸序列至少有75%同源性的核苷酸序列;
20、x选自1~10中的任意整数;
21、所述多个为2个至10个。
22、在本发明的一些具体实施方案中,上述引物探针组还包括内标引物探针组。
23、在本发明的一些具体实施方案中,上述引物探针组中:
24、所述内标引物探针组的上游引物具有:
25、(10)、如seq id no:31所示的核苷酸序列;或
26、(11)、如(10)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(10)的相同或相似;或
27、(12)、与如(10)或(11)所示的核苷酸序列至少有75%同源性的核苷酸序列;
28、所述内标引物探针组的下游引物具有:
29、(13)、如seq id no:32所示的核苷酸序列;或
30、(14)、如(13)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(13)的相同或相似;或
31、(15)、与如(13)或(14)所示的核苷酸序列至少有75%同源性的核苷酸序列;
32、所述内标引物探针组的探针具有:
33、(16)、如seq id no:33所示的核苷酸序列;或
34、(17)、如(16)所示的核苷酸序列经取代、缺失或添加一个或多个碱基获得的核苷酸序列,且功能与(16)的相同或相似;或
35、(18)、与如(16)或(17)所示的核苷酸序列至少有75%同源性的核苷酸序列;
36、所述多个为2个至10个。
37、本发明还提供了上述引物探针组在制备致泻大肠杆菌的多重检测试剂或试剂盒中的应用;
38、所述基因组合包括stp、sth、lt、stx1、stx2、ipah、aggr、asta、pic和eaea;
39、所述致泻大肠杆菌包括etec、ehec、eiec、eaec和epec。
40、本发明还提供了试剂,包括上述引物探针组,以及可接受的辅料和助剂。
41、本发明还提供了试剂盒,包括上述引物探针组或上述试剂,以及可接受的辅料和助剂。
42、在本发明的一些具体实施方案中,上述试剂盒包括:
43、反应体系分为反应体系1和反应体系2;
44、所述反应体系1包括反应液1和反应液2;
45、所述反应液1包括2% dmso、8%吐温20、30%peg6000、0.3~1μmol引物和0.3~1μmol探针;
46、所述反应液1中的所述探针包括序列为seq id no:3、seq id no:6、seq id no:9、seq id no:21、seq id no:24或seq id no:27的探针和内标;
47、所述反应液1还包括内标探针;
48、所述反应液2包括酶激活剂,所述酶激活剂包括镁离子;
49、所述反应体系2包括反应液3和反应液4;
50、所述反应液3包括2% dmso、8%吐温20、30%peg6000、0.3~1μmol引物和0.3~1μmol探针;
51、所述反应液3中的所述探针包括序列为seq id no:12、seq id no:15、seq id no:18或seq id no:30的探针;
52、所述反应液3还包括内标探针;
53、所述反应液4包括酶激活剂,所述酶激活剂包括镁离子;
54、序列为seq id no:3、seq id no:6、seq id no:9、seq id no:12或seq id no:15的探针5’端标记fam荧光基团;
55、序列为seq id no:18、seq id no:21、seq id no:24或seq id no:27的探针5’端标记rox荧光基团;
56、序列为seq id no:30的探针5’端标记cy5荧光基团;
57、序列为seq id no:3、seq id no:9、seq id no:21、seq id no:24或seq id no:27的探针3’端标记sq淬灭基团;
58、序列为seq id no:6的探针3’端标记mgb淬灭基团;
59、序列为seq id no:12或seq id no:15的探针3’端标记bhq1淬灭基团;
60、序列为seq id no:18或seq id no:30的探针3’端标记bhq2淬灭基团;
61、所述内标探针5’端标记hex荧光基团、3’端标记bhq2淬灭基团;
62、扩增程序包括:50℃2min;95℃2min;95℃10s,60℃22s,45个循环。
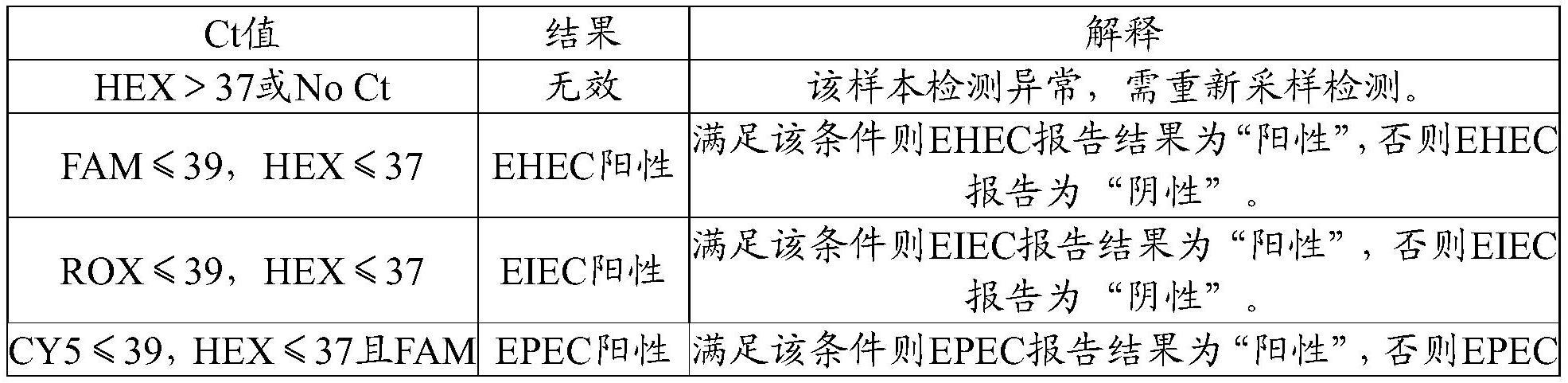
63、在本发明的一些具体实施方案中,上述试剂盒的检测结果的判定规则包括:
64、(a)、当所述反应体系1或反应体系2的hex通道的ct值>37或无ct值,则检测结果无效;和/或
65、(b)、当所述反应体系1的fam通道的ct值≤39,且hex通道的ct值≤37,则检测结果为etec阳性;和/或
66、(c)、当所述反应体系1的rox通道的ct值≤39,且hex通道的ct值≤37,则检测结果为eaec阳性;和/或
67、(d)、当所述反应体系2的fam通道的ct值≤39,且hex通道的ct值≤37,则检测结果为ehec阳性;和/或
68、(e)、当所述反应体系2的rox通道的ct值≤39,且hex通道的ct值≤37,则检测结果为eiec阳性;和/或
69、(f)、当所述反应体系2的cy5道的ct值≤39,且fam通道的ct值≥39或无ct值,且hex通道的ct值≤37,则检测结果为epec阳性。
70、本发明还提供了检测方法,包括使用上述引物探针组、上述试剂或上述试剂盒对待测样品进行检测,获得检测结果;
71、所述检测结果的判定规则包括:
72、(a)、当所述反应体系1或反应体系2的hex通道的ct值>37或无ct值,则检测结果无效;和/或
73、(b)、当所述反应体系1的fam通道的ct值≤39,且hex通道的ct值≤37,则检测结果为etec阳性;和/或
74、(c)、当所述反应体系1的rox通道的ct值≤39,且hex通道的ct值≤37,则检测结果为eaec阳性;和/或
75、(d)、当所述反应体系2的fam通道的ct值≤39,且hex通道的ct值≤37,则检测结果为ehec阳性;和/或
76、(e)、当所述反应体系2的rox通道的ct值≤39,且hex通道的ct值≤37,则检测结果为eiec阳性;和/或
77、(f)、当所述反应体系2的cy5道的ct值≤39,且fam通道的ct值≥39或无ct值,且hex通道的ct值≤37,则检测结果为epec阳性。
78、本发明的引物探针组及其应用有如下效果:
79、本发明针对特征基因设计特异性引物探针并采用实时荧光定量pcr技术与搭配核酸提取或纯化试剂(磁珠法),具有以下优点:
80、(1)本发明针对特征基因设计特异性引物探针,扩增试剂性能优异,具有高特异性和高灵敏度的优点;
81、(2)本发明搭配提取试剂为无醇试剂,不易挥发,无刺激性气味,不存在易燃易爆等安全隐患,且便于储存运输;
82、(3)本发明搭配提取试剂常温储存运输,使用便捷,扩增试剂2~8℃储存运输,避免了反复冻融,用户使用更为便捷;
83、(4)本发明扩增试剂搭配全自动核酸提纯及实时荧光pcr分析系统,上机后即可等待结果,极大的减少了人工操作步骤。
84、综上,本发明具有高通量、高灵敏度、高特异性、全自动的优势,为体外定性鉴定致泻大肠杆菌提供了高效的解决方法,具有重要的临床意义。
- 还没有人留言评论。精彩留言会获得点赞!