一种大位阻杂原子化合物的合成方法及其应用
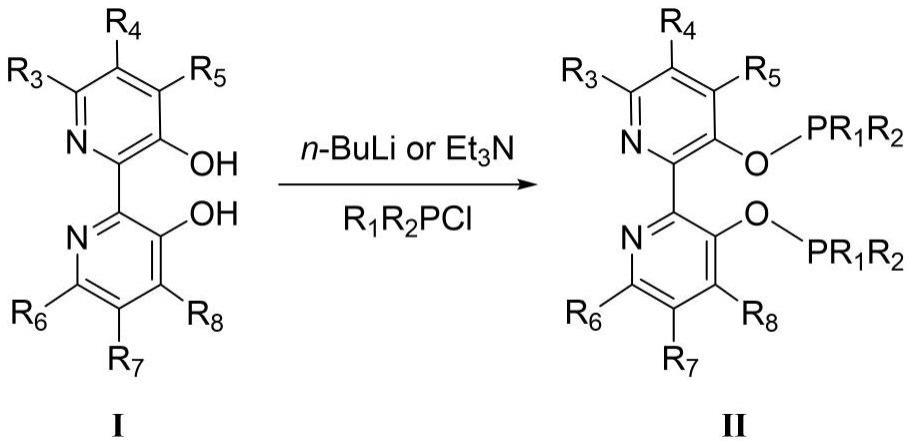
本发明涉及一种大位阻联吡啶基二酚及其双亚膦酸酯配体的制备合成方法,以及在丙烯和混合碳四氢甲酰化反应中的应用。
背景技术:
1、氢甲酰化反应自1938年被otto roelen教授发现以来(chemabstr,1994,38-550),在工业当中得到了非常巨大的应用。由于醛类物质可以非常容易地转化为相应的醇、羧酸、酯、亚胺等等在有机合成中具有重要用途的化合物,通过氢甲酰化反应合成的醛类物质在工业生产中被大规模合成。每年工业生产中通过氢甲酰化反应生产的醛类物质现已达到1000万吨(adv.synth.catal.2009,351,537–540)。
2、亚磷酸酯在工业上主要用途是在塑料、橡胶等高分子材料中用于抗氧化剂、热稳定剂、阻燃剂等。它是亚磷酸羟基衍生物,根据分子中羟基的多少,可以分为亚磷酸单酯rop(oh)2、亚磷酸二酯(ro)2poh和亚磷酸三酯(ro)3p。羟基或烷氧基被卤原子取代,形成卤代亚磷酸酯。在卤代亚磷酸酯中,以氯代亚磷酸酯为最重要的三价有机磷化合物中间体。最常见的的工业制备亚磷酸酯方法为直接酯化法,是指以三价磷的卤代物为原料,通过控制一定反应条件与醇类反应。
3、在氢甲酰化反应中,虽然双齿膦配体和四齿膦配体被国外大型化学公司如basf、dow、shell和eastman及一些研究小组广泛报导及专利化。现有技术中已知的双亚磷酸酯和多亚膦酸酯结构均以联苯二酚、联苯多酚(三酚和四酚)或蒽为骨架。以联苯为骨架的双亚膦酸酯配体受水、酸、碱等影响比较大,稳定性较差,而以联吡啶基为骨架的双酚骨架却少被报导(eur.j.inorg.chem.2011,4978–4984)。因此,开发具有联吡啶基新型结构且能改善配体活性、选择性(化学选择性和区域选择性)和稳定性的双亚膦酸酯配体具有重要意义和实用性。
4、
5、由丙烯为原料,其氢甲酰化反应产物丁醛,在经过羟醛缩合、加氢等一系列反应得到工业上广泛运用的增塑剂邻苯二甲酸二辛脂(dehp)。dehp在中国每年的产量高于300万吨,而世界的年产量则高达1000万吨。但是,由于丙烯原料价格逐年上涨,而且增塑剂dehp分子量较小,具有裂解性且易挥发,对人体毒害较大,已与2015年被欧盟列入reach法规禁止生产以及回收利用。目前的改进目前改进的工艺是通过混合/醚后丁烯的氢甲酰化反应得到戊醛,经过类似的后续反应生产高分子量的新型增塑剂dphp。dphp不易裂解且毒性低。目前,这一技术有望逐步取代传统技术。传统的基于pph3的技术只能实现1-丁烯的氢甲酰化反应,1-丁烯的产本高,更为廉价的原料为混合丁烯或醚后丁烯。国内的氢甲酰化工业装置主要以pph3和陶氏化学(dow chemical)所使用的双齿亚膦酸酯配体(biphephos)为主。使用国外的催化剂和工艺,除了需要支付高昂的专利费和工艺包转让费用以外,陶氏化学的biphephos配体在空气中长时间不稳定、容易水解、酸解且容易阻塞管路,还需要不定时的添加配体以保证催化活性。
6、相比于双齿亚膦酸酯配体biphephos而言,本发明中发展的一种联吡啶基双亚膦酸酯配体及其衍生物的制备具有易于合成且可以放大合成、收率较高、反应活性较好、直链醛产物收率高、对水氧极其稳定、不易分解等特点。同时,经过初步的工业小试研究以及对比biphephos和其它二齿膦配体,本发明开发的新型联吡啶基双亚膦酸酯配体在丙烯、混合碳四的氢甲酰化反应中可以实现较高的转化率、正异比以及较好的活性和稳定性,具有很大的潜力和实用价值。
技术实现思路
1、本发明目的是为了开发一种新型联吡啶基二酚及其双亚膦酸酯配体高效合成方法。其特点是:原料廉价易得、碳碳键偶联的金属配合物制备相对简单、后处理步骤少、联吡啶基二酚骨架偶联收率较高和可以放大合成。
2、本发明所述的新型联吡啶基二酚是一种制备新型联吡啶基双亚膦酸酯配体的重要中间体,该二酚化合物及其双亚膦酸酯化合物结构如式i、ii所示:
3、
4、本发明提供了一种大位阻杂原子化合物的合成方法,在通式i和ii所示结构中,r1、r2分别独立地为o、c(=o)o、oc(=o)、c1~c6烷氧基、苯基、苯氧基、萘基、萘氧基、四氢萘基、四氢萘氧基;当r4和r7的取代基为h或d时,r3~r8各基团分别独立地为c1-c4烷基、c1-c4烷氧基、c1-c4烷硫基。
5、进一步地,大位阻杂原子化合物根据以下任一方法制备:
6、方法一:
7、
8、方法二:
9、
10、方法三:
11、
12、进一步地,方法一中的催化前体为ni(oac)2或pd(oac)2时,配体为三苯基膦、xphos或bi-dime,碱金属盐为k2co3、na2co3、k3po4、na3po4中的一种或多种的混合。
13、进一步地,方法二中使用三氯化铁催化进行碳碳键偶联反应时,加入一定比例的有机碱tmeda或dmeda,用于活化c-h键提高偶联效率和反应收率。
14、进一步地,不同于方法一和二,方法三的起始原料为3-甲氧基吡啶,经过溴代后得到起始原料1。化合物1与镁反应得到吡啶氯化镁格氏试剂,经过镍或钯催化的kumada交叉偶联反应,得到二酚化合物。
15、进一步地,方法一、二和三中所涉及到傅克烷基化反应,需要在后处理中加入naoh、koh、na2co3或k2co3无机碱,将ph调至7以上,将产物游离至有机相。
16、进一步地,通过用丁基锂锂化或者有机弱碱做缚酸剂的大位阻联吡啶基二酚滴加到膦氯溶液中,得到新型联吡啶基双亚膦酸酯配体:
17、
18、具体操作如下:
19、第1步,于氮气氛围下向反应容器中依次加入联吡啶基二酚以及有机溶剂,得第一混合液;或者于氮气氛围下向反应容器中依次加入联吡啶基二酚以及有机溶剂,并在低温条件下滴加正丁基锂,滴加完毕后升至室温进行回流反应,得锂化后第一的混合液;
20、第2步,在低温条件下向所述锂化后第一混合液或第一混合液中滴加联苯基、亚甲基双苯基、联萘基、苯甲酸基、邻苯基或含有苯基、萘基和芳基型等的氯代亚膦酸酯的有机溶液或以上所列出的氯代亚膦酸酯和缚酸剂的混合溶液,滴加完毕后进行室温反应,经浓缩处理,即得;
21、上述反应中,正丁基锂的用量2~4当量,缚酸剂为三乙胺、n,n-二异丙基乙胺、吡啶中的任意一种,用量为5~20当量,反应温度为-78~80℃,反应时间12~48小时,反应溶剂为甲苯、四氢呋喃、乙醚、2-甲基四氢呋喃、甲基叔丁基醚、异丙醚、苯甲醚、乙二醇二甲醚、二乙二醇二甲醚、丁醚、环戊基甲醚或1,4-二氧六环中的任意一种;
22、其中,用通式ii表示的一类新型联吡啶基双亚膦酸酯配体结构如下:
23、
24、
25、上述酯化反应中,重结晶纯化大位阻联吡啶基双亚膦酸酯化合物的溶剂为乙酸乙酯、甲苯、二氯甲烷、乙醇、乙腈、石油醚、正己烷、四氢呋喃中的任意一种或几种。
26、本发明提供了一种用于催化烯烃氢甲酰化反应的金属有机络合物,所述金属有机络合物包括过渡金属前体和配体,所述配体包括上述任意一种或多种的双亚膦酸酯组合,所述过渡金属前体包括co、pt、ru、rh、ir或pd中的任意一种或至少两种组合。
27、进一步地,所述烯烃主要包括c3~c10的端烯和内烯烃,其中,碳三烯烃为纯丙烯或丙烷脱氢后的丙烯与烷烃混合物,碳四烯烃包括混合碳四(mto、醚前/醚后碳四)、二聚碳四(二异丁烯,即:2,4,4-三甲基-1-戊烯和2,4,4-三甲基-2-戊烯混合物)、或者1-丁烯、2-丁烯、异丁烯和丁烷的组合。
28、本发明提供了一种以大位阻联吡啶基双亚膦酸酯配体与过渡金属组成的催化络合物,应用于丙烯以及混合碳四氢甲酰化反应,包括上述的金属有机络合物,其特征在于,按照以下工艺步骤及参数实现:
29、步骤1,在一个带有搅拌和加热设备的反应釜内,于惰性气体保护下,依次加入一定比例的新型大位阻联吡啶基双亚膦酸酯配体与铑金属前体,膦铑摩尔比在1~6:1左右,室温下搅拌络合0.5~1小时;
30、步骤2,随后,于惰性气体保护下,往反应釜内充入一定压力的丙烯,或用柱塞泵往反应釜内加入液化的混合碳四,铑催化剂浓度为30~250ppm,配体浓度为30~1500ppm,室温搅拌5~10分钟;
31、步骤3,搅拌均匀后,向反应釜内充入一定压力的co与h2,氢气与一氧化碳摩尔比在1:1至1:3之间,总压为1.0mpa至3.0mpa之间;丙烯的压力为0.4至0.8mpa之间,反应的温度为70至100℃之间,反应时间为1至4小时。
- 还没有人留言评论。精彩留言会获得点赞!