对氰基苯甲酸的制备方法及其应用与流程
本发明属于有机合成领域,特别是有机药物领域,更为具体的说是涉及对氰基苯甲酸的制备方法及其应用。
背景技术:
1、氨甲环酸又称止血环酸,凝血酸,与止血芳酸相似。在临床上最初只作为止血剂使用,但在后续的应用实践中意外发现,它对于黄褐斑和淡化黑色素有非常好的作用。
2、因此,作为黄褐斑或者其他色素沉淀的常规治疗方案,口服氨甲环酸的临床应用越来月光。氨甲环酸的化学结构式如下:
3、
4、在该结构中,包含有两个手性碳离子,现有技术中以1,4-环己烷二甲醇为原料经溴化、氧化、氨化和氢化一系列步骤制备氨甲环酸,该反应第一步收率仅43%,且最后一步手性制备时产生大量异构体,造成产品纯度低,路线整体收率不到20%。
5、对氰基苯甲酸化学名4-氰基苯甲酸,其化学结构式如下,
6、
7、作为一种中间体化合物,经过反应能够得到氨甲环酸,为氨甲环酸合成提供了新的思路。
8、目前对氰基苯甲酸合成的方法主要有以下几种:
9、(1)以对氨基苯甲酸为起始原料,经氰化得到对氰基苯甲酸,该合成中需要用到剧毒氰化试剂,而且反应副产物多,对环境不友好,不适合绿色生产的需要。
10、(2)以对甲醇苯甲酸为起始原料,经二氧化锰氧化后,进一步氰化得到对氰基苯甲酸,该合成中需要用无水甲酸,不仅刺激性大,而且产物收率低,对环境污染严重。
11、(3)以氨氧化法合成对氰基苯甲酸,但是该合成中需要用到高温、高压条件,生产成本高,安全威胁大,不适合工业化生产。
12、(4)催化芳基卤代烃氰基化合成,该方法中使用的氰基化试剂或有剧毒,或本身不稳定,难于仓储,或带来重金属污染,或需要使用贵金属使得生产成本增高,因此不适合于工业化大生产。
技术实现思路
1、本发明所要解决的技术问题是提供一种新的对氰基苯甲酸的制备方法,从而能够避免现有合成方法中存在的毒性大、产率低、对环境不友好等问题。
2、为了解决上述技术问题,本发明公开了对氰基苯甲酸的制备方法,所述制备方法是以对二苯甲酸为原料依次经过酯化、酰胺化、氰化获得对氰基苯甲酸,其合成路线如下:
3、
4、其中r为c1-4烷基;
5、(1)为醇,包括但不限于甲醇、乙醇、异丙醇、叔丁醇;(2)为氨气;(3)为乙酸酐。
6、优选地,r为c1-4烷基是指包含c1-c4的直链烷基和支链烷基,包括但不限于甲基。
7、进一步优选地,化合物1与醇的摩尔比为1:1~3。
8、进一步优选地,所述化合物2与氨气的混合摩尔比为1:1~2。
9、进一步优选地,所述对氰基苯甲酸的制备方法包括以下步骤:
10、a.将对苯二甲酸、醇、浓硫酸加入反应溶剂a中,加热至回流,搅拌,反应,得到化合物1;
11、b.将化合物1加入反应溶剂b中,置换空气后,通入氨气,升温至80±10℃,封闭,搅拌,反应,得到化合物2;
12、c.将化合物2与乙酸酐混合溶解,加热至回流,搅拌,反应,加压浓缩至干,得到化合物3。乙酸酐即是反应物又是反应溶剂,反应后多余的溶剂通过加压浓缩能够完全排出,从而获得目标产物化合物3。
13、优选地,反应溶剂a与反应溶剂b均为甲苯。因此使得产品的处理工艺更加简单。
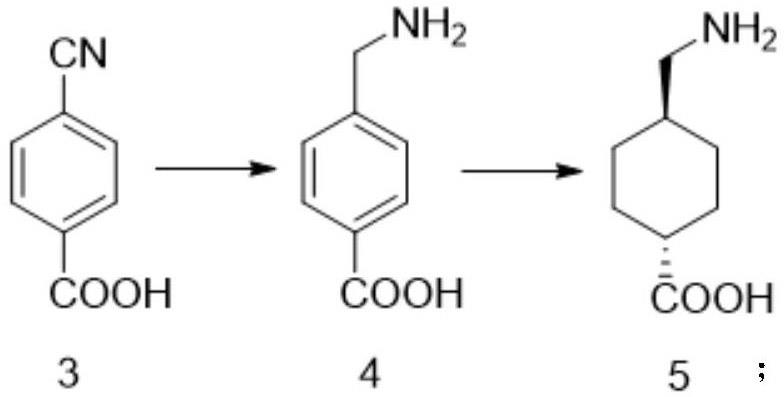
14、同时,本发明还进一步公开了化合物3(对氰基苯甲酸)在制备氨甲环酸中的应用,具体地,化合物3(对氰基苯甲酸)加氢还原形成化合物4后,进一步加氢还原形成目标手性化合物(化合物5),其合成路线如下:
15、
16、进一步优选地,所述化合物3加氢还原形成化合物4时,加氢压力为20~40bar。该反应中所用催化剂为无水cobr2。
17、进一步优选地,所述化合物4加氢还原形成化合物5时,加氢压力为0.5~1bar。该反应中所用催化剂为pto2。
18、进一步地,本发明还公开了化合物3合成化合物5的制备方法,具体包括以下步骤:
19、d.将化合物3加入含有无水cobr2和三乙基硼氢化钠的thf溶液体系中,置换空气后,通入氢气,并加压至20~40bar,升温至110~130℃反应;
20、反应产物经过滤后,取滤液,加入盐酸,得到白色沉淀,真空干燥得到化合物4;
21、e.将化合物4加入含有pto2的反应器中,再依次加入水、浓硫酸,置换空气后,通入氢气,并加压至0.5~1bar升温至40~50℃反应;
22、上述d和e为可分离的步骤。也即是说,可以采用d步骤制备得到化合物4后,以其他方式将化合物4进一步转化得到化合物5;或者先以其他方式将化合物3加氢还原得到化合物4,然后再以e的方式将化合物4转化为化合物5。
23、反应产物经过滤,取滤液升温至80~90℃,调节ph至7±0.5,过滤,滤液浓缩,得到浓缩残余物;
24、将浓缩残余物与碱混合并升温至250±10℃,反应;
25、反应物降温至70±5℃,加水,并调节溶液ph至5±0.5,过滤,滤液降温至5~10℃,搅拌、静置,析出晶体,过滤,得到化合物5。
26、优选地,浓缩残余物与碱混合反应中,碱为氢氧化钡。
27、优选地,化合物3制备化合物4的过程中,反应产物经过硅藻土过滤。
28、本发明公开了一种新的对氰基苯甲酸的制备方法,以对苯二甲酸为原料,通过酯化、酰胺化、氰化制备得到目标化合物对氰基苯甲酸,不仅收率大大提高,而且整个反应过程条件温和,无需使用毒性大、不稳定、危险性高的氰化试剂,特别是在氰化步骤中,利用易于除去的乙酸酐同时作为反应溶剂和反应物,可以过量添加,不仅反应收率和产物纯度进一步提高,而且后处理工艺简单。
29、本发明进一步利用制备得到的对氰基苯甲酸制备氨甲环酸,手性纯度可达99.76%,相比于传统的1,4-环己烷二甲醇作为原料的制备方法,不仅成本大大降低,而且收率大大提高,整个合成路线对环境友好度高,是一种适合于推广的工业化生产方法。
技术特征:
1.对氰基苯甲酸的制备方法,其特征在于:所述制备方法是以对二苯甲酸为原料依次经过酯化、酰胺化、氰化获得对氰基苯甲酸,其合成路线如下:
2.根据权利要求1所述的对氰基苯甲酸的制备方法,其特征在于:化合物1与醇的摩尔比为1:1~3。
3.根据权利要求1所述的对氰基苯甲酸的制备方法,其特征在于:所述化合物2与氨气的混合摩尔比为1:1~2。
4.根据权利要求1所述的对氰基苯甲酸的制备方法,其特征在于:所述对氰基苯甲酸的制备方法包括以下步骤:
5.根据权利要求4所述的对氰基苯甲酸的制备方法,其特征在于:反应溶剂a与反应溶剂b均为甲苯。
6.权利要求1至5中任意一项所述的对氰基苯甲酸制备氨甲环酸的方法,其特征在于:化合物3加氢还原形成化合物4后,进一步加氢还原形成化合物5,其合成路线如下:
7.权利要求1至5中任意一项所述的对氰基苯甲酸制备氨甲环酸的方法,其特征在于:化合物3加氢还原形成化合物4后,进一步加氢还原形成化合物5,其合成路线如下:
8.根据权利要求6所述的方法,其特征在于:所述化合物3加氢还原形成化合物4时,加氢压力为20~40bar。该反应中所用催化剂为无水cobr2。
9.根据权利要求7所述的方法,其特征在于:所述化合物4加氢还原形成化合物5时,加氢压力为0.5~1bar。该反应中所用催化剂为pto2。
10.根据权利要求6所述的方法,其特征在于:化合物3制备化合物4的过程中,反应产物经过硅藻土过滤。
技术总结
本发明属于有机合成领域,特别是有机药物领域,更为具体的说是涉及对氰基苯甲酸的制备方法及其应用,首先本发明公开了一种新的对氰基苯甲酸的制备方法,以对苯二甲酸为原料,通过酯化、酰胺化、氰化制备得到目标化合物对氰基苯甲酸,不仅收率大大提高,而且整个反应过程条件温和,无需使用毒性大、不稳定、危险性高的氰化试剂,特别是在氰化步骤中,利用易于除去的乙酸酐同时作为反应溶剂和反应物,可以过量添加,不仅反应收率和产物纯度进一步提高,而且后处理工艺简单。进一步地利用制备得到的对氰基苯甲酸制备氨甲环酸,手性纯度可达99.76%,而且收率大大提高,是一种适合于推广的工业化生产方法。
技术研发人员:朱小亮,平巍
受保护的技术使用者:上海绿智创领医药科技有限公司
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!