邻苯二甲酰亚胺类衍生物、包含其的药物组合物及其医药用途
本发明属于邻苯二甲酰亚胺类衍生物,具体涉及一种作为2型钾-氯共转运蛋白kcc2激动剂的邻苯二甲酰亚胺类衍生物及用途,以及相关药物筛选方法。
背景技术:
1、神经系统疾病包括脑或脊髓损伤、脑卒中、病理性疼痛、运动障碍性疾病、神经退行性病变、神经系统遗传及发育异常等,范围广泛,病情严重,往往会导致残疾,是目前对人类生命健康威胁最大的疾病种类。但是由于导致偏瘫的神经系统疾病的复杂性,相关研究尽管历经多年,但仍然缺乏有效的治疗药物,因而罹患这些疾病的患者无法得到有效的治疗,目前能促进偏瘫患者功能恢复的药物在市场上还是空白。
2、近期的科学研究证实脑卒中、脊髓损伤与癫痫等神经系统疾病与阳离子-氯离子共转运蛋白(cation-chloride cotransporters,cccs),包括纳-钾-2氯共转运蛋白1与2亚型(nkcc1,nkcc2),钾-氯共转运蛋白1-4亚型(kcc1-kcc4),纳-氯共转运蛋白(ncc)等的功能异常相关。这些共转运蛋白参与调节了神经元细胞内部氯离子浓度,进而维持神经元的兴奋性与抑制性的平衡。进一步的研究发现神经系统疾病与神经元细胞内部氯离子浓度和神经元功能异常有着非常显著的联系。比如,在中枢神经系统中,kcc2突变会显著影响其向细胞外转运氯离子的活性,进而引发神经系统疾病。
3、最近,为了治疗kcc2相关的神经系统疾病,来自加拿大的研究人员筛选了一系列kcc2的激动剂小分子化合物,最终发现一种kcc2特异性的clp系列化合物。初步的生化实验表明,clp257能显著提高kcc2向细胞外转运氯离子的活性(gagnon et al.,2013)。但是,近期的研究发现clp290药物的活性一般,水溶性差,生物利用度低,因此亟待筛选出新的效果更好与特异性更高的药物,以满足临床试验的要求(cardarelli et al.,2017)。
4、目前,无论是开发cccs的激动剂或是抑制剂类药物,都离不开对药物分子和靶标蛋白之间相互作用的识别。随着计算机技术发展和现代生物医学技术的推广,生物医学数据量呈现指数爆炸的增长态势。在足够的数据量的支持下,基于虚拟高通量筛选的人工智辅助药物设计己经成为药物化合物分子发现的重要技术。人工智能(ai)辅助虚拟药物筛选技术可以缩短药物的研发时间,节约研发成本。其中,基于准确靶标分子三维结构与序列层面的多模态信息的虚拟筛选技术是目前虚拟筛选中最具优势的方法。因此本发明基于这项技术,发现一系列活性强,选择性高、成药性好的小分子化合物。本发明包括这个小分子化合物的化学结构、用途、制备方法、筛选及优化方法。
技术实现思路
1、本发明的发明人发现,具有以下式(i)所示的结构的化合物在具有良好的2型钾-氯共转运蛋白kcc2激活活性,其靶向神经细胞上的离子通道,能够与其紧密结合并产生激动作用,从而起到神经性疾病的治疗和预防目的。这些化合物的新的药理活性是基于人工智能的方法获得的:首先从海量化合物库中(三千万化合物库中)进行初筛,基于人工智能模型对其亲和力进行预测、各化合物的成药性与理性化指标的评估结果,进行综合排序,对排名在前30的分子进行湿实验验证确定分子骨架,根据结果继续对候选化合物库进行缩库(缩至3万左右化合物),基于上述同样的方法进一步排序,对其前4个化合物进行湿实验,得到候选可成药的化合物;该方法的运用能缩短并加速很多新药的发现与筛选周期,节省药物研发成本,同时在药物设计过程中起到指导与启发的作用。
2、具体而言,本发明提供以下式(i)所示的邻苯二甲酰亚胺类化合物或者其药学上可接受的盐、酯、光学异构体、互变异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药,
3、
4、其中:
5、环a为饱和或部分不饱和的3-10元杂环基、饱和或部分不饱和的3-10元桥杂环基、取代或未取代的c6-14芳基、5-14元杂芳基;
6、e选自h、卤素、nh2、oh、sh、cn、胍基、c1-6烷基取代氨基、取代或未取代的c1-10的脂肪族烃基、取代或未取代的饱和或部分不饱和的3-10元桥环烷基、取代或未取代的饱和或部分不饱和的3-10元的杂环基、取代或未取代的饱和或部分不饱和的3-10元桥杂环基、取代或未取代的饱和或部分不饱和的3-10元稠杂环基、取代或未取代的c6-14芳基、或者取代或未取代的5-14元的杂芳基、-c(=o)r5、-oc(=o)r5、-c(=o)or5、-or5、-sr5、-s(=o)r5、-s(=o)2r5、-s(=o)2n(r5)2、-n(r5)2、-c(=o)n(r5)2、-nr5-c(=o)r5、-nr5-c(=o)or5、-nr5-s(=o)2-r5、c(=o)-n(r5)2、-c1-6亚烷基-n(r5)2、-c1-6亚烷基-or5、-c1-6亚烯基-or5和-o-c1-6亚烷基-n(r5)2、其中,r5为h、nh2、c1~c6烷基、饱和或部分不饱和的c3-6环烃基、饱和或部分不饱和的3-10元杂环基或者c6-10芳基;
7、l1和l2各自独立地表示化学键、或直链或支链的c1~c6的亚烷基链,其中所述直链或支链的c1~c6的亚烷基链可选地被一或多个选自-o-、-co-、-c(=o)o-、-conh-、-nhco-、-nhconh-、-nh-、-nr5-、-c(r5)2-、-s-、亚磺酰基、磺酰基、亚磺酰氧基、磺酰氧基、-氨基磺酰基氨基-、亚炔基、亚烯基、亚环烷基、或它们的任意组合中的二价基团中断一或多次;或者所述直链或支链的c1~c6的亚烷基链可以被选自-c(=o)r5、-oc(=o)r5、-c(=o)or5、-or5、-sr5、-s(=o)r5、-s(=o)2r5、-s(=o)2n(r5)2、-n(r5)2、-c(=o)n(r5)2、-nr5-c(=o)r5、-nr5-c(=o)or5、-nr5-s(=o)2-r5、-c(=o)-n(r5)2、-c(=o)-n(or5)r5、-c1-6亚烷基-n(r5)2、-c1-6亚烷基-or5、-c1-6亚烯基-or5和-o-c1-6亚烷基-n(r5)2中的一种或多种取代,
8、r1选自卤素、氰基、取代或未取代的c1-c3的烷基、取代或未取代的c1-c3的烷氧基、nh2、oh、sh、cn、胍基、c1-6烷基取代氨基;n为0-3的整数,n为2以上时,多个r1可以相同的也可以不同;多个r1连同它们所连接的苯环的碳原子可以形成3-7元的脂肪族环基或杂环基;
9、r2独立地选自取代或未取代的c1-c3烷基、羟基、卤素、氰基、氨基、c1-c3烷基取代氨基、取代或未取代的c1-c3烷氧基、取代或未取代的c3-c6环烷基、取代或未取代的c3-c6杂环基、取代或未取代的苯基、取代或未取代的5-6元的杂芳基、s(o)2rb1、s(o)2nh2、s(o)2nhrb1、s(o)2nrb1rb2、nhs(o)2rb1、nrb1s(o)2rb2、s(o)(nh)rb1、s(o)(nrb1)rb2、c(o)rb1、c(o)orb1、oc(o)rb1、nhc(o)rb1、nrb1c(o)rb2、nhc(o)orb1、nrb1c(o)orb2、c(o)nh2、c(o)nhrb1、c(o)nrb1rb2、c(o)nh s(o)2rb1、s(o)2nhc(o)rb1;rb1和rb2分别独立地选自取代或未取代的c1-c3的烷基、取代或未取代的3-6元的环烷基或杂环基,或者rb1和rb2连同它们所连接的n原子形成3-7元的杂环基;n为0-4的整数,n为2以上时,多个r2可以相同的也可以不同,
10、表示与母核连接的位置,―—”划过的环结构的表达方式,表示连接位点于该环结构上任意能够成键的位置,
11、上述的取代或未取代是指基团中的h被选自卤素、氰基、羟基、c1~c3烷氧基、c4~c6杂环烷基中的一种或者至少两种的组合以上的基团所取代,或者指基团中的-ch2-中的两个h被替换成氧代=o。
12、在本发明优选的实施方式中,环a及其r2的组合为选自以下的基团:
13、
14、
15、
16、
17、表示与母核连接的位置,hal表示卤原子,“—”划过的环结构的表达方式,表示连接位点于该环结构上任意能够成键的位置。
18、在本发明优选的实施方式中,l1和l2各自独立的表示单键或者式(v)所示的二价基团,
19、
20、n0为0或1;m为1-5的整数、优选为2或3;n1为0-3的整数,优选为1;n2为0-3的整数,优选为1;n3为0-3的整数,优选为1;n4为0-3的整数,优选为1;n5为0-3的整数,优选为1;
21、z0为单键、-ch2-、-chr9-、-nh-、-o-、-s-、
22、
23、-co-、或-c(=o)o-;
24、z1为单键、-ch2-、-chr9-、-nh-、-o-、-s-、
25、
26、-co-、或-c(=o)o-;
27、z2为单键、-ch2-、-chr9-、-nh-、-o-、-s-、
28、
29、-co-、或-c(=o)o-;
30、其中r9为c1-6烷基取代氨基、取代或未取代的c1-10的脂肪族烃基、-c(=o)r10、-oc(=o)r10、-c(=o)or10、-or10、-sr10、-s(=o)r10、-s(=o)2r10、-s(=o)2n(r10)2、-n(r10)2、-c(=o)n(r10)2、-nr10-c(=o)r10、-nr10-c(=o)or10、-nr10-s(=o)2-r10、c(=o)-n(r10)2、-c1-6亚烷基-n(r10)2、-c1-6亚烷基-or10、-c1-6亚烯基-or10和-o-c1-6亚烷基-n(r10)2;其中,r10为h、胍基、c1~c6烷基、饱和或部分不饱和的c3-6环烃基、饱和或部分不饱和的3-10元杂环基或者c6-10芳基;表示连接的位置,两端连接方向任意调换,
31、上述的取代或未取代是指基团中的h被选自卤素、氰基、硝基、羟基、氨基、醛基、酯基、c1~c30烷基、c1-6烷基取代氨基、c1~c30烷氧基、c2~c20杂环烷基、c1~c30烷基硅基、c6~c30芳基、c6~c30芳氧基、c3~c30杂芳基、c6~c30芳基氨基或c3~c30杂芳基氨基中的一种或者至少两种的组合以上的基团所取代,或者指基团中的-ch2-中的两个h被替换成氧代=o。
32、在本发明优选的实施方式中,l1为选自亚甲基、亚乙基、亚丙基、以及下述二价基团中的基团:
33、
34、l2为选自化学键、亚甲基、亚乙基、亚丙基以及下述二价基团中的基团:
35、
36、表示与母核连接的位置,“—”划过的环结构的表达方式,表示连接位点于该环结构上任意能够成键的位置。
37、在本发明优选的实施方式中,m为0~2的整数,r1选自卤原子、甲基、氨基、环丙基、丙基、以下基团:
38、
39、或者两个r1之间连接性形成取代或未取代的环戊烷或取代或未取代的环己烷结构,
40、上述的取代或未取代是指基团中的h被选自卤素、氰基、硝基、羟基、氨基、醛基、酯基、c1~c30烷基、c1-6烷基取代氨基、c1~c30烷氧基、c2~c20杂环烷基、c1~c30烷基硅基、c6~c30芳基、c6~c30芳氧基、c3~c30杂芳基、c6~c30芳基氨基或c3~c30杂芳基氨基中的一种或者至少两种的组合以上的基团所取代,或者指基团中的-ch2-中的两个h被替换成氧代=o,
41、表示与母核连接的位置,hal表示卤原子,“—”划过的环结构的表达方式,表示连接位点于该环结构上任意能够成键的位置。
42、本发明的另一方面提供一种药物组合物,其包含预防或治疗有效量的本发明的化合物或者其药学上可接受的盐、酯、光学异构体、互变异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药,以及药学上可接受的载体,所述药物组合物为固体制剂、半固体制剂、液体制剂或气态制剂。
43、在优选的实施方式中,所述的药物组合物的剂型为口服剂型或注射剂,所述口服剂型包括胶囊剂、片剂、丸剂、散剂和颗粒剂。用于口服给药的液体剂型包括药学上可接受的乳液、溶液、悬浮液、糖浆或酊剂,
44、所述注射剂包含生理上可接受的无菌含水或无水溶液、分散液、悬浮液或乳液,和用于重新溶解成无菌的可注射溶液或分散液的上述的化合物或者其药学上可接受的盐、酯、光学异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药的无菌粉末。
45、本发明提供上述式(i)所述化合物或其药学上可接受的盐、酯、光学异构体、互变异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药在制备2型钾-氯共转运蛋白kcc2激活剂中的用途。
46、本发明提供上述式(i)所述化合物或其药学上可接受的盐、酯、光学异构体、互变异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药在制备与2型钾-氯共转运蛋白kcc2相关疾病的药物中的用途。
47、优选的实施方式中,所述与2型钾-氯共转运蛋白kcc2相关疾病为脑或脊髓损伤、脑卒中、病理性疼痛、运动障碍性疾病、神经退行性病变、神经系统遗传及发育异常。
48、本发明提供上述式(i)所述化合物或其药学上可接受的盐、酯、光学异构体、互变异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药在制备治疗或预防神经系统疾病的药物中的用途。其中,所述神经系统疾病为脑或脊髓损伤、脑卒中、病理性疼痛、运动障碍性疾病、神经退行性病变、神经系统遗传及发育异常。
49、本发明的另一方面还提供一种治疗或预防神经系统疾病的药物的筛选方法,阳离子-氯离子共转运蛋白药物细胞筛选平台的建立步骤:通过病毒包装获得表达cl-敏感的荧光蛋白clomeleon的慢病毒lenti-puro-clomeleon,用该病毒感染ng108-15细胞系并经过抗生素筛选获得稳定表达clomeleon的ng108-cl细胞系,利用稳定表达clomeleon的ng108-cl细胞系目标化合物的2型钾-氯共转运蛋白kcc2激活活性进行测定。
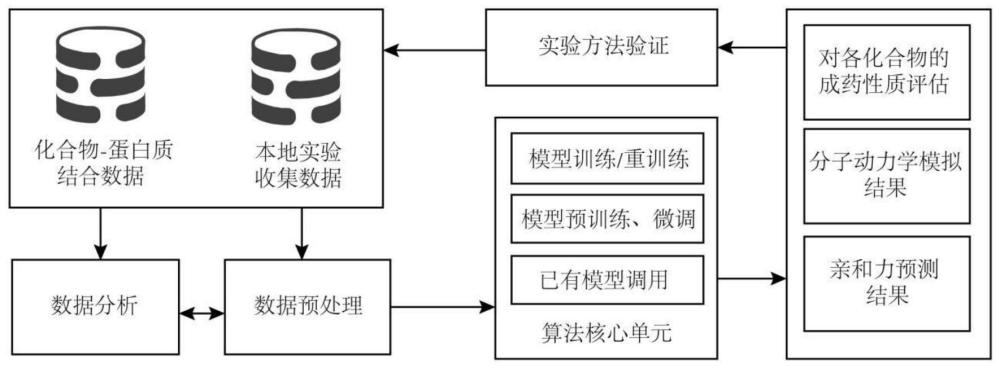
50、本发明的另一方面还利用候选化合物靶向kcc2蛋白激动剂的结合口袋,序列信息与结构信息,具有以下步骤并通过数据分析验证数据的质量、分布以及可学习性,应用数据预处理,将文本记录的数据进行向量化表征,以输入进算法核心单元,作为模型训练时的输入数据;
51、靶标蛋白确定和亲和力计算步骤,ai模型预测模块中,以kcc2蛋白作为靶标蛋白,提取该蛋白其结构信息与序列信息进行提取并表征,作为模型的第一输入信息;分别向量化表征化合物库中的每一个化合物分子信息,作为模型的第二输入信息,算法模型将结合化合物与靶蛋白信息,分别输出每一个化合物与该靶蛋白结合的亲和力数值;
52、分子对接步骤,以蛋白质的三维结构信息与化合物的三维结构信息通过分子动力学原理进行仿真模拟,并给出基于分子动力学的结合力预测分数结果;
53、成药性评估步骤,基于成药性原理,针对每一个化合物的性质,从亲脂性,分子质量,lipinski五原则以及qed进行综合评估;并基于化合物性质,给出化合物的成药的综合分数;
54、基于亲和力数值、结合力预测分数和化合物的成药的综合分数,通过加权求和,得到综合亲和力分数,并依据综合亲和力分数,给出待筛选的苗头化合物名单,
55、药理药化验证步骤,基于药化实验和药理实验对所筛化合物进一步验证,得到真实的苗头化合物;
56、本发明的另一方面还提供一种治疗或预防神经系统疾病的药物的筛选系统,其靶向kcc2蛋白激动剂的结合口袋,序列信息与结构信息的获得苗头化合物,
57、系统包含网络输入/输出接口,用户输入/输出接口、处理单元、存储单元以及算法引擎;其中算法引擎的效能为s3中所述;存储单元用于存本地数据与实时更新云端数据库中上传的新的实验数据,以定期增加训练样本的多样性并提高数据质量;处理单元主要包含中央处理单元与图像处理单元,中央处理单元用于支持用户执行或提交指令和任务,支持数据的传输以及系统正常运行所必要的功能,图像处理单元用于支持模型训练、模型调用以及数据预测等任务;网络输入/输出接口用于网关的连接,保证网络的可及性与流畅性;用户输入/输出接口用于支持用户在本地或远程访问系统,发送指令和任务,具备以下模块:
58、候选分子确定和处理模块,并通过数据分析验证数据的质量、分布以及可学习性,应用数据预处理,将文本记录的数据进行向量化表征,以输入进算法核心单元,作为模型训练时的输入数据;
59、靶标蛋白确定和亲和力计算模块,ai模型预测模块中,以kcc2蛋白作为靶标蛋白,提取该蛋白其结构信息与序列信息进行提取并表征,作为模型的第一输入信息;分别向量化表征化合物库中的每一个化合物分子信息,作为模型的第二输入信息,算法模型将结合化合物与靶蛋白信息,分别输出每一个化合物与该靶蛋白结合的亲和力数值;
60、分子对接模块,以蛋白质的三维结构信息与化合物的三维结构信息通过分子动力学原理进行仿真模拟,并给出基于分子动力学的结合力预测分数结果;
61、成药性评估模块,基于成药性原理,针对每一个化合物的性质,从亲脂性,分子质量,lipinski五原则以及qed进行综合评估;并基于化合物性质,给出化合物的成药的综合分数。
62、以下说明本发明其他各要素进行更加详细的说明。
63、定义
64、除非在下文中另有定义,本文中所用的所有技术术语和科学术语的含义意图与本领域技术人员通常所理解的相同。提及本文中使用的技术意图指在本领域中通常所理解的技术,包括那些对本领域技术人员显而易见的技术的变化或等效技术的替换。虽然相信以下术语对于本领域技术人员很好理解,但仍然阐述以下定义以更好地解释本发明。
65、所谓的“包括”、“包含”、“具有”、“含有”或“涉及”及其在本文中的其它变体形式为包含性的(inclusive)或开放式的,且不排除其它未列举的元素或方法步骤。
66、如本文中所使用,所谓的“亚烷基”表示饱和二价烃基,优选表示具有1、2、3、4、5或6个碳原子的饱和二价烃基,例如亚甲基、亚乙基、亚丙基或亚丁基。
67、如本文中所使用,所谓的“烷基”定义为线性或支化饱和脂肪族烃。在一些实施方案中,烷基具有1至12个,例如1至6个碳原子。例如,如本文中所使用,所谓的“c 1-6烷基”指1至6个碳原子的线性或支化的基团(例如甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基、异戊基、新戊基或正己基),其任选地被1或多个(诸如1至3个)适合的取代基如卤素取代(此时该基团被称作“卤代烷基”)(例如ch2f、chf2、cf3、ccl3、c2f5、c2cl5、ch2cf3、ch2cl或-ch2ch2cf3等)。所谓的“c1-4烷基”指1至4个碳原子的线性或支化的脂肪族烃链(即甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基或叔丁基)。
68、如本文中所使用,所谓的“烯基”意指线性的或支化的单价烃基,其包含一个双键,且具有2-6个碳原子(“c2-6烯基”)。所述烯基为例如乙烯基、1-丙烯基、2-丙烯基、2-丁烯基、3-丁烯基、2-戊烯基、3-戊烯基、4-戊烯基、2-己烯基、3-己烯基、4-己烯基、5-己烯基、2-甲基-2-丙烯基和4-甲基-3-戊烯基。当本发明的化合物含有烯基时,所述化合物可以纯e(异侧(entgegen))形式、纯z(同侧(zusammen))形式或其任意混合物形式存在。
69、如本文中所使用,所谓的“炔基”表示包含一个或多个三键的单价烃基,其优选具有2、3、4、5或6个碳原子,例如乙炔基或丙炔基。
70、如本文中所使用,所谓的“环烷基”指饱和的单环或多环(诸如双环)烃环(例如单环,诸如环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环壬基,或双环,包括螺环、稠合或桥连系统(诸如双环[1.1.1]戊基、双环[2.2.1]庚基、双环[3.2.1]辛基或双环[5.2.0]壬基、十氢化萘基等)),其任选地被1或多个(诸如1至3个)适合的取代基取代。所述环烷基具有3至15个碳原子。例如,所谓的“c3-6环烷基”指3至6个成环碳原子的饱和的单环或多环(诸如双环)烃环(例如环丙基、环丁基、环戊基或环己基),其任选地被1或多个(诸如1至3个)适合的取代基取代,例如甲基取代的环丙基。
71、如本文中所使用,所谓的“亚环烃基”、“环烃基”和“烃环”是指具有例如3-10个(适合地具有3-8个,更适合地具有3-6个)环碳原子的饱和(即,“亚环烷基”和“环烷基”)或不饱和的(即在环内具有一个或多个双键和/或三键)单环或多环烃环,其包括但不限于(亚)环丙基(环)、(亚)环丁基(环)、(亚)环戊基(环)、(亚)环己基(环)、(亚)环庚基(环)、(亚)环辛基(环)、(亚)环壬基(环)、(亚)环己烯基(环)等。
72、如本文中所使用,所谓的“杂环基”、“亚杂环基”和“杂环”是指具有例如3-10个(适合地具有3-8个,更适合地具有3-6个)环原子、其中至少一个环原子是选自n、o和s的杂原子且其余环原子是c的饱和(即,杂环烷基)或部分不饱和的(即在环内具有一个或多个双键和/或三键)环状基团。例如,“3-10元(亚)杂环(基)”是具有2-9个(如2、3、4、5、6、7、8或9个)环碳原子和独立地选自n、o和s的一个或多个(例如1个、2个、3个或4个)杂原子的饱和或部分不饱和(亚)杂环(基)。亚杂环基和杂环(基)的实例包括但不限于:(亚)环氧乙烷基、(亚)氮丙啶基、(亚)氮杂环丁基(azetidinyl)、(亚)氧杂环丁基(oxetanyl)、(亚)四氢呋喃基、(亚)二氧杂环戊烯基(dioxolinyl)、(亚)吡咯烷基、(亚)吡咯烷酮基、(亚)咪唑烷基、(亚)吡唑烷基、(亚)吡咯啉基、(亚)四氢吡喃基、(亚)哌啶基、(亚)吗啉基、(亚)二噻烷基(dithianyl)、(亚)硫吗啉基、(亚)哌嗪基或(亚)三噻烷基(trithianyl)。所述基团也涵盖双环系统,包括螺环、稠合或桥连系统(诸如8-氮杂螺[4.5]癸烷、3,9-二氮杂螺[5.5]十一烷、2-氮杂双环[2.2.2]辛烷等)。亚杂环基和杂环(基)可任选地被一个或多个(例如1个、2个、3个或4个)适合的取代基取代。
73、如本文中所使用,所谓的“(亚)芳基”和“芳环”指具有共轭π电子系统的全碳单环或稠合环多环芳族基团。例如,如本文中所使用,所谓的“c6-10(亚)芳基”和“c6-10芳环”意指含有6至10个碳原子的芳族基团,诸如(亚)苯基(苯环)或(亚)萘基(萘环)。(亚)芳基和芳环任选地被1或多个(诸如1至3个)适合的取代基(例如卤素、-oh、-cn、-no2、c1-6烷基等)取代。
74、如本文中所使用,所谓的“(亚)杂芳基”和“杂芳环”指单环、双环或三环芳族环系,其具有5、6、8、9、10、11、12、13或14个环原子,特别是1或2或3或4或5或6或9或10个碳原子,且其包含至少一个可以相同或不同的杂原子(所述杂原子是例如氧、氮或硫),并且,另外在每一种情况下可为苯并稠合的。特别地,“(亚)杂芳基”或“杂芳环”选自(亚)噻吩基、(亚)呋喃基、(亚)吡咯基、(亚)噁唑基、(亚)噻唑基、(亚)咪唑基、(亚)吡唑基、(亚)异噁唑基、(亚)异噻唑基、(亚)噁二唑基、(亚)三唑基、(亚)噻二唑基等,以及它们的苯并衍生物;或(亚)吡啶基、(亚)哒嗪基、(亚)嘧啶基、(亚)吡嗪基、(亚)三嗪基等,以及它们的苯并衍生物。
75、如本文中所使用,所谓的“芳烷基”优选表示芳基或杂芳基取代的烷基,其中所述芳基、杂芳基和烷基如本文中所定义。通常,所述芳基可具有6-14个碳原子,所述杂芳基可具有5-14个环原子,并且所述烷基可具有1-6个碳原子。示例性芳烷基包括但不限于苄基、苯基乙基、苯基丙基、苯基丁基。
76、作为更具体地术语解释如下:
77、“烷基”指饱和脂肪族烃基团,包括1-20个碳原子,或1-10个碳原子,或1-6个碳原子,或1-4个碳原子,或1-3个碳原子,或1-2个碳原子饱和直链或支链的单价烃基,其中烷基可以独立任选地被一个或多个本发明所描述地取代基所取代。烷基基团更近一步地实例包括,包括但不限于甲基、乙基、正丙基、异丙基、正丁基、异丁基、叔丁基、仲丁基、正戊基、1,1-二甲基丙基、1,2-二甲基丙基、2,2-二甲基丙基、1-乙基丙基、2-甲基丁基、3-甲基丁基、正己基、1-乙基-2-甲基丙基、1,1,2-三甲基丙基、1,1-二甲基丁基、1,2-二甲基丁基、2,2-二甲基丁基、1,3-二甲基丁基、2-乙基丁基、2-甲基戊基、3-甲基戊基、4-甲基戊基、2,3-二甲基丁基等。烷基可以是任选取代或未取代的。
78、“烯基”指2-12个碳原子,或2-8个碳原子,或2-6个碳原子,或2-4个碳原子直链或支链的一价烃基,其中至少一个c-c为sp2双键,其中烯基的基团可以独立任选地被1个或多个本发明所描述的取代基所取代,其中具体的实例包括,但并不限于乙烯基、烯丙基和烯丁基等等。烯基可以是任选取代或未取代的。
79、“环烷基”是指饱和或部分不饱和单环或多环环状烃取代基,环烷基环包括3至20个碳原子,优选包括3至12个碳原子,更优选包含3至6个碳原子。单环环烷基的非限制性实施例包括,但不限于环丙基、环丁基、环戊基、环戊烯基、环己基、环己烯基、环己二烯基、环庚基、环庚三烯基、环辛基等;多环环烷基包括螺环、稠环和桥环的环烷基。环烷基可以是任选取代的或未取代的。
80、“螺环烷基”指5至18元,两个或两个以上环状结构,且单环之间彼此共用一个碳原子(称螺原子)的多环基团,环内含有1个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统。优选为6至14元,更优选为7至10元。根据环与环之间共用螺原子的数目将螺环烷基分为单螺、双螺或多螺环烷基,优选为单螺和双螺环烷基,优选为4元/5元、4元/6元、5元/5元或5元/6元。“螺环烷基”的非限制性实施例包括但不限于:
81、
82、“稠环烷基”指5至18元,含有两个或两个以上环状结构彼此公用一对碳原子的全碳多环基团,一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统,优选为6至12元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环稠环烷基,优选为双环或三环,更优选为5元/5元或5元/6元双环烷基。“稠环烷基”的非限制性实施例包括但不限于:
83、
84、“桥环烷基”指5至18元,含有两个或两个以上环状结构,彼此共用两个不直接相连接碳原子的全碳多环基团,一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统,优选为6至12元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环桥环烷基,优选为双环、三环或四环,更有选为双环或三环。“桥环烷基”的非限制性实施例包括但不限于:
85、
86、所述环烷基环可以稠合于芳基、杂芳基或杂环基环上,其中与母体结构连接在一起的环为环烷基,非限制性实施例包括茚满基、四氢萘基、苯并环庚烷基等。
87、“杂环基”、“杂环”或“杂环的”在本技术中可交换使用,本技术中可交换使用,都是指包含3-12个环原子的饱和或部分不饱和的单环、双环或三环的非芳香性杂环基,其中至少一个环原子原子是杂原子,如氧、氮、硫原子等。优选具有5至7元单环或7至10元双-或三环,其可以包含1,2或3个选自氮、氧和/或硫中的原子。“杂环基”的实例包括但不限于吗啉基,氧杂环丁烷基,硫代吗啉基,四氢吡喃基,1,1-二氧代-硫代吗啉基,哌啶基,2-氧代-哌啶基,吡咯烷基,2-氧代-吡咯烷基,哌嗪-2-酮,8-氧杂-3-氮杂-双环[3.2.1]辛基和哌嗪基。所述杂环基环可以稠合于芳基、杂芳基或环烷基环上,其中与母体结构连接在一起的环为杂环基。杂环基可以是任选取代的或未取代的。
88、“螺杂环基”指5至18元,两个或两个以上环状结构,且单环之间彼此共用一个原子的多环基团,环内含有1个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统,其中一个或多个环原子选自氮、氧、硫或s(o)m的杂原子,其余环原子为碳,m=1或2。优选为6至14元,更优选为7至10元。根据环与环之间共用螺原子的数目将螺杂环基分为单螺杂环基、双螺杂环基或多螺杂环基,优选为单螺杂环基和双螺杂环基。更优选为4元/4元、4元/5元、4元/6元、5元/5元或5元/6元单螺杂环基。“螺杂环基”的非限制性实施例包括但不限于:
89、
90、“稠杂环基”指含有两个或两个以上环状结构彼此公用一对原子的全碳多环基团,一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统,其中一个或多个环原子选自氮、氧、硫或s(o)m的杂原子,其余环原子为碳,m=1或2。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环稠杂环基,优选为双环或三环,更优选为5元/5元或5元/6元双环稠杂环基。“稠杂环基”的非限制性实施例包括但不限于:
91、
92、“桥杂环基”指5至18元,含有两个或两个以上环状结构,彼此共用两个不直接相连接的原子的多环基团,一个或多个环可以含有一个或多个双键,但没有一个环具有完全共轭的π电子的芳香系统,其中一个或多个环原子选自氮、氧、硫或s(o)m的杂原子,其余环原子为碳,m=1或2。优选为6至14元,更优选为7至10元。根据组成环的数目可以分为双环、三环、四环或多环桥杂环基,优选为双环、三环或四环,更有选为双环或三环。“桥杂环基”的非限制性实施例包括但不限于:
93、
94、“芳基”是指含有一个或者两个环的碳环芳香系统,其中所述环可以以稠合的方式连接在一起。所谓的“芳基”包括比如苯基、萘基、四氢萘基的芳香基团。优选芳基为c6-c10芳基,更优选芳基为苯基和萘基,最优选为苯基。芳基可以是取代或未取代的。所述“芳基”可与杂芳基、杂环基或环烷基稠合,其中与母体结构连接在一起的为芳基环,非限制性实施例包括但不限于:
95、
96、“杂芳基”是指芳香族5至6元单环或9至10元双环,其可以包含1至4个选自氮、氧和/或硫中的原子。“杂芳基”的实施例包括但不限于呋喃基,吡啶基,2-氧代-1,2-二氢吡啶基、哒嗪基、嘧啶基、吡嗪基、噻吩基、异噁唑基、噁唑基、噁二唑基、咪唑基、吡咯基、吡唑基、三唑基、四唑基、噻唑基、异噻唑基、1,2,3-噻二唑基、苯并间二氧杂环戊烯基、苯并咪唑基、吲哚基、异吲哚基、1,3-二氧代-异吲哚基、喹啉基、吲唑基、苯并异噻唑基、苯并噁唑基和苯并异噁唑基。杂芳基可以是任选取代或未取代的。所述杂芳基环可以稠合于芳基、杂环基或环烷基环上,其中与母体结构连接在一起的环为杂芳基环,非限制性实施例包括但不限于:
97、
98、“烷氧基”是指(烷基-o-)的基团。其中,烷基见本文有关定义。c1-c6的烷氧基为优先选择。其实例包括,但不限于:甲氧基、乙氧基、正丙氧基、异丙氧基、正丁氧基、异丁氧基、叔丁氧基等。
99、“卤代烷基”指具有一个或者多个卤素取代基的烷基,其中烷基基团具有如本发明所述的含义。卤代烷基的实例包括,但并不限于氟甲基、二氟甲基、三氟甲基、全氟乙基、1,1-二氯乙基、1,2-二氯丙基等。
100、“羟基”指-oh基团。
101、“卤素”是指氟、氯、溴和碘,优选氟、氯和溴。
102、“氨基”指-nh2。
103、“氰基”指-cn。
104、“硝基”指-no2。
105、“苄基”指-ch2-苯基。
106、“羧基”指-c(o)oh。
107、“乙酰基”指-c(o)ch3或ac。
108、“羧酸酯基”指-c(o)o(烷基)或(环烷基),其中烷基、环烷基的定义如上所述。
109、如本文中所使用,所谓的“卤代”或“卤素”基团定义为包括f、cl、br或i。
110、如本文中所使用,所谓的“含氮杂环”指饱和或不饱和的单环或双环基团,其在环中具有2、3、4、5、6、7、8、9、10、11、12或13个碳原子和至少一个氮原子,其还可任选地包含一个或多个(例如一个、两个、三个或四个)选自n、o、c=o、s、s=o和s(=o)2的环成员,其通过所述含氮杂环中的氮原子以及任一其余环原子与分子的其余部分连接,所述含氮杂环任选地为苯并稠合的,并且优选通过所述含氮杂环中的氮原子以及所稠合的苯环中的任一碳原子与分子的其余部分连接。
111、所谓的“取代”指所指定的原子上的一个或多个(例如一个、两个、三个或四个)氢被从所指出的基团的选择代替,条件是未超过所指定的原子在当前情况下的正常原子价并且所述取代形成稳定的化合物。取代基和/或变量的组合仅仅当这种组合形成稳定的化合物时才是允许的。
112、如果取代基被描述为“任选地被取代”,则取代基可(1)未被取代或(2)被取代。如果取代基的碳被描述为任选地被取代基列表中的一个或多个取代,则碳上的一个或多个氢(至存在的任何氢的程度)可单独和/或一起被独立地选择的任选的取代基替代。如果取代基的氮被描述为任选地被取代基列表中的一个或多个取代,则氮上的一个或多个氢(至存在的任何氢的程度)可各自被独立地选择的任选的取代基替代。
113、“单键”,“化学键”的表述可以认为表示相应位置不存在基团和原子。
114、如果取代基被描述为“独立地选自”一组,则各取代基独立于另一者被选择。因此,各取代基可与另一(其他)取代基相同或不同。
115、如本文中所使用,所谓的“一个或多个”意指在合理条件下的1个或超过1个,例如2个、3个、4个、5个或10个。
116、除非指明,否则如本文中所使用,取代基的连接点可来自取代基的任意适宜位置。
117、当取代基的键显示为穿过环中连接两个原子的键时,则这样的取代基可键连至该可取代的环中的任一成环原子。
118、本发明还包括所有药学上可接受的同位素标记的化合物,其与本发明的化合物相同,除了一个或多个原子被具有相同原子序数但原子质量或质量数不同于在自然界中占优势的原子质量或质量数的原子替代。适合包含入本发明的化合物中的同位素的实例包括(但不限于)氢的同位素(例如氘(2h)、氚(3h));碳的同位素(例如11c、13c及14c);氯的同位素(例如36cl);氟的同位素(例如18f);碘的同位素(例如123i及125i);氮的同位素(例如13n及15n);氧的同位素(例如15o、17o及18o);磷的同位素(例如32p);及硫的同位素(例如35s)。某些同位素标记的本发明的化合物(例如掺入放射性同位素的那些)可用于药物和/或底物组织分布研究(例如分析)中。放射性同位素氚(即3h)及碳-14(即14c)因易于掺入且容易检测而特别可用于该目的。用正电子发射同位素(例如11c、18f、15o及13n)进行取代可在正电子发射断层显像术(pet)研究中用于检验底物受体占据情况。被同位素标记的本发明的化合物可通过与描述于随附路线和/或实施例及制备中的那些类似的方法通过使用适当的被同位素标记的试剂代替之前采用的非标记的试剂来制备。本发明的药学上可接受的溶剂合物包括其中结晶溶剂可被同位素取代的那些,例如,d2o、丙酮-d6或dmso-d6。
119、“取代的”指基团中的一个或多个氢原子,优选为最多5个,更优选为1-3个氢原子彼此独立地被相应数目的取代基取代。不言而喻,取代基仅处在它们的可能的化学位置,本领域技术人员能够在不付出过多努力的情况下确定(通过实验或理论)可能或不可能的取代。例如,具有游离氢的氨基或羟基与具有不饱和(如烯属)键的碳原子结合时可能是不稳定的。
120、本说明书所述的“取代”或“取代的”,如无特别指出,均是指基团可被一个或多个选自以下的基团取代:烷基、烯基、炔基、烷氧基、烷硫基、烷基氨基、卤素、疏基、羟基、硝基、氰基、环烷基、杂环基、芳基、杂芳基、环烷氧基、杂环烷氧基、环烷硫基、杂环烷硫基、氨基、卤代烷基、羟烷基、羧基、羧酸酯基、=o、-c(o)rb、-oc(o)rb、-nrbrb、-c(o)nrbrb、-nrbc(o)rb、-s(o)nrbrb或-s(o)2nrbrb,其中,rb的定义如通式(i)中所述。
121、此处使用的“儿科病人”一词是指在诊断或治疗时未满16岁的病人。“儿童”一词还可分为以下几个亚类:新生儿(从出生到出生第一个月);婴儿(1个月至两岁);儿童(2岁至12岁);青少年(12岁至21岁(直到但不包括22岁生日))。berhman re,kliegman r,arvinam,nelson we.尼尔森儿科教科书,第15版。费城:w.b.saunders公司,1996年;rudolph am,等人。鲁道夫的儿科,第21版。纽约:mcgrow-hill,2002年;和avery md,第一lr。儿科医学,第二版。巴尔的摩:williams&wilkins;1994。
122、如本文所用,化合物的“有效量”是指足以负调节或激动相应靶标的量。
123、如本文所用,化合物的“治疗有效剂量”是指足以改善或以某种方式减少症状、停止或逆转病情进展、或负调节或激动相应靶标的量。这种剂量可以作为单一剂量使用,也可以按照一种方案服用,从而有效。
124、如此处所用,“治疗”是指以任何方式改善或以其他方式改变患者的病情、紊乱或疾病的症状或病理。
125、如本文所述,“通过使用某一特定化合物或药物组合物来改善某一特定疾病的症状”是指可归因于或与该组合物的使用有关的任何减少,不论是永久性的还是暂时性的、持久的或暂时性的。
126、本发明中立体化学的定义和惯例的使用通常参考以下文献:
127、s.p.parker,ed.,mcgraw-hill dictionary of chemical terms(1984)mcgraw-hillbook company,new york;and eliel,e.and wilen,s.,"stereochemistry oforganic compounds",john wiley&sons,inc.,new york,1994.本发明的化合物可以包含不对称中心或手性中心,因此存在不同的立体异构体。本发明的化合物所有的立体异构形式,包括但绝不限于,非对映体,对映异构体,阻转异构体,和它们的混合物,如外消旋混合物,组成了本发明的一部分。非对映异构体可以以其物理化学差异为基础,通过层析、结晶、蒸馏或升华等方法被分离为个别非对映异构体。对映异构体可以通过分离,使手性异构混合物转化为非对映异构混合物,其方式是与适当光学活性化合物(例如手性辅助剂,譬如手性醇或mosher氏酰氯)的反应,分离非对映异构体,且使个别非对映异构体转化为相应的纯对映异构体。本发明的中间体与化合物也可以不同互变异构形式存在,且所有此种形式被包含在本发明的范围内。很多有机化合物都以光学活性形式存在,即它们有能力旋转平面偏振光的平面。在描述光学活性化合物时,前缀d、l或r、s用来表示分子手性中心的绝对构型。前缀d、l或(+)、(-)用来命名化合物平面偏振光旋转的符号,(-)或l是指化合物是左旋的,前缀(+)或d是指化合物是右旋的。这些立体异构体的原子或原子团互相连接次序相同,但是它们的立体结构不一样。特定的立体异构体可以是对映体,异构体的混合物通常称为对映异构体混合物。50:50的对映体混合物被称为外消旋混合物或外消旋体,这可能导致化学反应过程中没有立体选择性或立体定向性。所谓的“外消旋混合物”和“外消旋体”是指等摩尔的两个对映异构体的混合物,缺乏光学活性。
128、“互变异构体”或“互变异构的形式”是指不同能量的结构的同分异构体可以通过低能垒互相转化。例如质子互变异构体(即质子移变的互变异构体)包括通过质子迁移的互变,如酮式-烯醇式和亚胺-烯胺的同分异构化作用。原子价(化合价)互变异构体包括重组成键电子的互变。除非其他方面表明,本发明所描述的结构式包括所有的同分异构形式(如对映异构,非对映异构,和几何异构):例如含有不对称中心的r、s构型,双键的(z)、(e)异构体,和(z)、(e)的构象异构体。因此,本发明的化合物的单个立体化学异构体或其对映异构体,非对映异构体,或几何异构体的混合物都属于本发明的范围。
129、“药学上可接受的盐”指本发明化合物的盐,这类盐用于人或动物体内时具有安全性和有效性。化合物的盐可以通过在纯的溶液或合适的惰性溶解中用足量的碱或酸获得相应的加成盐。可药用的碱加成盐包括钠、钾、钙、铵、有机氨或镁盐等,可药用的酸加成盐包括无机酸盐和有机酸盐,所述的无机酸和有机酸包括盐酸、氢溴酸、碳酸、碳酸氢根、磷酸、磷酸一氢根、磷酸二氢根、硫酸、硫酸一氢根、乙酸、马来酸、丙二酸、琥珀酸、饭丁烯二酸、邻苯二甲酸、苯磺酸、对甲苯磺酸、柠檬酸和甲磺酸等(参见berge et al.,“pharmaceuticalsalts”,journal of pharmaceutical science 66:1-19(1977))。
130、本文中可使用实线实楔形或虚楔形描绘本发明的化合物的化学键。使用实线以描绘键连至不对称碳原子的键欲表明,包括该碳原子处的所有可能的立体异构体(例如,特定的对映异构体、外消旋混合物等)。使用实或虚楔形以描绘键连至不对称碳原子的键欲表明,存在所示的立体异构体。当存在于外消旋混合物中时,使用实及虚楔形以定义相对立体化学,而非绝对立体化学。除非另外指明,否则本发明的化合物意欲可以立体异构体(其包括顺式及反式异构体、光学异构体(例如r及s对映异构体)、非对映异构体、几何异构体、旋转异构体、构象异构体、阻转异构体及其混合物)的形式存在。本发明的化合物可表现一种以上类型的异构现象,且由其混合物(例如外消旋混合物及非对映异构体对)组成。
131、本发明涵盖本发明的化合物的所有可能的结晶形式或多晶型物,其可为单一多晶型物或多于一种多晶型物的任意比例的混合物。
132、还应当理解,本发明的某些化合物可以游离形式存在用于治疗,或适当时,以其药学上可接受的衍生物形式存在。在本发明中,药学上可接受的衍生物包括但不限于,药学上可接受的盐、酯、溶剂合物、n-氧化物、代谢物、螯合物、络合物、包合物或前药,在将它们向需要其的患者给药后,能够直接或间接提供本发明的化合物或其代谢物或残余物。因此,当在本文中提及“本发明的化合物”时,也意在涵盖化合物的上述各种衍生物形式。
133、本发明的化合物的药学上可接受的盐包括其酸加成盐及碱加成盐,包括但不限于含有氢键或配位键的盐。
134、适合的酸加成盐由形成药学可接受盐的酸来形成。实例包括乙酸盐、己二酸盐、天冬氨酸盐、苯甲酸盐、苯磺酸盐、碳酸氢盐/碳酸盐、硫酸氢盐/硫酸盐、硼酸盐、樟脑磺酸盐、柠檬酸盐、环己氨磺酸盐、乙二磺酸盐、乙磺酸盐、甲酸盐、延胡索酸盐、葡庚糖酸盐、葡糖酸盐、葡糖醛酸盐、六氟磷酸盐、海苯酸盐、盐酸盐/氯化物、氢溴酸盐/溴化物、氢碘酸盐/碘化物、羟乙基磺酸盐、乳酸盐、苹果酸盐、顺丁烯二酸盐、丙二酸盐、甲磺酸盐、甲基硫酸盐、萘甲酸盐(naphthylate)、2-萘磺酸盐、烟酸盐、硝酸盐、乳清酸盐、草酸盐、棕榈酸盐、双羟萘酸盐、磷酸盐/磷酸氢盐/磷酸二氢盐、焦谷氨酸盐、糖二酸盐、硬脂酸盐、丁二酸盐、单宁酸盐、酒石酸盐、甲苯磺酸盐、三氟乙酸盐及昔萘酸盐(xinofoate)。
135、适合的碱加成盐由形成药学可接受盐的碱来形成。实例包括铝盐、精氨酸盐、苄星青霉素盐、钙盐、胆碱盐、二乙胺盐、二乙醇胺盐、甘氨酸盐、赖氨酸盐、镁盐、葡甲胺盐、乙醇胺盐、钾盐、钠盐、氨丁三醇盐及锌盐。
136、适合的盐的综述参见stahl及wermuth的“handbook of pharmaceutical salts:properties,selection,and use”(wiley-vch,2002)。用于制备本发明的化合物的药学上可接受的盐的方法为本领域技术人员已知的。
137、如本文中所使用,所谓的“酯”意指衍生自本技术中各个通式化合物的酯,其包括生理上可水解的酯(可在生理条件下水解以释放游离酸或醇形式的本发明的化合物)。本发明的化合物本身也可以是酯。
138、本发明的化合物可以溶剂合物(优选水合物)的形式存在,其中本发明的化合物包含作为所述化合物晶格的结构要素的极性溶剂,特别是例如水、甲醇或乙醇。极性溶剂特别是水的量可以化学计量比或非化学计量比存在。
139、本领域技术人员会理解,由于氮需要可用的孤对电子来氧化成氧化物,因此并非所有的含氮杂环都能够形成n-氧化物;本领域技术人员会识别能够形成n-氧化物的含氮杂环。本领域技术人员还会认识到叔胺能够形成n-氧化物。用于制备杂环和叔胺的n-氧化物的合成方法是本领域技术人员熟知的,包括用过氧酸如过氧乙酸和间氯过氧苯甲酸(mcpba)、过氧化氢、烷基过氧化氢如叔丁基过氧化氢、过硼酸钠和双环氧乙烷(dioxirane)如二甲基双环氧乙烷来氧化杂环和叔胺。这些用于制备n-氧化物的方法已在文献中得到广泛描述和综述,参见例如:t.l.gilchrist,comprehensive organic synthesis,vol.7,pp748-750;a.r.katritzky和a.j.boulton,eds.,academic press;以及g.w.h.cheeseman和e.s.g.werstiuk,advances in heterocyclic chemistry,vol.22,pp 390-392,a.r.katritzky和a.j.boulton,eds.,academic press。
140、在本发明的范围内还包括本发明的化合物的代谢物,即在给药本发明的化合物时体内形成的物质。这样的产物可由例如被给药的化合物的氧化、还原、水解、酰胺化、脱酰胺化、酯化、酶解等产生。因此,本发明包括本发明的化合物的代谢物,包括通过使本发明的化合物与哺乳动物接触足以产生其代谢产物的时间的方法制得的化合物。
141、本发明在其范围内进一步包括本发明的化合物的前药,其为自身可具有较小药理学活性或无药理学活性的本发明的化合物的某些衍生物当被给药至身体中或其上时可通过例如水解裂解转化成具有期望活性的本发明的化合物。通常这样的前药会是所述化合物的官能团衍生物,其易于在体内转化成期望的治疗活性化合物。关于前药的使用的其他信息可参见“pro-drugs as novel delivery systems”,第14卷,acs symposium series(t.higuchi及v.stella)。本发明的前药可例如通过用本领域技术人员已知作为“前-部分(pro-moiety)(例如“design of prodrugs”,h.bundgaard(elsevier,1985)中所述)”的某些部分替代本发明的化合物中存在的适当官能团来制备。
142、本发明还涵盖含有保护基的本发明的化合物。在制备本发明的化合物的任何过程中,保护在任何有关分子上的敏感基团或反应基团可能是必需的和/或期望的,由此形成本发明的化合物的化学保护的形式。这可以通过常规的保护基实现,例如,在t.w.greene&p.g.m.wuts,protective groups in organic synthesis,johnwiley&sons,1991中所述的那些保护基,这些参考文献通过援引加入本文。使用本领域已知的方法,在适当的后续阶段可以移除保护基。
143、所谓的“约”是指在所述数值的±10%范围内,优选±5%范围内,更优选±2%范围内。
144、本发明的优选化合物
145、已经记载本发明化合物的通式和优选范围。进一步优选地,本发明化合物的具体例子可以选自如下结构的任意一种,但是并不限于以下化合物:
146、在本发明优选的实施方式中,其为以下具体化合物中的一种:
147、基于本发明的筛选方法,ai筛选模型提示以下化合物其具有kcc2激活活性。ai筛选出来的化合物的结果受输入的具体目标分子的影响较大,本次筛选前期获得的这一系列分子有着共同的共性就是邻苯二甲酰亚胺的分子片段。发明人有意以邻苯二甲酰亚胺为母核,基于生物电子等排原理等,再两端分别尝试连接常见药效基团,有意逐步增加了类似的目标分子在ai筛选模型中的输入,对这类化合物统一计算了分子重量、油水分配系数、类药性评估分数、五倍率法则,评估了其与kcc2的亲和稳定性,以及这些化合物与kcc2的亲和力,这些内容都在实施例部分中示出,计算结果显示这些化合物都与kcc2的亲和力良好,提示具有kcc2的激活活性,图5和图6中示出的化合物均为优选化合物,另外以下化合物也是优选化合物。
148、
149、
150、
151、本发明化合物获得的一般方法
152、本发明通式(i)化合物的合成方法可以参照后述的具体实施例中的合成方法,本领域技术人员可通过替换相应的原料和中间体的方法,获得各种目标化合物。作为通用的策略,附图4中给出了三种代表性化合物的通用合成方法,这些制备方法中,提供碱性条件的试剂选自有机碱或无机碱类,所述的有机碱类包括但不限于三乙胺、n,n-二异丙基乙胺、正丁基锂、二异丙基氨基锂、双三甲基硅基胺基锂、醋酸钾、醋酸钠、叔丁醇钠、甲醇钠和叔丁醇钾中的一种或多种,所述的无机碱类为氢化钠、磷酸钾、碳酸钠、碳酸钾、醋酸钾、碳酸铯、氢氧化钠、氢氧化钾、碳酸氢钠和氢氧化锂中的一种或多种;
153、提供酸性条件的试剂包括但不限于氯化氢、氯化氢的1,4-二氧六环溶液、三氟乙酸、甲酸、乙酸、盐酸、硫酸、甲磺酸、硝酸和磷酸中的一种或多种;
154、金属催化剂包括但不限于钯/碳、雷尼镍、四-三苯基膦钯、二氯化钯、醋酸钯、[1,1'-双(二苯基膦基)二茂铁]二氯化钯(pd(dppf)cl2)、[1,1'-双(二苯基膦基)二茂铁]二氯化钯二氯甲烷络合物、双三苯基磷二氯化钯(pd(pph3)cl2)和三(二亚苄基丙酮)二钯(pd2(dba)3)中的一种或多种;
155、配体包括但不限于2-双环己基膦-2,6'-二甲氧基联苯(sphos)、4,5-双二苯基膦-9,9-二甲基氧杂蒽(xantphos)、2-二环己基磷-2,4,6-三异丙基联苯(xphos)、2-二环己膦基-2'-(n,n-二甲胺)-联苯(davephos)、1,1'-双(二苯基膦)二茂铁(dppf)和1,1'-联萘-2,2'-双二苯膦(binap)中的一种或多种,优选为4,5-双二苯基膦-9,9-二甲基氧杂蒽(xantphos);
156、缩合剂包括但不限于二环己基碳二亚胺(dcc)、二异丙基碳二亚胺(dic)、1-(3-二甲胺基丙基)-3-乙基碳二亚胺(edc)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺(edci)、2-(7-氧化苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸酯(hatu),2-(1h-苯并三偶氮l-1-基)-1,1,3,3-四甲基脲四氟硼酸酯(tbtu),1-羟基苯并三唑(hobt)和1-丙基磷酸酐(t3p)中的一种或多种。
157、上述反应优选在溶剂中进行,所用溶剂包括但不限于:n,n-二甲基甲酰胺、二甲基亚砜、1,4-二氧六环、水、四氢呋喃、二氯甲烷、1,2-二氯乙烷、醋酸、甲醇、乙醇、甲苯、石油醚、乙酸乙酯、正己烷、丙酮、乙醚、二甘醇及其混合物。
158、本发明的典型化合物包括但不限于如上表格中的化合物,本发明中的化合物命名遵循系统命名,或者,使用chemdraw软件进行命名。
159、药物组合物、医药用途和治疗方法
160、本发明提供一种药物组合物,其包含有效量的本发明化合物或其药学上可接受的盐、酯、光学异构体、立体异构体、多晶型物、溶剂合物、n-氧化物、同位素标记的化合物、代谢物、螯合物、络合物、包合物或前药,以及药学上可接受的载体,所述药物组合物优选为固体制剂、半固体制剂、液体制剂或气态制剂。
161、本发明中“药学上可接受的载体”是指与治疗剂一同给药的稀释剂、辅剂、赋形剂或媒介物,并且其在合理的医学判断的范围内适于接触人类和/或其它动物的组织而没有过度的毒性、刺激、过敏反应或与合理的益处/风险比相应的其它问题或并发症。
162、在本发明的药物组合物中可使用的药学上可接受的载体包括但不限于无菌液体,例如水和油,包括那些石油、动物、植物或合成来源的油,例如花生油、大豆油、矿物油、芝麻油等。当所述药物组合物通过静脉内给药时,水是示例性载体。还可以使用生理盐水和葡萄糖及甘油水溶液作为液体载体,特别是用于注射液。适合的药物赋形剂包括淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽糖、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂奶粉、甘油、丙二醇、水、乙醇等。所述组合物还可以视需要包含少量的湿润剂、乳化剂或ph缓冲剂。口服制剂可以包含标准载体,如药物级的甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、纤维素、碳酸镁等。适合的药学上可接受的载体的实例如在remington’s pharmaceuticalsciences(1990)中所述。
163、本发明的药物组合物可以系统地作用和/或局部地作用。为此目的,它们可以适合的途径给药,例如通过注射(如静脉内、动脉内、皮下、腹膜内、肌内注射,包括滴注)或经皮给药;或通过口服、含服、经鼻、透粘膜、局部、以眼用制剂的形式或通过吸入给药。
164、对于这些给药途径,可以适合的剂型给药本发明的药物组合物。
165、所述剂型包括但不限于片剂、胶囊剂、锭剂、硬糖剂、散剂、喷雾剂、乳膏剂、软膏剂、栓剂、凝胶剂、糊剂、洗剂、软膏剂、水性混悬剂、可注射溶液剂、酏剂、糖浆剂。
166、本发明所述药物组合物,含有安全有效量的本发明化合物以及药学上可接受的载体或赋形剂。这类载体包括(但并不限于):盐水、缓冲液、葡萄糖、水、甘油、乙醇、粉剂等中的一种或几种。药物制剂应与给药方式相匹配。
167、本发明的药物组合物可以被制成针剂形式,例如用生理盐水或含有葡萄糖和其他辅剂的水溶液通过常规方法进行制备。诸如片剂和胶囊之类的药物组合物,可通过常规方法进行制备。药物组合物如针剂、溶液、片剂和胶囊宜在无菌条件下制造。本发明的药物组合物也可以被制成粉剂用于雾化吸入。
168、活性成分的给药量是治疗有效量,例如每天约1微克/千克体重-约50毫克/千克体重;优选地,为约5微克/千克体重-约10毫克/千克体重;进一步优选地,为约10微克/千克体重-约5毫克/千克体重。此外,本发明化合物还可与其他治疗剂一起使用。
169、对于本发明的药物组合物,可通过常规的方式施用于所需的对象(如人和非人哺乳动物)。代表性的施用方式包括(但并不限于):口服、注射、雾化吸入等。
170、使用药物组合物时,是将安全有效量的药物施用于哺乳动物,其中该安全有效量通常至少约10微克/千克体重,而且在大多数情况下不超过约50毫克/千克体重,较佳地,该剂量是约10微克/千克体重-约20毫克/千克体重。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。
171、下面结合具体实施例,进一步阐述本发明。实施本发明的过程、条件、试剂、实验方法等,除以下专门提及的内容之外,均为本领域的普遍知识和公知常识,本发明没有特别限制内容。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
172、如本文中所使用的所谓的“有效量”指被给药后会在一定程度上缓解所治疗病症的一或多种症状的化合物的量。具体而言,如本文所用,化合物的“有效量”是指足以激活2型钾-氯共转运蛋白kcc2。如本文所用,化合物的“治疗有效剂量”是指足以改善或以某种方式减少症状、停止或逆转病情进展、或激活2型钾-氯共转运蛋白kcc2的量。这种剂量可以作为单一剂量使用,也可以按照一种方案服用,从而有效。
173、可调整给药方案以提供最佳所需响应。例如,可给药单次推注,可随时间给药数个分剂量,或可如治疗情况的急需所表明而按比例减少或增加剂量。要注意,剂量值可随要减轻的病况的类型及严重性而变化,且可包括单次或多次剂量。要进一步理解,对于任何特定个体,具体的给药方案应根据个体需要及给药组合物或监督组合物的给药的人员的专业判断来随时间调整。
174、如此处所用,“治疗”是指以任何方式改善或以其他方式改变患者的病情、紊乱或疾病的症状或病理。如本文所述,“通过使用某一特定化合物或药物组合物来改善某一特定疾病的症状”是指可归因于或与该组合物的使用有关的任何减少,不论是永久性的还是暂时性的、持久的或暂时性的。
175、如本文所使用的“个体”包括人或非人动物。示例性人个体包括患有疾病(例如本文所述的疾病)的人个体(称为患者)或正常个体。本发明中“非人动物”包括所有脊椎动物,例如非哺乳动物(例如鸟类、两栖动物、爬行动物)和哺乳动物,例如非人灵长类、家畜和/或驯化动物(例如绵羊、犬、猫、奶牛、猪等)。
176、如在此所使用的,所谓的“有效量”意指一种化合物或组合物的足以显著和积极改变有待治疗的症状和/或病症(例如,提供积极临床响应)的量。用于一种药物组合物中的活性成分的有效量将随着正在被治疗的具体病症、该病症的严重性,治疗的持续时间、同步治疗的性质,该一种或多种使用的具体的活性成分,一种或多种所使用的药学上可接受的赋形剂/载体、以及主治医生的知识和专业技能内的类似因素而变化。
177、具体地,用于在神经系统疾病治疗中使用的具有化学式(i)的化合物的一个有效量是足以对症减轻在人中神经系统疾病的症状的量,以减缓神经系统疾病的进展,或减少患有神经系统疾病的患者中症状恶化的风险。在一些实施方案中,本发明的药物组合物还可以包含一种或多种另外的治疗剂或预防剂。
- 还没有人留言评论。精彩留言会获得点赞!