一种pan-KRAS抑制剂化合物及其制备方法和用途与流程
本发明涉及一种化合物,具体地涉及一种高活性的pan-kras抑制剂及其合同方法以及用途。
背景技术:
1、ras是人类肿瘤中最常发生突变的基因之一,其突变发生在约30%的肿瘤患者中,其中kras约占ras突变的85%。在88%的胰腺癌、50%的结直肠腺癌以及32%的肺腺癌中均存在kras的突变,靶向kras抑制剂的开发有重大的临床意义与价值。
2、kras是一种具有gtp酶活性的膜结合蛋白,其通过核苷酸交换,在gdp结合的非活性构象和gtp结合的活性构象之间循环,执行“分子开关”的功能。gtp结合状态下的kras能够激活下游包括raf-mek-erk、pi3k-akt在内的多条信号通路,调控细胞生长、增殖、分化和凋亡等生命过程。
3、kras突变(比如g12c、g12d、g12v、g13d等)会影响gtp酶激活蛋白(gtpaseactivating proteins,gaps)介导的gtp水解,使处于gtp结合的激活状态的kras增加,过度激活下游信号通路,最终导致肿瘤的发生和发展。然而,由于kras蛋白缺乏相应的、适合药物结合的疏水口袋,同时其与gtp和gdp的亲和力在皮摩尔级别(~20pm),导致竞争性结合kras的抑制剂研发十分困难,在过去的几十年中,kras一直被认为是不可成药的靶点。
4、2021年5月,amg510经fda批准上市,用于治疗携带krasg12c突变的局部晚期或转移性非小细胞肺癌,打破了kras“不可成药”的历史。但是,g12c突变仅占kras突变的一小部分,对于kras其它位点的突变,目前尚缺乏令人满意的有效的抑制剂化合物,有大量的临床需求尚未被满足,因此,研发有效的pan-kras抑制剂化合物,是现有技术中的需要。
技术实现思路
1、本发明提供一种pan-kras抑制剂。此类结构不同于现有的通过共价结合发挥作用的krasg12c抑制剂,而是通过介导细胞内普遍存在的伴侣蛋白(如cyclophilin a)与kras蛋白形成三元复合物来发挥作用。三元复合物的形成能够通过空间位阻阻断kras与其下游效应分子(如,raf)的结合,抑制mapk、pi3k-akt信号通路的激活,进而抑制肿瘤的发生与发展,发挥治疗肿瘤等疾病的作用。
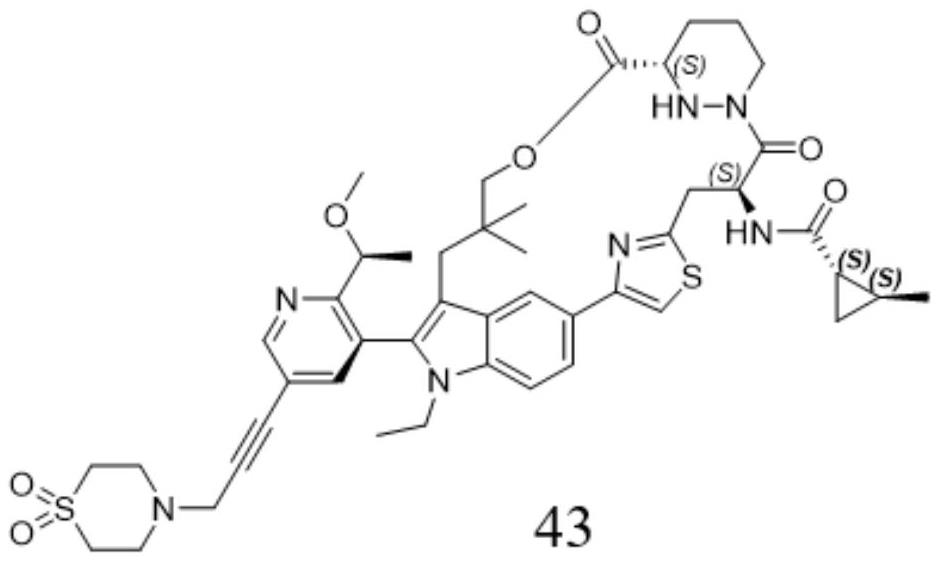
2、在一个方面,本发明提供一种具有式43结构的kras抑制剂化合物:
3、
4、在本发明的一些实施方式中,所述化合物通过中间体化合物int-3制备:
5、
6、在本发明的一些实施方式汇总,中间体化合物int-3的制备包括如下步骤:
7、
8、第一步:将化合物int-2e溶于二氯甲烷中,加入三氟乙酸,室温反应2小时,lcms监测原料反应完全,反应液直接减压浓缩,残留物溶于dcm,饱和nahco3水溶液洗两次,有机相水洗,硫酸钠干燥,过滤,浓缩得黄色固体化合物int-3a;第二步:将化合物int-3a和化合物int-3b溶于乙腈中,0℃下加入n,n,n',n'-四甲基氯甲脒六氟磷酸盐,和1-甲基咪唑,0℃反应1小时,lcms监测原料反应完全,反应液倒入水,二氯甲烷萃取,有机相水洗,拌样过柱纯化得白色固体化合物int-3c;第三步:将化合物int-3c,2-二环己基膦-2′,6′-二甲基-联苯,三(二亚苄基丙酮)二钯,乙酸钾溶于甲苯中,氮气保护下加入频那醇硼烷,滴加完毕,氮气保护下50℃反应3小时,lcms监测原料反应完全,反应液过滤,经硅胶柱层析纯化得黄色固体化合物int-3。
9、在本发明的一些实施方式中,化合物43的制备包括如下步骤:
10、
11、第一步:将中间体int-3和中间体int-38溶于1,4-二氧六环和水的混合溶剂中,加入1,1-双(二苯基膦)二荗铁二氯化钯和磷酸钾,反应体系置换氮气后加热至70℃搅拌12小时,待反应液冷却至室温,反应液用硅藻土过滤,滤液浓缩。残余物用制备薄层色谱(二氯甲烷/甲醇=30/1)纯化得到化合物43a;第二步:将化合物43a溶于dmf中,加入碳酸铯,随后将碘乙烷滴加至反应液中,反应液在室温下搅拌6小时,lcms检测反应结束,向反应体系中加入饱和食盐水,乙酸乙酯萃取,合并有机相,并用饱和食盐水洗涤,无水硫酸钠干燥,过滤浓缩,得到化合物43。
12、在又一个方面,本发明还提供了药物组合物,其包括前述任一所述的化合物或其药学上可接受的盐、同位素衍生物、立体异构体。
13、在一个方面,本发明还提供了前述化合物或其药学上可接受的盐、同位素衍生物、立体异构体以及药物组合物在制备用于预防和/或治疗癌症、肿瘤、炎症性疾病、自身免疫性疾病或免疫介导性疾病的药物中的用途。
14、特别注意的是,在本文中,当提及式(i)、式(ii)结构的“化合物”时,一般地还涵盖其立体异构体、非对映异构体、对映异构体、外消旋混合物和同位素衍生物。
15、本领域技术人员公知,一种化合物的盐、溶剂合物、水合物是化合物的替代性存在形式,它们都可以在一定条件下转化为所述化合物,因此,特别注意的是在本文中当提到式(i)、式(ii)结构的化合物时,一般地还包括它的可药用盐,进而还包括其溶剂合物和水合物。
16、相似地,在本文中当提到一种化合物时,一般地还包括其前药、代谢产物和氮氧化物。
17、本发明所述的可药用盐可使用例如以下的无机酸或有机酸而形成:“可药用盐”是指这样的盐,在合理的医学判断范围内,其适用于接触人和较低等动物的组织,而没有不适当的毒性、刺激性、过敏反应等,称得上合理的受益/风险比。可以在本发明化合物的最终分离和纯化期间原位制备所述盐,或单独通过将游离碱或游离酸与合适的试剂反应制备所述盐,如下概述。例如,游离碱功能可以与合适的酸反应。
18、本发明的可药用盐可通过常规方法制备,例如通过将本发明的化合物溶解于与水可混溶的有机溶剂(例如丙酮、甲醇、乙醇和乙腈),向其中添加过量的有机酸或无机酸水溶液,以使得盐从所得混合物中沉淀,从中除去溶剂和剩余的游离酸,然后分离所沉淀的盐。
19、本发明所述的前体或代谢物可以本领域公知的前体或代谢物,只要所述的前体或代谢物通过体内代谢转化形成化合物即可。例如“前药”是指本发明化合物的那些前药,在合理的医学判断范围内,其适用于接触人和更低等动物的组织,而没有不适当的毒性、刺激性、过敏反应等,称得上合理的受益/风险比并且对其预期用途有效。术语“前药”是指在体内迅速经转化产生上述式的母体化合物的化合物,例如通过在体内代谢,或本发明化合物的n-去甲基化。
20、本发明所述的“溶剂合物”意指本发明化合物与一个或多个溶剂分子(无论有机的还是无机的)的物理缔合。该物理缔合包括氢键。在某些情形中,例如当一个或多个溶剂分子纳入结晶固体的晶格中时,溶剂化物将能够被分离。溶剂化物中的溶剂分子可按规则排列和/或无序排列存在。溶剂合物可包含化学计量或非化学计量的溶剂分子。“溶剂合物”涵盖溶液相和可分离的溶剂合物。示例性溶剂合物包括但不限于水合物、乙醇合物、甲醇合物和异丙醇合物。溶剂化方法是本领域公知的。
21、本发明所述的“立体异构”分为构象异构和构型异构,构型异构还可分为顺反异构和旋光异构(即光学异构),构象异构是指具有一定构型的有机物分子由于碳、碳单键的旋转或扭曲而使得分子各原子或原子团在空间产生不同的排列方式的一种立体异构现象,常见的有烷烃和环烷烃类化合物的结构,如环己烷结构中出现的椅式构象和船式构象。“立体异构体”是指当本发明化合物含有一个或多个不对称中心,因而可作为外消旋体和外消旋混合物、单一对映异构体、非对映异构体混合物和单一非对映异构体。本发明化合物有不对称中心,每个不对称中心会产生两个光学异构体,本发明的范围包括所有可能的光学异构体和非对映异构体混合物和纯的或部分纯的化合物。本发明所述的化合物可以以互变异构体形式存在,其通过一个或多个双键位移而具有不同的氢的连接点。例如,酮和它的烯醇形式是酮-烯醇互变异构体。各互变异构体及其混合物都包括在本发明的化合物中。所有化合物的对映异构体、非对映异构体、外消旋体、内消旋体、顺反异构体、互变异构体、几何异构体、差向异构体及其混合物等,均包括在本发明范围中。
22、本发明的“同位素衍生物”是指在本文中化合物被同位素标记的分子。通常用作同位素标记的同位素是:氢同位素,2h和3h;碳同位素:11c,13c和14c;氯同位素:35cl和37cl;氟同位素:18f;碘同位素:123i和125i;氮同位素:13n和15n;氧同位素:15o,17o和18o和硫同位素35s。这些同位素标记化合物可以用来研究药用分子在组织中的分布情况。尤其是氘3h和碳13c,由于它们容易标记且方便检测,运用更为广泛。某些重同位素,比如重氢(2h),的取代能增强代谢的稳定性,延长半衰期从而达到减少剂量的目而提供疗效优势的。同位素标记的化合物一般从已被标记的起始物开始,用已知的合成技术象合成非同位素标记的化合物一样来完成其合成。
23、本发明还提供了本发明化合物在制备用于预防和/或治疗癌症、肿瘤、炎症性疾病、自身免疫性疾病或免疫介导性疾病的药物中的用途。
24、此外,本发明提供了用于预防和/或治疗癌症、肿瘤、炎症性疾病、自身免疫性疾病、神经退行性疾病、注意力相关疾病或免疫介导性疾病的药物组合物,其包含本发明化合物作为活性成分。所述药物组合物可任选地包含可药用的载体。
25、此外,本发明提供了一种预防和/或治疗癌症、肿瘤、炎症性疾病、自身免疫性疾病、神经退行性疾病、注意力相关疾病或免疫介导性疾病的方法,其包括向有此需要的哺乳动物施用本发明化合物。
26、癌症或肿瘤的代表性实例可包括但不限于,皮肤癌、膀胱癌、卵巢癌、乳腺癌、胃癌、胰腺癌、前列腺癌、结肠癌、肺癌、骨癌、脑癌、神经细胞瘤、直肠癌、结肠癌、家族性腺瘤性息肉性癌、遗传性非息肉性结直肠癌、食管癌、唇癌、喉癌、下咽癌、舌癌、唾液腺癌、胃癌、腺癌、甲状腺髓样癌、乳头状甲状腺癌、肾癌、肾实质癌、卵巢癌、宫颈癌、子宫体癌、子宫内膜癌、绒毛膜癌、胰腺癌、前列腺癌、睾丸癌、泌尿癌、黑素瘤、脑肿瘤诸如成胶质细胞瘤、星形细胞瘤、脑膜瘤、成神经管细胞瘤和外周神经外胚层肿瘤、霍奇金淋巴瘤、非霍奇金淋巴瘤、伯基特淋巴瘤、急性淋巴性白血病(all)、慢性淋巴性白血病(cll)、急性骨髓性白血病(aml)、慢性粒细胞白血病(cml)、成人t细胞白血病淋巴瘤、弥漫性大b细胞淋巴瘤(dlbcl)、肝细胞癌、胆囊癌、支气管癌、小细胞肺癌、非小细胞肺癌、多发性骨髓瘤、基底细胞瘤、畸胎瘤、成视网膜细胞瘤、脉络膜黑素瘤、精原细胞瘤、横纹肌肉瘤、颅咽管瘤、骨肉瘤、软骨肉瘤、肌肉瘤、脂肪肉瘤、纤维肉瘤、尤因肉瘤或浆细胞瘤。
27、当将本发明化合物或其可药用盐与另外的用于治疗癌症或肿瘤的抗癌剂或免疫检查点抑制剂组合施用时,本发明化合物或其可药用盐可提供增强的抗癌作用。
28、当将本发明化合物或其可药用盐与另外的用于治疗炎症性疾病、自身免疫性疾病和免疫介导性疾病的治疗剂组合施用时,本发明化合物或其可药用盐可提供增强的治疗作用。
29、除此之外,本发明还提供了一种预防和/或治疗肿瘤、癌症、病毒感染、器官移植排斥、神经退行性疾病、注意力相关疾病或自身免疫性疾病的方法,其包括向有此需要的哺乳动物施用本发明的化合物或本发明的药物组合物。
30、可根据常规方法中的任何一种将本发明药物组合物配制成用于口服施用或肠胃外施用(包括肌内、静脉内和皮下途径、瘤内注射)的剂型,例如片剂、颗粒、粉末、胶囊、糖浆、乳剂、微乳剂、溶液或混悬液。
31、发明描述示例性实施方案的过程中,本发明的其它特征将变得显而易见,给出所述实施方案用于说明本发明而不意欲成为其限制,以下实施例使用本发明所公开的方法制备、分离和表征。
32、可以用有机合成领域的技术人员已知的多种方式来制备本发明的化合物,可使用下述方法以及有机合成化学领域中已知的合成方法或通过本领域技术人员所了解的其变化形式来合成本发明化合物。优选方法包括但不限于下文所述的这些。在适用于所使用试剂盒材料和适用于所实现转变的溶剂或溶剂混合物中实施反应。有机合成领域的技术人员将理解,分子上存在的官能性与所提出的转变一致。这有时需要加以判断改变合成步骤的顺序或原料以获得期望的本发明化合物。
- 还没有人留言评论。精彩留言会获得点赞!