一种口蹄疫疫苗中146S抗原的检测方法与流程
本发明属于检测,具体涉及一种口蹄疫疫苗中146s抗原的检测方法。
背景技术:
1、口蹄疫(foot-and-mouth disease,fmd)作为一类烈性传染病,传播速度快、范围广、危害大,主要危害猪、牛、羊等偶蹄动物,发病率极高,给我国畜牧产业带来巨大的经济损失。尽管目前已有口蹄疫重组亚单位疫苗、合成肽疫苗等,但目前我国对口蹄疫依然采取以灭活病毒疫苗免疫为主的防控策略,相比其他类型的疫苗表现出更优的免疫保护效果。
2、在口蹄疫疫苗中起到最主要的保护作用的有效抗原是其完整病毒146s。口蹄疫病毒146s是无囊膜的rna病毒,呈二十面体对称,直径为28~30nm,包含a型、o型、c型、南非1型(sat 1型)、南非2型(sat 2型)、南非3型(sat 3型)和亚洲1型(asia1型)等七种血清型。不同血清型之间无交叉保护,同一血清型的各亚型之间仅有部分交叉免疫。146s较差的稳定性是口蹄疫疫苗的挑战。在生产和运输过程中146s极易裂解成无免疫活性的五聚体12s并释放出内部的病毒rna而影响免疫效果。因此为了保证疫苗产品质量,避免免疫失败导致的重大经济损失,口蹄疫灭活病毒疫苗中146s含量的准确测定是口蹄疫疫苗生产、质控的关键问题。此外,由于不同血清学之间的交叉保护效果差,商业化疫苗的趋势是开发多价疫苗提高疫苗的免疫效果和保护范围。
3、目前,口蹄疫疫苗抗原定量检测方法主要包括elisa法、蔗糖密度梯度离心法及高效液相尺寸排阻色谱法(hpsec)。其中,elisa法虽然可以区分不同血清型,具有较高的检测通量,但往往难以完全区分完整146s与其裂解产物,因此,难以准确测定有效抗原量。
4、cn101655452a及cn 110095425 a公开了一种蔗糖密度梯度紫外光定量法检测口蹄疫抗原146s含量的方法,先对待测病毒浓缩液进行蔗糖密度梯度超速离心分离,再用紫外光分光光度计对各个级份连续测定od259nm值;然后计算被检测样品od值峰面积。然而,超速离心法存在自动化程度低操作复杂、准确性及重复性差、耗时长(完成测定通常需要超过4h)、检测通量低(1天10~12个样品)、设备昂贵等缺点;同时,由于不同血清型的146s具有相近的沉降系数,所以超速离心法无法对不同血清型的146s进行区分。
5、cn104634891a及文献《应用体积排阻色谱法测定口蹄疫灭活疫苗中的146s抗原含量》公开了一种采用hpsec法测定口蹄疫疫苗抗原146s的方法。该方法首先利用尺寸排阻色谱柱将146s与其他杂质进行分离,再对146s的色谱峰的紫外吸收峰面积进行积分;通过对不同浓度的146s标准品紫外吸收峰与其浓度的关系,建立吸收峰面积和146s浓度的标准曲线,从而计算未知样品中146s的含量。虽然hpsec法具有检测速度快(30min)、高灵敏度、操作简单、低样品体积(100ul)、重复性好等优点,但尺寸排阻色谱是根据被分析样品的尺寸大小进行分离,而多价疫苗样品不同血清型146s病毒粒子尺寸相近,同样无法实现分型检测。此外,一台设备同时仅能检测一个样品,1天最大检测量为48个样品。
6、cn 112034028 a中公开了一种基于毛细管电泳法的146s定量新方法,实现单价、双价及多价口蹄疫灭活疫苗中不同血清型146s抗原定量,且操作时间仅30min。但毛细管电泳设备的成本高昂,对人员要求高,同时仅能检测一个样品,1天最大检测量为48个样品。
7、综上,口蹄疫疫苗还需要建立准确、快速、高通量且具有分析多价疫苗能力的146s定量方法。
技术实现思路
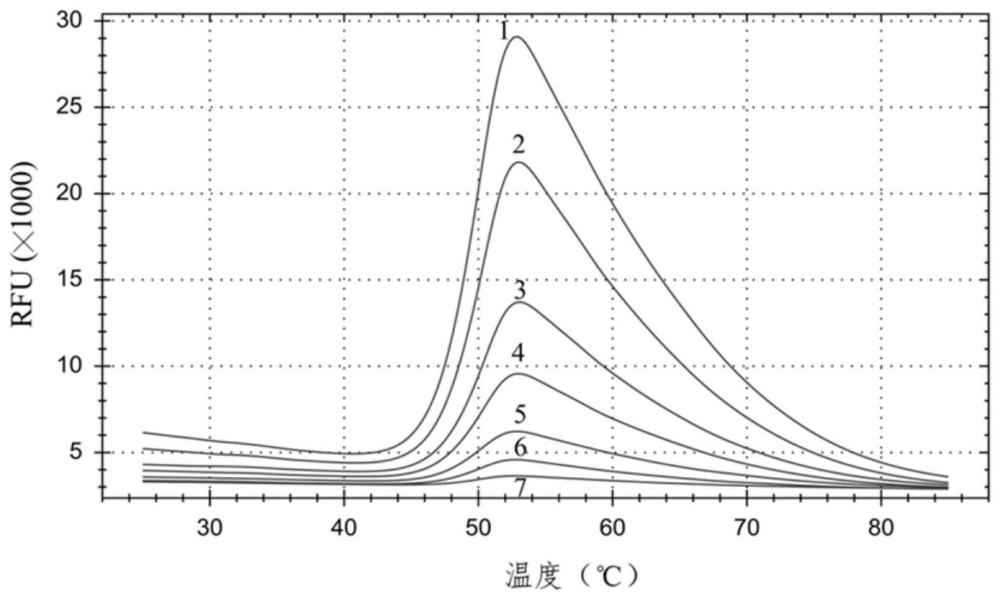
1、为了提供一种准确、快速、高通量且具有分析多价疫苗能力的146s抗原定量方法,本发明利用口蹄疫146s受热会完全裂解释放出核酸的特性,基于差示扫描荧光技术(dsf),通过一个逐渐升温的过程使病毒在特定温度下裂解释放核酸,利用核酸染料与释放出的核酸结合后激发产生荧光信号且荧光强度与结合的核酸量成正比,通过测定荧光强度的变化实现完整病毒的含量测定;又利用不同血清型衣壳蛋白序列存在差异,会在不同的温度下发生裂解,实现同时检测不同血清型病毒的核酸释放过程,对多价抗原定量。升温和检测可以通过荧光定量pcr仪实现。
2、本发明虽然利用核酸染料和荧光定量pcr仪,但不同于核酸荧光定量技术。荧光定量pcr检测需要特定的引物对病毒核酸进行扩增,所得含量为病毒特定序列的拷贝数,可能包含已裂解的病毒核酸而不仅仅是146s的含量。而本发明并不需要核酸引物,也不需进行pcr扩增过程。
3、具体地,为了解决上述技术问题,本发明公开了一种口蹄疫疫苗中146s抗原的定量检测方法,包括如下步骤:
4、(1)样品前处理:向口蹄疫疫苗水相样品中加入核酸染料,得到待测样品;
5、(2)检测:取样加入pcr管中,放入荧光定量pcr仪,以升温速率45~240℃/h,升温范围15-100℃进行检测,检测结束后对荧光信号进行一阶导数处理;
6、(3)计算:计算最低点的drfu/dt,其中,rfu为相对荧光强度值,根据定量标准曲线得到不同血清型146s抗原的浓度。
7、其中,步骤(1)中,口蹄疫样品与核酸染料的体积比为500~5000:1;优选地,所述口蹄疫样品与核酸染料的体积比为2000:1。
8、其中,对于染料的种类不加严格限制,本领域技术人员可以从常用可结合dna或rna的核酸染料中选择,所述染料可以选自sybr green ii、sybr green i、sybr gold、sybrsafe、溴化乙锭、gelred、gelgreen、gold view i、gold view ii、ribogreen中的任意一种,优选地,所述染料为sybr green ii或ribogreen。
9、步骤(2)中,所述升温速率为60~120℃/h,所述升温范围为20~90℃;优选地,所述升温速率为60~90℃/h,所述升温范围为25~85℃。
10、步骤(2)中,取样加入pcr管中时,所述取样体积为25~100μl;优选地,所述取样体积为40~100μl;更优选地,所述取样体积为40μl。
11、步骤(3)中,对于多价抗原,根据单价血清型的一阶导数图谱,对多价抗原的一阶导数图谱进行多元回归拟合,得到各单价血清型抗原的占比和拟合后各自的信号,再将各单价血清型抗原信号峰最低点的drfu/dt带入定量标准曲线得到多价抗原中不同血清型146s抗原的浓度。
12、具体地,步骤(1)中,所述口蹄疫疫苗的水相样品为口蹄疫疫苗破乳后的上清、细胞培养后的病毒培养液、灭活后的病毒培养液、纯化中成品或配苗前的纯品中的任意一种。
13、进一步地,为了获得口蹄疫疫苗的水相样品,对成品口蹄疫疫苗样品,先对样品进行破乳得到水相样品再进行检测;对半成品口蹄疫疫苗的水相,直接进行检测;对非纯化样品或纯度不高的样品,如细胞培养后和纯化中间品抗原,在检测前加入50~200u/ml核酸酶在4~37℃下反应后去除宿主残留核酸后检测。
14、在一种实施方式中,破乳方法为:在所述口蹄疫疫苗中加入破乳剂,混合,离心,取底部水相。在一个更具体的实施方式中,破乳方法为:按照疫苗原液体积加入正戊醇,原液体积与正戊醇的体积比为9:1,混匀后在4℃下静置1h后,6000rpm离心10min,收集含抗原的底层溶液作为水相样品进行进样。
15、本发明的方法可以用于检测口蹄疫疫苗中不同血清型146s抗原的浓度,所述血清型为a型、o型、asia 1型、c型、南非1型、南非2型和南非3型中的任意一种。
16、本发明进一步提出了上述方法在口蹄疫疫苗中146s抗原的定量检测方法中的应用。
17、有益效果:与现有技术相比,本发明至少具有以下有益效果:
18、(1)本发明提供的方法可用于单价、双价甚至三价以上口蹄疫疫苗的分型检测,进而还能对不同血清型的146s定量检测,且不需要对样品进行特别的分离过程,操作简单,避免了密度梯度离心及液相色谱检测法对146s的结构破坏与吸附损失,提高了检测的准确性;
19、(2)本发明提供的方法重复性好、灵敏度高,使用的设备及耗材成本低,检测通量高、样品损耗低,1h可检测96~384个样品,远高于现有技术水平,从而能满足疫苗生产企业生产质量控制和大量研发实验的需求。
- 还没有人留言评论。精彩留言会获得点赞!