宫颈癌中胞葬作用风险评估模型及其应用和构建方法与流程
本发明属于宫颈癌研究领域,尤其涉及宫颈癌中胞葬作用风险评估模型及其应用和构建方法。
背景技术:
1、宫颈癌(cervical cancer,cc)是最常见的妇科恶性肿瘤之一,其发病率和死亡率仅次于乳腺癌。据估计,2018年全球有57万例宫颈癌病例和31.1万例死亡病例。cc从良性疾病发展到恶性疾病大约需要10到20年,鳞状细胞癌是其最常见的亚型。尽管在筛查和各种治疗方面取得了重大进展,如手术、放疗和化疗,但仍有不足之处。近年来,随着生物医学大数据的普及和共享,通过生物信息学方法筛选与cc相关的有效分子靶点成为可能。以往的研究报道了一些关于cc治疗的靶向分子,但临床应用非常有限甚至几乎没有。因此,继续探索cc的生物标志物是一项紧迫而具有挑战性的任务。
2、胞葬作用(efferocytosis)是细胞生物学所描述的吞噬细胞将程序性死亡的凋亡细胞移除的过程;这一过程可以理解为埋葬凋亡的细胞,因而称“胞葬”。巨噬细胞在机体生理(组织重构)和病理状态(炎症和组织损伤)下都具有至关重要的作用,包括清除凋亡细胞,也就是胞葬作用。凋亡细胞又可以活化巨噬细胞中受体依赖的信号通路,启动胞葬作用,从而抑制机体炎症,促进机体净化修复。胞葬作用涉及多个信号通路,包括受体网络、细胞溶质信号分子、细胞骨架快速重排、凋亡细胞消化和免疫代谢通路,这些通路运行不畅则有可能导致多种胞葬缺陷相关疾病,胞葬作用通过不同途径影响疾病进展。因此,胞葬作用对机体健康来说是双刃剑。目前还没有关于胞葬作用在cc中的生信研究,因此本研究基于tcga和geo数据库,探索cc的胞葬作用相关生物标志物,并建立一个预后模型,希望可以为cc的临床诊疗提供一定的参加。
技术实现思路
1、针对上述问题,本发明提供宫颈癌中胞葬作用风险评估模型及其应用和构建方法,主要为解决目前暂无通过生信分析对于宫颈癌的胞葬作用进行分析预测手段等问题。
2、为了解决上述问题,本发明采用如下技术方案:
3、本发明第一方面涉及检测itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna基因表达量的试剂的组合在制备预测宫颈癌中胞葬作用发生风险的产品中的应用,为多因素联合应用,联合应用后可以有效的预测风险结果,用于预测宫颈癌中胞葬作用发生为高风险或低风险,可以更为准确的进行风险评分,使得结果更为直观和准确。在此应用中,可为多个分别单独检测基因表达量的试剂的组合,也可为基因芯片等,其目前在于获取上述7个基因的表达情况。此应用可行的基础在于上述7个基因表达情况的组合应用可以对宫颈癌中胞葬作用发生风险疾病预测,结合具体的分析公式可以得出风险评分。基因表达量可从待检对象的细胞组织等中获取,主要是从宫颈癌相关部位组织中检测。
4、本发明第二方面涉及宫颈癌中胞葬作用风险评估模型,包括7个关键模型指标,建立形成宫颈癌中胞葬作用风险预测模型公式
5、riskscore=0.228956048*exp(itga5)-0.3336414*exp(snrpf)+0.509562825*exp(egl n1)-0.159621416*exp(ndufb7)-0.144489876*exp(ndufa2)-0.225660885*exp(srgap3)-0.121663983*exp(pcna);
6、式中itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna均为相应基因的表达量,表达量可采用常规手段进行标引,将表达量进行量化然后代入公式计算可得风险评分。exp函数为以自然常数e为底的指数函数,比如exp(itga5)则为e^(itga5)。
7、就本方面而言,其各特征的可选限定为:
8、其中,当riskscore与阈值对比时:riskscore>阈值则宫颈癌中胞葬作用高风险,riskscore=阈值则待估(比如采用四舍五入使其偏向于一方,或采用其他界定方式),riskscore<阈值则宫颈癌中胞葬作用低风险;
9、其中,阈值为通过r软件包计算获取的最佳阈值,具体的分析计算方法可采用现有技术,当然即便计算获得最佳阈值,该临界值在实际应用是也可根据临床要求在一定范围内浮动。具体可在某一特定人群中开展,然后依据该人群开展风险分数计算,然后对该人群宫颈癌中发生胞葬作用进行风险评估;当时实际应用时,是要应用本模型就应当视为在本发明范围内,不过多考虑阈值。具体的,获取最佳阈值常用的方法是选择使得模型的真正例率与假正例率之差最大的阈值作为最佳阈值,该方法被称为最大化youden指数方法,即找到使得tpr-fpr最大的闻值,可以通过计算不同阈值下的tpr和ppr,然后找到最大的tpr-fpr值对应的阈值,除了最大化youden指数方法外;还有一种常用的方法是选择使得模型的受试者工作特征曲线下面积(area under curve,简称auc)最大的阈值作为最佳阈值,auc值越大,说明模型的性能越好,可以通过计算roc曲线下的面积来得到auc值,然后选择使得auc值最大的阈值。除了利用r软件包计算获取最佳阈值外,还可以根据实际应用的需求来确定最佳阈值,例如某些场景中,将假正例视为重要错误,而将假负例视为一般错误,那么可以通过调整阈值来使得模型在假正例上的性能更好,对于另一些场景中,将假负例视为重要错误,而将假正例视为一般错误,那么可以通过调整闯值来使得模型在假负例上的性能更好。
10、其中,所述宫颈癌中胞葬作用风险为宫颈癌治疗后1年或3年或5年内的胞葬作用风险。
11、本发明第三方面涉及前述任一所述的宫颈癌中胞葬作用风险评估模型在制备评估宫颈癌中胞葬作用风险的产品中的应用。该模型可应用在部分分析产品中,比如一些自动化分析系统,将样本置入后通过基于宫颈癌中胞葬作用风险评估模型的软件就可以直接获得结果。还包括前述任一所述的宫颈癌中胞葬作用风险评估模型在制备宫颈癌预后风险评估的产品中的应用,在此应用中,风险评估模型具有作为疾病独立预后因素的能力,其获得评分结果足以作为宫颈癌预后风险评估的一个重要的指标,并且可以被认定为为属于高风险因素(参见具体实施例部分的独立预后分析部分已经验证了宫颈癌中胞葬作用风险评估模型作为独立预后因素可行性),该风险可为疾病预后复发风险或生存风险。
12、本发明第四方面涉及宫颈癌中胞葬作用风险评估装置,包括
13、样本检测模组:用于对样本进行检测,并获取样本中itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna基因表达量;
14、风险评估模组:将itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna基因表达量输入宫颈癌中胞葬作用风险预测模型公式并计算获得riskscore,公式为
15、riskscore=0.228956048*exp(itga5)-0.3336414*exp(snrpf)+0.509562825*exp(egl n1)-0.159621416*exp(ndufb7)-0.144489876*exp(ndufa2)-0.225660885*exp(srgap3)-0.121663983*exp(pcna);
16、结果比对模组:将获得的riskscore与阈值进行比对,riskscore>阈值则输出结果为宫颈癌中胞葬作用高风险,riskscore=阈值则输出结果为待估,riskscore<阈值则输出结果为宫颈癌中胞葬作用低风险。
17、就本方面而言,其特征的可选限定为:
18、其中,所述阈值为通过r软件包计算获取的最佳阈值;所述最佳阈值通过r软件包分析待检测人群获得,具体的分析计算方法可采用现有技术。
19、样本经过本风险评估装置评估后,可以对不同的样本进行风险分析,尤其是针对某一特定群体分析时,能够获得更为精准的结果。
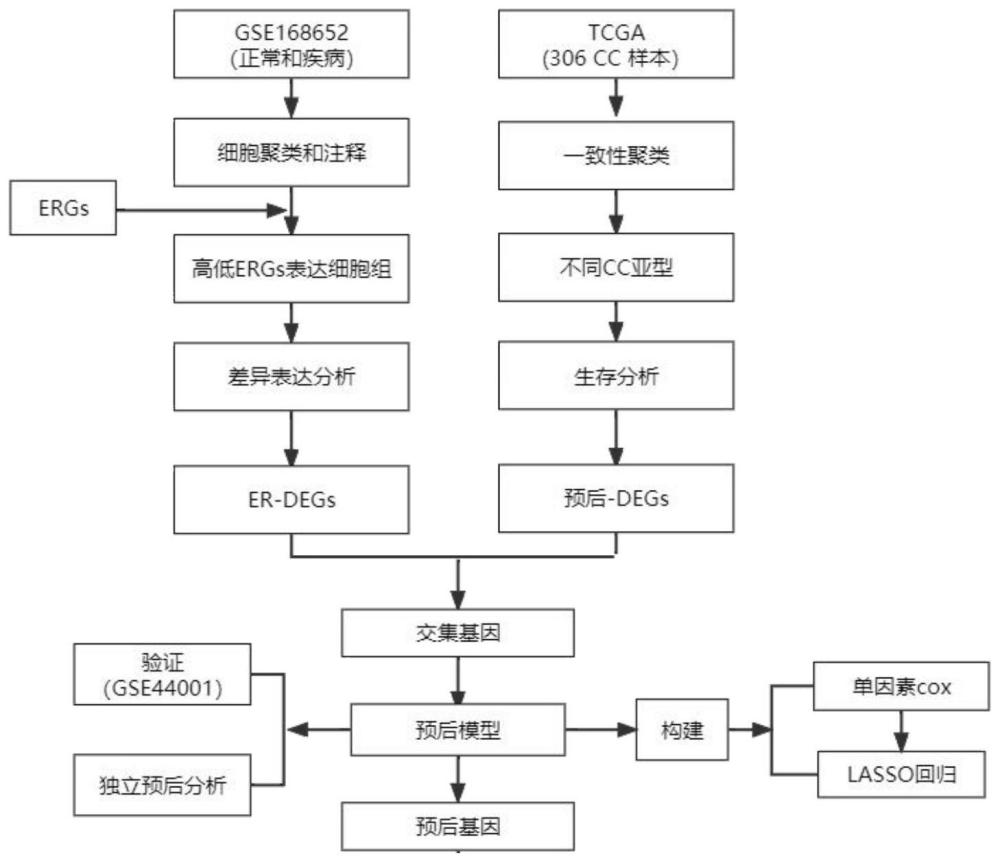
20、本发明第五方面涉及宫颈癌中胞葬作用风险评估模型的构建方法,具体包括下述步骤:
21、收集病例信息;
22、数据统计分析:基于收集的病例信息,通过多因素cox比例风险回归分析鉴定出宫颈癌中胞葬作用的预测因子,获得模型指标;
23、模型指标筛选:依据lasso回归分析,通过构造一个罚函数得到一个较为精炼的模型,使得它压缩一些系数,同时设定一些系数为零,当lambda最小时获得最优模型,并筛选获得7个模型指标itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna;
24、建立预测模型:将7个关键模型指标纳入预测模型中进行cox回归以计算每个变量的偏回归系数,建立宫颈癌中胞葬作用风险预测模型公式
25、riskscore=0.228956048*exp(itga5)-0.3336414*exp(snrpf)+0.509562825*exp(egl n1)-0.159621416*exp(ndufb7)-0.144489876*exp(ndufa2)-0.225660885*exp(srgap3)-0.121663983*exp(pcna),
26、式中itga5、snrpf、egln1、ndufb7、ndufa2、srgap3、pcna均为相应基因的表达量。
27、本发明的有益效果是:
28、明确了部分与宫颈癌中胞葬作用相关的预后基因,为宫颈癌中胞葬作用的风险评估提供了可靠的分析模型,可以获得更为精准的结果,且具有较高的特异性和敏感性,也为宫颈癌的治疗预后等提供了更多的分析手段。
- 还没有人留言评论。精彩留言会获得点赞!