一种制备肺组织单细胞悬液的试剂盒及其使用方法与应用与流程
本发明涉及生物,尤其是涉及一种制备肺组织单细胞悬液的试剂盒及其使用方法与应用。
背景技术:
1、单细胞测序技术是在单个细胞水平上,对基因组、转录组及表观基因组水平进行测序分析的技术,能够检出多细胞测序所无法得到的异质性信息。单细胞悬液的制备是单细胞测序实验的重要一环。细胞捕获上机对于单细胞悬液的要求十分严苛。
2、不同组织中细胞的连接方式不同,不同细胞之间的连接紧密程度也不同。因此,不同组织的单细胞悬液的制备难度也不同,需要根据组织特异性使用不同的方法进行制备。肺是机体重要的呼吸器官,研究肺组织细胞的主要细胞类型与稀有细胞类型,挖掘肺组织细胞的异质性有利于进一步深入了解肺部疾病的生理机制。而相关技术中,市场上相关的单细胞悬液制备试剂盒用于制备肺组织单细胞悬液时,也常出现解离时间过长、细胞死亡率较高、细胞碎片多、细胞背景不干净或损伤细胞聚集导致的细胞结团率高等问题,且解离效果不稳定,从而导致单细胞悬液质量差,进一步影响测序质量。
3、因此,提供一种适用于制备细胞死亡率低、细胞碎片少、细胞背景干净、结团率低的肺组织单细胞悬液的试剂盒非常重要。
技术实现思路
1、本发明旨在至少解决现有技术中存在的技术问题之一。为此,本发明提出一种制备肺组织单细胞悬液的试剂盒,其能够快速解离肺组织,制备单细胞悬液,且制备得到的单细胞悬液的细胞浓度高,细胞活性高,结团率低,背景干净无杂质,能够用于单细胞捕获、反转录建库以及高通量上机等后续实验操作。
2、本发明还提供一种制备肺组织单细胞悬液的方法。
3、本发明还提供上述试剂盒或方法在单细胞测序中的应用。
4、根据本发明的第一方面实施例的一种制备肺组织单细胞悬液的试剂盒,包括:
5、解离酶a液,所述解离酶a液含有0.20w/v%~0.30w/v%的胰蛋白酶和0.02w/v%~0.04w/v%的edta;
6、解离酶b液,所述解离酶b液含有0.5~1.2mg/ml的胶原酶ii、1.25~2.75mg/ml的胶原酶ⅳ、13.0~17.0μg/ml的dnase i和0.04~0.06mg/ml的dispaseⅱ;
7、红细胞裂解液;
8、其中,解离酶a液和解离酶b液的液体介质为等渗溶液。
9、根据本发明实施例的试剂盒,至少具有如下有益效果:
10、实施例的试剂盒中的解离酶a液用于消化上皮组织,解离酶b液用于消化细胞之间的细胞基质(如桥粒连接、黏着斑等)。其可以在10~20分钟内完成组织解离,在50~60分钟内制备得到细胞浓度高(可达百万以上),细胞活性高,结团率低,背景干净无杂质的单细胞悬液,且不用去除死细胞,可解离组织中大部分细胞,能够保留细胞多样性,可降低细胞捕获时双胞的概率。且该试剂盒用于制备单细胞悬液,无明显的批次效应,稳定性好;针对不同离体时间内的肺组织均可以稳定获得活性高,结团率低的单细胞悬液。制得的单细胞悬液可用于细胞原代培养、流式细胞术、单细胞捕获、反转录建库以及高通量上机等。
11、根据本发明的一些实施例,所述等渗溶液包括pbs、生理盐水、hank’s液或细胞培养基。等渗溶液是具有与细胞相同的盐浓度的溶液。
12、根据本发明的一些实施例,所述等渗溶液的ph为7.6~8.0。
13、根据本发明的一些实施例,所述细胞培养基包括细胞基础培养基。所述细胞基础培养基可以为本领域常用的各种基本培养基。例如,可以为bme细胞培养基、dmem细胞培养基、dmem/f12细胞培养基、fischer’s细胞培养基、imdm细胞培养基、199细胞培养基、mem细胞培养基、f10细胞培养基、f12细胞培养基或1640细胞培养基。
14、根据本发明的一些实施例,所述解离酶b液还包括抗细菌剂、抗真菌剂、丙酮酸钠、非必需氨基酸中的至少一种。所述抗细菌剂的浓度为1~2v/v%;所述抗真菌剂的浓度为2~4v/v%;所述丙酮酸钠的浓度为0.10~0.12mg/ml。例如:抗细菌剂可以为青霉素或链霉素;抗真菌剂可以为两性霉素b、奥昔康唑、硫康唑、噻苯咪唑、特比萘芬或托萘酯。在解离过程中,丙酮酸钠作为碳源参与细胞代谢。相比于葡萄糖等其他碳源,丙酮酸钠能够避免导致细胞代谢变化产生不一样的转录本,利于保持细胞状态以及下游实验的进行。
15、根据本发明的一些实施例,所述解离酶b液还可以包括其他碳源(包括但不限于乳酸钠、葡萄糖等)。
16、根据本发明的一些实施例,所述试剂盒还包括消化终止液。
17、根据本发明的一些实施例,所述消化终止液为包括血清、bsa中的至少一种的等渗溶液。后续细胞需要用于测序等下游实验时,所述消化终止液优选为含bsa的等渗溶液。所述消化终止液中,bsa的浓度为0.02w/v%~0.05w/v%。例如:具体可以为0.03w/v%。
18、根据本发明的第二方面实施例的一种制备肺组织单细胞悬液的方法,所述方法采用上述第一方面实施例中所述的试剂盒进行单细胞悬液的制备;包括以下步骤:
19、s1、采用所述解离酶a液处理肺组织,分离得到第一细胞悬液和未解离组织;
20、s2、采用所述解离酶b液处理所述未解离组织,分离得到第二细胞悬液;
21、s3、采用所述红细胞裂解液处理所述第一细胞悬液和所述第二细胞悬液,分离得到所述单细胞悬液。由于方法采用了上述实施例的试剂盒的全部技术方案,因此至少具有上述实施例的技术方案所带来的所有有益效果。
22、根据本发明的一些实施例,所述肺组织的来源哺乳动物和鸟类动物。
23、根据本发明的一些实施例,所述哺乳动物包括但不限于鼠、牛、猪、羊、犬、兔、猫或马。例如:具体可以为小鼠。
24、根据本发明的一些实施例,所述鸟类动物包括但不限于鹌鹑、鸡、麻雀、鸭或鹅。
25、根据本发明的一些实施例,步骤s1还包括对肺组织进行预处理。所述预处理包括清洗、剪碎中的至少一种。所述剪碎于所述解离酶a液中进行;需剪碎至肉眼可视无明显大块组织。所述清洗包括去除血液、脂肪等杂质。
26、根据本发明的一些实施例,所述肺组织的用量不低于30mg。例如:可以为30mg、40mg、50mg、60mg、70mg、80mg、90mg、100mg、110mg、120mg、130mg、140mg、150mg、160mg、170mg、180mg、190mg、200mg、210mg或220mg。
27、根据本发明的一些实施例,所述解离酶a液与所述肺组织的体积质量比为1ml:40~60mg。例如:可以为1ml:40mg、1ml:42mg、1ml:44mg、1ml:46mg、1ml:48mg、1ml:50mg、1ml:52mg、1ml:54mg、1ml:56mg、1ml:58mg或1ml:60mg。如果肺组织量过低,会过度解离,可能造成细胞活率降低或细胞状态受影响,以及试剂的浪费;如果肺组织量过高,可能会导致对样本的解离程度不够,获得的细胞异质性较差。
28、根据本发明的一些实施例,所述步骤s1的处理温度为20℃~30℃。例如:可以为20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃或30℃。
29、根据本发明的一些实施例,所述步骤s1的处理时间为8min~12min。例如:可以为8min、9min、10min、11min或12min。
30、根据本发明的一些实施例,步骤s1还包括第一解离后处理。所述第一解离后处理包括采用消化终止液终止解离、洗涤细胞中的至少一种。所述采用所述消化终止液终止解离具体可以为:包括向解离后的细胞组织混合液中加入3倍体积以上的所述消化终止液。
31、根据本发明的一些实施例,步骤s1中,所述分离的方法包括离心、静置沉降、过滤中的至少一种。所述离心的温度为2℃~6℃;所述离心的转速为200×g~400×g;所述离心的时间为4min~6min。所述静置沉降的温度为20℃~30℃;所述静置沉降的时间为0.5min~2min。所述过滤的温度为20℃~30℃;所述过滤经由筛网进行;所述筛网的孔径为35μm~45μm。。
32、根据本发明的一些实施例,所述解离酶b液与所述肺组织的体积质量比为1ml:40mg~60mg。
33、根据本发明的一些实施例,步骤s2还包括第二解离后处理。所述第二解离后处理包括采用所述消化终止液终止解离、洗涤细胞中的至少一种。具体可以为:向解离后的细胞悬液中加入2倍体积以上的所述消化终止液。
34、根据本发明的一些实施例,所述步骤s2的处理温度为36.0℃~38.0℃。例如:可以为36.0℃、36.5℃、37℃、37.5℃或38.0℃。如果温度过高或过低均会导致解离酶的活性降低,从而导致解离效果达不到预期。
35、根据本发明的一些实施例,所述步骤s2的处理时间为16~22min。例如:可以为16min、17min、18min、19min、20min、21min或22min。
36、根据本发明的一些实施例,步骤s2中,所述分离得到第二细胞悬液的方法包括过滤。
37、根据本发明的一些实施例,所述过滤经由筛网进行。所述筛网的孔径为35μm~45μm。例如:具体可以为35μm、36μm、37μm、38μm、39μm、40μm、41μm、42μm、43μm、44μm或45μm。
38、根据本发明的一些实施例,所述步骤s3还包括红细胞裂解前处理。所述红细胞裂解前处理包括分离所述第一细胞悬液和所述第二细胞悬液中的细胞。后续采用所述红细胞裂解液处理分离的细胞。所述分离的方法包括离心;所述离心的温度为2℃~6℃;所述离心的转速为200×g~400×g;所述离心的时间为4min~6min。
39、根据本发明的一些实施例,所述红细胞裂解液与所述肺组织的体积质量比为1ml:40mg~60mg。
40、根据本发明的一些实施例,所述步骤s3还包括红细胞裂解后处理。所述红细胞裂解后处理包括采用所述消化终止液终止裂解、过滤、洗涤细胞中的至少一种。具体可以为:向裂解红细胞后的细胞悬液中加入6倍体积以上的所述消化终止液。
41、根据本发明的一些实施例,所述红细胞裂解液的处理时间为5min~8min。例如:可以为5min、6min、7min或8min。如果处理时间较短,红细胞会有部分残留;若处理时间较长,会导致得到的单细胞悬液的细胞活性降低。
42、根据本发明的一些实施例,所述红细胞裂解液的处理温度为20℃~30℃。例如:可以为20℃、21℃、22℃、23℃、24℃、25℃、26℃、27℃、28℃、29℃或30℃。
43、根据本发明的一些实施例,步骤s1、s2或s3中所述的洗涤细胞均可以通过消化终止液洗涤。步骤s1、s2或s3中所述的洗涤细胞的重复次数分别独立选自为2~3次。洗涤后的细胞分离可以通过离心实现。所述离心的温度为2℃~6℃;所述离心的转速为200×g~400×g;所述离心的时间为4min~6min。
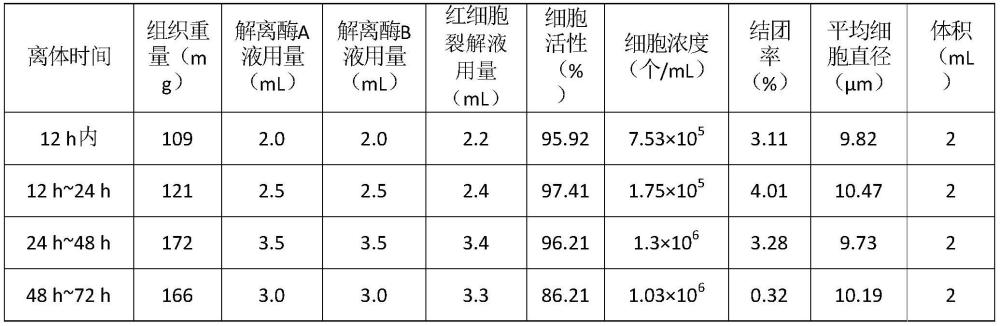
44、根据本发明的一些实施例,所述方法还包括对所述第一细胞悬液、所述第二细胞悬液或所述单细胞悬液进行质检。所述质检包括但不限于检测细胞浓度、活率、结团率、细胞直径、细胞悬液背景。
45、根据本发明的第三方面实施例的上述试剂盒或上述方法在单细胞测序、细胞原代培养、流式细胞术、单细胞捕获或反转录建库中的应用。
46、本发明的其它特征和优点将在随后的说明书中阐述,并且,部分地从说明书中变得显而易见,或者通过实施本发明而了解。
- 还没有人留言评论。精彩留言会获得点赞!