一种手性反式-N-BOC-1-氨基环戊烷-3-甲酸的制备方法与流程
本发明属于有机合成,具体涉及一种手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,尤其涉及一种收率高的手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法。
背景技术:
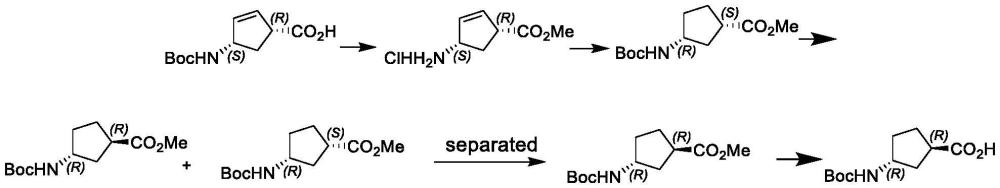
1、反式的手性1-氨基环戊烷-3-甲酸是核苷类似物逆转录酶抑制剂的关键片段,也是很多新型抗癌药物的关键片段,常规制备方法采用如下步骤:
2、
3、其中第三步差化过程制备分离反式目标物,存在分离过程困难,制备分离昂贵的问题,无法实现工业化生产,为反式手性1-氨基环戊烷-3-甲酸的大规模应用造成了阻碍。因此,如何提供一种收率高、制备方法简单、成本低且光学纯度高的反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,成为了亟待解决的问题。
技术实现思路
1、针对现有技术的不足,本发明的目的在于提供一种手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,尤其提供一种收率高的手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法。本发明提供的制备方法相比现有技术,反应步骤、工序明显减少,整体过程更加简单,总收率更高,大幅降低了生产成本,适合工业化生产。
2、为达到此发明目的,本发明采用以下技术方案:
3、本发明提供了一种手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,所述制备方法包括以下步骤:
4、(1)将(1r,4s)-4-((叔丁氧基羰基)氨基)环戊-2-烯甲酸与甲醇混合酯化,得到化合物1;
5、(2)将化合物1与碱、二碳酸二叔丁酯混合反应,得到化合物2;
6、(3)将化合物2与碳酸钾混合反应,得到化合物3;
7、(4)将化合物3与硼氢化钠、催化剂混合反应,得到化合物4;
8、(5)将化合物4与碱混合水解,得到所述手性反式-n-boc-1-氨基环戊烷-3-甲酸。
9、反应流程如下:
10、
11、上述方法通过采用双键迁移、再进行还原的方式,有效避免了现有技术中的差化过程造成的分离困难问题,反应步骤、工序明显减少,整体过程更加简单,总收率更高,大幅降低了生产成本,适合工业化生产。
12、优选地,步骤(1)所述反应的温度为10-80℃,时间为2-8h,其中温度可以是10℃、15℃、20℃、25℃、30℃、35℃、40℃、45℃、50℃、55℃、60℃、65℃、70℃、75℃或80℃等,时间可以是2h、2.5h、3h、3.5h、4h、4.5h、5h、5.5h、6h、6.5h、7h、7.5h或8h等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
13、优选地,步骤(2)所述反应的温度为10-30℃,时间为8-16h,其中温度可以是10℃、15℃、20℃、25℃或30℃等,时间可以是8h、9h、10h、11h、12h、13h、14h、15h或16h等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
14、优选地,步骤(3)所述化合物2与碳酸钾的摩尔比为1:(1.5-2.5),例如1:1.5、1:1.6、1:1.7、1:1.8、1:1.9、1:2、1:2.1、1:2.2、1:2.3、1:2.4或1:2.5等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
15、优选地,步骤(3)所述反应的温度为50-80℃,时间为8-15h,其中温度可以是50℃、55℃、60℃、65℃、70℃、75℃或80℃等,时间可以是8h、9h、10h、11h、12h、13h、14h或15h等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
16、优选地,步骤(4)所述催化剂包括l-焦谷氨酸、l-脯氨酸、l-丙氨酸或l-羟脯氨酸中任意一种或至少两种的组合,优选l-焦谷氨酸。
17、上述特定催化剂能够有效催化反应生成目标手性产物,同时选择特定催化剂,能够进一步提高产品的光学纯度。
18、优选地,步骤(4)所述化合物3与催化剂、硼氢化钠的摩尔比为1:(0.3-0.5):(1-5),其中,催化剂的份数可以是0.3、0.35、0.4、0.45或0.5等,硼氢化钠的份数可以是1、2、3、4或5等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
19、优选地,步骤(4)所述反应的温度为10-30℃,时间为8-16h,其中温度可以是10℃、15℃、20℃、25℃或30℃等,时间可以是8h、9h、10h、11h、12h、13h、14h、15h或16h等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
20、优选地,步骤(5)所述碱包括氢氧化锂、氢氧化钠或氢氧化锂中任意一种或至少两种的组合。
21、优选地,步骤(5)所述化合物4与碱的摩尔比为1:(1.5-2.5),例如1:1.5、1:1.6、1:1.7、1:1.8、1:1.9、1:2、1:2.1、1:2.2、1:2.3、1:2.4或1:2.5等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
22、优选地,步骤(5)所述反应的温度为-10~5℃,时间为2-5h,其中温度可以是-10℃、-9℃、-8℃、-7℃、-6℃、-5℃、-4℃、-3℃、-2℃、-1℃、0℃、1℃、2℃、3℃、4℃或5℃等,时间可以是2h、2.5h、3h、3.5h、4h、4.5h或5h等,但不限于以上所列举的数值,上述数值范围内其他未列举的数值同样适用。
23、与现有技术相比,本发明具有如下有益效果:
24、本发明提供了一种手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,通过采用双键迁移、再进行还原的方式,有效避免了现有技术中的差化过程造成的分离困难问题,反应步骤、工序明显减少,整体过程更加简单,总收率更高,大幅降低了生产成本,适合工业化生产。
技术特征:
1.一种手性反式-n-boc-1-氨基环戊烷-3-甲酸的制备方法,其特征在于,所述制备方法包括以下步骤:
2.根据权利要求1所述的制备方法,其特征在于,步骤(1)所述反应的温度为10-80℃,时间为2-8h。
3.根据权利要求2所述的制备方法,其特征在于,步骤(2)所述反应的温度为10-30℃,时间为8-16h。
4.根据权利要求1-3中任一项所述的制备方法,其特征在于,步骤(3)所述化合物2与碳酸钾的摩尔比为1:(1.5-2.5)。
5.根据权利要求1-4中任一项所述的制备方法,其特征在于,步骤(3)所述反应的温度为50-80℃,时间为8-15h。
6.根据权利要求1-5中任一项所述的制备方法,其特征在于,步骤(4)所述催化剂包括l-焦谷氨酸、l-脯氨酸、l-丙氨酸或l-羟脯氨酸中任意一种或至少两种的组合,优选l-焦谷氨酸。
7.根据权利要求1-6中任一项所述的制备方法,其特征在于,步骤(4)所述化合物3与催化剂、硼氢化钠的摩尔比为1:(0.3-0.5):(1-5)。
8.根据权利要求1-7中任一项所述的制备方法,其特征在于,步骤(4)所述反应的温度为10-30℃,时间为8-16h。
9.根据权利要求1-8中任一项所述的制备方法,其特征在于,步骤(5)所述碱包括氢氧化锂、氢氧化钠或氢氧化锂中任意一种或至少两种的组合。
10.根据权利要求1-9中任一项所述的制备方法,其特征在于,步骤(5)所述化合物4与碱的摩尔比为1:(1.5-2.5);
技术总结
本发明提供了一种手性反式‑N‑BOC‑1‑氨基环戊烷‑3‑甲酸的制备方法,所述制备方法包括以下步骤:(1)将(1R,4S)‑4‑((叔丁氧基羰基)氨基)环戊‑2‑烯甲酸与甲醇混合酯化,得到化合物1;(2)将化合物1与碱、二碳酸二叔丁酯混合反应,得到化合物2;(3)将化合物2与碳酸钾混合反应,得到化合物3;(4)将化合物3与硼氢化钠、催化剂混合反应,得到化合物4;(5)将化合物4与碱混合水解,得到所述手性反式‑N‑BOC‑1‑氨基环戊烷‑3‑甲酸。本发明提供的制备方法相比现有技术,反应步骤、工序明显减少,整体过程更加简单,总收率更高,大幅降低了生产成本,适合工业化生产。
技术研发人员:史曼曼,翟志扬,袁心康,吴天俊
受保护的技术使用者:上海馨远医药科技有限公司
技术研发日:
技术公布日:2024/3/27
- 还没有人留言评论。精彩留言会获得点赞!