一种评估间充质干细胞免疫调控能力的方法与流程
本发明属于生物医药,具体涉及一种评估间充质干细胞免疫调控能力的方法。
背景技术:
1、目前,淋巴细胞增殖抑制实验(朱海鹏,彭亮,王培培等.羊水、脐带和骨髓来源间充质干细胞对淋巴细胞增殖的抑制效果比较[j].新医学,2013,44(11):743-747.)可用于评估间充质干细胞的免疫调节功能(刘梦婷,饶巍,韩兵,肖翠红,武栋成.人脐带间充质干细胞的体外免疫调节特性[j].中国组织工程研究,2020,24(7):1063-1068.)。现有的淋巴细胞增殖抑制检测所采用的外周血单个核细胞(peripheralblood mononuclear cell,pbmc)来源于外周血,不同批次的pbmc细胞波动大,导致间充质干细胞体外检测淋巴细胞增殖抑制水平存在较大差异,数据不稳定。因此,急需开发新的评估间充质干细胞的免疫调节功能的方法。
技术实现思路
1、有鉴于此,本发明的目的在于提供一种评估间充质干细胞免疫调控能力的方法,根据bv2细胞增殖抑制率来评价msc的免疫调控功能,可获得准确可靠的评估结果。
2、本发明提供了一种评估间充质干细胞免疫调控能力的方法,包括以下步骤:
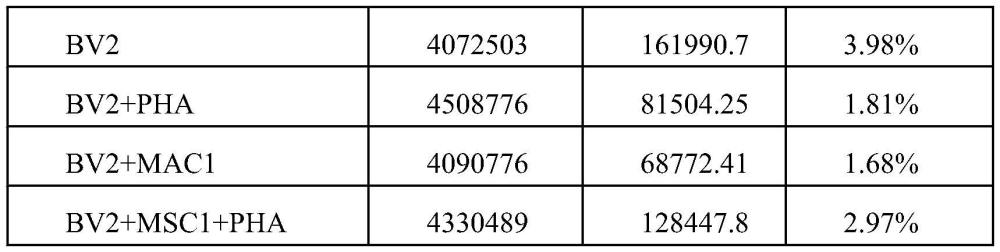
3、将置于培养基中培养的bv2细胞记为第一组,将置于含植物血凝素pha的培养基中培养的bv2细胞记为第二组,将置于含植物血凝素pha的培养基中培养的bv2细胞和去增殖剂处理的间充质干细胞或间充质干细胞上清液记为第三组,将置于培养基中培养的bv2细胞和去增殖剂处理的间充质干细胞或间充质干细胞上清液记为第四组;
4、将所述第一组、第二组、第三组和第四组培养后,与细胞活性检测试剂混合,检测各组的发光读数,根据公式i计算bv2细胞增殖抑制率;
5、bv2细胞增殖抑制率=1-[rlus(第三组)-rlus(第四组)]/[rlus(第二组)-rlus(第一组)]×100%公式i;
6、其中,rlus(第一组)、rlus(第二组)、rlus(第三组)、rlus(第四组)依次表示第一组、第二组、第三组和第四组发光读数结果;
7、所述bv2细胞增殖抑制率与间充质干细胞免疫调控能力呈正比。
8、优选的,所述去增殖剂处理的间充质干细胞的制备方法,为采用丝裂霉素c处理活化的间充质干细胞,洗涤,得到去增殖剂处理的间充质干细胞。
9、优选的,所述丝裂霉素c的处理浓度为8~12μg/ml;
10、所述丝裂霉素c的处理时间为50~70min。
11、优选的,所述植物血凝素pha的浓度为8~12μg/ml。
12、优选的,所述bv2细胞和去增殖剂处理的间充质干细胞的数量比为0.8~1.2:0.8~1.2。
13、优选的,当第三组或第四组中添加间充质干细胞上清液时,bv2细胞与间充质干细胞上清液混合;
14、所述bv2细胞的密度为(1~5)×105/ml。
15、优选的,所述第一组、第二组、第三组和第四组培养的时间为70~74h;
16、所述第一组、第二组、第三组和第四组培养的温度为36~38℃;
17、所述第一组、第二组、第三组和第四组培养的二氧化碳的浓度为5%。
18、优选的,所述细胞活性检测试剂和去增殖剂处理的间充质干细胞悬液或间充质干细胞上清液的体积比为1:1。
19、优选的,所述细胞活性检测试剂包括cell viability assay试剂。
20、优选的,所述间充质干细胞包括以下至少一种:脐带来源的间充质干细胞、羊膜来源的间充质干细胞和胎盘来源的间充质干细胞。
21、本发明提供了一种评估间充质干细胞免疫调控能力的方法,包括以下步骤:将置于培养基中培养的bv2细胞记为第一组,将置于含植物血凝素pha的培养基中培养的bv2细胞记为第二组,将置于含植物血凝素pha的培养基中培养的bv2细胞和去增殖剂处理的间充质干细胞或间充质干细胞上清液记为第三组,将置于培养基中培养的bv2细胞和去增殖剂处理的间充质干细胞或间充质干细胞上清液记为第四组;将所述第一组、第二组、第三组和第四组培养后,与细胞活性检测试剂混合,检测各组的发光读数,根据公式i计算bv2细胞增殖抑制率;bv2细胞增殖抑制率=1-[rlus(第三组)-rlus(第四组)]/[rlus(第二组)-rlus(第一组)]×100%公式i;所述bv2细胞增殖抑制率与间充质干细胞免疫调控能力呈正比。本发明基于bv2细胞(小鼠小胶质细胞而获得的永生细胞系)为永生化细胞,具有不断分裂、更长的寿命和更高的增殖能力,批间差异小,随用随取,可长期冻存的特点,代替批间波动较大的外周血单个核细胞,实验证明,bv2细胞更适合用来评估间充质干细胞免疫调控能力。实验表明,本发明提供的方法得到的bv2细胞增殖抑制率与淋巴细胞增殖抑制检测结果以及tnf-α抑制率、th1抑制率、th17抑制率和treg抑制率的均值具有可比性,说明bv2细胞检测间充质干细胞的免疫调节活性可行。由此可见,本发明提供的方法能够得到相对稳定的增殖抑制率。
技术特征:
1.一种评估间充质干细胞免疫调控能力的方法,其特征在于,包括以下步骤:
2.根据权利要求1所述方法,其特征在于,所述去增殖剂处理的间充质干细胞的制备方法,为采用丝裂霉素c处理活化的间充质干细胞,洗涤,得到去增殖剂处理的间充质干细胞。
3.根据权利要求2所述方法,其特征在于,所述丝裂霉素c的处理浓度为8~12μg/ml;
4.根据权利要求1所述方法,其特征在于,所述植物血凝素pha的浓度为8~12μg/ml。
5.根据权利要求1所述方法,其特征在于,所述bv2细胞和去增殖剂处理的间充质干细胞的数量比为0.8~1.2:0.8~1.2。
6.根据权利要求1所述方法,其特征在于,当第三组或第四组中添加间充质干细胞上清液时,bv2细胞与间充质干细胞上清液混合,所述bv2细胞悬液中细胞密度为(1~5)×105/ml。
7.根据权利要求1所述方法,其特征在于,所述第一组、第二组、第三组和第四组培养的时间为70~74h;
8.根据权利要求1所述方法,其特征在于,所述细胞活性检测试剂和去增殖剂处理的间充质干细胞悬液或间充质干细胞上清液的体积比为1:1。
9.根据权利要求8所述方法,其特征在于,所述细胞活性检测试剂包括cellviabilityassay试剂。
10.根据权利要求1~9中任意一项所述方法,其特征在于,所述间充质干细胞包括以下至少一种:脐带来源的间充质干细胞、羊膜来源的间充质干细胞和胎盘来源的间充质干细胞。
技术总结
本发明提供了一种评估间充质干细胞免疫调控能力的方法,属于生物医药技术领域。本发明针对传统的淋巴细胞增殖抑制实验评估间充质干细胞免疫调节功能时,不同批次的PBMC细胞波动大,评估结果不稳定的问题,本发明用BV2细胞代替PBMC细胞进行了增殖抑制共培养实验,并用间充质干细胞的培养上清液和BV2细胞共培养进行实验,均得到了相对稳定的增殖抑制率,从而为间充质干细胞临床应用提供了基础。
技术研发人员:蒋雨薇,华江舟
受保护的技术使用者:长沙干细胞与再生医学工业技术研究院有限公司
技术研发日:
技术公布日:2024/3/24
- 还没有人留言评论。精彩留言会获得点赞!