一种用于hiPSC源外泌体纯度检测的方法及其专用消化剂与流程
本发明属于生物,具体涉及一种用于hipsc源外泌体纯度检测的方法及其专用消化剂。
背景技术:
1、外泌体是一类具有生物学活性的,由细胞分泌的细胞外囊泡。其粒径范围为30-150 nm,具有磷脂双分子层结构。外泌体携带供体细胞的分子生物学信息,如核酸、蛋白质和脂质等,参与细胞通讯及多种生理病理过程的调节。人诱导多能干细胞(human inducedpluripotent stem cell,hipsc)是一种具有强大分化再生潜力的类胚胎干细胞,可分化为人体各个器官和组织所需要的各种细胞类型。由hipsc分泌的外泌体(以下称hipsc源外泌体)已被证明具有强大的再生和抗炎作用,对心肌细胞具有保护作用,改善细胞凋亡和肥大引起的心肌损伤(admiak marta, 等人. "induced pluripotent stem cell (ipsc)-derived extracellular vesicles are safer and more effective for cardiacrepair than ipscs." circulation research122.3 (2018): 296-309.),对急性肾损伤大鼠模型也表现显著的保护效果(collino federica, 等人. "extracellular vesiclesderived from induced pluripotent stem cells promote renoprotection in acutekidney injury model." cells9.2 (2020): 453.)。因此,对hipsc源外泌体进行提纯、鉴定、检测和利用具有非常重要的临床应用价值。
2、外泌体可利用多种方法进行鉴定和检测,如纳米粒子跟踪分析(nanoparticletracking analysis,nta)、western blot等。这些方法均是针对外泌体样本总体进行检测,无法对单颗粒进行表征,也无法对外泌体与其他颗粒杂质进行区分。虽然透射电镜可以对单颗粒进行表征,但这种方法的样品制备繁琐、检测效率低、设备昂贵,并且无法进行定量。随着技术的发展,纳米流式检测法已被广泛应用于外泌体的检测(例如纯度检测),并且该方法已被外泌体协会纳入团体标准。
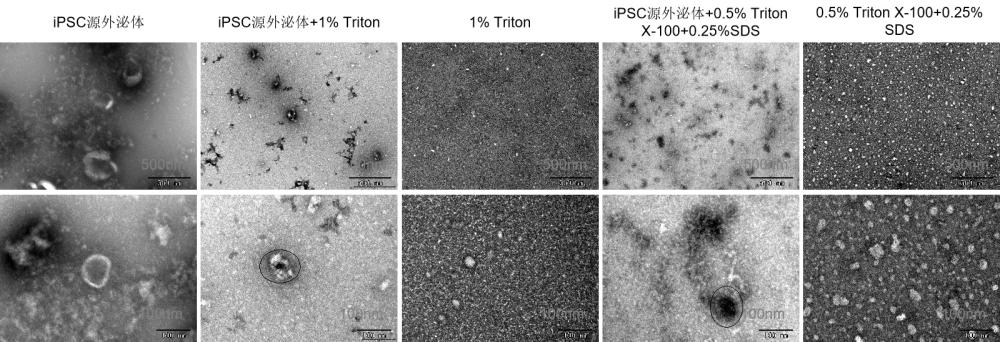
3、已知外泌体囊泡的脂质膜相比于蛋白聚集物,对表面活性剂的敏感度更高,因此在用纳米流式检测法对外泌体进行检测时,通常需要不同类型的表面活性剂来破坏外泌体囊泡的膜结构(cloutier nathalie, 等人. "the exposure of autoantigens bymicroparticles underlies the formation of potent inflammatory components: themicroparticle-associated immune complexes." embo molecular medicine5.2 (2013):235-249;wu cheng yeu, 等人. "membrane vesicles nucleate mineralo-organicnanoparticles and induce carbonate apatite precipitation in human bodyfluids." the journal of biological chemistry288.42 (2013): 30571-30484;rousseau matthieu, 等人. "detection and quantification of microparticles fromdifferent cellular lineages using flow cytometry. evaluation of the impact ofsecreted phospholipase a2 on microparticle assessment." plos one10.1 (2015):e0116812;arraud n, 等人. "a simple flow cytometry method improves thedetection of phosphatidylserine-exposing extracellular vesicles." journal of thrombosis and haemostasis: jth13.2 (2015): 237-247. )。目前,常用纳米流式检测经表面活性剂triton x-100处理前后的外泌体,通过颗粒数(通常为30 nm~200 nm粒径范围内的颗粒)的变化,来确定外泌体的纯度(györgy bence, 等人. "detection andisolation of cell-derived microparticles are compromised by protein complexesresulting from shared biophysical parameters." blood117.4 (2011): e39-e48.)。虽然这种方法可适用于多种来源(例如293t细胞、间充质干细胞、牛乳等)的外泌体的纯度检测,但是,这种基于triton x-100的外泌体纯度检测法并不是通用的,其在针对hipsc源外泌体时,无法检测hipsc源外泌体纯度。其他表面活性剂,例如sds(十二烷基硫酸钠)、tween20或脱氧胆酸盐虽然也可用于坏外泌体囊泡的膜结构(osteikoetxea xabier, 等人. "differential detergent sensitivity of extracellular vesicle subpopulations." organic&biomolecular chemistry13.38 (2015): 9775-9782.),但这些表面活性剂在单独使用时也均不能充分破坏hipsc源外泌体囊泡的膜结构,因此不能单独用于对hipsc源外泌体的纯度进行检测。因此,本领域亟需一种可对hipsc源外泌体纯度进行检测的有效方法。
技术实现思路
1、针对现有技术中存在的问题的一个或多个,本发明的一个方面提供一种用于hipsc源外泌体纯度检测的方法,其使用由triton x-100和sds组合的消化剂对hipsc源外泌体样品进行消化处理,并利用纳米流式对消化处理后的样品进行检测,其中所述tritonx-100的使用终浓度为0.1%~1%,所述sds的使用终浓度为0.1%~0.5%。
2、在一些实施方式中,所述方法包括以下操作:
3、1)使用所述消化剂对hipsc源外泌体样品进行消化处理,作为表面活性剂处理组,并同步使用与所述消化剂同体积的dpbs对hipsc源外泌体样品进行消化处理,作为dpbs处理组;
4、2)利用纳米流式检测所述表面活性剂处理组和dpbs处理组的颗粒数(例如在30-200 nm范围内的颗粒数),并按照下式(i)计算hipsc源外泌体的纯度:
5、 (i)
6、式(i)中:
7、所述表面活性剂是指:triton x-100和sds;
8、所述表面活性剂本底颗粒数是指:当所述消化剂中表面活性剂浓度超过临界胶束浓度时,表面活性剂在水溶液中自发形成胶束,胶束尺寸分布广泛,其中存在与hipsc源外泌体粒径相接近的胶束,这些胶束颗粒为本底颗粒。
9、在一些实施方式中,所述方法还包括对经所述消化剂处理后的hipsc源外泌体样品进行超声处理。
10、在一些实施方式中,所述超声处理的条件为在500w以上条件下超声处理5 min以上。
11、在一些实施方式中,所述超声处理的条件为500-600w条件下超声处理5-10 min。
12、本发明另一方面提供一种用于hipsc源外泌体纯度检测的专用消化剂,其由使用终浓度为0.1%~1%的triton x-100和使用终浓度为0.1%~0.5%的sds组合而成。
13、本发明提供的所述的专用消化剂在检测hipsc源外泌体纯度中的应用以及在破坏hipsc源外泌体囊泡的膜结构中的应用也属于本发明的内容。
14、基于以上技术方案提供的用于hipsc源外泌体纯度检测的方法为使用由终浓度为0.1%~1%的triton x-100和终浓度为0.1%~0.5%的sds组合的消化剂对hipsc源外泌体样品进行消化处理,此种方法能够针对性地充分裂解hipsc源外泌体囊泡的膜结构,进而可以准确检测hipsc源外泌体的纯度。因此,本发明还提供一种专用于检测hipsc源外泌体的纯度的消化剂,其由使用终浓度为0.1%~1%的triton x-100和使用终浓度为0.1%~0.5%的sds组合而成。
- 还没有人留言评论。精彩留言会获得点赞!