一种检测二氧化硫的荧光探针及其制备方法和应用与流程
本发明属于分析化学技术领域,具体涉及一种检测二氧化硫的荧光探针及其应用。
背景技术:
二氧化硫是最常见、最简单的硫氧化物。大气主要污染物之一。火山爆发时会喷出该气体,在许多工业过程中也会产生二氧化硫。在日常生活中,so2及其衍生物被广泛应用在工业生产、食品加工和医药制造等方面。工业上常利用二氧化硫的漂白性来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可以用作食物和干果的防腐剂。按照标准规定合理使用二氧化硫不会对人体健康造成危害,但长期超限量接触二氧化硫可能导致人类呼吸系统疾病及多组织损伤。
研究发现,暴露于高剂量的硫酸氢盐中,不仅是导致呼吸疾病,也与肺癌,心血管疾病的原凶,同时与许多神经系统疾病,如中风、偏头痛、阿尔兹海默症也有不可分的关系。二氧化硫吸入后会溶解到人体的血液中。轻度中毒时,发生流泪、畏光、咳嗽、咽喉痛;严重中毒者可在数小时之内发生肺水肿,出现心慌、胸闷、呼吸困难、咯血。长期低浓度接触,可出现头痛、头昏、乏力等全身症状。由于环境中so2及其衍生物的含量低,传统的检测方法受限,因而急需开发一种灵敏度高、选择性好且成本低的方法,用于快速测定so2含量,因此开发一种有效快速检测二氧化硫及其衍生物的技术具有重要意义。
近年来,对环境中和生物体中重要的物种进行识别和检测是一个重要的研究课题。与其他分析工具相比,荧光探针具有操作简单,检测限低,灵敏度高等优点,被广泛用于生物化学,药学以及环境研究和工业领域中的诊断,监测和分析工具。
技术实现要素:
针对现有技术中的问题,本发明提供一种快速检测二氧化硫的荧光探针,响应速度快、抗干扰能力强。
本发明的另一目的是提供一种上述荧光探针在检测溶液中或生物细胞内亚硫酸氢盐的应用。
为实现上述目的,本发明采用如下技术方案。
一种检测二氧化硫的荧光探针,简称sop,其化学结构如式(i)所示:
式(i)。
上述荧光探针的制备方法,包括以下步骤:
(1)取2,7-萘二酚和二甲胺在焦亚硫酸钠存在下加热反应,得到化合物(1):
(2)在氮气保护下,化合物(1)和化合物(2)在浓h2so4中加热反应,分离纯化后得到荧光探针化合物:
步骤(1)中,2,7-萘二酚和二甲胺的摩尔比为1:4。
步骤(1)中,反应温度为150℃。
步骤(1)中,还包括分离纯化步骤:反应结束后反应液中加入饱和nacl洗涤,用乙酸乙酯萃取,无水硫酸钠干燥后旋蒸干,产物再以二氯甲烷:甲醇=40:1v/v为淋洗液过硅胶色谱柱。
步骤(2)中,化合物(1)和化合物(2)的摩尔比为1:1。
步骤(2)中,反应温度为90℃。
步骤(2)中,所述分离纯化步骤为:反应结束后待反应液冷却到室温后,将其滴加到0℃冰水中,搅拌下加入hclo4,用二氯甲烷萃取后,用无水硫酸钠干燥然后旋蒸干,产物再以二氯甲烷:甲醇=30:1v/v为淋洗液过硅胶色谱柱。
一种上述荧光探针在检测溶液、细胞或生物体中亚硫酸氢根或亚硫酸根的应用。
本发明的机理如下:
本文根据亚硫酸氢或亚硫酸盐的亲核性,我们设计了以c=c键为反应活性中心,亚硫酸氢或亚硫酸盐通过亲核加成进攻不饱和c=c键,使so2衍生物与其进行加成反应,从而得到了此种so2荧光探针对于研究其在环境中的检测研究具有重要的意义。
本发明具有以下优点:
本发明的探针合成路径简单,合成方法快捷易制得,毒性小且易操作。在检测方面具有快速响应选择性好等优点且可以应用于生物成像。
附图说明
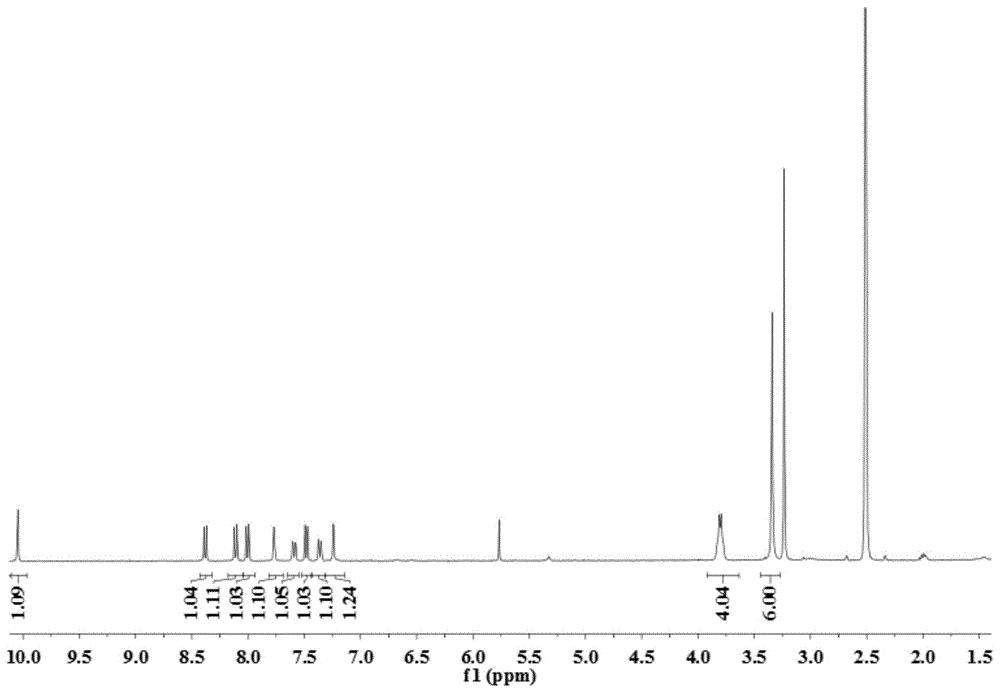
图1是探针sop的1hnmr谱图;
图2是探针sop对不同浓度二氧化硫的响应的荧光光谱;
图3是探针sop检测亚硫酸氢钠的动力学实验;
图4是探针sop在不同ph的pbs缓冲液中的荧光光谱;
图5是探针sop对不同离子的选择性响应;
图6是探针sop及探针识别亚硫酸氢钠后的稳定性;
图7是探针sop在活细胞中的成像。
具体实施方式
下面结合实施例和附图对本发明做进一步说明,但本发明不受下述实施例的限制。
实施例1荧光探针sop的合成
(1)化合物(1)的合成:
取2,7-萘二酚(1.69g,10mmol)加入装有一定量蒸馏水的圆底烧瓶中,再加入焦亚硫酸钠(3.8g,20mmol)和33%的二甲胺(15.4g,40mmol),在冰浴下搅拌10min,然后在150℃下搅拌3h,得到化合物(1),反应结束后加入饱和nacl洗涤,用乙酸乙酯萃取,无水硫酸钠干燥后旋蒸干,经硅胶色谱柱(淋洗液为二氯甲烷:甲醇=40:1v/v)提纯后进行下一步反应;
(2)化合物sop的合成:
取化合物(1)(2.9g,15.5mmol)和化合物(2)(3.0g,15.5mmol)加入到100ml烧瓶中,加入10ml浓h2so4,在氮气保护下,加热至90℃搅拌3h,反应结束后待其冷却到室温后,将其滴加到冰水中,搅拌下加入1mlhclo4,用二氯甲烷萃取后,用无水硫酸钠干燥然后旋蒸干,经色谱柱(淋洗液为二氯甲烷:甲醇=30:1v/v)提纯后得到化合物sop。其1hnmr图谱如图1:1hnmr(400mhz,dmso)δ10.05(s,1h),8.38(d,j=8.9hz,1h),8.11(d,j=9.5hz,1h),8.00(d,j=9.1hz,1h),7.77(s,1h),7.59(dd,j=9.4,2.0hz,1h),7.48(d,j=8.8hz,1h),7.36(dd,j=9.1,2.2hz,1h),7.24(s,1h),3.80(d,j=6.8hz,2h),3.37(d,j=24.5hz,3h),1.29(t,j=7.0hz,3h)。
实施例2荧光探针对不同浓度亚硫酸氢钠的响应
配制浓度为1mm的本发明所述检测二氧化硫荧光探针sop的二甲基亚砜(dmso)的测试母液溶液待用。测试试液为2ml体系,使得测试液中,探针的浓度为10μm,测试使用的亚硫酸氢钠的浓度分别为5µm、10µm、15µm、20µm、30µm、40µm、50µm、70µm、100μm,其中含dmso的体积分数为20%。继而进行荧光光谱测试和荧光检测(λex=365nm,λem=425nm),得各体系中荧光强度,建立荧光强度与亚硫酸氢钠浓度标准曲线。如图2所示,随着亚硫酸氢钠浓度的增加,该探针的荧光强度显著增强,当亚硫酸氢钠浓度达到100μm时,反应体系荧光强度达到饱和状态。
实施例3荧光探针对亚硫酸氢钠的响应动力学
配制体积为2ml,探针终浓度为10μm,含20%dmso溶液的pbs溶液,体系ph为7.4,加入亚硫酸氢钠(100μm),每隔2秒进行荧光检测(λex=365nm,λem=425nm)。得各体系中荧光强度,建立荧光强度与时间的标准曲线。如图3所示,在3秒内荧光强度变化达到稳定。
实施例4不同ph对荧光探针响应亚硫酸氢钠的影响
配制体积为2ml,探针终浓度为10μm,含20%dmso溶液的pbs溶液,(pbs缓冲液的ph值分别为4.0、4.5、5.0、5.5、6.0、6.5、7.0、7.5、8.0、8.5、9.0)分别测试探针的荧光光谱和探针加亚硫酸氢钠的荧光光谱,得各体系中荧光强度,建立荧光强度与ph值的标准曲线。如图4所示,在ph值在6-9时探针对so2有较好的响应,可以用于生理条件下检测亚硫酸氢根。
实施例5荧光探针对不同物质的选择性
配制浓度为1mm的本发明所述检测二氧化硫的荧光探针sop的二甲基亚砜(dmso)的测试母液溶液待用。测试试液为20%的dmso和pbs缓冲液组成的2ml体系,使测试液中,探针的浓度为10μm。配制浓度为100mm的各种不同离子,氨基酸和活性氧/活性氮溶液作为备用。测试离子的浓度为2.5mm,氨基酸的浓度为5mm,活性氧活性氮浓度为100μm。摇匀后进行荧光检测(λex=365nm,λem=425nm),建立荧光强度与各离子的柱状图,如图5所示,1-19号加入的溶液分别是氯化铝,氯化钡,丙二醛,氯化钙,氯化铜,半胱氨酸,硫酸亚铁,过氧化氢,谷胱甘肽,次氯酸钠,同型半胱氨酸,氯化钾,碘化钾,硝酸钾,溴化钠,磷酸钠,氟化钠,亚硝酸钠,亚硫酸钠,亚硫酸氢钠的溶液。由图可看出只有亚硫酸钠和亚硫酸氢钠有较强响应。
实施例6荧光探针的稳定性
配制体积为2ml,探针终浓度为10μm,含20%dmso溶液的pbs溶液,体系ph为7.4,加入亚硫酸氢钠(100μm),每隔2min进行荧光检测(λex=365nm,λem=425nm)。得各体系中荧光强度,建立荧光强度与时间的标准曲线。如图6所示,探针在该条件下性质较稳定,在识别so2后在35min后性质达到稳定,荧光强度不再显著改变。
实施例7荧光探针在活细胞中的成像应用
将适当密度的hela细胞接种到灭菌的35mm成像培养皿中,在co2培养箱(温度为37℃,5%co2)中培养,待细胞贴壁后,向培养皿中加入本发明所述检测二氧化硫的荧光探针sop,使其终浓度均为5μm。继续培养0.5h,弃掉培养基,用pbs缓冲液冲洗细胞2次,加入培养基,随后进行成像实验;然后再加入亚硫酸氢钠溶液使其浓度为50μm,再进行成像实验。如图7所示,只加入探针时,细胞具有微弱的绿色荧光,加入亚硫酸氢钠后,细胞产生强烈的绿色荧光信号。
- 还没有人留言评论。精彩留言会获得点赞!