一种基于氧分子活化的高级氧化-絮凝水处理方法与流程
本发明属于环境技术领域,具体涉及一种基于氧分子活化的高级氧化-絮凝水处理方法。
背景技术:
芬顿(Fenton)法具有反应迅速、条件温和且环境友好等优点,是一种很有应用前景的废水处理技术。然而传统的Fenton法存在着H2O2使用成本高、Fe2+再生困难、污染物降解不彻底等缺点。电芬顿(E-Fenton)方法是传统Fenton方法的发展,目前已经衍生出多种电芬顿的方法。例如,依靠电化学方法产生Fe2+或者产生H2O2来构成Fenton试剂,或者依靠阴极的作用,促使Fe2+的再生速率来提高Fenton反应氧化降解有机污染物的效率。Fenton方法和E-Fenton方法,被广泛地应用于染料、农药、抗生素、垃圾渗滤液等废水的处理。
对E-Fenton体系而言,其氧化效率除了与H2O2的生成效率有关外,还与Fe2+的再生密切相关。文献报道,要实现Fe2+的有效再生,一般要求E-Fenton体系的pH值小于2.5,因为pH值大于2.5时,一方面Fe3+的沉淀会降低可溶性Fe3+的浓度,不利于Fe2+的再生;另一方面,pH值大于2.5时,Fe3+水解产生的FeOOH附着在阴极表面进而阻碍Fe2+的再生。然而这种低pH值的要求不利于E-Fenton体系在实际废水处理中的应用,在E-Fenton体系中加入配合剂,通过对Fe3+和Fe2+的配合作用,使得体系能在中性甚至弱碱性范围内避免Fe3+的沉淀,拓宽E-Fenton体系的pH值适用范围;同时,还可以通过配合亚铁离子的强还原作用,实现对氧分子的活化,产生H2O2,并进一步促进体系对有机污染物的氧化效果。目前,常用的铁离子配合剂包括乙二胺四乙酸(EDTA)、四聚磷酸盐等配合剂,但EDTA这一类有机配合剂的加入会与待降解物竞争羟基自由基,影响有机物的降解,同时自身也不稳定,不能形成持久配合。四聚磷酸盐作为一种无机配合剂,其加入也可以促进体系对于污染物的降解,但是处理之后溶液中的磷难以去除,含磷废水的排放会造成水体的富营养化。因此,对于实际的废水处理,EDTA和四聚磷酸盐等配合剂并不适合作为电芬顿体系的亚铁配合物。
技术实现要素:
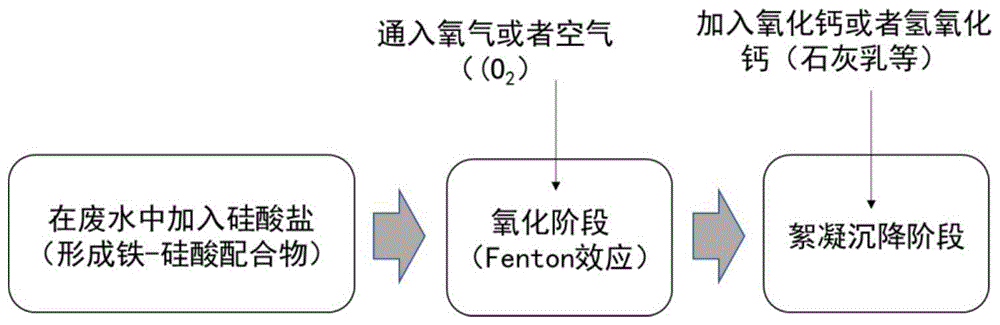
为克服现有技术方法的不足,本发明提出了一种基于氧分子活化的氧化-絮凝水处理方法。本方法在原E-Fenton体系的基础上,将常用的Na2SO4电解质换为硅酸盐溶液,硅酸盐不仅可以起到电解质的作用,同时作为配合剂,能够降低Fe3+/Fe2+的氧化还原电位,使得溶解氧发生单电子还原,最终生成大量的羟基自由基对污染物进行高效的降解矿化。硅酸盐作为一种无机配合剂,不会与待降解污染物竞争羟基自由基,同时,阴极上产生的过氧化氢也能够与亚铁-硅酸根配合离子产生电Fenton效应,增强污染物的处理效果。这一氧化过程的原理图,可以用图1表示。在废水的氧化处理完成后,如果存在其他的非氧化还原活性的水体污染物,可以通过加入氧化钙等物质生成硅酸钙和氢氧化铁沉淀,产生絮凝、共沉淀效果,不仅可以将污染物去除,还可以将其中的硅酸根去除,不会带来任何的硅酸根残留。
为实现上述目的,本发明采取如下的技术方案:
一种基于氧分子活化的高级氧化-絮凝水处理方法,包括以下步骤:
(1)向有机废水中加入硅酸盐,控制体系的pH值为5-9,然后通入氧气或空气,进行电解;其中,阴极采用钌钛、碳毡或活性炭纤维材料,阳极为铁阳极或惰性电极,所述的惰性电极采用石墨、钌钛或金刚石材料;当阳极为惰性电极时,向有机废水中加入二价铁盐;
(2)当有机废水被完全分解后,停止电解和通入氧气或空气,加入氧化钙或氢氧化钙,搅拌后静置,即成。
优选地:
所述的硅酸盐为偏硅酸钠或二硅酸钠。
所述的二价铁盐为硫酸亚铁,所述的铁阳极采用铸铁、纯铁或碳钢材料。
通入氧气或空气的速率为1mL/s~100mL/s。
步骤(1)电解过程中所施加的电流密度为1-50mA/cm2。
步骤(1)体系中硅酸盐的浓度为2-20mmol/L。
所述的有机废水为氯酚污染水或砷酸根污染水。
本发明的发明原理如下:
本发明将硅酸盐作为电解质,在阴阳极通电流,铁阳极会溶出Fe2+(或者使用惰性阳极材料,则直接外加一定量的Fe2+),Fe2+与硅酸盐形成配合物,具有更强的还原能力,氧气被还原为超氧阴离子自由基(·O2-)并被进一步还原为H2O2,加之阴极的电还原产生H2O2,两方面产生的H2O2与Fe2+形成Fenton效应,产生羟基自由基,实现对污染物的氧化去除。同时,Fe3+在阴极被还原,实现Fe2+的再生。当体系中的可被氧化的污染物被分解后,不再通入氧气,电解停止。在溶液中进一步加入氧化钙或氢氧化钙,生成硅酸钙和氢氧化铁的混合沉淀,不仅可以产生絮凝效果,去除其他的污染物,同时也去除了体系中的硅酸盐。
污染物的氧化去除过程中包括几个重要反应:包括溶解氧分子在阴极上的电化学还原过程,单电子还原过程,以及Fenton反应和Fe2+的再生过程。如下所示,其中硅酸盐用SIL(silicate)表示:
O2+2e-+2H2O→2H2O2(氧分子的阴极电化学还原产生过氧化氢)
[SIL-Fe2+]+O2→[SIL-Fe3+]+·O2-(氧分子活化第一步)
[SIL-Fe2+]+·O2-+2H2O→[SIL-Fe3+]+H2O2+2OH-(氧分子活化第二步)
[SIL-Fe2+]+H2O2→[SIL-Fe3+]+·OH+OH-(Fenton效应)
[SIL-Fe3+]+e-→[SIL-Fe2+](亚铁配合物的再生)
金属离子为外部加入时,阳极材料包括石墨、钌钛、金刚石(BDD);金属离子为阳极溶出时,阳极材料包括铸铁、纯铁和碳钢等。以上两种情况下,阴极材料主要包括钌钛、碳毡。可以采用碳毡作为体系的阴极,碳毡作为阴极时,可以提高阴极电生H2O2的量,从而提高体系对污染物的去除能力。
体系的pH值为5-9,低于该pH范围,亚铁离子主要以非配合形式存在,还原能力较弱,无法形成稳定的配合;高于该pH范围,亚铁离子与氢氧根形成配合,也不会还原氧气分子,生成过氧化氢。
本发明具有以下优点和有益效果:
(1)本发明利用常见的硅酸盐作为电解质,硅酸盐与亚铁离子形成氧化还原电位更低的配合物,使得O2更容易发生单电子还原,生成超氧阴离子自由基(·O2-),超氧阴离子自由基进一步被还原为H2O2,增强了有机废水的氧化效果;氧化反应结束后,硅酸盐与钙离子形成硅酸钙沉淀,易于除去,硅酸盐相比其他含碳有机配合剂或者聚磷酸系列配合物,不会带来二次污染,更加环保和具有实用价值。
(2)本发明在氧化阶段完成后加入的氢氧化钙或氧化钙原料成本低,操作简便,不仅能与硅酸盐形成沉淀,同时能与亚铁离子形成絮凝物,从而除去其他污染物。
(3)本发明在接近中性的体系中进行电解,更符合污水处理的实际情况,更具适用性。
附图说明
图1为基于分子氧活化的高级氧化-絮凝水处理方法示意图;
图2为铁阳极模式氧化阶段的原理示意图;
图3为本发明阳极采用铁阳极时的装置示意图;
图4为实施例1以偏硅酸钠作为配合剂和采用Na2SO4作电解质时污染物去除率随时间的变化对比图;
图5为实施例2以二硅酸钠作为配合剂时氯酚以及TOC的去除率随时间的变化图;
图6为实施例3以二硅酸钠作为配合剂时污染物在不同pH条件下的去除效果图。
具体实施方式
以下通过具体实施例来进一步阐述本发明的技术方案,但本发明的保护范围并不局限于以下实施例。
实施例1
如图3所示的实验装置,采用铸铁阳极和钌钛阴极作为电极,反应器内装175mL氯酚污染水,其中氯酚的初始浓度为20mg/L,外部循环水的温度设置为25℃,使用偏硅酸钠作为配合剂,偏硅酸钠的浓度为5mmol/L,体系初始pH值为7.5,电流为10mA,通入氧气。在特定的时间点测定体系中氯酚的浓度,结果如图4所示。可以看出,相比于Na2SO4作电解质,使用偏硅酸钠(图4中用SS表示)做电解质时,经过三个小时的反应,体系中氯酚的浓度不断地下降,最后的去除率达到了45%以上,作为对比,Na2SO4体系中氯酚的降解只有10%。
实施例2
如图1所示的实验装置,采用铸铁阳极和钌钛阴极,反应器内装175mL氯酚污染水,其中氯酚的浓度为20mg/L,外部循环水的温度为25℃,使用二硅酸钠作为配合剂,二硅酸钠的浓度为5mmol/L,体系初始pH值为7.5,电流为20mA,通入氧气。在特定的时间点测定体系中氯酚的浓度以及TOC的值。结果如图5所示,可以看出,使用二硅酸钠作为电解质时,经过三小时的反应,氯酚被降解了95%以上,TOC也下降了40%,这说明该方法对于氯酚的降解和矿化十分有效。
实施例3
如图1所示的实验装置,采用铸铁阳极和钌钛阴极,反应器内装175mL氯酚污染水,其中氯酚的浓度为20mg/L,外部循环水的温度为25℃,使用二硅酸钠作为配合剂,二硅酸钠的浓度为5mmol/L,体系初始pH值分别为5、7、7.5、8,电流为10mA,通入氧气。在特定的时间点测定体系中氯酚的浓度。结果如图6所示,可以看出,使用二硅酸钠作为电解质时,在中性甚至偏碱性的pH范围内,体系对氯酚的降解效果依然比较良好。
实施例4
如图1所示的实验装置,采用金刚石薄膜阳极(BDD阳极)和碳毡阴极,反应器内装175mL氯酚污染水,其中氯酚的浓度为20mg/L,外部循环水的温度为25℃,使用二硅酸钠作为配合剂,二硅酸钠的浓度为5mmol/L,体系初始pH值分别为7.5,电流为10mA,通入氧气,反应开始前向体系中加入硫酸亚铁,硫酸亚铁的浓度为1mmol/L。在特定的时间点测定体系中氯酚的浓度。结果显示,氯酚在1小时内被降解完全。
实施例5
如图1所示的实验装置,采用金刚石薄膜阳极和钌钛阴极,反应器内装175mL氯酚污染水,其中氯酚的浓度为20mg/L,外部循环水的温度为25℃,使用二硅酸钠作为配合剂,二硅酸钠的浓度为5mmol/L,体系初始pH值分别为7.5,电流为10mA,通入氧气,反应开始前向体系中加入硫酸亚铁,硫酸亚铁的浓度为1mmol/L。反应1小时后,对反应液进行固相微萃取,并通过气相色谱-质谱联用测定反应体系中的降解产物,可以发现反应液中已经不含有氯酚,有机物均为苯环开环之后的小分子有机物。该结果表明,本方法对氯酚具有较为彻底的降解能力,通过延长反应时间,可以达到污染物的彻底矿化。
实施例6
如图3所示的实验装置,采用金刚石薄膜阳极和钌钛阴极,反应器内装175mL氯酚和砷酸根的溶液,其中氯酚的浓度为20mg/L,砷酸根的浓度为10mg/L,外部循环水的温度为25℃,使用二硅酸钠作为配合剂,二硅酸钠的浓度为5mmol/L,体系初始pH值分别为7.5,电流为10mA,通入氧气,反应开始前向体系中加入硫酸亚铁,硫酸亚铁的浓度为1mmol/L。反应2小时后,向反应液中加入氧化钙,氧化钙的加入量为2g,经过搅拌静置,取上清液,测量其中的氯酚、砷酸根及硅酸盐的浓度。结果表明,上清液中氯酚的已经无法检测到,砷酸根的浓度为0.05mmol/L;硅酸盐的浓度为0.3mmol/L。这一结果说明,通过氧化和絮凝沉降两个步骤,污染物氯酚和砷酸根得到了有效去除,同时硅酸钙沉淀法也去除水中多余的硅酸盐。
- 还没有人留言评论。精彩留言会获得点赞!