用于微生物菌落取样的端部配件和装置及使用它们的取样方法与流程
目前,使用可被消毒的工具或一次性使用的工具如接种环(oese)(也称为接种圈)、棍、管或锥形管对培养皿中的琼脂培养基或其他任何培养基上培养的微生物(细菌、霉菌、酵母等)的菌落取样。
然而,这些工具不能可靠和有效地对所有类型的微生物取样,因为后者可以具有非常不同的形状、大小、粘稠度、结构或外观。
此外,这些消耗品不容易使在分析介质(例如用于maldi-tof型质谱分析的板)上的取样的生物物质得到最佳涂布(deposit)。此外,能够对细菌菌落或该样品的部分进行取样而不对菌落下的培养基取样也是非常重要的。这实际上可扭曲后续分析的结果。
分析结果的质量也可能取决于由所取样品形成的生物物质涂布物的浓度,以及它在其所涂布的介质上的均匀性。maldi-tof微生物分析的情况尤其如此,其中样品必须形成薄而均匀的层才能够进行最佳分析。
一次性使用或可用火焰消毒的接种环通常用于在培养皿上取样微生物的菌落,并将生物物质涂布在maldi-tof板上。该种操作行之不易,需要一些灵活性。用拇指和食指夹持这种工具会导致肌肉骨骼问题。接种环通常握在远离其端部的位置,这样操作人员的手就不会污染样品。但是手在这个位置使得接种环端部移动的精确性更加困难,特别是当需要在几mm2数量级小面积上产生薄而均匀的涂布物时。所以,已设计用于取样已校准给定数量的微生物(一般在1μl至10μl之间)的接种环,在其端部包括直径通常大于1mm的金属或塑料环。该尖端可比将形成的涂布物的表面大。此外,(金属或塑料的)接种环的刚性性质并不特别适合用于在硬表面上将微生物菌落铺成薄而均匀的层。
也可利用其他的消耗品如拭子、木棍,微量移液管端部配件。
因此,文件us9,181,522描述了一种用于无菌转移生物物质的方法和装置。该装置由双层壁腔室组成,所述双层壁腔室用于容纳单一尺寸的端部配件,所述端部配件在首端具有球,用于以无菌方式将生物物质从一个地方转移到另一个地方。这种装置的第一个缺点是设计相对复杂,其具有一个用于端部配件的紫外线消毒的集成系统,其双层壁结构及其用于端部配件的内部加载和弹出的系统。这种复杂性无疑影响单位成本,从而影响销售价格。此外,用于使球存在于一次性端部配件首端的材料是由金属或聚丙烯类的硬质材料制成,这不利于取样过程,但最重要的是其不利于生物物质(如细菌菌落)的涂布,特别是在maldi-tof型质谱分析板上。
文件fr2668495描述了一种用于细菌学用途的无菌取样锥形管
申请人之前已经通过提出一种方法来解决上述全部或部分缺点,所述方法用于对与琼脂培养基接触生长的生物物质样品的全部或部分取样(其使用装备有末端的探针)。所述取样方法基本上是基于冷却探针末端,通过使末端与生物物质样品接触或通过由末端所发挥的施加在生物物质样品上的压力,使得粘住全部或部分待取样的生物物质样品,然后通过加热探针末端释放全部或部分生物物质样品。该方法描述于专利申请wo2012/004545。
这一方法的主要缺点是它需要相对庞大的设备来冷却探针,这消耗了能量,意味着高的经济成本。
对现有技术的分析的结果表明,目前不存在用于对生物物质取样的易于使用的系统,该系统设计简单且采用具有不但适合于取样而且适合于涂布生物物质如细菌菌落的物理特性的一次性取样端部配件。
因此,本发明的目的是通过提供一种设计简单、易于生产的端部配件来应对这些缺点,使得当放置在用于生物物质取样装置上时精确取样和涂布该生物物质,尤其是在maldi-tof型质谱分析板上。
这些目的尤其通过本发明实现,本发明首先涉及一种能够适于安装在用于微生物来源的生物物质的手动或自动取样装置的主体上的端部配件,包含:
a)远端,其包含用于对微生物来源的生物物质取样的工具(moyen),
b)近端自由端,用于与所述取样装置的主体接触,并使所述端部配件能够连接到所述主体上,
所述端部配件的特征在于全部或部分自由远端由具有至少等于30%孔隙率的纤维材料组成。
微生物来源的生物物质基本上是指由细菌、酵母或霉菌组成的生物物质。
在一个有利的实施方案中,根据本发明的端部配件完全由具有至少等于30%孔隙率的纤维材料组成。
纤维材料优选具有大于50%的孔隙率,优选大于70%。
有利地,纤维材料选自以下:聚乙烯、聚酯、聚对苯二甲酸乙二醇酯(pet)、pet/聚乙烯共聚物、pet/pet共聚物、聚酰胺、棉。
取样端部配件具有大体上圆锥形或截锥形的整体形状。对此部分,有利地,取样工具是圆柱形、截锥形或球形的整体形状。
本发明的另一个目的涉及一种取样微生物来源的生物物质的装置,包括:
根据本发明的端部配件
包括至少以下的主体:
近端部分,其至少部分地作为用于夹持所述装置的区域,和
远端部分,其具有与所述端部配件连接的自由端。
该装置还包括用于弹出端部配件的系统。有利地,所述弹出系统包括位于所述主体内部并且可平移(entranslation)移动的杆,以便按压端部配件从而将其弹出。
在一个具体实施方案中,所述杆通过按钮平移移动。
本发明的另一个目的涉及一种取样微生物来源的生物物质的方法,包括以下步骤:
a)将根据本发明的端部配件放置在取样装置的远端部分
b)将取样装置放置在培养基上存在的微生物来源的生物物质的菌落附近,以使所述端部配件的取样工具与生物物质接触,
c)借助于取样装置对全部或部分生物物质取样,使取样的生物物质附着在取样工具上。
本发明的另一个目的涉及从生物物质样品制备用于maldi-tof型质谱微生物分析的分析板的方法,包括以下步骤:
a)将端部配件放置在根据本发明的取样装置的远端部分上,
b)将取样装置放置在培养基上存在的微生物来源的生物物质的菌落附近,以使所述端部配件的取样工具与生物物质接触,
c)借助于取样装置对全部或部分生物物质取样,使取样的生物物质附着在取样工具上,
d)通过使取样工具与maldi-tof型质谱分析板的至少一个分析区域的表面接触,将所取样的生物物质均匀地涂布在所述至少一个分析区域上。
微生物分析是基本上指能够鉴定微生物(例如细菌或酵母)的任何分析,而且能够显示任何抗微生物抗性标志物、分型的任何特征、或显示所述微生物的毒力因子的表达。
本发明的另一个目的涉及在琼脂培养基上分离微生物来源的生物物质的方法,包括以下步骤:
a)获得与根据本发明的取样装置的端部配件的取样工具接触的生物物质的样品,
b)将取样装置放置在琼脂培养基表面附近,使得取样工具与所述表面接触,
c)移动取样装置,使取样工具在培养基表面上移动,同时保持与之接触,从而将与所述取样工具接触的全部或部分生物物质的样品释放到所述培养基的表面上。
在一个具体实施方案中,上文描述的所有方法进一步包括弹出取样端部配件的最后步骤。
生物物质的样品可以通过上述取样方法从生物物质的菌落中获得。
另选地,生物物质的样品可以从生物物质的悬浮液中获得。传统意义上,这种悬浮液是通过将一个或多个生物物质菌落置于盐水溶液中的悬浮液而获得的。根据这一另选方案,由于构成所述取样工具的纤维材料的吸附能力,取样端部配件浸入悬浮液的一部分中,以便使取样工具能够吸附液体。之后,生物物质与所述取样工具接触。细菌悬浮液的浓度由本领域技术人员根据有关微生物的生长特征来确定。这形成他们的普通背景知识的一部分。同样地,也特意确定了用于给端部配件装填生物物质的悬浮部分。有利地,从几微升到几十微升。
根据以下本发明的详细和非限制性描述并参照给出的附图,将更好地理解本发明的目标和优点,其中:
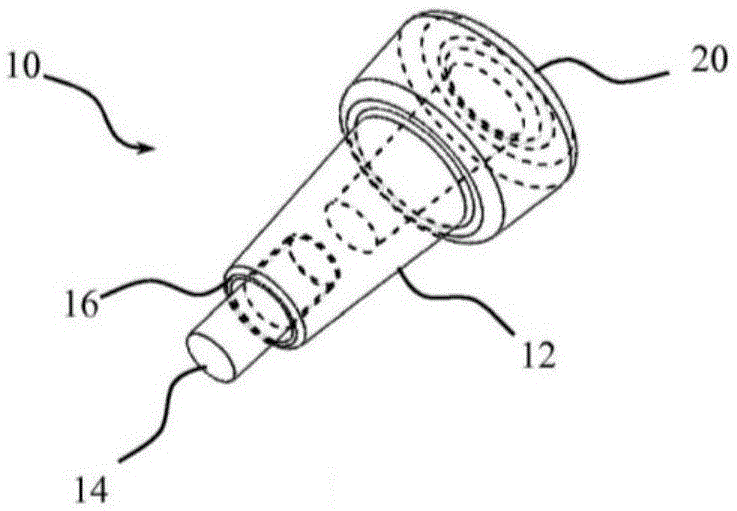
图1a表示根据本发明第一实施方案的取样端部配件的透视图。
图1b表示图1a所示的端部配件的侧视图。
图1c表示根据第二实施方案的取样端部配件的透视图。
图2a表示根据第一实施方案的生物物质取样装置的侧视图。
图2b表示图2a所示的生物物质取样装置的分解侧视图。
图2c表示图2a所示的生物物质取样装置的主体的透视图。
图2d表示图2a所示的生物物质取样装置的侧视图,其配置用于弹出取样端部配件。
图3a表示根据第二实施方案的生物物质取样装置的侧视图。
图3b表示图3a所示的生物物质取样装置的分解侧视图。
图3c表示用于将推环固定到图3a所示的取样装置的杆上的系统的更大比例的分解透视图。
图4a表示根据第三实施方案的生物物质取样装置的侧视图。
图4b表示图4a所示的生物物质取样装置的分解侧视图。
图4c表示用于弹出图4a所示的取样装置的端部配件的机构的更大比例的视图。
图5a表示根据第四实施方案的生物物质取样装置的透视图。
图5b表示图5a所示的生物物质取样装置的分解透视图。
图5c表示图5a所示的生物物质取样装置的透视图,其配置用于弹出取样端部配件。
在图1a中,用透视图表示根据第一实施方案的端部配件10。图1b表示的是它的侧视图。根据该实施方案,端部配件10是截锥形的整体形状。然而,根据本发明的端部配件10变为一个不同的形状是完全可行的。它由三个独立的部分构成。首先,基本为截锥形的远端部分12。该远端部分12构成接纳取样工具14的部分。为此,远端部分12具有形成盲腔18的自由端16,取样工具14位于盲腔18中。为此,腔18和取样工具14的形状必须是互补的。理想情况下,取样工具14的尺寸必须略小于腔18的尺寸,以使其能够插入。然而,它们优选相对靠近以防止取样工具从腔中脱落。端部配件10还包括近端部分20,近端部分20也是截锥形,但较远端部分12更短更宽。近端部分20的端部22是自由端并包括盲腔24,取样装置的远端容纳于盲腔24中。
端部配件10可以由通常用于模制移液管端部配件的材料模制。该材料可以是例如聚烯烃类型的聚合物。这种类型的材料一般不贵,可以消毒,并且适合用于生产一次性产品。
对于取样工具14,构成取样工具14的材料是非常重要的。事实上,取样工具具有双重技术约束,即必须提供生物物质(例如细菌菌落)取样,同时当所述生物物质涂布在分析装置(如质谱分析板)上时释放所述生物物质。因此,本发明人发现,用于制备取样工具14的材料的孔隙率是使得在取样和释放生物物质的性能之间实现良好折衷的基本特征。
此外,除了取样工具的固有特征,重要的是记住当要取样的生物物质是细菌菌落时,细菌菌落在采样过程中或涂布过程中的表现可能因细菌空间而变化。事实上熟知的是,细菌菌落依据相关的细菌空间或多或少是粘稠的,或多或少是粘滞的,或多或少是线状的。因此,无论细菌菌落的性质如何,具有能够操纵任何类型的细菌菌落的取样工具是重要的。
因此,本发明人确定至少等于30%的孔隙率是获得所需性能所必需的。理想情况下,至少等于70%的孔隙率能够获得最佳结果。
材料的孔隙率是指固体材料中可填充流体(液体或气体)的所有空隙(孔)。我们同样通过定义为空隙体积与相关多孔介质总体积之间比率的物理参数表达孔隙率。
材料的孔隙率以如下方式测量:
采集干燥纤维材料的样品。
样品第一次称重。
将样品浸入水中足够长的时间,使其完全浸透。
再称重浸透样品。
通过计算浸透材料的质量与干燥材料的质量之间的差,推导出材料中截留的水的质量。
每单位体积水的质量接近1,推导出截留的水的体积以及由此推导出材料中空隙的体积。
然后测量浸透样品的体积。
将上述获得的材料样品中的空隙值除以浸透样品的测量体积,从而可以获得材料的孔隙率的值。
特别适合于生产取样工具的材料可以是纤维材料。在这些材料中,可提及合成材料,如聚乙烯、聚酯、聚酰胺。在聚酯中,可提及聚对苯二甲酸乙二醇酯(pet)。它们也可以是共聚物,例如聚乙烯/聚酯聚合物,例如聚乙烯/pet共聚物或是pet/pet共聚物。当它是纤维材料时,纤维可由单组分或双组分材料组成。双组分纤维可以由例如pet芯和聚乙烯鞘组成。
也可以同样使用天然纤维材料。在这种情况下尤其是棉纤维。
在图1c中表示第二实施方案的端部配件。该端部配件11由三部分组成:基本上是圆柱形或可能是截锥形的近端部分13。相比于第一实施方案,近端部分13的自由端15没有盲腔并且被堵塞。事实上,根据这个实施方案,取样装置的远端不会插入端部配件11。与此形成对比的是,端部配件11被插入取样装置的远端,并且更精确地说是其近端15。当然,要做到这一点,取样装置必须具有能够接收端部配件11的自由远端。因此,它必须包括腔以接收端部配件11,所述腔的尺寸必须略大于近端部分13的尺寸。端部配件11包括能够在使用后弹出所述端部配件的凸缘17。当端部配件11插入取样工具时,它也可以作为支座。最后,端部配件11包括用于接收取样工具14的远端部分19,如根据第一实施方案的端部配件10的情况。为此,远端部分19具有自由端21,其中形成盲腔23,取样工具14位于盲腔23中。
根据取样端部配件11的变形实施方案,近端13可包括能够在远端和近端之间形成通孔(trou)的孔口(orifice)。这样就可以使用更长的取样工具,其定位在通孔中,并固定在近端或两端孔口水平处的端部配件上。这种变形设计更简单,因此制造成本更低。
图1a至1c所示的取样工具14为圆柱形。尽管如此,取样工具14可以是不同的形状。因此,后者的自由端可能是例如圆锥形以进一步提高取样和涂布生物物质的准确性。端部配件14的自由端也可以具有适合于取样生物物质的任何其他形状。
根据本发明的一种变体,取样端部配件可以设想为完全由多孔材料组成。根据该变体实施方案,取样端部配件也将构成取样工具。
根据本发明的另一种变体,取样工具、取样端部配件和取样装置可以是相同的。事实上,可以设想一种一次性使用的取样装置,其中多孔取样端部配件固定在所述取样装置。或者,取样装置可以完全由多孔材料制成。为此,取样工具的尺寸必须允许易于抓取和操纵。
取样端部配件与取样工具连接或仅与取样工具连接,如果它与取样端部配件是一体的,其可适于在自动化系统中用于取样生物物质。例如,这种系统可以自动取样培养皿上的细菌菌落并制备质谱分析板。
图2a表示根据第一实施方案的取样装置30。取样装置30包括远端部分32、中间部分34和近端部分36。基本上为截锥形的远端部分32的功能是携带根据本发明的取样端部配件10。同样为圆柱形的中间部分34的功能是允许使用者夹持取样装置30。最后,近端部分36具有桶状整体形状,其内径略大于中间部分34的外径,以便近端部分能够部分地覆盖中间部分的近端。
图2b用分解图表示取样装置30,其中该装置的每个组件均分别表示。由此可见,远端部分32和中间部分34实际上是一个构成取样装置主体的相同组件38。
如图2c所示,这个基本上是圆柱形的主体38具有穿过它的纵向周边开口382连同中心开口384。开口382的布置使得每个开口接收杆40的叶片401,如图2b所示。对于开口384,它适于接收螺旋弹簧42,如图2b所示。因此,杆40主要由三个叶片401构成,其底座固定在环形支座402上。杆40位于装置的主体38内,将叶片401的自由端引入开口382,直到环形支座402支撑中间部分34的远端部分,而远端部分32穿过所述环形支座402的开口。在主体38的另一端,螺旋弹簧42的下端被安置在开口384中,而它的上端被放置在与取样装置的近端部分36的内表面接触的位置,其用来盖住主体38。当使用取样端部配件10时,该近端部分充当弹出取样端部配件10的推杆构件。
叶片401比中间部分34长,因此当杆40位于主体38内时,叶片401的自由顶端从开口382露出。当弹簧就位时,这些自由端固定到推杆构件36。这种固定可以是机械的。因此,可以设想在叶片401的自由端附近放置径向突出的凸耳,这些凸耳安装在推杆构件36内壁形成的开口中。或者,可以通过化学键将叶片401的自由端固定到推杆构件36的内表面。
如图2d所示,当沿取样装置的纵轴对推杆构件36施加压力时,推杆构件36在主体38上滑动。该滑动动作传达给杆40,杆40固定到推杆构件36并在主体38内滑动。这种滑动通过推环构件402的平行移动在取样装置的远端显示。由于后者支撑着端部配件10的近端,所以它驱动所述端部配件平行移动,使得其与取样装置30的远端32分离。推杆构件36施加在螺旋弹簧42上的压力导致其压缩。如上文所述的滑动,这种压缩传递到杆40。当近端部分36上的压力释放时,弹簧42趋向于返回到其不再压在杆40上的静止位置。然后,后者通过反向平行移动恢复其初始位置,释放远端部分32,远端部分32随后可用于接收另一取样端部配件。
因此,使用具有取样端部配件10的取样装置30的方法的各个步骤可以总结如下:
端部配件10位于取样装置的自由端32上。这一步骤通常通过将装置放置在与无菌端部配件对齐的垂直位置上来执行,所述端部配件通常放置在适当的支架上。取样装置的远端部分32的端部随后插入到端部配件10的近端部分20的腔24中,直到其紧靠在腔24底部。
为了在琼脂培养基上取样生物物质如微生物菌落,取样装置被定位在使得端部配件的取样工具与微生物菌落接触的位置。然后对菌落的全部或部分取样。
为了将全部或部分取样的生物物质涂布在表面例如maldi-tof质谱分析板的表面上,将取样装置朝所述表面移动,以便携带生物物质的取样工具的末端与表面接触。然后利用取样装置进行小的圆周运动以在所述表面上涂布一层生物物质。
一旦涂布已经完成,将取样端部配件通过驱动弹出工具弹出并扔进垃圾桶。就图3至5表示的取样装置来说,通过向近端部分36施加压力来实现弹出。
图3a到3c表示第二实施方案的取样装置,该取样装置50由基本圆柱形的空心主体52组成。该主体52在其远端部分具有基本上为截锥形的自由端521,用于携带取样端部配件10。该自由端521通过限定三个间隙空间的三个翼片(未示出)固定到主体52。主体52还包括连接系统或夹子522,使得取样装置能够例如像钢笔一样连接到衣服的口袋上。最后,在图3a中还可以看到一个从主体52的近端退出的按钮54。如图3b所示,按钮54固定在在主体52内的杆56上。在大比例视图3c中特写表示,这个基本上是圆柱形的杆56结束于三个连接凸耳561的末端。所述连接凸耳561之间的中心空间用于接收螺旋弹簧58,如图3b所示。
杆56通过主体52的近端插入主体52,首先插入螺旋弹簧58。所述螺旋弹簧58被放置用来支撑翼片和远端521的上部。一旦插入,杆56放置使其横跨在弹簧上,使得连接凸耳561穿过翼片片之间限定的间隙,并且围绕自由端521出现在主体52的基部。环60安装在自由端521周围。该环60具有三个开口601,用于接收连接凸耳561的端部。连接凸耳在其端部具有径向凸片5611,一旦凸耳被放置在环60内部,径向凸片5611将锁定在开口601中,从而将环60和杆56固定在一起。或者,为了简化机械装置的目的,完全可以用包括没有卡在环上的凸片的凸耳的系统来代替此机械固定系统。如图3a所示,由于螺旋弹簧58的作用,螺旋弹簧58对杆56施加朝向主体52的上部的排斥力,环60在自由端521的上部水平面支撑主体52。
对于第一实施方案中的取样装置30,当沿取样装置的纵轴的压力施加在按钮54上时,该压力传递到固定在按钮54上的杆56。后者随后滑入主体52内部,从而压缩螺旋弹簧58。这种滑动通过环60的平行移动在取样装置的远端表现出来,使得后者支撑在端部配件10的近端,并驱动后者平移移动直到其与取样装置50的远端521分离。当杆56施加在螺旋弹簧58上的压力被释放时,因为释放了按钮54上的压力,所以后者的弹簧恢复其静止位置。杆56被弹簧的压力沿反向平移移动方向驱动,直到环60支撑主体52,使远端部分521再次可接近以接收另一取样端部配件10。
图4a至4c表示第三实施方案中的取样装置。该取样装置70由基本上圆柱形的中空主体72组成。该主体72在其远端部分具有基本上为截锥形的用于携带取样端部配件10的自由端721。该自由端721通过限定三个间隙空间的三个翼片(未示出)固定到主体72。还可以看到一个位于主体72侧面的按钮74,其插入在主体72侧壁形成的开口722中,如图4b所示。它还包括插入到主体72的上端的杆76。该杆76由基本矩形截面的一体式近端部分761和由三个连接凸耳762组成的远端部分组成。在与远端部分的交界处,近端部分761在这两个相对的面上具有斜肩7611,用来与按钮74配合。杆76通过取样装置70的近端插入取样装置70的主体72中。一旦插入了杆76,连接凸耳762穿过固定自由端721的翼片之间所限定的间隙,并在所述自由端721周围的主体72的底部退出。在自由端721周围插入环78。该环78与上述环60相似,并包括用于接收连接凸耳762的端部的三个开口,还设有径向凸片762并用于与环78中的开口配合将杆76固定到环78,如图4c所示。
按钮74具有倒u形截面,旨在使其能够位于围绕和横跨在杆76的近侧部分761,特别是在倾肩7611的水平面。按钮74在两侧面的每一侧都有三个凸耳741,防止其一旦放置在壳体722中时脱落。当杆76和按钮74位于取样装置70的主体72中时,按钮74在其远端部分的水平面支撑斜肩7611,防止杆76脱落。按钮和斜肩7611之间的相互作用使得杆76能够在静止位置和用于弹出取样端部配件10的位置之间移动。事实上,当端部配件10位于取样装置70的远端721上时,后者支撑环78。然后,后者被放置在靠着主体72的高位置,如图4a所示。随后杆处于静止位置,按钮74再次处于高位置。
当取样装置70的使用者希望弹出取样端部配件10时,他们对按钮74施加压力。这种压力导致按钮在壳体722中被压下,然后按钮在斜肩7611上滑动。按钮不能横向移动,它在斜肩7611上的滑动导致杆76水平平移地朝向主体72的远端移动。杆随后从其静止位置移动到它用于弹出端部配件的位置,其中弹出环78在向端部配件施加压力之后再次处于低位置,从而导致后者弹出,如图4c所示。
图5a到5c中表示第四实施方案。该实施方案在涉及取样装置的操作方面与第三实施方案非常类似。实际上,图5a至5c所示的取样装置80由基本上圆柱形的中空主体82组成。主体82是一体的,并在其远端部分具有基本上截锥形的自由端821。该端821被圆形孔口822刺入。该孔口用于接收取样端部配件11的近端部分13,如参考图1c所述。在这种构型中,将取样端部配件11压入取样装置80的主体中,直到端部配件11的凸缘17支撑主体82的端部821。主体82还包括横向放置于主体82上的按钮84,所述主体插入在主体82侧壁中形成的壳体823中。最后它包括上端插入主体82中的杆86。杆86由一个基本矩形截面的一体近端部分861,一个基本圆形截面的一体远端部分862(以螺纹接头863结束)组成。在近端部分861和远端部分862之间的界面处,在近端部分861的相对侧上各形成两个斜肩8611。这些肩8611和按钮84通过与上文所述相同的机制与如图4a至4c所示的取样装置70进行协作,以便当用户按下按钮84时,它们触发杆86在主体82的开口处向后者的远端平移移动。螺纹接头863随后支撑端部配件11的近端部分13的自由端15,并对后者施加压力,使得端部配件11通过平移移动从取样装置80中弹出。这在图5c中清楚地表示出。当在取样装置80上放置新的配件11时,通过孔口822刺入主体82中的开口的近端部分13向相反方向推动杆86,由于与按钮84配合的斜肩8611,导致按钮84通过垂直平移移动而上升。
可以设想其他取样装置的实施方案。因此,一个可能的其他实施方案包括位于主体的远端但是在主体的外部部分的机械系统,所述机械系统用来支撑端部配件从而允许其弹出。例如,取样装置的主体上有可移动的套筒,可与取样端部配件接触,当使用者移动时,使取样端部配件弹出。
可以设想用于制备生物物质样品以便使用取样装置进行分析的其它方案。因此,一旦生物物质被取样,就可以在特定溶液(如盐水溶液)中制备生物物质的悬浮液。为此,可以设想将携带生物物质的取样端部配件直接释放到含有一定量的溶液的悬浮液的管中。将含有端部配件的管涡流搅拌,随后将能够释放保留在纤维材料上的生物物质。
取样装置还可用于在琼脂培养基上进行分离。这种分离可以直接从用根据本发明的取样装置取样的菌落中进行,然后直接在琼脂培养基上重新接种。它同样可以在取样装置的帮助下由生物物质的悬浮液产生,如上文所述。
当使用取样装置进行分离时,取样工具优选具有球形的端部,并且在其端部具有足够的直径,以防止将其压向琼脂培养基而破坏琼脂培养基。例如合适的直径介于2到7毫米(mm)之间,有利地,介于2到4毫米之间。
可从细菌悬浮液进行分离,悬浮液的浓度为,例如107cfu(菌落形成单位)/ml(毫升)。在这种浓度下,使用取样工具的5微升(μl)悬浮液样品足以在琼脂培养基上能够进行良好质量的分离。5μl悬浮液由构成取样工具的材料吸入。所述装有悬浮液的取样工具随后能够在将该悬浮液应用于琼脂培养基时使该悬浮液逐渐释放。由于构成取样工具的材料具有吸收性,这种逐渐释放是允许的。这样做的结果是提高了分离质量。
所述分离可以按照传统技术进行,例如所谓的“dial”技术或者所谓的“spiral”技术
实施例:
实施例1:具有取样端部配件的取样装置在制备maldi-tof分析板中的用途
在本实施例中使用的取样设备表示在图2a至2d中,如上文所述。
取样端部配件由塑料材料制成,例如那些通常用于生产一次性移液管端部配件的塑料材料。它包括直径2mm、长度6mm的圆柱形取样工具。它由聚对苯二甲酸乙二醇酯(pet)/pet共聚物纤维组成,这种材料由porex公司以参考号psu-832销售。
取样装置的主体由聚丙烯注塑成型。它的长度有120毫米,并具有一个六边形的截面,六边形的相对面之间有8.2毫米,这使得握起来像铅笔一样容易,而没有肌肉骨骼问题的风险
取样装置用于对在columbia琼脂+5%绵羊血(cos细胞系)培养基(由申请人以参考号43041销售)上生长的不同物种的细菌的菌落取样。
取样的菌落被涂布在具有48个位置的一次性maldi-tof分析板(由申请人以参考号410893销售)上。
在选择的物种中,已知有一些形成难以取样的菌落。例如地衣芽孢杆菌(bacilluslichenformis)、肺炎克雷伯氏菌(klebsiellapneumoniae)、奇异变形菌(proteusmirabilis)或星状诺卡氏菌(nocardiaasteroides)。
该方法按照以下步骤进行:
1.将取样端部配件放置在取样装置上。
2.在cos细胞系型培养基上,借助于取样装置,通过使由取样端部配件携带的纤维材料制成的取样工具与菌落接触,来对细菌菌落取样。
3.通过使携带细菌样品的取样工具与maldi-tof板接触,施加压力并涂抹样品,将细菌样品涂布在maldi-tof分析板为此目的所提供的48个位置之一上。施加在取样工具的纤维材料上的压力使得剩余的样品能够保留在所述纤维材料上。当想要重复分析时,可以在分析板上的不同位置进行连续涂布。这些其他涂布可以使用相同的端部配件完成。
4.当所有涂布完成后,通过向按钮施加压力,将取样端部配件弹出到垃圾桶中,如上文所述。
5.通过使用微量移液管,在生物物质的每个涂布上涂布1μl的基质(现成的α-氰基-4-羟基肉桂酸,biomerieux,参考号411071)。
6.对希望分析的每个菌落重复步骤1至5
7.根据步骤1-5,还涂布了用于校准和作为阳性对照的大肠杆菌(e.coli)atcc8739菌株。
8.分析板被储存必要的时间使其基质干燥。
9.当板完全干燥时,将其引入到申请人销售的maldi-tof
10.利用专家系统和
使用采用接种环的maldi-tof分析板制备的传统方法分析细菌的相同菌落,并且是本领域技术人员熟知的。
两种分析板制备方法所得结果列于表1,并比较。
符号"√"表示光谱具有良好的质量,并能够进行预期的物种鉴定。
符号“x”表示光谱的质量不足以鉴定物种。
表1
从表1的分析,使用采用根据本发明的取样工具的方案,所有分析的物种都通过使用
通过比较,按照传统使用接种环的方案对细菌的菌落进行采样,13个被分析的物种中只有6个被正确鉴定。在尚未鉴定的物种中,大多数是已知形成难以操纵的菌落的物种。
因此,以特别有利的方式,本发明的方法能够取样和涂布形成具有非典型粘稠度菌落的细菌物种。因此,通过maldi-tof质谱法可以容易地获得对粉状和成壳(incrustantes)物种如地衣芽孢杆菌或皮疽诺卡氏菌,粘附物种如肺炎克雷伯氏菌,以及在琼脂上扩散的物种如奇异变形菌的优异鉴定结果。
也发现用根据本发明的取样装置涂布48个样品所需的时间(12分钟)比用接种环的时间(16分钟)短。
因此,本发明的方法比现有技术的参考方法更符合人体工程学,更易于使用,更快,并且能够获得更好的结果。
实施例2:使用不同纤维材料通过质谱分析鉴定不同细菌物种的性能比较
在该实施例中,特别是测试了具有不同孔隙率的多个纤维材料它们能够有效地取样来自不同细菌物种的菌落的生物物质的能力,以及同等地,它们在maldi-tof分析板上产生均匀涂布的能力。事实上,不论材料的数量或涂布的均匀性如何,通过maldi-tof质谱鉴定细菌物种的性能直接与分析板上生物物质涂布的质量相关。
因此,对各种物种进行maldi-tof质谱分析以鉴定它们
分析方案是实施例1中描述的方案,包括其取样装置。
所测试的材料列于下表2:
表2
表2中显示了所用材料样品的尺寸。此外,还指出了通过上述方法计算孔隙率的值。
材料psu892是从双组分纤维获得的材料,由聚对苯二甲酸乙二醇酯外壳和聚酯芯组成。这种材料由
xa-20521-ps材料是基于聚乙烯的材料。这种材料由
为了进行测试,使用了三种不同物种的细菌:
·表皮葡萄球菌(atcc12228菌株)
·肺炎克雷伯氏菌(atcc13883菌株)
·大肠杆菌(atcc25922菌株)
这些物种均在含有5%绵羊血(cos)的columbia琼脂培养基上接种,所述培养基由申请人以参考号43041销售。
对于每个物种,使用根据本发明的取样装置对菌落取样,并在maldi-tof分析板的四个相邻位置处进行四个涂布。
结果列于下表3:
表3
可以看出,对于高孔隙率值(大于70%)的材料,鉴定性能优异,所有物种都被正确鉴定。这是用棉花或材料psu892的结果。
另一方面,当使用具有较低孔隙率的材料时,发现鉴定性能受到影响。因此,对于具有39%孔隙率的xa-20521-ps材料,可以看到,四个大肠杆菌涂布中的两个不允许鉴定这种细菌。因此结果鉴定率仅为83.3%。
- 还没有人留言评论。精彩留言会获得点赞!