一种适用于中药水溶性热敏成分的提取方法与流程
本发明涉及医药化工生产
技术领域:
,尤其涉及一种适用于中药水溶性热敏成分的提取方法。
背景技术:
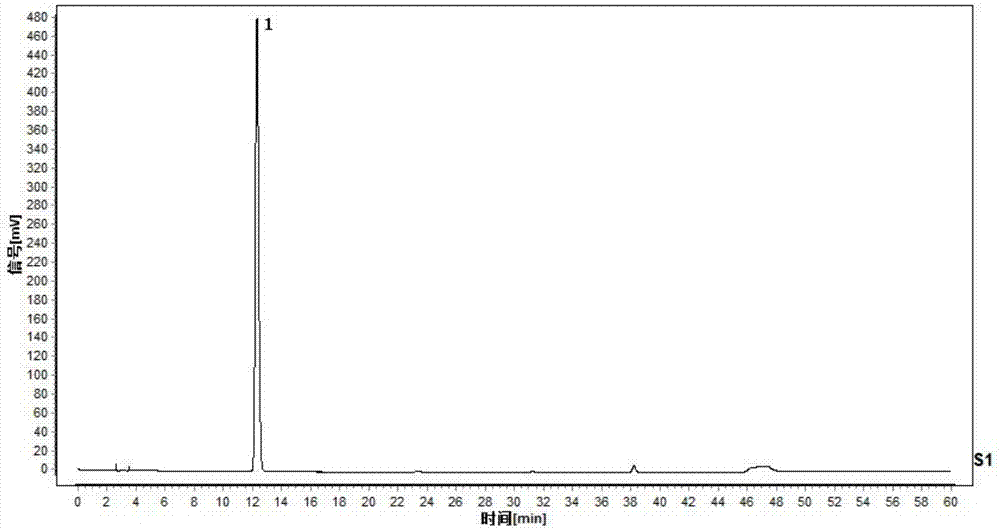
:随着科学技术的不断进步,中药剂型已不仅仅局限于传统的汤、丸、散、膏等剂型,像中药配方颗粒这样的新剂型已经被广大患者接收与使用。中药配方颗粒又名免煎中药饮片、新饮片、精制饮片等,是指经由中药制剂的浸提法,选用适当的溶剂和工艺,使传统中药饮片中的有效成分浸出,再经由浓缩、干燥、制成颗粒,最后进行单味剂量定量包装。中药颗粒不需要煎煮,临用时使用温开水冲服即可,避免了患者对传统中药饮片进行煎煮时出现的如不懂煎煮方法、掌握不好煎煮时间等因素造成的疗效下降的现象,具有方便携带、安全卫生、保质期长等优点,获得了广大患者的欢迎。中药颗粒的有效成分是由中药饮片中提取出来的,因此,其制备工艺是保证其成品药效的关键所在。由于配方颗粒的开发中只能使用水作为提取溶剂,但水存在沸点高,受热升温慢等缺陷,且目前的提取设备多为静态单罐提取设备,升温多为蒸汽直通、旁通加热方式,提取过程对药材中热敏成分损害较大,严重影响了成品的药效。技术实现要素:针对现有提取中药工艺对药材中热敏性成分损害较大,严重影响配方颗粒药效的问题,本发明提供一种适用于中药水溶性热敏成分的提取方法。为解决上述技术问题,本发明提供的技术方案是:一种适用于中药水溶性热敏成分的提取方法,包括以下步骤:向药材中加入95~100℃的水,加热保持温度为95~100℃,浸泡提取15~30min,提取次数为2~3次。相对于现有技术,本发明提供的适用于中药水溶性热敏成分的提取方法,充分考虑中药热敏性成分不耐热、受热易分解或者转化为其他组分的特点,采用95~100℃的沸水,保温对中药材进行多次浸泡提取,通过第一次加入的沸水将药材细胞膜破坏,高温加速了热敏成分的溶出,并且持续加热保温提高了热敏成分在溶媒中的溶解度;通过后续的沸水提取将药材中残留的热敏成分充分溶出,降低药材中热敏成分残留,通过严格控制浸泡时间以及提取次数,既保证有效成分的充分浸出,又降低了热敏性成分的损失。本发明采用的沸水还可杀灭水中及提取液中的微生物,延长提取液的存放时间,降低成品菌检不合格的风险,同时还降低了药材中水溶性杂质的溶出物,提高了有效成分含量,减少病患服药量。相比较于冷浸法,本发明提供的适用于中药水溶性热敏成分的提取方法,具有提取效率高、出液量小、提取液不易变质的特点;相比较于渗滤法,具有提取药材量大、对药材片形限制较低的特点;相比较于超声提取法,更适合于工业化大生产,成本低;相比较于动态逆流提取法,具有设备占地面积小,可进行小批量提取的特点。在此基础上,能够最大限度降低药材中热敏成分在提取中的损失,提高成品中热敏成分含量,提高产品的药效。可选的,要提取药材是花类、叶类、全草类中药,则不需要粉碎,饮片状态即可;若是果实类、种子类、根茎类中药,则需要粉碎成粗颗粒至最粗粉的状态。粗颗粒是指粒径为0.1~1cm的颗粒,最粗粉是指全部通过1号筛,但混有能通过三号筛不超过20%的粉末。优选的,提取次数为2次,提取时间为20~30min。优选的,向药材中加入所述药材重量10~12倍量的95~100℃的水,加热保持温度为95~100℃,浸泡提取20~30min,过滤;向过滤所得滤渣中加入所述药材重量8~10倍量的95~100℃的水,浸泡20~30min,过滤;合并滤液,浓缩,干燥,得提取物。现有技术中采用的蒸汽直通加热过程中,高温蒸汽直接与被提取物(药材)接触,对热敏成分破坏严重;而蒸汽旁通加热的方式,又受提取罐内径限制,内径越大,溶媒受热升温越慢,被提取物受热时间延长,且由于热扩散原理,极易出现受热不均匀的现象,导致药材中有效成分提取不充分。本发明优选的两次沸水提取法,依据药材的细胞膜中蛋白质高温失活的生物特性,第一次沸水提取将药材细胞膜破坏,高温加速了热敏成分的溶出,并提高了热敏成分在溶媒中的溶解度;第二次沸水提取将药材中残留的热敏成分充分溶出,降低药材中热敏成分残留,既保证了有效成分的充分溶出,又最大限度的降低了热敏成分的损失。优选的,浓缩时采用真空浓缩的方法,压力为-0.09~-0.07mpa,浓缩温度为60~70℃。优选的真空浓缩的压力和温度,可极大地降低热敏性成分在浓缩过程造成的损失。优选的,经真空浓缩所得浓缩液的相对密度为1.02~1.10(60℃)。经真空浓缩获得相对密度为1.02~1.10(60℃),有利于后续喷雾干燥工艺的进行。优选的,采用喷雾干燥方法进行干燥,喷雾干燥的进风温度为160~170℃,出风温度为75~85℃。应用喷雾干燥作为干燥方式,将进风口温度控制为160~170℃,瞬时高温干燥可极大保留住干膏粉中热敏性成分,同时提高出粉率。而且,通过限制出风温度为75~85℃,可保证膏粉在干燥完成后处于一个相对较低的温度环境内,避免过度干燥,同时降低热敏成分的损失。可选的,所述药材为红花、连翘、金银花、合欢花、丹参或忍冬藤。可选的,所得中药提取物可加工为任何一种药剂学上所说的剂型。优选的,所得中药提取物可加工为颗粒剂、散剂、冲剂、片剂或胶囊。通过本发明提取方法获得的提取物中有效成分含量高,将其制成各种剂型方便患者服用。附图说明图1为绿原酸对照品的高效液相色谱图;图2为金银花药材的高效液相色谱图;图3为实施例1制备的金银花膏粉的高效液相色谱图;图4为对比例1制备的金银花膏粉的高效液相色谱图;图5为槲皮苷对照品的高效液相色谱图;图6为合欢花药材的高效液相色谱图;图7为实施例2中制备的合欢花膏粉的高效液相色谱图;图8为对比例2中制备的合欢花膏粉的高效液相色谱图;图9为丹酚酸b对照品的高效液相色谱图;图10为丹参药材的高效液相色谱图;图11为实施例3制备的丹参膏粉的高效液相色谱图;图12为对比例3制备的丹参膏粉的高效液相色谱图。具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。实施例1一种金银花药材的提取方法:称取金银花饮片20kg,除去可见异物与杂质,将金银花饮片投入静态多功能提取罐中,加入金银花药材重量10倍量的95~100℃沸水,打开旁通加热,温度为95~100℃,浸泡提取30分钟,过滤;药渣中再次加入金银花药材重量8倍量的95~100℃沸水,打开旁通加热,保温温度为95~100℃,浸泡提取20分钟,过滤;合并二次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.08mpa,浓缩温度为60℃,浓缩液相对密度为1.04(60℃),将浓缩液导入到预热罐中,升温至75℃,进行喷雾干燥,进风温度为167℃,出风温度为82℃,及时收集干膏粉,取样,待检测。实施例2一种合欢花药材的提取方法:称取合欢花药材,除去可见异物与杂质,将合欢花饮片投入静态多功能提取罐中,加入合欢花重量11倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取25分钟,过滤;药渣中再次加入合欢花重量9倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取25分钟,过滤;合并二次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.07mpa,浓缩温度为65℃,浓缩液相对密度为1.02(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为160℃,出风温度为75℃,及时收集干膏粉,取样,待检测。实施例3一种丹参药材的提取方法:称取丹参药材,使用粉碎机将丹参药材粉碎成粗颗粒,粒径在1cm以下。将粉碎后的丹参饮片投入静态多功能提取罐中,加入丹参药材重量12倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取20分钟,过滤;药渣中加入丹参药材重量10倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取30分钟,过滤;合并二次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.09mpa,浓缩温度为70℃,浓缩液相对密度为1.10(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为170℃,出风温度为85℃,及时收集干膏粉,取样,待检测。实施例4一种丹参药材的提取方法:称取丹参药材,使用粉碎机将丹参药材粉碎成粗颗粒,粒径在1cm以下。将粉碎后的丹参饮片投入静态多功能提取罐中,加入丹参药材重量8倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取15分钟,提取3次,过滤,合并3次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.09mpa,浓缩温度为70℃,浓缩液相对密度为1.10(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为170℃,出风温度为85℃,及时收集干膏粉。实施例5一种丹参药材的提取方法:称取丹参药材,使用粉碎机将丹参药材粉碎成粗颗粒,粒径在1cm以下。将粉碎后的丹参饮片投入静态多功能提取罐中,加入丹参药材重量6倍量的95~100℃沸水,打开旁通加热,保持温度为95~100℃,浸泡提取20分钟,提取3次,过滤,合并3次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.09mpa,浓缩温度为70℃,浓缩液相对密度为1.10(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为170℃,出风温度为85℃,及时收集干膏粉。其它含热敏性成分的药材如红花、连翘,忍冬藤等均可按照实施例1-5的方法提取,也可达到相同的效果,有效降低热敏性物质的损失。实施例1-5得到的干膏粉,可加入制剂学中常规的辅料,按照常规的工艺制备各种所需的剂型,如颗粒剂、散剂、冲剂、片剂或胶囊等。对比例1称取金银花饮片20kg,除去可见异物与杂质。将金银花饮片投入静态多功能提取罐中,加入金银花药材重量10倍量的常温水,打开旁通加热,加热至95~100℃之间,提取30分钟,过滤;药渣中再次加入金银花药材重量的8倍量的常温水,打开旁通加热,加热至95~100℃之间,提取20分钟,过滤;合并两次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.08mpa,浓缩温度为60℃,浓缩液相对密度为1.04(60℃),将浓缩液导入到预热罐中,升温至75℃,进行喷雾干燥,进风温度为167℃,出风温度为82℃,及时收集干膏粉,取样,待检测。对比例2称取合欢花药材,除去杂质,将合欢花饮片投入静态多功能提取罐中,加入合欢花重量11倍量的常温水,打开旁通加热,加热至95~100℃之间,提取25分钟,过滤;药渣中再次加入合欢花重量9倍量的常温水,打开旁通加热,加热至95~100℃之间,提取25分钟,过滤;合并二次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.08mpa,浓缩温度为65℃,浓缩液相对密度为1.02(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为160℃,出风温度为75℃,及时收集干膏粉,取样,待检测。对比例3称取丹参药材,使用粉碎机将丹参药材粉碎成粗颗粒,粒径在1cm以下。将粉碎后的丹参饮片投入静态多功能提取罐中,加入丹参药材重量12倍量的常温水,打开旁通加热,加热至95~100℃之间,提取20分钟,过滤;药渣中加入丹参药材重量10倍量的常温水,打开旁通加热,加热至95~100℃之间,提取30分钟,过滤;合并二次提取液,将提取液导入真空单效浓缩罐中,打开蒸汽阀门和真空泵,进行真空干燥,压力为-0.09mpa,浓缩温度为70℃,浓缩液相对密度为1.10(60℃),将浓缩液导入到预热罐中,升温至70℃,进行喷雾干燥,进风温度为170℃,出风温度为85℃,及时收集干膏粉,取样,待检测。实施例6取实施例1和对比例1的提取液适量,按照按如下方法测定,并计算理论出膏率、含量转移率。理论出膏率精密移取25ml提取液,置于已干燥至恒重的称量瓶中,水浴蒸干,再放入烘箱105℃干燥3h,置于干燥器冷却30min,迅速精密称定重量,计算理论出膏率,每组平行测定两份。理论出膏率(%)=(加样烘干后蒸发皿恒重-未加样蒸发皿恒重)×提取液总体积÷25÷投料量绿原酸照高效液相色谱法(通则0512)测定。以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相a,以0.4%磷酸溶液为流动相b;按表1中的规定进行梯度洗脱,流速为1.0ml/min;柱温为35℃;检测波长327nm;理论塔板数按绿原酸峰计算应不低于3000。表1绿原酸含量测定色谱条件时间(分钟)流动相a(%)流动相b(%)0~1590→9010→1015~2090→8510→1520~5085→8015→2050~6080→7020→30对照品溶液的制备精密称取绿原酸对照品适量,精密称定,置棕色量瓶中,加70%甲醇制成每1ml含绿原酸0.28mg的对照品溶液。供试品溶液的制备金银花膏粉称取实施例1、对比例1膏粉约0.1g,精密加入70%甲醇,称定重量,超声处理(功率200w,频率40khz)30分钟,取出,放冷,再称定重量,用70%甲醇补足减失的重量,摇匀,滤过,取续滤液,即得。金银花药材取金银花粉末(过四号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加入50%甲醇50ml,称定重量,超声处理(功率250w,频率35khz)30分钟,放冷,再称定重量,用50%甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置25ml棕色量瓶中,加50%甲醇至刻度,摇匀,0.45μm微孔滤膜过滤,取续滤液,即得。测定法分别精密吸取对照品溶液与供试品溶液各2μl,注入液相色谱仪,测定,结果见表2。表2理论出膏率绿原酸含量含量转移率实施例134.4%91.6mg/g87.5%对比例142.5%47.1mg/g55.1%药材——3.6%——实施例7取实施例2、对比例2提取液适量,按如下方法测定,并计算理论出膏率、含量转移率。理论初膏率的测试方法与实施例6相同,此处不再赘述。槲皮苷照高效液相色谱法(通则0512)测定。色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1%磷酸(23:77)为流动相,流速:1.0ml/min;检测波长为256nm。理论板数按槲皮苷峰计算应不低于3000。参照物溶液的制备精密称取槲皮苷对照品适量,加稀乙醇制成每lml含87.5μg的溶液,即得。合欢花膏粉取实施例2、对比例2适量,研细,取约0.1g,精密称定,置具塞锥形瓶中,精密加入稀乙醇25ml,称定重量,超声处理(功率250w,频率40khz)10分钟,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,即得。合欢花药材取合欢花粉末(过三号筛)约0.25g,精密称定,置具塞锥形瓶中,精密加入稀乙醇50ml,称定重量,加热回流30分钟,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。测定法分别精密吸取对照品溶液与供试品溶液各1μl,注入液相色谱仪,测定,结果见表3。表3理论出膏率槲皮苷含量含量转移率实施例221.4%42.3mg/g75.5%对比例225.5%22.6mg/g48.1%药材——1.2%——实施例8取实施例3、对比例3提取液适量,按如下方法测定,并计算理论出膏率、含量转移率。理论初膏率的测试方法与实施例6相同,此处不再赘述。丹酚酸b照高效液相色谱法(通则0512)测定。色谱条件:色谱柱:agilentzorbaxsbc18(2.1×100mm,1.8μm);流动相:0.1%h3po4水溶液:乙腈(80:20);流速:0.5ml/min;检测波长:286nm;进样量:1μl;柱温:30℃。对照品溶液的制备取丹酚酸b对照品适量,精密称定,加甲醇-水(8-2)制成每lml含0.10mg的溶液,即得。供试品溶液的制备丹参膏粉取实施例3、对比例3膏粉0.3g,精密称定,置50ml量瓶中,加水45ml,超声处理10min(575w,37khz),放冷,加水定容至刻度,摇匀,0.22μm微孔滤膜过滤,取续滤液,即得。丹参药材取本品粉末(过三号筛)约0.15g,精密称定,置具塞锥形瓶中,精密加入甲醇-水(8:2)混合溶液50ml,密塞,称定重量,超声处理(功率140w,频率42khz)30分钟,放冷,再称定重量,用甲醇-水(8:2)混合溶液补足减失的重量,摇匀,滤过,精密量取续滤液5ml,移至10ml量瓶中,加甲醇-水(8:2)混合溶液稀释至刻度,摇匀,0.22μm微孔滤膜过滤,取续滤液,即得。测定法分别精密吸取对照品溶液与供试品溶液各2μl,注入液相色谱仪,测定,结果见表4。表4出膏率丹酚酸b含量含量转移率实施例335.1%54.1mg/g80.5%对比例345.2%22.1mg/g44.6%药材——2.3——由上述实施例和对比例的测试结果可知,与旁通加热提取方法相比,本发明提供的提取方法能够最大限度的降低药材中热敏成分在提取中的损失,提高有效成分的含量,含量转移量与常规的旁通加热法相比提高了一倍以上。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换或改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1