负载在玻璃泡沫和/或玻璃陶瓷泡沫上的金属氧化物纳米颗粒及其在气相和/或液相中用于多相催化的用途
1.本发明涉及一种多孔材料,该多孔材料包含由玻璃泡沫载体和/或玻璃陶瓷泡沫载体吸附的金属氧化物纳米颗粒,用于液相和/或气相中的多相催化中的应用。
2.本发明特别适用于处理室内空气或工业空气和水的领域,例如在voc的氧化、新兴微污染物的降解、臭氧的降解、烯烃的还原或nox和nh3的处理等方面。
3.在以下描述中,括号([])中的参考文献是指文本末尾提供的参考文献列表。
背景技术:
[0004]
催化是现代化学中的一个基本过程,其中超过80%的工业化学反应需要至少一个催化步骤。它可以显著加快化学反应的速度,以便朝着更小的反应器、提高生产率,以及在更温和的压力和温度条件下工作的方面发展。催化剂通过降低反应所需的活化能且不被消耗来参与反应机制。因此,催化中的一个基本问题是回收和再循环催化剂,从而可以延长催化剂的使用寿命。
[0005]
许多常规反应需要使用催化剂(氢化、费托法、氧化、傅克酰基化、偶联反应、复分解等)。与计量化学相比,催化是通过限制废料、处理和毒性风险,以及通过其在空气处理(挥发性有机化合物、废气等的处理)或水处理(催化臭氧化、芬顿法等)中的应用以减少微污染的绿色、对社会负责和对环境友好的化学的一部分。其中催化剂以固体形式存在的多相催化通常优于均相催化,因为它有利于催化剂的回收、可能的再生和再利用。
[0006]
最常见的多相催化剂分为三种类型:(i)负载型过渡金属(有机或无机载体);(ii)半导体或非半导体微米金属氧化物(al2o3、v2o5、tio2、fe3o4等);(iii)沸石。金属氧化物纳米颗粒在许多应用中具有相当高的催化活性,并且具有非常好的稳定性,特别是在氧化条件下。这些活性金属物质的载体性质可能不同(惰性氧化物、陶瓷、活性炭、沸石等)。载体呈粉末(用于固定床或流化床)、球粒(固定床或流化床)或整料(固定床)的形式。近年来,结构化催化剂(诸如整料催化剂)受到特别关注,与具有相同孔隙率和比表面积的粉末或球粒相比,这些结构化催化剂具有大大简化实施的优点,因为它们由单个块组成并且限制了水头损失。这些整料的主要应用是作为催化转化器。然而,构成整料的平行通道的直线性质仍然是它们的主要缺点之一,因为这会导致材料和热量的径向交换不良,以及流体分布不良。此外,用于形成整料的挤压技术仍然相对复杂且实施起来昂贵。几十年来,在更机密的层面上,已经开发出结构化的多孔载体,诸如陶瓷泡沫或金属泡沫,其特征在于具有高度开口孔隙率(互连孔)的“海绵”状结构。通过多面体孔之间的大量互连,这些多孔载体的盘绕结构与整料的盘绕结构有很大不同,从而使反应流体能够更好地径向扩散。总的来说,这些泡沫具有大孔结构。因此,自20世纪80年代以来,金属泡沫一直用于催化。然而,金属泡沫的成本似乎阻碍了它们的工业发展。由于其相对较低的成本,陶瓷泡沫在过去15年中开始出现在催化应用的文献中。然而,陶瓷泡沫需要相对苛刻的制造条件(从1100℃至1700℃的烧结),并需要在沉积活性物质之前使用浸渍层(载体涂料)。该载体涂料(最常见的由γ-氧化铝组
成)的沉积,可以增加载体材料(泡沫或整料)的比表面积,并促进催化活性物质的附着。然而,这涉及另外的制备步骤。
[0007]
国际申请wo 2017/064418[1]描述了使用玻璃泡沫作为金属纳米颗粒的载体以用作催化剂,该金属纳米颗粒基本上由处于0氧化态的金属组成。
[0008]
lebullenger等人的出版物(非晶态固体杂志,2010年,第356期:第2562-2568页)[2]描述了一种玻璃泡沫,其外部使用刷子吸附了tio2,因为它的表面光催化活性(因为uv辐射不会穿透到泡沫的体积中),以用于在气相中分解甲苯。
技术实现要素:
[0009]
发明人已经开发了一种催化材料,其包括或由玻璃泡沫和/或玻璃陶瓷泡沫(即,由在泡沫形成步骤中玻璃失透或部分结晶产生的分散在玻璃相中的铁矿石和熔砂的微晶组成的材料)组成,作为由至少11%、至少30%、至少50%、至少70%或至少90%的至少一种氧化金属组成的金属纳米颗粒的载体,用于在气相或液相的多相氧化催化中的应用。这些玻璃泡沫和/或玻璃陶瓷泡沫是陶瓷泡沫和用作固定床的整料的替代方案。这些泡沫可以通过直接浸渍(通过浸没)包含纳米颗粒的溶液并通过干燥蒸发溶液以获得最终材料来快速生产,同时可以回收玻璃废料,从而使本发明有助于循环经济。通过调节初始混合物的组成参数和/或泡沫形成的热分布(温度、时间),可以根据需要来控制孔的尺寸和泡沫的孔隙率。
[0010]
本发明材料的这种玻璃泡沫和/或玻璃陶瓷泡沫具有现有技术泡沫的优点,此外,由于多种原因,具有比陶瓷泡沫更大的潜力。其结果是,玻璃废料(钠钙硅玻璃、硼硅酸盐玻璃、食品包装玻璃、玻璃珠、平板玻璃等)的回收率达到90%以上(高达97.5%),这是一种可持续的资源。其生产速度快、所需步骤少、生产条件的限制性和能耗低于制造陶瓷泡沫时实施的生产条件,后者需要1100℃至1700℃的烧结温度。实际上,玻璃泡沫是通过简单地混合磨碎的玻璃废料、一种或多种发泡剂(ain、caco3、c、sic、mno2等)(其中一些也可能是废料),以及任选地一种或几种掺杂剂来生产的。随后将混合物加热至介于750℃至900℃的温度以形成泡沫,这是由发泡剂产生的“惰性”气体(co2、n2、o2等)形成的结果。在使用的温度下,这些气泡以浆态留在玻璃中。其孔隙率和其孔径可根据组分、加热技术和设定的温度梯度来调整。出于上述各种原因(废料回收、步骤数量有限等),其成本较低。
[0011]
各向异性金属氧化物纳米颗粒在玻璃泡沫和/或玻璃陶瓷泡沫中的附着是通过湿法(直接)途径在泡沫的整个全质量(或其核心)中浸渍来实现的,使用在纳米尺度上预先稳定水相中的颗粒的技术,从而能够很好地控制活性物质的尺寸。因此,泡沫在泡沫的所有可用表面(即,外表面和内表面)上吸附的(过渡或后过渡)金属氧化物具有受控的纳米形态和尺寸,从而使催化剂具有良好的比表面积,同时受益于泡沫的大孔结构,以限制使用所设计材料期间的水头损失。应当回顾的是,本发明不需要使用厚度为约10μm至200μm、通常为约50μm的载体涂料来将金属纳米颗粒粘附到玻璃泡沫和/或玻璃陶瓷泡沫上。相反,所述泡沫在其制备之后可以经历旨在改变其可用表面积以更好地吸附金属纳米颗粒的步骤。导致例如在玻璃泡沫和/或玻璃陶瓷泡沫的表面形成小于10μm厚的层的功能化示例是:用一种或多种金属氧化物(例如fe2o3、tio2)对玻璃泡沫和/或玻璃陶瓷泡沫进行掺杂,从而有助于催化活性;在氨气氛下对玻璃泡沫和/或玻璃陶瓷泡沫进行氮化,以便通过用对所吸附的金属
具有更大亲和力的氮原子替换氧原子来改变表面功能;或者通过热处理使玻璃泡沫和/或玻璃陶瓷泡沫部分结晶(《20%)。
[0012]
此外,最重要的是,发明人已经完全出乎意料地证明,本发明的催化材料包括或由玻璃泡沫和/或玻璃陶瓷泡沫组成,该玻璃泡沫和/或玻璃陶瓷泡沫作为由至少11%、至少30%、至少50%、至少70%或至少90%的至少一种氧化金属组成的纳米颗粒的载体,通常产生比国际申请wo 2017/064418[1]更好的voc还原率。例如,当所述材料包含由玻璃泡沫吸附在玻璃泡沫的所有可用表面(即,外表面和内表面)上的mno2、cuo或fe2o3纳米颗粒时,(即,通过深度浸渍或完全浸渍,使金属纳米颗粒通过玻璃泡沫和/或玻璃陶瓷泡沫的孔扩散)在300℃或350℃的温度下处理空气中的烃类(例如,烷烃),已经证明了这一点。
[0013]
到目前为止,本发明的催化材料已经通过在玻璃泡沫上使用锰氧化物而不使用载体涂料成功地实现了气相氧化(即,通过催化臭氧化和热催化处理空气)。这些金属氧化物通过浸渍然后干燥以纳米尺寸的各向异性颗粒的形式附着到载体上。这种附着技术是温和的,因为它在水相中、在环境温度和空气中进行,并且没有后续的煅烧步骤。这些金属颗粒的尺寸和形态通过合适的还原技术(氢气、化学还原剂、氧化还原法)然后是本领域技术人员已知的吸附技术来控制。催化活性可以基于所设想的应用,通过选择负载金属(或金属混合物)确定,也可以通过载体的结构(不同程度的孔隙率等)来确定。
[0014]
因此,可以设想气体或液体或气相/液相应用,特别是用于不使用臭氧的(热)催化氧化,或用于(热)催化剂臭氧化,其中例如,在玻璃泡沫的所有可用表面(即,外表面和内表面)上使用由玻璃泡沫吸附的mno2纳米颗粒与使用处于0氧化态的ru纳米颗粒相比,能够实现良好和更好的污染物(具体地烃类)氧化(参见表1)。
[0015]
本发明的一个主题是一种催化材料,该催化材料包括:
[0016]
(a)玻璃泡沫载体和/或玻璃陶瓷泡沫载体,
[0017]
(b)由所述载体吸附的金属纳米颗粒,这些金属纳米颗粒由至少11%的至少一种氧化态金属组成;
[0018]
所述玻璃泡沫和/或玻璃陶瓷泡沫具有相对于总孔隙率至少75%的开口孔隙率;
[0019]
所述金属氧化物纳米颗粒包含选自过渡金属和后过渡(或不良)金属的至少一种金属。
[0020]
由于无需煅烧步骤以形成金属氧化物纳米颗粒和/或将其分散在载体中,因此该材料即可使用。所述载体可以是例如单块或整料的形式、珠粒的形式或球粒的形式。可以根据期望的用途选择载体的体积和形式。例如,载体可以具有0.5cm3的最小体积。
[0021]
根据本发明的材料的具体实施方案,金属氧化物纳米颗粒与玻璃泡沫和/或玻璃陶瓷泡沫的所有可用表面直接接触。
[0022]
根据本发明的材料的具体实施方案,玻璃泡沫和/或玻璃陶瓷泡沫具有至少60%、优选地至少70%、优先地至少75%、并且最优先地至少80%的总孔隙率。
[0023]
根据本发明的材料的具体实施方案,玻璃泡沫和/或玻璃陶瓷泡沫的孔的平均直径d
p
为0.01mm至1mm,优选地0.2mm至0.8mm;优先地0.4mm至0.7mm。这是平均值,其中孔能够具有更大的直径,最多3mm-4mm。
[0024]
根据本发明的材料的具体实施方案,球形形态的纳米颗粒具有1nm至10nm、优选地2nm至8nm、优先地约5nm的平均直径。它们也可以呈各向异性形式(棒状、蠕虫状、树枝状),
例如截面尺寸为约3nm-4nm,长度为约10nm-100nm。
[0025]
根据本发明的具体实施方案,过渡金属和后过渡金属例如选自mn、fe、co、ni、cu、zn、al、mo、se、sn、pt、ru、rh、zr、re、pd、w、ir、os、nb、ta、bi、au、ag、ti。
[0026]
根据本发明的具体实施方案,催化材料包括直接吸附在玻璃泡沫上的mno2、cuo、fe2o3、优选地mno2的纳米颗粒。
[0027]
本发明的另一主题是一种用于制备根据本发明的材料的方法,该方法包括通过深度浸渍或完全浸渍(即,通过浸没)使悬浮在溶剂中的由至少11%的本发明所定义的至少一种氧化金属组成的金属纳米颗粒与玻璃泡沫和/或玻璃陶瓷泡沫接触的步骤。
[0028]
根据本发明,一方面玻璃泡沫和/或玻璃陶瓷泡沫,另一方面金属纳米颗粒在接触步骤之前彼此分开制备。
[0029]
根据本发明的具体实施方案,该方法还包括在使用材料之前干燥形成的材料的步骤,以便消除其中金属纳米颗粒已经悬浮的溶剂。例如,干燥步骤在烘箱中在90℃至200℃、特别地90℃至120℃、具体地约100℃的温度下进行。
[0030]
根据本发明的具体实施方案,重复接触和干燥步骤,优选地直到金属纳米颗粒完全吸附在玻璃泡沫的所有可用表面上。这种迭代方法可以增加以这种方式吸附的金属纳米颗粒的量。通过跟踪金属纳米颗粒悬浮液在每次浸渍时的颜色损失,可以在视觉上或通过光谱方法监测所有金属纳米颗粒的吸附。
[0031]
根据本发明的方法的具体实施方案,金属纳米颗粒的悬浮液包括能够防止纳米颗粒聚集并控制金属纳米颗粒平均直径的稳定剂,优选地选自聚合物、离子液体、磷基和/或硫基和/或者氮基和/或氧基配体、环糊精、树枝状聚合物、杯芳烃和表面活性剂。例如,表面活性剂为季铵型,具体地:
[0032]
(i)式(i)r1r2r3n
+
(ch2)
n-oh,x-的n-(羟烷基)铵,其中
[0033]
r1和r2相同或不同,有利地相同,并且表示c1至c6芳基或烷基,特别地c1至c3烷基,具体地c1烷基;
[0034]
r3为c6至c
20
芳基或烷基,特别地c
10
至c
18
烷基,具体地c
16
烷基;
[0035]
n=2至6,特别地2至4,具体地2至3;
[0036]
x为选自cl、br、i、f、ch3so3、cf3so3、ntf2、bf4、pf6、oh、hco3、rcoo(例如乳酸、癸酸)的一价抗衡阴离子;或者
[0037]
(ii)式(ii)r3n
+
[(ch2)
n-oh]3,x-的n-三(羟烷基)铵,其中r3、x和n如上所定义。
[0038]
根据本发明的具体实施方案,稳定剂优选地n,n-二甲基-n-十六烷基-n-(2-羟乙基)铵。
[0039]
根据本发明的方法的具体实施方案,溶剂为水或醇(例如甲醇),或它们的混合物。
[0040]
本发明的另一主题是通过根据本发明的制备方法获得的材料。
[0041]
本发明的另一主题是包含根据本发明的材料的催化反应器。
[0042]
出于本发明的目的,“催化反应器”旨在表示可以含有本发明的催化材料的载体,例如选自管或罐。
[0043]
本发明的另一主题是根据本发明的材料在处理存在于空气或水中的污染物中的用途。例如,污染物为烃类,具体地烷烃。
附图说明
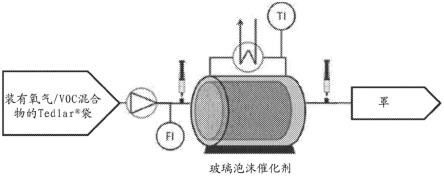
[0044]-图1描绘了利用催化玻璃泡沫对voc进行热催化氧化的设施。
具体实施方式
[0045]
实施例
[0046]
实施例1:材料和方法
[0047]
1)玻璃泡沫的制备和表征
[0048]
实施例1.1:
[0049]
将477.5g磨碎的具有小于350微米粒度(泡沫总重量的95.5%)的钠钙硅玻璃(食品包装玻璃或窗玻璃)、15g aln(m
总
的3%)和7.5g tio2掺杂剂(m
总
的1.5%)混合并放置在容器中,然后将其引入烘箱中。在不同的温度和不同的固化时间下制备三种泡沫以便改变开口孔隙率。
[0050]
[表1]
[0051]
玻璃泡沫时间(h)温度(℃)开口孔隙率(%)gf1289085gf21.588083gf3485077
[0052]
实施例1.2:
[0053]
根据相同的方法,第四泡沫由200g磨碎的玻璃、2重量%的aln和1重量%的tio2在850℃的温度下保持1小时40分钟来制备。
[0054]
随后测定玻璃泡沫gf4的特性:
[0055]
[表2]
[0056]
pappppyc开口孔隙率%闭合孔隙率%总孔隙率%0.392.0681384
[0057]
实施例1.3:
[0058]
玻璃泡沫gf5由玻璃粉末(95.5%)、1.5重量%的aln和3重量%的tio2在880℃的温度下保持2小时40分钟来制备。
[0059]
实施例1.4:
[0060]
玻璃泡沫gf6由玻璃粉末(93.5%)、0.75重量%的aln、4.5重量%的mno2和1.25重量%的tio2在880℃的温度下保持2小时30分钟来制备。
[0061]
实施例1.5:
[0062]
玻璃泡沫gf7至gf14由玻璃粉末、具有不同百分比的aln、tio2和/或mno2根据下表3中提到的温度和时间条件来制备。
[0063]
[表3]
[0064][0065][0066]
实施例1.6:玻璃泡沫的氮化
[0067]
将根据实施例1.1的玻璃泡沫样品放置在陶瓷炉中的陶瓷坩埚中。在氮气流下,在1小时15分钟内达到750℃的温度。在750℃下35分钟后,用氨流替换氮气流。在氨流下维持加热24小时,然后在氮气流下在约2小时内将泡沫自然冷却。
[0068]
2)纳米颗粒水性悬浮液的制备:
[0069]
i)钌(0)
[0070]
在搅拌下,将10ml含有49.7mg(1当量,1.9
×
10-4
mol)rucl3,3h2o的水性溶液和37ml含有133mg(2当量,3.8
×
10-4
mol)n,n-二甲基-n-十六烷基-n-(2-羟乙基)铵的水性溶液添加到3ml含有nabh4(2.5当量,4.75
×
10-4
mol)的水性溶液。将混合物在环境压力和大气压下持续搅拌1天。
[0071]
ii)二氧化锰(mno2)
[0072]
将1ml含有硼氢化钠(2.5当量,9.5
×
10-5
mol,3.6mg)的水性溶液添加到含有合适的表面活性剂(5当量、7当量或10当量)的水性溶液(5ml)中。随后在剧烈搅拌下将该混合溶液快速添加到含有金属前体kmno4(1当量,3.8
×
10-5
mol,6mg)的水性溶液(4ml)中,以获得mno2的水性胶体悬浮液(iv)(10ml)。还原立即发生,并反映在从粉红色到棕色的颜色变化中。
[0073]
iii)fe2o3[0074]
将10ml 1m盐酸溶液、253.5mg(2
×
10-3
mol,1当量)无水氯化亚铁fecl2和649.0mg(4
×
10-3
mol,2当量)无水三氯化铁fecl3引入250ml圆底烧瓶中,借助磁力搅拌器进行搅拌。将混合物持续搅拌10分钟,然后引入3ml含有35%w/w的氨的水性溶液,这导致从橙色溶液中形成深棕色沉淀物。使用外部永磁体通过磁沉降分离该沉淀物,并用6ml高氯酸和44ml蒸馏水洗涤以获得酸性溶液,或用25ml四甲基氢氧化铵(以25%w/w溶解于甲醇)和25ml蒸馏水洗涤以获得碱性溶液。
[0075]
iv)cuo
[0076]
将47.4mg(1.9
×
10-4
mol,1当量)五水硫酸铜cuso4·
5h2o、597.8mg(1.71
×
10-3
mol,9当量)hea16cl和45.4ml超纯水(milliq)引入带有磁力搅拌器的100ml圆底烧瓶中。
将混合物在环境温度下持续搅拌至少20分钟,直到出现浑浊的淡蓝色。随后,逐滴添加2.66ml含有0.5m氢氧化钠(1.33
×
10-3
mol,7当量)的水性溶液,该溶液几乎立即呈现浑浊的棕色。将混合物持续搅拌20分钟,然后引入1.9ml 1m的肼的thf(1.9
×
10-3
mol,10当量)溶液,该溶液迅速变色,形成鲜艳的橙色。随后,将悬浮液在不断搅拌下储存在锥形瓶中最多两周。
[0077]
v)co3o4[0078]
将228mg(5.7
×
10-3
mol,1.5当量)氢氧化钠naoh、14.25g(2.06
×
10-1
mol,54.4当量)亚硝酸钠nano2和90ml超纯水(milliq)引入配备有冷凝器和磁力搅拌器的250ml双颈圆底烧瓶中。在搅拌下,将混合物在105℃的油浴中加热,同时借助穿过隔垫的针吹入空气。在105℃下15分钟之后,逐滴引入10ml含有1.1g(3.8
×
10-3
mol,1当量)硝酸钴(ii)六硫酸盐co(no3)2.6h2o的溶液。钴溶液在氢氧化钠溶液存在下由深粉红色变为蓝色,再次添加后最终变为浑浊的粉红色。不到一小时后,形成棕色沉淀物,其在接下来的两小时内逐渐变黑。3小时后,停止反应并将混合物离心。除去上清液并用蒸馏水和足够量的盐酸填充管以消除过量的亚硝酸钠(直到不再产生nox气体)。随后,进行若干(至少3个)离心步骤以便获得黑色的氧化钴纳米颗粒。将这些纳米颗粒在超声作用下分散在超纯水中,并在锥形瓶中保持磁力搅拌。
[0079]
3)由玻璃泡沫吸附的纳米颗粒的制备
[0080]
将第2)点中获得的260μl每种悬浮液浸渍到玻璃泡沫gf5上。将溶液沉积在泡沫的每个表面上,每次沉积之间有一定停顿。回收过量的悬浮液体积并重新用于新的沉积,以便进行定量浸渍。然后将泡沫在烘箱中干燥(温度=100℃)。
[0081]
实施例2:在烷烃的情况下评估由玻璃泡沫吸附的ru(0)、mno2、fe2o3或cuo催化剂的性能
[0082]
该热催化氧化装置由固定床反应器组成,该反应器连续供应所需浓度的受voc污染的空气(图1)。将40l或100l袋填充有氧气,然后蒸发液体voc,直到达到所需浓度。随后,使用knf(德国)为此应用专门设计的隔膜泵,将受污染的空气从袋中泵入由玻璃泡沫制成的催化剂(反应器),并将其插入烘箱中,烘箱的温度控制为介于100℃至400℃(精度为
±
10℃)。在开始消除voc的实验之前,烘箱已达到所需温度。用流量计(brooks r-15-c)监测气体流速,该气体流速介于4.92nl h-1
至21.9nl h-1
。根据催化剂的尺寸(直径为16mm,长度为40mm至94mm),气体速度在0.006m.s-1
至0.032m.s-1
之间变化,气时空速(ghsv)介于270h-1
至1236h-1
。
[0083]
在反应器的入口和出口使用气密注射器取出气体样品。所有实验进行至少1/2个小时,以便确保平衡条件(通过在实验期间取出若干样品进行验证,几分钟之后出口处的浓度保持恒定),并且未观察到催化剂失活。
[0084]
通过热催化氧化测试庚烷和甲苯的消除。庚烷的入口浓度测试为1g.m-3
、1.354g.m-3
或2g.m-3
,甲苯的入口浓度为1.731g.m3。选择这些值是为了考虑可能遇到高浓度的内部工业空气。
[0085]
通过气相色谱法(gc)分析voc。gc设备(agilent 6890n)配备有db-624色谱柱(30m
×
0.53mm)和火焰离子化检测器。将进样器加热至150℃,检测器加热至250℃。载体气体为h2。将烘箱加热至300℃。保留时间为约4分钟。
[0086]
根据以下等式,基于入口浓度[voc]
入口
和出口浓度[voc]
出口
以及在催化剂中的停留时间τ(计算为空容器)来计算反应速率(r en g.m-3
.s-1
):
[0087][0088]
表4和表5中呈现的结果清楚地证明了催化玻璃泡沫作为催化剂处理voc的功效,特别是与处于0氧化态的浸渍有金属纳米颗粒的催化材料相比,浸渍有mno2、cuo和fe2o3纳米颗粒的玻璃泡沫的功效有所提高。
[0089]
[表4]
[0090][0091]
[表5]
[0092]
vocru(0)的npcuo的npfe2o3的np庚烷-1.354g.m-3-350℃0.095g.m-3
.s-1
0.202g.m-3
.s-1-甲苯-1.731g.m-3-350℃0.039g.m-3
.s-1
0.104g.m-3
.s-1
0.043g.m-3
.s-1
[0093]
参考文献列表
[0094]
1.国际申请wo 2017/064418
[0095]
2.lebullenger等人,非晶态固体杂志,2010年,第356期:第2562-2568页。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1