基于二氧化碳捕获碳化电解精炼高纯金属的方法
1.本技术属于化学冶金技术领域,具体涉及基于二氧化碳捕获碳化电解精炼高纯金属的方法。
背景技术:
2.目前对能源和材料的更高需求导致二氧化碳排放的增加,但这与绿色化学的概念相违背,对于建立一个可持续发展的社会,无疑是一个严重的问题。二氧化碳排放被认为是全球气候变化的主要因素。人们提出了各种解决二氧化碳排放的方法,例如减少排放、改变可再生能源,安全捕获、储存二氧化碳等。
3.然而,由于化石燃料在能源工业中仍旧发挥主导作用,通过减少化石燃料的使用来减少二氧化碳排放在近期内难以实现。因此,高效、低成本的二氧化碳捕获和储存、转换和利用技术被认为是最有前途的技术。大规模二氧化碳捕获的技术主要包括溶剂基化学吸附技术、碳酸盐环状技术和氧燃料过程转换技术。转换技术主要包括以下五种:二氧化碳化学转换为氢化材料;二氧化碳光化学转换成甲酸、甲烷;二氧化碳电化学或光电化学转换成一氧化碳、甲酸、甲醇或碳;二氧化碳生物转化成乙醇、糖;二氧化碳与乙酸重整生成一氧化碳和氢气。
4.在二氧化碳转换方法中,电化学还原二氧化碳为碳基产物的反应容易控制,而且产物提供了一种环境友好的能源。例如在水溶液、离子液体和熔盐中可以发生二氧化碳的电化学还原为碳。但是,二氧化碳在水溶液中的溶解度较低,二氧化碳的电还原电位与水分解电位非常接近,限制了二氧化碳在水溶液中的实际电化学转化。
5.电解精炼是指利用不同元素的阳极溶解或阴极析出难易程度的差异而提取纯金属的技术。
6.电解时用高温还原得到的粗金属制成阳极,用含有目标金属化合物的盐溶液做电解液,控制一定电位使溶解电位比精炼金属正的杂质存留在阳极或沉积在阳极泥中(其中往往含有贵金属),用其他方法分离回收;溶解电位比精炼金属负的杂质则溶入溶液,不在阴极上析出,从而在阴极上可得到精炼的高纯金属。然而现有的熔盐电脱氧工艺产出二氧化碳、可溶阳极精炼工艺也有co及温室气体的排出。
技术实现要素:
7.有鉴于此,一些实施例公开的技术方案是基于二氧化碳捕获碳化电解精炼高纯金属的方法,具体包括:
8.以金属氧化物电极为第一阴极、石墨电极为第一阳极、熔盐电解质组成第一电解体系;
9.将二氧化碳气体通入第一电解体系进行恒电压电解,作为第一阴极的金属氧化物脱除部分氧离子;二氧化碳在熔盐电解质中反应生成碳酸根离子,生成的碳酸根离子在第一阴极上被还原为单质碳;单质碳和脱除部分氧离子的金属氧化物在第一阴极上反应生成
金属碳氧固溶体;
10.以形成金属碳氧固溶体的第一阴极为第二阳极,金属电极为第二阴极,与熔盐电解质组成第二电解体系;
11.第二电解体系进行恒电压电解,金属碳氧固溶体被氧化,生成的金属离子在第二阴极被还原析出高纯金属,生成的碳氧化物以气体形态释放、收集。
12.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,熔盐电解质为cacl2、cacl
2-cao或cacl
2-cao-na2co3。
13.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,恒电压电解的电压设定范围为1~10v。
14.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,恒电压电解的电解温度设定范围为450~960℃。
15.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,第一电解体系中恒电压电解的电解时间设定范围为4~10h。
16.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,第二电解体系中恒电压电解的电解时间设定范围为4~10h。
17.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,通入二氧化碳的流量范围为1~10cm3/s。
18.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,金属氧化物包括:钛、锆、铪、钽、铌、钒、钼、钨、铼、铬或镍的氧化物。
19.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,金属电极包括:钛、锆、铪、钽、铌、钒、钼、钨、铼、铬或镍电极。
20.一些实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,金属电极的金属与金属氧化物中的金属为同一种金属元素。
21.本技术实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法将二氧化碳气体作为反应物加入熔盐电解体系,二氧化碳在熔盐中转化为碳酸根离子,碳酸根离子进一步在阴极上还原为单质碳,金属氧化物脱除部分氧离子,单质碳与脱除部分氧离子的金属氧化物在阴极反应生成金属碳氧固溶体,生成的金属碳氧固溶体进一步被还原,生成高纯金属和二氧化碳气体,生成的二氧化碳可以进一步收集,实现对二氧化碳的循环利用。基于二氧化碳捕获碳化电解精炼高纯金属的方法生产成本低、工艺简单、无污染,在精炼金属领域、二氧化碳的循环利用领域有良好应用前景。
附图说明
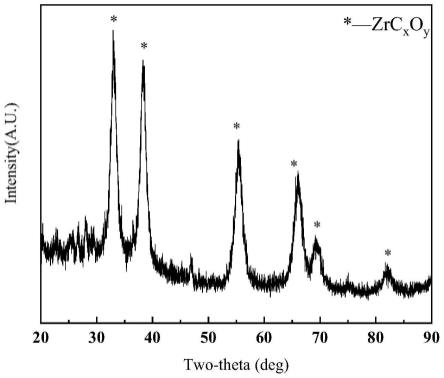
22.图1实施例1第一电解体系电解后第一阴极表面产物的xrd图;
23.图2实施例3基于二氧化碳捕获碳化电解精炼高纯金属的装置组成示意图。
具体实施方式
24.在这里专用的词“实施例”,作为“示例性”所说明的任何实施例不必解释为优于或好于其它实施例。本技术实施例中性能指标测试,除非特别说明,采用本领域常规试验方法。应理解,本技术中所述的术语仅仅是为描述特别的实施方式,并非用于限制本技术公开
的内容。
25.除非另有说明,否则本文使用的技术和科学术语具有本技术所属技术领域的普通技术人员通常理解的相同含义;作为本技术中其它未特别注明的试验方法和技术手段均指本领域内普通技术人员通常采用的实验方法和技术手段。
26.本文所用的术语“基本”和“大约”用于描述小的波动。例如,它们可以是指小于或等于
±
5%,如小于或等于
±
2%,如小于或等于
±
1%,如小于或等于
±
0.5%,如小于或等于
±
0.2%,如小于或等于
±
0.1%,如小于或等于
±
0.05%。在本文中以范围格式表示或呈现的数值数据,仅为方便和简要起见使用,因此应灵活解释为不仅包括作为该范围的界限明确列举的数值,还包括该范围内包含的所有独立的数值或子范围。例如,“1~5%”的数值范围应被解释为不仅包括1%至5%的明确列举的值,还包括在所示范围内的独立值和子范围。因此,在这一数值范围中包括独立值,如2%、3.5%和4%,和子范围,如1%~3%、2%~4%和3%~5%等。这一原理同样适用于仅列举一个数值的范围。此外,无论该范围的宽度或所述特征如何,这样的解释都适用。
27.在本文中,包括权利要求书中,连接词,如“包含”、“包括”、“带有”、“具有”、“含有”、“涉及”、“容纳”等被理解为是开放性的,即是指“包括但不限于”。只有连接词“由
……
构成”和“由
……
组成”是封闭连接词。
28.为了更好的说明本技术内容,在下文的具体实施例中给出了众多的具体细节。本领域技术人员应当理解,没有某些具体细节,本技术同样可以实施。在实施例中,对于本领域技术人员熟知的一些方法、手段、仪器、设备、原料组成、分子结构等未作详细描述,以便凸显本技术的主旨。在不冲突的前提下,本技术实施例公开的技术特征可以任意组合,得到的技术方案属于本技术实施例公开的内容。本技术述及的第一、第二仅为表述不同的部件,并不表示其先后顺序。
29.在不冲突的前提下,本技术实施例公开的技术特征可以任意组合,得到的技术方案属于本技术实施例公开的内容。
30.在一些实施方式中,以金属氧化物为第一阴极、石墨电极为第一阳极、熔盐电解质组成第一电解体系;在熔盐电解质中能够以较低成本捕获和电化学转化二氧化碳,熔融态熔盐电解质具有高离子电导率,有利于生成的离子快速迁移;一般地,含氧离子的熔盐电解质被加热到熔融态后,熔融态电解质中含有氧离子,该氧离子能够与二氧化碳反应生成碳酸根离子,实现对二氧化碳的捕捉;金属氧化物第一阴极电解过程中也释放氧离子,释放的氧离子能够与二氧化碳反应生成碳酸根离子,实现对二氧化碳的捕捉;
31.将熔盐电解质设置在电解池中,根据熔盐电解质的熔点设定电解池的温度,将熔盐电解质熔融;一般地,设定的电解池加热温度高于熔盐电解质的熔点,有利于得到电化学性能优良的电解质;
32.将金属氧化物电极和石墨电极设置在电解池中的熔盐电解质中;
33.将二氧化碳气体通入第一电解体系,调节电解池的电压至预设电压进行恒电压电解;
34.第一电解体系在恒电压电解过程中,二氧化碳在熔盐电解质中反应生成碳酸根离子,生成的碳酸根离子在第一阴极上被还原为单质碳;金属氧化物meo
x
脱除部分氧离子转化为meoz;生成的单质碳和meoz在第一阴极上反应,析出金属碳氧固溶体mecyoz;金属氧化
物中脱除的氧离子部分参与对二氧化碳的捕捉,部分在第一阳极发生氧化,生成氧气;
35.第一电解体系电解过程中发生的化学反应和电化学反应包括:
36.熔盐电解质
ꢀꢀꢀꢀ
co2+o
2-→
co
32-;
37.第一阳极
ꢀꢀꢀꢀꢀꢀ
2o
2-‑
4e
ꢀ→ꢀ
o2;
38.第一阴极
ꢀꢀꢀꢀꢀꢀ
meo
x
→
meoz+(x-z)o
2-;其中x的取值范围为大于1;2co
32-+8e
→
2c+6o
2-;
39.meoz+yc
→
mecyoz,其中y,z的取值范围均为0~1;
40.以形成金属碳氧固溶体的第一阴极为第二阳极,金属电极为第二阴极,与熔盐电解质组成第二电解体系;一般地,以形成金属碳氧固溶体的第一阴极作为第二阳极,通常是指将第一阴极与附着在第一阴极上的金属碳氧固溶体一起作为一个整体作为第二阳极,无需将金属碳氧固溶体剥离;
41.将形成金属碳氧固溶体的第一阴极和金属电极设置在电解池中的熔盐电解质中,并调节电解池的电压至预设电压进行恒电压电解;一般地,第一电解体系的电解过程与第二电解体系的电解过程在同一个电解池中进行;
42.第二电解体系恒电压电解过程中,金属碳氧固溶体被氧化,生成的金属离子迁移至第二阴极,在第二阴极被还原以高纯金属形式析出;在第二阳极上产出二氧化碳或一氧化碳;一氧化碳作为能源气体使用,二氧化碳在收集后实现其循环利用;
43.第二电解体系电解过程中发生的电化学反应包括:
44.第二阳极mecyo
z-e
→
me
+
+cyoz;其中y,z的取值范围均为0~1;
45.第二阴极me
+
+e
→
me;
46.总反应mecyoz→
me+cyoz,
47.在一些实施方式中,熔盐电解质为cacl2、cacl
2-cao或cacl
2-cao-na2co3。
48.作为可选实施方式,选用cacl2作为电解质,cacl2廉价易得,易于与产物分离;cacl2在熔融态下,具有相对热稳定性,粘度小,流动性好,有利于电解过程中产生的气体的排出和电解质成分的均匀化;cacl2对氧离子有较高的溶解度,易于及时溶解电解过程中第一阴极反应得到的氧离子;cacl2导电率高,有利于氧离子在熔盐中的迁移。
49.作为可选实施方式,选用cacl
2-cao作为电解质,cao溶解在cacl2基熔盐中,会大大提高cao循环活性。
50.作为可选实施方式,选用cacl
2-cao-na2co3作为电解质,na2co3溶解在cacl2基熔盐中,能够给第一电解体系提供碳源。
51.通常熔盐电解质在电解进行之前需要经过一定的预处理过程,除去其中的水分,并进行预熔融,使其达到恒电压电解需要的熔融态。
52.作为可选实施方式,熔盐电解质的预处理过程包括:
53.向氧化铝坩埚中加入设定比例的无水cacl2和cao,混合得到熔盐电解质;
54.将熔盐电解质放置在真空中干燥以去除水分,得到预制好的熔盐电解质,备用。
55.作为可选实施方式,熔盐电解质的预处理过程包括:
56.向氧化铝坩埚中加入设定比例的无水cacl2、cao和na2co3,混合得到熔盐电解质;
57.将熔盐电解质放置在真空中干燥以去除水分,得到预制好的熔盐电解质,备用。
58.在一些实施方式中,恒电压电解的电压设定为1~10v。电压的选择与电解质和电
极的种类相关,不同的电解质种类和电极种类所需的电解电压不同,从经济和节能减排的角度考虑适合电解体系的电流效率高电解能耗低的电解电压。
59.在一些实施方式中,恒电压电解的电解温度设定为450~960℃。一般电解温度的选择要考虑到熔盐的电化学窗口、反应过程的中间产物、熔盐对反应物和产物的溶解性、熔盐的环境友好性、挥发性、粘度等。若要发生固态还原反应则反应物和产物都应高于熔盐的工作温度,若是液态沉积反应则选择的熔盐工作温度要比产物的熔点要高。
60.在一些实施方式中,第一电解体系中恒电压电解的电解时间设定为4~10h。电解时间一般不宜过短或过长,电解时间过短可能会导致电解不完全,电解时间过长会增加不必要的能耗、造成资源的浪费。
61.在一些实施方式中,第二电解体系中恒电压电解的电解时间设定为4~10h。
62.在一些实施方式中,通入二氧化碳的流量为1~10cm3/s。二氧化碳连续通入电解体系可以实现对二氧化碳的持续捕捉固定,将二氧化碳的流量控制在合理范围有利于对二氧化碳的完全捕捉,提高捕捉效率。
63.作为可选实施方式,第一电解体系中恒电压电解的电压设定为3v。
64.作为可选实施方式,第一电解体系中恒电压电解的电解温度设定为850℃。一般地,电解温度即为第一电解体系中熔融态电解质的温度,一般地电解温度高于电解质的熔点温度,以便维持其熔融态;例如,电解温度高于电解质的熔点温度50℃以上,可以使熔盐电解质具有良好的导电性、流动性,有利于得到良好的电解效果。
65.作为可选实施方式,第一电解体系中恒电压电解的电解时间设定为8h。
66.作为可选实施方式,第一电解体系中通入二氧化碳的流量为2cm3/s。
67.作为可选实施方式,第二电解体系中恒电压电解的电压设定为3v。
68.作为可选实施方式,第二电解体系中恒电压电解的电解温度设定为850℃。
69.作为可选实施方式,第二电解体系中恒电压电解的电解时间设定为8h。
70.在一些实施方式中,金属氧化物包括:钛、锆、铪、钽、铌、钒、钼、钨、铼、铬或镍的氧化物。上述的金属氧化物具有较高的电子导电性和较低的离子导电性,并且形成的氧化膜层足够稳定,不挥发,不与电解质反应,能够经受足够高的电化学阳极转化,能够很好地保护金属基体。
71.在一些实施方式中,金属电极包括:钛、锆、铪、钽、铌、钒、钼、钨、铼、铬或镍电极。
72.在一些实施方式中,金属电极选用的金属材料与金属氧化物中的金属材料为同一种金属。例如,当金属氧化物为氧化钛时,选用金属钛作为金属电极材料。
73.作为可选实施方式,第一阴极为二氧化锆电极,第二阴极为金属锆电极;金属锆电极不仅具有良好的力学性能和传热性能,金属锆电极表面还能在室温下形成氧化膜,形成的氧化膜使得锆具有优良的抗腐蚀性能。
74.以下结合实施例对技术细节做进一步示例性说明。
75.实施例1
76.实施例1为基于二氧化碳捕获碳化电解精炼高纯金属的方法的电解可行性的验证实验,具体包括:
77.向氧化铝坩埚中加入约150g无水cacl2、1.5gcao,混合均匀得到熔盐电解质;
78.将熔盐电解质放置在300℃的真空环境中干燥12小时以去除水分,得到预制好的
熔盐电解质;
79.将预制好的熔盐电解质设置在电解池中,根据熔盐电解质的熔点设定电解池的温度为850℃,将电解池升温至设定温度,使熔盐电解质转变为熔融态;
80.将二氧化碳通入电解池;待通入二氧化碳半小时,电解池中充满二氧化碳气体后,再将第一阴极二氧化锆电极和第一阳极石墨电极插入熔盐电解质中组成第一电解体系;
81.第一电解体系进行恒电压电解,电解电压设定为3v;
82.观察第一电解体系中的电流变化,第一电解体系电流变化不明显且示数偏低时,停止电解;
83.电解池温度降至室温,取出第一阴极,对第一阴极进行干燥处理,并做xrd图谱分析。
84.图1为实施例1公开的第一电解体系电解后第一阴极表面产物的xrd图。
85.如图1所示,xrd检测结果显示第一阴极上有锆碳氧固溶体生成,说明基于二氧化碳捕获碳化电解精炼高纯金属的方法具有可行性。
86.实施例2
87.实施例2公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,具体包括:
88.以二氧化锆电极为第一阴极、石墨电极为第一阳极、cacl
2-cao为熔盐电解质,组成第一电解体系;
89.将cacl
2-cao设置在电解池中,设定电解池的加热温度为850℃,将电解池加热到850℃,使cacl
2-cao加热转变为熔融态;
90.将二氧化锆电极和石墨电极设置在熔融态cacl
2-cao中,将二氧化碳气体通入第一电解体系,并调节电解池的电压至3v进行恒电压电解;
91.第一电解体系恒电压电解过程中,二氧化碳在熔融态cacl
2-cao中与氧离子反应生成碳酸根离子,生成的碳酸根离子在二氧化锆电极上被还原为单质碳;电解进行8小时;
92.zro2脱除部分氧转化为zroy,脱除的氧离子部分参与在熔盐电解质中捕获二氧化碳,部分在石墨电极反应生成氧气;
93.生成的单质碳和zroy在二氧化锆电极上反应,析出锆碳氧固溶体;
94.第一电解体系中发生的化学反应和电化学反应包括:
95.熔盐电解质
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
co2+o
2-→
co
32-;
96.第一阳极
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2o
2-‑
4e
→
o2;
97.第一阴极
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
zro2→
zroy+(2-y)o
2-;
98.2co
32-+8e
→
2c+6o
2-;
99.zroy+xc
→
zrc
x
oy;x,y的取值范围均为0~1;
100.以形成锆碳氧固溶体的二氧化锆电极为第二阳极,金属锆电极为第二阴极,设置在同一电解池中,组成第二电解体系;
101.保持电解池温度为850℃,cacl
2-cao保持熔融态,并调节电解池的电压至3v进行恒电压电解;
102.第二电解体系电解过程中,锆碳氧固溶体被氧化,生成的锆离子迁移至金属锆电极,在金属锆电极以金属锆形式还原析出;生成的碳氧化物以气体形态释放,收集;电解进行8小时;
103.第二电解体系中发生的化学反应和电化学反应包括:
104.第二阳极
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
zrc
xoy-xe
→
zr
x+
+c
x
oy;
105.第二阴极
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
zr
x+
+xe
→
zr;
106.总反应
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
zrc
x
oy→
zr+c
x
oy;x,y的取值范围均为0~1。
107.实施例3
108.实施例3公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法,在如图2所示的电化学电解装置中进行,该电化学电解装置包括电解池,设置在电解池中的熔盐电解质cacl
2-cao-na2co3,石墨电极graphite、金属氧化物电极meo
x
和金属电极me三个电极设置在熔盐电解质中,三个电极之间根据电解方法需要设置为电连接以组成需要的电解体系,二氧化碳co2通入管的出口端设置在熔盐电解质中以向电解质中通入二氧化碳,同时在电解池中设置有碳氧化物co x
收集管,以便收集第二电解体系电解产生的二氧化碳和一氧化碳;
109.该电解装置中,基于二氧化碳捕获碳化电解精炼高纯金属的方法具体包括:
110.将cacl
2-cao-na2co3设置在电解池中,根据cacl
2-cao-na2co3的熔点设定电解池的温度,将其熔融;
111.将金属氧化物电极、石墨电极、金属电极均设置在电解池中的熔融态cacl
2-cao-na2co3中;
112.以金属氧化物电极为第一阴极、石墨电极为第一阳极,接通两电极之间的电路组成第一电解体系,将二氧化碳气体从管道通入电解池中,调节电解池的电压至预设电压进行恒电压电解;
113.第一电解体系中,二氧化碳在熔融态cacl
2-cao-na2co3中反应生成碳酸根离子,生成的碳酸根离子在金属氧化物电极上被还原为单质碳;金属氧化物脱除部分氧离子;生成的单质碳和脱除部分氧离子的金属氧化物在第一阴极上反应生成金属碳氧固溶体;电解完全后断开电路;
114.以形成金属碳氧固溶体的金属氧化物电极为第二阳极,金属电极为第二阴极,接通两电极之间的电路组成第二电解体系;并调节电解池的电压至预设电压进行恒电压电解;
115.第二电解体系中,金属碳氧固溶体被氧化,生成的金属离子迁移至金属电极,在金属电极被还原以高纯金属形式析出;在碳氧化物阳极上产出二氧化碳或一氧化碳。一氧化碳作为能源气体使用,二氧化碳在收集后实现其循环利用。
116.本技术实施例公开的基于二氧化碳捕获碳化电解精炼高纯金属的方法将二氧化碳气体作为反应物加入熔盐电解体系,二氧化碳在熔盐中转化为碳酸根离子,碳酸根离子进一步在阴极上还原为单质碳,单质碳与金属氧化物在阴极反应生成金属碳氧固溶体,生成的金属碳氧固溶体进一步被还原,生成高纯金属和二氧化碳气体,生成的二氧化碳可以进一步收集,实现对二氧化碳的循环利用。基于二氧化碳捕获碳化电解精炼高纯金属的方法生产成本低、工艺简单、无污染,在精炼金属领域、二氧化碳的循环利用领域有良好应用前景。
117.本技术公开的技术方案和实施例中公开的技术细节,仅是示例性说明本技术的发明构思,并不构成对本技术技术方案的限定,凡是对本技术公开的技术细节所做的常规改
变、替换或组合等,都与本技术具有相同的发明构思,都在本技术权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1