一种基于二维硼碳基材料高效还原二氧化碳的方法
1.本发明属于二氧化碳电催化技术领域,具体涉及一种新型二维硼碳基材料作催化剂高效还原二氧化碳的方法。
背景技术:
2.随着能源匮乏、环境污染等问题的日益加剧,开发先进的催化材料用于清洁能源转换和生态环境保护等领域已成为了人们的关注焦点。多年来,各种类型的催化剂已被充分探索和广泛制备,但大多数催化剂依旧存在成本高昂、催化效率低、污染环境以及稳定性差等问题。因此,开发具有低成本、高性能、环境友好和稳定性好等特性的催化剂有重要意义。
3.目前,来源广泛、环境友好且化学组分可控的二维碳基催化剂引起了广泛的研究。而利用尺寸和厚度工程、相和应变、异质结构建、杂原子掺杂等结构工程设计手段,可以极大的提高二维碳基材料的电催化活性。硼作为一种缺电子元素,在引入二维碳基材料后,会破坏其电子平衡,导致电子重分配,从而在体系内产生催化活性位点。因此,经过结构设计的二维硼碳基材料具有作为高性能电催化剂的潜力。
4.在二氧化碳电还原领域,2015年chemical communications上的文献《metal-free boron-doped graphene for selective electroreduction of carbon dioxide to formic acid/formate》报告了硼掺杂石墨烯在还原二氧化碳方面的催化作用,研究结果表明,硼掺杂石墨烯可以将co2还原为甲酸盐,并且在催化过程中没有明显的降解,保持了结构的稳定。密度泛函理论计算表明,石墨烯中的硼掺杂引入了不对称的自旋密度,提高了co2在硼掺杂石墨烯上的吸附性,从而促进了电催化还原co2的过程。二维硼碳基材料在二氧化碳电催化领域展现出了优秀的催化活性。因此,利用结构工程设计手段调控二维硼碳基材料提升其催化性能,对新型催化剂的研究有着重要的意义。
技术实现要素:
5.本发明提供一种基于二维硼碳基材料高效还原二氧化碳的方法,通过对bc
20
单层的催化还原co2的反应机理以及潜在的her副反应的研究,表明bc
20
电还原co2的最终产物是甲酸,较低的还原电位(0.73v)与较高的副反应自由能变化(+0.17ev)证明了bc
20
作为co2电还原催化剂有良好的催化活性与催化选择性。
6.为实现上述目的,本发明采用的技术方案具体如下:
7.步骤s1:利用vesta软件构建新型二维硼碳基材料(bc
20
)的几何结构;
8.步骤s2:利用步骤s1得到的bc
20
作为基底,构建co2还原过程中的初态、中间体、末态吸附结构;
9.步骤s3:利用vienna ab initio simulation package(vasp)软件对步骤s2构建的吸附结构进行第一性原理结构优化计算,得到合理的吸附构型,并获取体系基态能量;
10.步骤s4:利用vasp软件对步骤s3优化后的结构进行振动频率计算,获得各个中间
产物的零点能;
11.步骤s5:对步骤s3、s4的计算结果进行处理,通过吉布斯自由能公式得到二氧化碳电催化各步骤的吉布斯自由能变化。
12.步骤s6:对步骤s5的吉布斯自由能变化做比较,找出最佳的催化反应路径,得出最低的还原电势。
13.进一步地,所述步骤s2中构建co2还原过程中初态、中间体、末态吸附结构的具体操作为:co2的催化还原过程可以理解为co2不断质子化的过程。首先是co2吸附到基底上形成初态结构,接着质子与氧原子结合形成中间体*ocho,然后质子再与碳原子结合形成中间体*och2o,随后质子与*och2o结合形成*ohch2o,潜在的末态结构为hcooh吸附到基底上。
14.进一步地,所述步骤s3中,*och2o中间体与bc
20
基底上的硼原子间距达到了意味着此时发生了较弱的吸附,*och2o中间体能脱附形成潜在的催化产物hcooh。
15.进一步地,所述步骤s4中振动频率计算的具体操作为:固定基底bc
20
,放开吸附的中间体,只考虑吸附物的振动频率进行计算。
16.进一步地,所述步骤s5中,吉布斯自由能的计算结果表明co2还原路线中的第一次电子转移形成了*ocho,自由能变化为+0.73ev,为吸热反应,在第二次电子转移中*ocho加氢形成*och2o的过程是放热的,自由能变化为-0.72ev。
17.进一步地,所述步骤s6中,发现co2还原路线中的第一次电子转移构成了势能决定步骤,bc
20
单层能在-0.73v下将co2催化还原为hcooh。
18.相比现有技术,本发明的有益效果如下:
19.本发明利用新型二维硼碳基材料作为还原二氧化碳的催化剂,相较传统催化剂,硼碳基催化剂有着价格低廉,环境友好,组分可控等特点,同时还原电位与金属基催化剂相当,低于石墨烯类催化剂。因此能将二氧化碳在较低的还原电位与较少的副反应下还原为工业原料甲酸,实现二氧化碳的高效处理。
附图说明
20.图1为“formate”路线中的中间体结构。
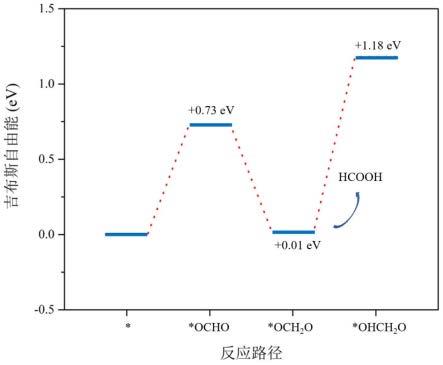
21.图2为“formate”路线的吉布斯自由能反应能谱图。
22.图3为“co-hydro”路线的中间体结构。
23.图4为“co-hydro”路线的吉布斯自由能反应能谱图。
24.图5为h*在bc
20
表面的吸附构型。
25.图6为bc
20
表面析氢反应的吉布斯自由能反应能谱图。
具体实施方式
26.下面结合附图和具体实施例进一步说明本发明的技术方案。
27.实施例1:
28.步骤1:利用vesta软件设置的真空层,构建新型二维硼碳基材料(bc
20
)的几何结构,其晶格常数为γ=73.19
°
。
29.步骤2:利用步骤1得到的bc
20
作为基底,构建co2还原过程中的初态、中间体、末态
吸附结构。在co2电还原过程中,其中一条反应路径为“formate”路线:首先是co2吸附到基底上形成初态结构,接着质子与氧原子结合形成中间体*ocho(*+co2+h++e
‑→
*ocho),然后质子再与碳原子结合形成中间体*och2o(*ocho+h++e
‑→
*och2o),随后质子与*och2o结合形成*ohch2o(*och2o+h++e
‑→
*ohch2o),潜在的末态结构为hcooh吸附到基底上。
30.步骤3:利用vienna ab initio simulation package(vasp)软件对步骤2构建的吸附结构进行第一性原理结构优化计算,得到合理的吸附构型,如图1所示。从图中可以看到,由于硼作为杂原子引入石墨烯中,破坏了原本石墨烯的电子平衡,导致电子重分配,在硼原子附近产生了催化活性位点。*ocho和*ohch2o两种中间体与bc
20
基底上的硼原子间距分别为并且基底表面发生了形变,表明这两个中间体存在较强的吸附作用。而*och2o中间体与bc
20
基底上的硼原子间距达到了相比于其他的中间体,意味着此时发生了较弱的吸附,*och2o中间体变成了催化产物hcooh逐渐脱附基底。最后从优化结果中获取体系基态能量记为e。
31.步骤4:将步骤3优化后的结构固定基底bc
20
,放开吸附的中间体,只考虑吸附物的振动频率,利用vasp软件进行计算,获取中间体的零点能,记为e
zpe-ts。
32.步骤5:对步骤3、4的计算数据进行处理,通过吉布斯自由能公式:δg=δe+δe
zpe-tδs,其中t=298.15k,得到二氧化碳电催化各步骤的吉布斯自由能,如图2所示。吉布斯自由能的计算结果表明co2还原路线中的第一次电子转移形成了*ocho,自由能变化为+0.73ev,为吸热反应,在第二次电子转移中*ocho加氢形成*och2o的过程是放热的,自由能变化为-0.72ev。而后续第三次电子转移形成*ohch2o的过程存在较大的自由能变化,达到了+1.17ev。
33.步骤6:对步骤5中计算出的吉布斯自由能变化做比较,得出结论在“formate”路线中hcooh是最有利的催化产物,第一次质子与氧原子结合形成*ocho的过程为决速步,还原电势为0.73v。
34.实施例2:
35.步骤1:利用vesta软件设置的真空层,构建新型二维硼碳基材料(bc
20
)的几何结构,其晶格常数为γ=73.19
°
。
36.步骤2:利用步骤1得到的bc
20
作为基底,构建co2还原过程中的初态、中间体、末态吸附结构。在co2电还原过程中,另一条反应路径为“co-hydro”路线:首先是co2吸附到基底上形成初态结构,接着质子与氧原子结合形成中间体*cooh(*+co2+h++e
‑→
*cooh),然后质子再与碳原子结合形成中间体*co(*cooh+h++e
‑→
*co+h2o),随后质子与*och2o结合形成*cho(*co+h++e
‑→
*cho),潜在的末态结构为cho吸附到基底上。
37.步骤3:利用vienna ab initio simulation package(vasp)软件对步骤2构建的吸附结构进行第一性原理结构优化计算,得到合理的吸附构型,如图3所示。从图中可以看到,由于硼作为杂原子引入石墨烯中,破坏了原本石墨烯的电子平衡,导致电子重分配,在硼原子附近产生了催化活性位点。三种中间体的硼碳键长度分别为较短的b-c键与基底表面发生的形变说明了三者的化学吸附优先于物理吸附,潜在还原产物cho难以脱附基底。最后从优化结果中获取体系基态能量记为e。
38.步骤4:将步骤3优化后的结构固定基底bc
20
,放开吸附的中间体,只考虑吸附物的
振动频率,利用vasp软件进行计算,获取中间体的零点能,记为e
zpe-ts。
39.步骤5:对步骤3、4的计算数据进行处理,通过吉布斯自由能公式:δg=δe+δe
zpe-tδs,其中t=298.15k,得到二氧化碳电催化各步骤的吉布斯自由能,如图4所示。co2加质子形成*cooh的自由能变化为+0.88ev,下一步质子化后自由能变为+0.50ev,意味着反应放热自发进行。
40.步骤6:对步骤5中计算出的吉布斯自由能变化做比较,显然,co2质子化形成*cooh的自由能变化高于案例1中的*ocho,意味着在co2第一次质子化时,在热力学上更倾向于*ocho。产生这种现象的原因可能是硼是一种缺电子元素,会吸引富电子的元素。相比碳元素,氧作为一个电负性更强的元素可以更多地把电子从硼原子中拉走,从而形成一个比b-c键更强的b-o键。通过对两条不同催化路线的对比,发现案例1所述的“formate”路线是更高效的反应路径。
41.实施例3:
42.步骤1:利用materials studio软件设置的真空层,构建新型二维硼碳基材料(bc
20
)的几何结构,其晶格常数为γ=73.19
°
。
43.步骤2:利用步骤1得到的bc
20
作为基底,构建析氢反应过程中的初态、中间体、末态吸附结构。首先是h
+
吸附到基底上形成初态结构,接着质子与h
+
结合形成中间体h*,最后质子再与h*结合形成末态结构h2。
44.步骤3:利用vienna ab initio simulation package(vasp)软件对步骤2构建的吸附结构进行第一性原理结构优化计算,得到合理的吸附构型,如图5所示,b
–
h键的键长为说明发生了较为稳定的化学吸附。从优化结果中获取体系基态能量记为e。
45.步骤4:将步骤3优化后的结构固定基底bc
20
,放开吸附的中间体,只考虑吸附物的振动频率,利用vasp软件进行计算,获取中间体的零点能,记为e
zpe-ts。
46.步骤5:对步骤3、4的计算数据进行处理,通过吉布斯自由能公式:δg=δe+δe
zpe-tδs,其中t=298.15k,得到析氢反应各步骤的吉布斯自由能,如图6所示。从*到h*的过程是吸热的,
△
g=0.17ev,意味着h*的吸附不能自发反应。
47.步骤6:对步骤5中计算出的吉布斯自由能变化做比较,cu(211)作为经典的co2电催化剂,其副反应为析氢反应,
△
g=-0.03ev,为放热反应,h*的吸附为自发过程。与cu(211)相比,bc
20
单层的副反应更难以发生,说明了bc
20
作co2还原电催化剂具有更好的催化选择性和更高的副反应热力学势垒。
48.基于二维硼碳基材料高效还原二氧化碳的方法包括但不限于以上实例。
49.以上所述仅为本发明的实施例,并非因此而限制本专利的范围,凡是利用本发明书和附图内容所做的等效结构和方法,均同理包含在本发明的专利保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1