一种实时精准控制观测点动态生化因子浓度的微流控芯片的制作方法
本发明属于细胞生物学实验装置领域,是基于流体力学和微流控芯片技术的用于观察、检测动态浓度生化因子刺激下细胞生物学效应的实验装置,具体为通过控制流量波形实时精准控制微通道观测点处生化刺激因子浓度的微流控芯片。
背景技术:
细胞微环境和细胞的相互作用在近年来成为细胞生物学领域的研究热点之一。观察、检测细胞在动态浓度的生化因子刺激下所产生的一系列变化是研究细胞微环境和细胞相互作用的常用手段之一。微流控芯片以其独有的优势成为模拟细胞动态微环境的理想实验平台,在细胞生物学研究领域中具有广泛的应用。现有的研究多数是通过调节微通道入口的动态生化因子浓度,经过微通道流场传输后达到控制、改变观测点处动态浓度的目标;然而,生化因子浓度波形在微流通道传输过程中不仅会发生衰减、滤波以及非线性幅频调制现象,而且会产生波形延迟,造成入口输入波形在观测点处动态浓度波形的失真和滞后,无法实现观测点动态浓度波形的实时、精准控制。因此,需要一种能够实时、精准控制观测点处生化因子动态浓度波形的微流控芯片。
技术实现要素:
本发明的目的在于提供一种通过流量法实时、精准地控制微流通道观测点处动态浓度波形的微流控芯片。通过流量法,单纯的控制不同入口的流量即可实时、精准地控制不同感兴趣观测点处的浓度,且浓度变化与y型微流控装置下端入口与上端入口的流量比间具有线性关系。
本发明的技术方案如下:
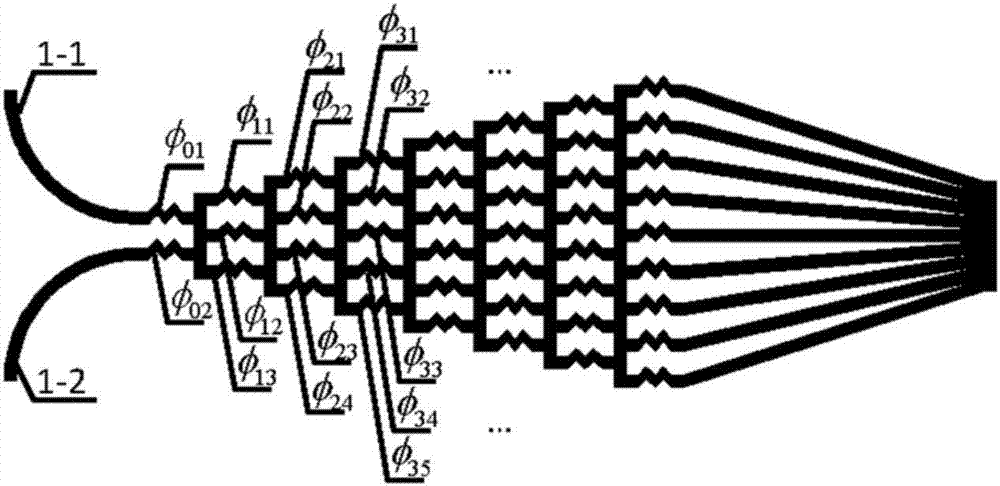
一种通过流量法实时、准确地控制观测点生化因子动态浓度波形的微流控芯片,其在结构上可以分成两部分,一是对传统“圣诞树”状空间浓度梯度生成器改进的装置a,二是y型微流控装置b,如图1所示。其中,改进的“圣诞树”状空间浓度梯度生成装置的出口1-3与y型通道的入口2-1连接,y型通道的入口2-2通入无溶质的缓冲液(即浓度为零),这样便可在y型主通道2-3内形成上下两层、空间上浓度存在梯度分布,即,上层为具有空间近似线性浓度梯度的溶液,下层是缓冲液,浓度恒为零。
本发明中,改进的“圣诞树”状浓度梯度生成装置是在传统“圣诞树”结构的基础上进行改良设计的,旨在空间上形成线性的浓度梯度。传统“圣诞树”状单调浓度梯度生成装置,以七级九分叉的结构为例(图2),其在空间上形成单调浓度梯度的原理如下:设入口1-1注入含有溶质(如生化刺激物、荧光素等)的溶液,假定初始浓度φ01为1;入口1-2注入不含溶质的溶剂(如pbs缓冲液等),则初始浓度φ02为0。根据物质守恒和浓度扩散原理,在“圣诞树”的第一级各分支处的浓度值为:
这样,第二级各分支处浓度大小为:
以此类推,第三级各分支处浓度分别为φ31=1、
进一步地,为了在空间上形成线性分布的浓度梯度,在传统设计的基础上对“圣诞树”状结构加以改进。改进的浓度梯度生成装置与传统结构的主要区别在于最后一级各分支通道的宽度,通道宽度不再保持一致。具体改进方法如下:以归一化空间距离xn作为横坐标,归一化浓度φ作为纵坐标,传统结构中最后一级各分支通道的宽度相等,则对应坐标点分别为(0,1)、
以此方法,就可以计算出每阶台阶的宽度,即可确定最后一级各分支通道的宽度比例关系。经过计算,对于图2所示的七级九分叉的“圣诞树”状结构,其最后一级各分支通道的比例关系为1:8:28:56:70:56:28:8:1,以此确定归一化距离与归一化浓度间的关系如图3所示。这样,由于分子扩散现象,经过一段距离的传输后,便会在纵向上形成线性的浓度梯度,最终得到了图1所示改进的“圣诞树”状空间线性浓度梯度生成装置a。
另外,对于高度远小于宽度和长度几何尺寸、且几何尺寸在微米和毫米量级的y型微通道内的流体表现为层流特性,流体在y轴方向的运动和变化可以忽略,定常流或脉动流条件下溶液在y型主通道2-3内的流速均可用泊肃叶定律近似表达为:
其中p为压强,μ为溶液粘度系数。对上式沿z轴方向积分,可得到单位宽度的流量q满足:
在假设注入入口2-1的溶液1和入口2-2的溶液2的粘度系数近似相等的情况下,溶液1和溶液2在单位宽度上的流量相等,即:
其中q1和q2分别表示溶液1和溶液2的流量,w1和w2则分别表示溶液1和溶液1在y型主通道2-3内所占的宽度。
由以上推导可知,在y型主通道2-3溶液1和溶液2的流场分界线与两者的流量比有关,控制该流量比即可改变流场分界线的位置。也就是说,保持浓度梯度生成装置a的入口1-1和入口1-2的流量不变,即y型通道入口2-1的总流量不变,通过改变入口2-2的流量便能够控制上层浓度空间线性分布的溶液与下层浓度为零的缓冲液的分界线上下移动。假定选择的观测点为y型主通道2-3中轴线上的一点(其他点亦可),保持浓度梯度生成装置a入口1-1的流量q1-1和入口1-2的流量q1-2均保持不变(亦可变化),则其出口1-3的总流量不变,即流入y型通道上端入口2-1的流量q1不变,q1=q1-1+q1-2。在这种条件下,通过改变y型通道下端入口2-2的流量q2即可控制分界线的纵向位置,进而改变观测点处浓度。当y型通道下端入口2-2的流量大于或等于上端入口2-1的流量时,即q2≥q1,y型主通道2-3内具有空间线性浓度梯度的上层溶液与浓度为零的下层溶液间的分界线位于主通道2-3中轴线(图4点划线)的上方或刚好处于此中轴线上,此时观测点处的浓度为零;反之,分界线则位于中轴线的下方,即图4所示情况,则观测点的浓度将随着流量q2的变化而变化。
当q2<q1时,为计算观测点处浓度与y型通道下端入口2-2流量q2间的数值关系,建立如图4所示的平面直角坐标系,原点位于y型主通道2-3内上层溶液与下层溶液的分界线上,主通道2-3位于y∈[-w2,w1]的区间内,则中轴线位于
因此,观测点处的浓度即可求得:
即,当q2<q1时,观测点处的浓度φd与y型通道下端入口2-2的流量q2呈线性反比关系。
综上,可得观测点处的浓度大小φd与y型通道上端入口2-1的流量q1和下端入口2-2的流量q2间的关系如下:
由此,根据公式(8),通过控制y型通道下端入口2-2的流量即可控制不同观测点处的动态浓度波形。
本发明可实现对不同观测点处动态浓度波形实时、准确的控制,有效消除常规方法存在的时间延迟、幅值衰减、非线性幅频调制等不足之处,可用于观察、检测不同动态浓度生化因子刺激下的细胞生物学效应。
附图说明
图1是微流控芯片结构图。
图2是传统“圣诞树”状空间单调浓度梯度生成装置示意图。
图3是七级九分叉的传统与改进的“圣诞树”状浓度梯度生成装置产生的浓度梯度与理想线性浓度梯度对比图。
图4是y型主通道2-3内溶液分层情况。
图5是实验系统示意图。
图6是在观测点实现的“w”字形动态生化因子浓度波形。
图中的具体标注如下:
图中:
a改进的“圣诞树”状空间线性浓度梯度生成装置;by型微流控装置;
1-1含有某溶质(如生化刺激物、荧光素等)的溶液入口;
1-2浓度为零的溶剂入口;1-3空间上具有类线性浓度梯度溶液汇合出口;
2-1空间上具有类线性浓度梯度溶液入口;2-2浓度为零的溶剂入口;
2-3主通道;
(i)可编程注射泵流动控制系统;(ii)微流控芯片;
(iii)激光共聚焦或荧光显微镜;(iv)计算机显示系统;(v)废液回收处理。
i-1含有某溶质(如生化刺激物、荧光溶液等)的溶液;
i-2浓度为零的溶剂;i-3浓度为零的溶剂。
具体实施方式
图1所示为一种通过流量法实时精准地控制观测点处动态浓度波形的微流控芯片结构图,主要由两个部分结构组成:改进的“圣诞树”状空间线性浓度梯度生成装置a和y型微流控装置b,包括含有某溶质(如生化刺激物、荧光溶液等)的溶液入口1-1,浓度为零的溶剂入口1-2,空间上具有类线性浓度梯度溶液出口1-3,空间上具有类线性浓度梯度溶液入口2-1,浓度为零的溶剂入口2-2和主通道2-3;其中,出口1-3与入口2-1连接。芯片所有通道结构采用标准化的微加工方法,用pdms制作完成,并与洁净玻璃片键合密封,构成常见的玻璃-pdms芯片。
本实施例中,微流控芯片内部的所有通道高度均为30μm,改进的“圣诞树”状空间线性浓度梯度生成装置a内除最后一级分叉通道外,其余微通道宽度均为0.2mm,最后一级分叉通道根据上述计算结果1:8:28:56:70:56:28:8:1的比例进行设置,最终汇合出口1-3的宽度为1.8mm;y型微流控装置b中,入口2-1的宽度与汇合出口1-3保持一致,入口2-2宽为1.5mm,主通道长为20mm,宽为3.6mm。
本实施例中,该微流控芯片与可编程注射泵、激光共聚焦(或荧光)显微镜、计算机构成了完整的空间线性浓度生成、控制与检测系统(图5)。装有荧光溶液的注射器i-1、装有细胞缓冲液(浓度为零)的注射器i-2与i-3分别与芯片的入口1-1、入口1-2与入口2-2连接,并将所有注射器与可编程注射泵相连。通过注射泵控制三个入口的流量q1-1、q1-2和q2,本实施例中控制流量q1-1、q1-2保持不变,恒等于10μl/min;改变流量q2,使其按照图6所示的“m”字波形变化。然后,利用摄像机拍摄通道内荧光强度情况,选定一感兴趣的观测点,本实施例中选取主通道中轴线上任意一点作为观测点,采用图形分析方法对其进行灰度提取,用灰度数据表征荧光强度,即可得到观测点处浓度随时间变化情况,如图6所示的“w”字形动态生化因子浓度波形。本发明可根据研究需要,选择不同的生化刺激因子,并且依照需要使流量随时间发生动态变化,实现实时、精准地控制感兴趣观测点处的动态浓度波形,可用来观察、检测不同动态浓度生化因子刺激下细胞生物学效应。
- 还没有人留言评论。精彩留言会获得点赞!