中空柱液相色谱系统和使用该系统进行的物质分离的制作方法
本发明涉及一种使用中空柱液相色谱进行的物质分离分析方法。
背景技术:
色谱法,作为一种分离分析手段,是一种通用的可以用在几乎所有领域如医学、工学、药学、医学,可以说是支持目前科学研究和社会生活的基础技术之一也并不夸张。随着社会和科技的发展,虽已实现更高灵敏度、高选择性、高降解性、高速、自动化和小型化,但在生命科学和纳米技术领域,期望更好的分离分析方法。例如,近年来,在对环境样本和生物样本进行分析时,为了减轻环境压力提高分离能力,特别是小分子量化合物,更期待高分子化合物、纳米粒子的高效分离提纯方法。
(1)已提出环保化学的理念,期待一种和该理念相应的利于环保的中空柱液相色谱。
(2)蛋白质是一种由氨基酸残基组成的聚合物,具有线状结构,所述线状被折叠以形成特定结构,在活体内起到重要的作用。另一方面,已经发现许多例子是由于折叠不能精确地进行或由于所形成的结构的变形而引起了疾病。在最近的新药中,使用称为蛋白质制剂的蛋白质的药物比例正在迅速增加,并且预计该比例将来会进一步增加。当蛋白质保持其原本结构时,蛋白质制剂表现出所需的功效,但由于结构的变化,它不但没有药效,而且还可能使疾病恶化。尽管蛋白质的结构与功能密切相关,但是存在蛋白质吸附到常规液相色谱中使用的柱中填充的填料的问题(参考非专利文献1和非专利文献2)。在传统的液相色谱中,不可能在保持其结构的同时分离和分析蛋白质。
(3)已知所谓的折叠疾病如阿尔茨海默氏病和朊病毒病是由于组织中包含的蛋白质结构的变化导致的异常聚集引起的。例如,怀疑与阿尔茨海默氏病的发病密切相关的β淀粉样蛋白形成不同的结构,已知每种结构具有不同的物性,例如毒性。由于在蛋白质聚集过程中产生的中间体的尺寸大到几nm到十几μm,它不能从通用柱中的填料之间的间隙通过,因此,不能对其进行分析。此外,可以预计,由于蛋白质被柱内的填料吸附而导致结构发生变化。
现有技术文献
非专利文献
非专利文献1:goda,r.etal.,biomedicalchromatography2007,21(10),1005-1015.
非专利文献2:goda,r.etal.,journalofchromatographyb-analyticaltechnologiesinthebiomedicalandlifescience2012,895,137-145.
技术实现要素:
本发明要解决的问题
本发明的目的为提供一种液相色谱系统,其采用了未填充填料的长柱并利用弱填充力,使用传统的液相色谱系统的情况下由于分离作用力小而不能分离的物质通过本发明的液相色谱系统能够进行分离。
解决问题的手段
液相色谱法是一种分离方法,利用流动相进入固相时每种物质移动速度的差异。通常,固相作为填料填充在柱中。为实现分离,需要各种调节主要的固相和流动相。例如,关于固相,材料、表面改性、尺寸、形状、表面积等会影响分离能力。特别是使用何种填料是很重要问题。另一方面,关于流动相,流动相的组成和组分的分配比是影响分离的分离影响因子。为实现良好的材料分离,必须适当地调整固相和流动相的上述因子。
本发明人对去除了填料、并且流动相不会成为较大的分离影响因子的液相色谱分离方法进行了深入研究。结果,开发了一种能够在不考虑分析条件的情况下分离物质分离方法。
在不考虑填充剂和流动相的分离因子的情况下,用于分离的柱和要从流动相中分离的物质之间的相互作用变弱而不能实现分离,这一点也想到过。
然而,本发明人发现了一种系统,该系统能够利用待分离物质与柱内壁之间较弱的相互作用和流体力学的流动影响来分离物质。根据本发明的方法,预计可以使用任何流动相。此外,通过延长柱的长度可以解决分离所需的相互作用较弱的问题,可以提高分离物质的能力。通过增加柱的长度,可以增加分离所需的相互作用发生的频率。即使待分离的物质之间的移动速度差很小,但是,由于理论塔板数增加,也能够把现有方法难以分离的物质的检测峰分开。
此外,将本发明的分析系统微量化的结果,能够减少溶剂的使用量,进一步,还可以不使用有机溶剂,而使用纯水或磷酸盐缓冲生理盐水(pbs)等作为流动相,可以实现环境负担较小的分析。
即,本发明如下所述。
[1]一种用于分离生理活性物质的液相色谱系统,其至少具备中空柱,所述中空柱为没有被填料填充的由未经处理的石英硅或天然石英制成的中空毛细管柱,控制生理活性物质与中空柱的内部表面之间的静电相互作用。
[2]如[1]所述的液相色谱系统,其中,通过调节柱的长度、柱的内径以及流动相的离子强度来控制生理活性物质与中空柱的内部表面之间的静电相互作用。
[3]如[1]或[2]所述的液相色谱系统,其中,进而通过改变选自流速、流动相粘度和柱温度的条件来控制生理活性物质与中空柱的内部表面之间的静电相互作用。
[4]如[1]至[3]中任一项所述的液相色谱系统,其中,中空柱为熔融石英二氧化硅或掺杂石英二氧化硅。
[5]如[1]至[4]中任一项所述的液相色谱系统,其中,中空柱的长度为3-100m。
[6]如[1]至[5]中任一项所述的液相色谱系统,其中,用纯水或磷酸盐缓冲生理盐水作为流动相。
[7]如[1]至[6]中任一项所述的液相色谱系统,其中,流动相通过柱的流速为1.3-89mm/sec(0.039-2.6μl/min)。
[8]如[1]至[7]中任一项所述的液相色谱系统,其中,用磷酸盐缓冲生理盐水作为流动相来分解蛋白质。
[9]如[1]至[8]中任一项所述的液相色谱系统,其中,用水作为流动相来分离高分子物质。
[10]一种生理活性物质分离分析方法,其中,用[1]至[9]中任一项所述的液相色谱系统对生理活性物质进行分离分析
[11]一种生理活性物质分离分析方法,其利用液相色谱系统对生理活性物质进行分离分析,所述液相色谱系统至少具备中空柱,其中,中空柱为没有被填料填充的由未经处理的石英硅或天然石英制成的中空毛细管柱,通过控制生理活性物质与中空柱的内部表面之间的静电相互作用,从而对生理活性物质进行分离分析。
[12]如[11]所述的生理活性物质分离分析方法,其中,通过改变柱的长度、柱的内径、流动相的离子强度来控制生理活性物质与中空柱的内部表面之间的静电相互作用。
[13]如[11]或[12]所述的生理活性物质分离分析方法,其中,进而通过改变选自流速、流动相粘度和柱温度的条件来控制生理活性物质与中空柱的内部表面之间的静电相互作用。
[14]如[11]至[13]中任一项所述的生理活性物质分离分析方法,其中,中空柱为熔融石英二氧化硅或掺杂石英二氧化硅。
[15]如[11]至[14]中任一项所述的生理活性物质分离分析方法,其中,中空柱的长度为3-100m。
[16]如[11]至[15]中任一项所述的生理活性物质分离分析方法,其中,用水、磷酸盐缓冲生理盐水或氯化钠溶液作为流动相。
[17]如[11]至[16]中任一项所述的生理活性物质分离分析方法,其中,流动相通过柱的流速为1.3-89mm/sec(0.039-2.6μl/min)。
[18]如[11]至[17]中任一项所述的生理活性物质分离分析方法,其中,用水作为流动相来分离高分子物质。
发明效果
通过使用本发明的具有中空柱的液相色谱系统,可以利用弱作用力分离不能通过现有系统予以分离的物质。
当使用纯水或磷酸盐缓冲生理盐水作为流动相时,可以不必通过改性而完整地将待分离物质分离提纯。
附图说明
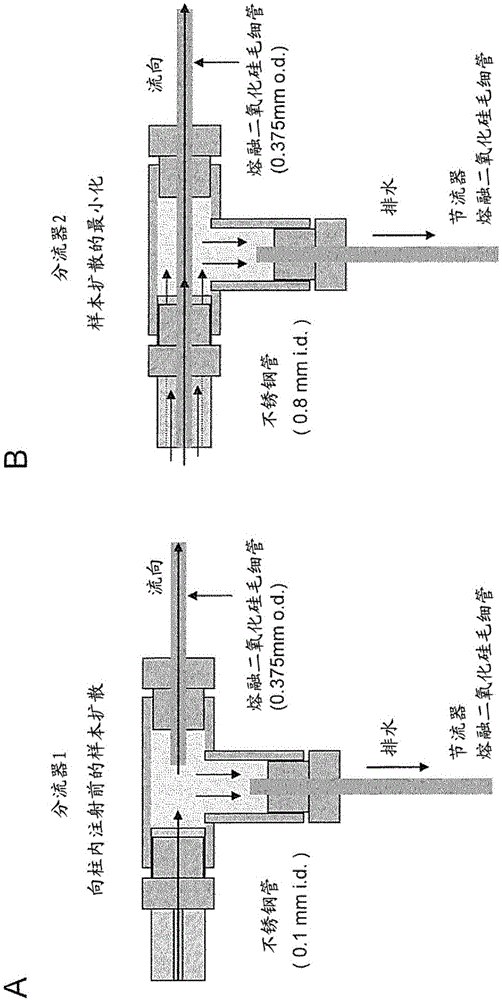
图1是表示所用分流器的结构图。
图2是表示所用液相色谱系统的概要图。
图3是表示分流器的分流效果图。
图4是表示中空柱的长度对柱内输送流速和柱内样本注入量的影响的图。
图5是表示色谱柱的理论塔板数、色谱柱长度和线性流速的关系的图。
图6是表示通过使用液相色谱系统1和系统2分析所获得的色谱图的比较图。
图7是表示通过使用液相色谱系统2和系统3分析所获得的色谱图的比较图。
图8是表示在液相色谱系统2中利用具有不同内径的中空柱分析的色谱图的比较图。
图9是表示在液相色谱系统2中使用具有不同长度的中空柱分析的色谱图的比较图。
图10是表示对柱的内径和长度研究的结果的概要图。
图11-1是表示低分子中性硫脲和低分子量带电物质分离结果的图。
图11-2是表示低分子量带电物质的相对保留时间的图。
图12-1是表示从硫脲中分离具有不同分子量和电荷数的fitc-葡聚糖的结果的图。
图12-2是表示各分子量的fitc-葡聚糖相对于硫脲的相对保留时间的图。
图13是表示所使用的异硫氰酸荧光素(fitc)-葡聚糖的特性的图。
图14是表示dna、罗丹明b和分子量标记的分离结果的图。
图15是表示低分子物质和高分子物质同时分离的结果的图。
图16是表示流动相的盐浓度对分离的影响的图。
图17是表示盐浓度对相对保留时间的影响的图。
图18是表示中空柱的内壁与待分离物质之间的相互作用的图。
图19是表示当磷酸盐缓冲生理盐水(pbs)用作流动相时蛋白质分离的结果的图。
图20是表示蛋白质的相对保留时间、理论塔板数和等电点(pi)的关联的图。
图21是表示四种样本的同时分析的结果的图。
图22是双电层厚度与负电荷物质从管内壁排除的距离的比较图。
图23是基于层流特性的溶出时间模型图,通过雷诺数评估柱中的流动状态。
图24是表示柱中负电荷物质的分布的图。
图25是表示研究物质的特性的图。
图26是表示基于分子量计算的粒度(图25)与相对保留时间之间的理论关系的图。
图27是表示从管内壁排除的距离x与柱长之间的关系的图。
图28是表示柱内径与相对保留时间之间的关系的图。
图29是表示从管内部排除的距离x与柱内径之间的关系的图。
图30-1是基于流动相的nacl浓度的4kdafitc-葡聚糖和硫脲的分离色谱图。
图30-2是基于流动相的nacl浓度的40kdafitc-葡聚糖和硫脲的分离色谱图。
图30-3是基于流动相的nacl浓度的500kdafitc-葡聚糖和硫脲的分离色谱图。
图30-4是基于流动相的nacl浓度的2000kdafitc-葡聚糖和硫脲的分离色谱图。
图31是表示盐浓度和相对保留时间之间的关系的图。
图32是表示从管内壁排除的距离x与流动相nacl浓度之间的关系的图。
图33是表示在高浓度nacl的分析条件下fitc-葡聚糖的粒度与相对保留时间之间的关系的图。
图34是表示温度和相对保留时间之间的关系的图。
图35是表示从管内壁排除的距离x与柱温之间的关系的图。
图36是通过分析刀豆蛋白a和罗丹明b的混合样本所获得的色谱图。
图37是通过分析过氧化氢酶和罗丹明b的混合样本所获得的色谱图。
具体实施方式
本发明是生理活性物质提纯工艺中使用的液相色谱系统。本发明的液相色谱系统至少包括中空柱,还可以进一步包括微型泵、分流器(splitter)、检测部和连接部等。
用于本发明的中空柱是未填充填料的柱,是尚未经过修饰处理的未处理中空柱,所述修饰处理例如为将固相负载在内壁上的处理。它也可以称为中空柱或中空毛细管柱。
该柱由石英二氧化硅或天然石英制成,优选由石英二氧化硅制成。更优选由熔融石英二氧化硅(石英玻璃)或掺杂石英二氧化硅制成的柱。
作为中空柱,可以使用市售的熔融石英二氧化硅(石英玻璃)或由掺杂石英二氧化硅制的毛细管,例如,可以使用“polymicrotechnologies”(商标)毛细管(phoenix,az,usa)。
由于在本发明的液相色谱系统中使用的中空柱不含填料,因此将其分离而不会引起填料和待分离物质之间的相互作用,例如,待分离物质被填料吸附。在使用填充有填料的柱的情况下,当要分离诸如蛋白质等的高分子物质时,待分离的物质可能被填料吸附而难以很好地分离,但是,本发明的液相色谱系统没有这样的问题。
本发明的液相色谱系统中采用的中空柱的长度为3-100m,优选3-72m,更优选8-72m。柱可以是直线状,如果比较长,也可以形成为线圈状的柱,以节省安装空间。较长的色谱柱可以提高分离能力。另外,柱优选使用一个连续柱,最好不要在中间具有连接部。通常,使用长柱时,背压会增加。在本发明中,通过使用未填充的中空柱,可以降低背压。
关于本发明的液相色谱系统中使用的中空柱,从背压的观点来看,随着内径增加,供液会更容易。然而,本发明的液相色谱系统中使用的中空柱的分离作用力与内壁的薄层有关,所以柱的内径不重要,可以使用任何内径。然而,当柱的内径为1μm以下时,薄层的厚度不能忽略,容易受内径的影响。因此,优选为1μm以上,进一步优选为5μm以上,更优选为25μm以上。中空柱的内径的上限为50μm,优选为40μm,更优选为30μm。中空柱的内径越小,分离能力越好。
在使用由石英二氧化硅制成的中空柱的情况下,在中空柱的内壁上存在带负电荷的石英玻璃的硅烷醇基(sih3oh-),并且在待分离物质与中空柱内壁的硅烷醇基之间会产生弱的静电荷相互作用。这种弱的相互作用有助于带电物质的溶出,其结果,能够提高中空柱的分离能力。
微型泵是一种以低流速供液的泵,可以最大限度地减少脉冲。微型泵可以使用市售的微型泵。
分流器是将流动相的流分成两个部分的部件。分流器将流动相分成两股流,一股通过分离柱,一股通过泄液柱。可以适当地调节流动相在两股流中的比率。通过使用分流器,可以实现低流速、稳定的高压流。分流器可以用市售的液相色谱系统用的分流器。控制分流器中流速的部分称为限流器(restrictor)。
检测部中具备检测单元,通过中空柱后被分离的物质从上述检测单元中通过,通过吸光光度计检测器或荧光检测器测定和量化从检测单元内通过的物质的吸光度和荧光等。检测单元的内径优选小于中空柱的内径。
连接部是连接各部件的部分。
而且,本发明的液相色谱系统可包括自动进样器。市售自动进样器的精密注入量为1μl以上,优选在将nl有序样本引入柱内之前,将自动进样器设置在分流器前。
在使用中空柱的情况下,使用上述微型泵,分流器等,可以实现微量的供液速度(nl/min)、微量的样本注入(nl/注射)、死体积的最小化以及样本扩散的最小化等。
作为流动相,可以使用任何流动相,只要它是可用于液相色谱的流动相即可。可以根据分析目的自由使用。例如,可例举纯水或磷酸盐缓冲生理盐水(pbs)。也可以使用盐溶液,例如氯化钠(nacl)、氯化钾(kcl)、高氯酸钠(naclo4)溶液等。在使用磷酸盐缓冲生理盐水(pbs)或盐溶液的情况下,可以通过改变盐的种类和盐浓度而使流动相的离子强度改变,双电层的厚度改变,进而改变所述分离条件。由于流动相中不包括有机溶剂和表面活性剂,因此待分离的物质不会受到有机溶剂或表面活性剂的改性作用。
本发明的中空柱只通过流入氢氧化钠就可以洗涤,并且可以长时间使用。
本发明的液相色谱系统中的物质分离利用待分离物质与中空柱的内壁之间发生的作用来实现,即,利用其与中空柱的内表面之间的静电相互作用以及流体动力学流动作用来实现。与中空柱的内表面之间的相互作用基于其与中空柱的内壁上的硅烷醇基团之间的弱静电相互作用。关于流体动力学流动,流动相作为层流流动,并且物质分离受层流的影响。层流是指,在流中,液体的每个部分不相互混合而与柱的管轴平行流动的合流。层流越接近柱,则流速越小,柱的中心处流速最大。在柱中不同扩散程度的物质通过层流分离。在柱的内径、流速、流动相的粘度等条件一定的情况下,形成层流。只要使用具有上述内径的柱,就会形成层流。
基于层流特性制备的溶出时间(okadat,2010.j.liq,chromatogr.rel.technol.33:1116-29)示于图3中。通过雷诺数评估柱中的流动状态。由于雷诺数在0.04至0.9的范围内,因此认为柱中的流动是层流。然后基于层流特性评估溶出时间模型。由于内壁附近的流速被认为是0,因此作为中性低分子的硫脲的溶出(流速)是水的平均流速。中心的最大线性流速是平均流速的两倍。在该图中,柱的内径由a表示,注入柱中的样本体积的截面半径由r表示。通过积分求出样本的溶出体积。根据负电荷化合物的溶出和平均流速的比,可以求出r。此外,由a-r表示的距离是样本从内壁排除的距离。
当使用本发明的具有中空柱的液相色谱系统时,物质可以在低压下分离并且可以以低流速分离。因此,可以提高理论塔板数,可以期待分离能力的提高。利用本发明的系统分离物质时的流速为1.3~89mm/sec(0.039~2.6μl/min),在柱内通过分流器分流的样本的注入量为0.20~4.9×103nl。
使用本发明的液相色谱系统时,可以从低分子物质到蛋白质等大分子物质进行广泛分离和分析。特别从待分离物质不改姓这一点来看,适合于生理活性物质的分离,本发明的液相色谱系统可以用于生理活性物质的分离工艺。这里,生理活性物质是指。作用于活体并对各种生物反应进行控制的化学物质,包括低分子物质到高分子物质。生物活性物质也包含蛋白质、dna、rna等核酸、糖、脂质等。
由于本发明的液相色谱系统的柱是不具有填料的中空柱,因此在柱中具有很大的空隙,可以使高分子物质通过。
尤其是也能够分析蛋白质的聚集体,也可以分离蛋白质的聚合物、聚集体和单体。例如,根据本发明的液相色谱系统,可以分离和检测由阿尔茨海默病、朊病毒病等所谓的折叠疾病中的结构变化引起的异常聚集的蛋白质。作为这样的蛋白质可以列举出与阿尔茨海默氏病相关的淀粉样蛋白β(aβ)。健康人体内也存在aβ,并且在日常生活中在体内合成和分泌。但健康人群中aβ不会累积,它会累积在患有阿尔茨海默病的患者身上,从而导致阿尔茨海默病的发病。通过使用本发明的液相色谱系统详细分析aβ的聚合和积累机理,可以认为阿尔茨海默病的发病机制将变得明确。如果可以明确详细的聚合过程并且抑制其反应,则可以抑制阿尔茨海默病的发作。此外,如果可以分解聚合物,则认为可以治疗阿尔茨海默病。
使用本发明的液相色谱系统时,具有电荷的物质可以通过与中空柱的内壁的静电相互作用而分离。
例如,当使用在诸如由熔融石英二氧化硅制的柱等的内壁上具有带负电荷的基团的柱并且使用纯水作为流动相时,具有负电荷的物质在离子排斥效应作用下,具有正电荷的物质在离子交换效应作用下而实现分离。即,中空柱中的双电层变厚,并且带负电的物质被排除在柱的内壁之外并且分布在柱内的中心。这里,双电层是这样的层,其中,在溶液的主体部分之间产生足够远离表面的电位差,在表面上具有离子浓度梯度。图24a表示负电荷较小的物质的分布,图24b表示负电荷较大的物质的分布。如图所示,负电荷较大的物质较早溶出。图24c表示了从流动方向观察的状态。在图24中,外侧的粗线表示柱的管壁,硅烷醇基(sih3oh-)存在于柱的内壁上。在柱的内壁上在带负电的硅烷醇基(sih3oh-)的影响下形成双电层,并且带负电的物质从柱的内壁排除并离开内壁而流过柱的中心附近。箭头表示流动相的流向。平行于柱管壁的细实线表示在该部分中形成双电层。此外,由虚线包围的部分表示了聚集待分离物质的样本区域,并且样本区域中的矩形表示要分离的物质。当盐浓度降低时,双电层变厚,并且当柱的内壁上存在带负电的基团如硅烷醇基时,带负电的物质从柱的内壁离开,分布在柱内的中心。结果,相对保留时间减少。由于柱管中的流体是层流,中心流体的线性流速比内壁附近的线性流速快,因此,由于受到的线性速度的影响,因此分布在中心的物质提前溶出。即,当盐的浓度小时,分离和改善带负电物质的能力增加。当与流动相接触的毛细管内壁相对于流动相的运动连动移动时,从流动相与内壁接触的接触相表面具有一定厚度的层中的溶液由于粘性与接触相一起移动。内壁上存在的双电层(1000nm以内)不容忽视,可视为动态双层而非静态双层。
此外,例如,当使用磷酸盐缓冲生理盐水作为流动相时,离子交换效应施加在带正电的物质如蛋白质上,并按等电点的大小顺序溶出。本发明包括:利用本发明的液相色谱系统,作为流动相使用磷酸盐缓冲生理盐水(pbs)分离蛋白质的方法。
使用磷酸盐缓冲生理盐水或nacl溶液等的盐溶液作为流动相,使用本发明的液相色谱系统分离物质时,可通过改变离子强度来改变分离条件。通过改变流动相的离子强度,改变了双电层的厚度,改变了物质从柱的内壁排除的距离。即,随着盐浓度增加,双电层变薄,与内壁的相互作用变弱,从内壁排除的距离变小。结果,相对保留时间减少溶出更快。此外,当盐浓度变大时,例如,改变具有大分子量的物质的形状(结构),从而将拉伸形状的物质改变为球形。具有球形结构的物质具有较小的粒径和较低的相对保留时间比率。因此,通过改变流动相的盐浓度或通过改变柱温,可以控制待分离物质与柱内壁之间的相互作用,并且可以控制多种物质分离。
在使用本发明的液相色谱系统分离蛋白质的情况下,理论塔板数为10,000以上,这大于使用常规液相色谱系统分离时的理论塔板数。
在使用本发明的液相色谱系统分离物质时,当分离且温度变化时,影响柱温的因素变多,例如,布朗运动、物质本身的结构、物质的表面电荷、物质与内壁之间的相互作用等。通常,希望在低温条件下分析样本,可以在0℃下分析样本。当温度太高时,由于柱的品质也会受到影响,因此优选在约70℃以下的条件进行分析。即,可以通过改变柱温来控制待分离物质与柱内壁之间的相互作用。
当分离蛋白质等高分子物质时,通过共存低分子物质如罗丹明b,而使低分子物质吸附在高分子物质上,延迟保留时间,延迟溶出。这是因为通过低分子物质的吸附改变了高分子物质表面上的电荷或改变了高分子物质的结构,并且通过吸附低分子物质改变了保留时间。即,通过将高分子物质和低分子物质共存,可以控制高分子物质的保留时间。分析共存物质的目的是通过吸附共存物质来微调蛋白质的表面和结构从而改变分离能力。
在本发明的液相色谱系统中,通过调节柱长、柱的内径、流动相的离子强度、流速、流动相的粘度和柱温等,可以控制待分离物质与中空柱的内表面的静电相互作用。
本发明的液相色谱系统是通过利用弱相互作用而分离物质的色谱,可以在维持蛋白质的结构和生理效应的条件进行分离。
另外,本发明涉及一种通过液相色谱分离和分析生理活性物质的方法,其中,通过调节选自柱长、柱内径、流动相的离子强度、柱温的条件,控制活性物质与中空柱内表面的静电相互作用,以分离和分析生理活性物质。
通过以下实施例具体描述本发明,但本发明不受这些实施例的限制。
实施例1具有中空柱的液相色谱系统的构建
在实施例中,使用了以下的液相色谱系统。
系统1:
mp711泵(glscience,东京,日本)
mi709自动进样器(glscience)
从泵到自动进样器的连接l:中空毛细管(内径30μm,0.73m)
amicro21uv-02紫外线阵列探测器(jasco,东京,日本)
hplc系统组织者(ezchromelitev.3.1.7j)
毛细管:polymicro技术(美国亚利桑那州凤凰城)
连接部:glscience
系统2:
mp711泵(glscience,东京,日本)
c4手动进样器(viciag,schenkon,瑞士)
泵与手动进样器之间无连接部,直接连接
电泳系统(agilent7100毛细管电泳系统)
连接部:glscienceptfe管
系统3:
配置:泵ncp-3200rs纳米/帽泵,wps-3000pl(rs)(thermofisherscientific,日本)
注入部:wps-3000fc自动进样器(thermofisherscientific,日本)
从泵到自动进样器的连接l:中空毛细管(内径20μm,1.5m)
检测部:vwd-3100和vwd-3400rs((thermofisherscientific,日本),一种可变波长检测器,能够通过一次色谱记录多个吸收光谱,
检测单元为内径20μm、长度50cm的毛细管)
分流器:t形分流器(lcap分流器,glsciences,日本)
连接部:ptfe管,thermofisherscientific
毛细管:polymicro技术(美国亚利桑那州凤凰城)
系统1和2中使用的分流器1在图1a中表示,在系统3中使用的分流器2在图1b中表示。每个系统的概要如图2所示。图2a表示了系统1,图2b表示了系统2,图2c表示了系统3。
柱由熔融二氧化硅制成,并且使用不含填料的中空毛细管柱。
(1)微量供液(nl/min)和样本注入(nl/注入)
为了进行微量供液(nl/min)和样本注入(nl/注入),使用系统1的液相色谱系统研究了分流器的分流性能。分流器的分流效果如图3所示。如图3所示,分流器的分流比由柱的压力和分流的压力确定。柱和分流器的分流的内径都设为25μm,柱的长度被设定为10m。泵的供液为定值1μl/min,通过将分流器的分流长度从0.5调节至2.3m,可将分流器的分流比率从81%调节至26%,进一步,可以确认毛细管柱内通过的流动相的流速从0.81μl/min调节至0.26μl/min(图3a)。然后,将分流器的分流长度降低到0.1m,通过将泵的供液从7调节至13μl/min,使来自泵的供液从17%调整至11%,此外,证实:柱内通过的流动相的流速调节到0.1μl/min。如此,当泵的供液为9μl/min以上时,再现性良好,分流比恒定,比较稳定(图3b)。
在系统3中,在9-72m的柱长范围内,即使完全除去分流,通过将泵的供液设定为1000μl/min,也能够实现分流器的微量供液(0.04μl/min以上,1.3mm/s),柱内通过的流动相的微量注入量(0.8nl)也能够实现。图4表示了毛细管柱的长度对色谱柱中供液流速和色谱柱内样本注入量的影响。
图5表示了在上述研究中获得的柱的理论塔板数、柱长和线性速度之间的关系。
(2)系统的死体积(deadvolume)的最小化和样本扩散的抑制
为使系统的死体积最小化,并最大限度抑制样本扩散,柱采用一个较长的毛细管柱,而不是将多个柱连接。另外,系统流路中除了柱之外的部分的体积被最小化。即,如系统3所示,毛细管柱从分流器的内部通过(图1b中的分流器2),将毛细管柱和自动进样器的供液出口直接连接在一起。此外,检测部的检测单元的内径比柱的内径25μm还要小,所采用的检测器具有20μm的毛细管。
(3)荧光素和fitc-葡聚糖的分离
使用系统1和系统2的液相色谱系统进行了分离实验。分离的样本采用了荧光素(fluorescein)和异硫氰酸荧光素(fitc)-葡聚糖(fluoresceinisothiocyanate-dextran(fitc-dextran))。平均分子量分别为20kda和70kda。
在系统1和2中,中空毛细管柱采用了内径25μm、长度10m的由熔融二氧化硅制成的中空毛细管柱。使用纯水作为流动相。
结果如图6所示。图6a表示了系统1的分离结果,图6b表示了系统2的分离结果。最后的峰是荧光素峰,之前的峰是异硫氰酸荧光素(fitc)-葡聚糖的峰。
系统1的检测部的毛细管单元的内径为75μm,大于柱的内径,注入的样本通过柱并到达检测部时扩散,其结果,所检测到的峰的宽度变宽。而在系统2中,通过在中空毛细管柱形成检测窗来设置检测部,因此,检测部的内径和中空毛细管柱的内径是相同的。其结果,检测到的峰的宽度变小,可以进行更好的分离。
(4)dna和荧光素的分离
使用系统2和系统3的液相色谱系统进行了分离实验。作为待分离的样本,在使用系统2的分离实验中使用dna(源自鲑鱼的dna,90-270bp)和荧光素。在使用系统3的分离实验中使用dna(源自鲑鱼的dna,90-270bp)和罗丹明b(rhodamineb)。
对于中空毛细管柱,系统2和系统3均使用内径为25μm且长度为9m的由熔融二氧化硅制成的中空毛细管柱。使用纯水作为流动相。
结果如图7所示。图7a表示了系统2的分离结果,图7b表示了系统3的分离结果。最初的峰是dna峰,之后的峰是罗丹明b峰。
在系统3中,中空毛细管柱穿过分流器的内部直接连接到自动进样器的供液出口(使用图1b中的分流器2)。作为检测部的检测单元,使用比柱内径25μm小的内径为20μm的毛细管单元。结果,可以提高dna检测峰的准确度。
实施例2关于柱的内径和柱长对分离能力的影响的研究
(1)柱的内径对分离能力的影响
使用系统2的液相色谱系统进行了分离实验。作为待分离的样本,使用了dna(源自鲑鱼的dna,90至270bp)和荧光素。
中空毛细管柱使用了以下中空毛细管柱,即:内径为50μm长度为17.8m的由熔融二氧化硅制成的中空毛细管柱;内径为25μm长度为47.6m的由熔融二氧化硅制成的中空毛细管柱;内径为5μm长度为5.0m的由熔融二氧化硅制成的中空毛细管柱。作为流动相,使用纯水。
结果如图8所示。图8a表示使用内径为50μm长度为17.8m的柱的结果,图8b表示使用内径为25μm长度为47.6m的柱的结果,图8c表示使用内径为5μm长度为5.0m的柱的结果。
如图8所示,柱的内径越小,分离能力越好。当使用内径为50μm长度为17.8μm的柱时,流速为0.43μl/min,使用内径为25μm长度为47.6m的柱时,流速为0.33μl/min,使用内径为5μm长度为5.0m的柱时,流速为0.0015μl/min。
(2)柱长对分离能力的影响
使用系统2的液相色谱系统进行了分离实验。作为待分离的样本,使用dna(源自鲑鱼的dna,90至270bp)和荧光素。
使用由内径为25μm、长度为3.1m、6.0m、9.0m或47.6m的由熔融二氧化硅制成的中空毛细管柱作为中空毛细管柱。使用纯水作为流动相。
结果如图9所示。图9a、b、c和d分别表示使用长度分别为3.1m、6.0m、9.0m或47.6m的柱的结果。
如图9所示,色谱柱长越长,分离能力越高。当使用长度为3.1m的柱时,流速为0.61μl/min,当使用长度为6.0m的柱时,流速为0.46μl/min,当使用长度为9.0m的柱时,流速为0.22μl/min,当使用长度为47.6m的柱时,流速为0.33μl/min。
图10表示了色谱柱的内径和柱长的研究结果的总结。
实施例3使用液相色谱系统进行的分离
1.用纯水作为流动相进行分析
(1)低分子物质的分离
由于中性低分子物质的硫脲(0)可以忽略电荷和尺寸大小的影响并且可以呈现流动相的溶出,因此,可被用作标准物质,能够与电荷低分子物质bcecf(2’,7'-双(羧乙基)-4或5-羧基荧光素(-4)、荧光素(-2)、罗丹明(0)、若丹明6g(+1)进行标准物质的分离。括号中的数字表示电荷数。作为色谱柱,使用内径为25μm、长度为9.0m的由熔融二氧化硅制成的中空毛细管柱,使用纯水作为流动相。线性速度(流速)为1.8±0.1mm/s,以uv254nm进行了检测。
分离的结果如图11-1所示。
将硫脲和电荷低分子物质bcecf(-4)、荧光素(-2)、罗丹明(0)、或罗丹明6g(+1)的分离结果分别示于图11-1a、b、c和d。另外,图11-2表示了各低分子带电物质的相对保留时间。
(2)高分子物质的分离
使用负电荷高分子的异硫氰酸荧光素(fitc)-葡聚糖(分子量4kda(-0.2)、40kda(-4.8)、500kda(-83.4)和2000kda(-444.4),括号中的数值表示电荷数)和硫脲进行了分离。用图13表示异硫氰酸荧光素(fitc)-葡聚糖的特性(分子量,取代度,电荷数,流体动力学半径等)。作为柱,使用内径为25μm、长度为9.0m的熔融二氧化硅制成的中空毛细管,使用纯水作为流动相。线性速度(流速)为2.6±0.3mm/s,以uv254nm进行了检测。
硫脲和异硫氰酸荧光素(fitc)-葡聚糖4kda(-0.2)、40kda(-4.8)、500kda(-83.4)、2000kda(-444.4)的分离结果分别如图12-1a、b、c和d所示。fitc-葡聚糖的检测峰取决于分子量、产物形式、硫脲的相对保留时间和电荷数。预计和表面电荷密度及结构也相关。另外,图12-2分别显示了相对于硫脲的各分子量的fitc-葡聚糖的相对保留时间。
(3)dna和罗丹明b的分离
同样地,使用内径为25μm、长度为9.0m的由熔融二氧化硅制成的中空毛细管柱,纯水作为流动相,进行了dna(10bp)或dna(90bp-270bp)和罗丹明b、分子量标记物(12kda-225kda)的分离。
结果显示在图14中。图14a显示了10bp的dna和罗丹明b的分离结果,图14b显示了90至270bp的dna和罗丹明b的分离结果,图14c显示了90至270bp的dna和罗丹明b、分子量标记物的分离结果。
(4)低分子物质和高分子物质的同时分析
同样地,使用内径为25μm、长度为72m的由熔融二氧化硅制成的中空毛细管柱,使用纯水作为流动相,同时分离异硫氰酸荧光素(fitc)-葡聚糖、荧光素、硫脲和罗丹明b。
结果显示在图15中。如图15所示,可以同时分离低分子物质和高分子物质。
实施例4流动相的盐浓度对fitc-葡聚糖的相对保留时间比率的影响
使用内径为25μm、长度为60m的由熔融二氧化硅制的中空毛细管柱,作为流动相采用nacl溶液,进行了异硫氰酸荧光素(fitc)-葡聚糖和硫脲的分离。nacl浓度为5×10-3m、5×10-4m、5×10-5m、5×10-6m和0m。
结果如图16所示,如图16所示nacl浓度越低,分离越好。图16a、b、c、d和e分别显示nacl浓度为5×10-3m、5×10-4m,5×10-5m,5×10-6m和0m的结果。
为研究盐浓度对相对保留时间的影响,使用内径为25μm、长度为60m的由熔融二氧化硅制成的中空毛细管柱,测量异硫氰酸荧光素(fitc)-葡聚糖(电荷-83)的相对保留时间。结果显示在图17中。如图17所示,盐浓度越小,相对保留时间越短。
分离受盐影响的事实表明中空毛细管柱中存在双电层。盐浓度降低,双电层变厚,相对保留时间变短(图17)。该结果表明,通过降低盐的浓度,改善了负电荷物质的分离改善能力。
实施例5通过ph研究柱内壁的相互作用
为确认柱的内壁是否存在相互作用,使用内径为25μm、长度为9m的由熔融二氧化硅制成的中空毛细管柱,并使用缓冲液作为流动相,分离了罗丹明b和甲酸(pka3.77)。缓冲液通过调制a溶液0.2m柠檬酸和b溶液0.05m磷酸氢二钠十二水合物。通过混合176ml的a溶液和24ml的b溶液,获得了ph3的缓冲液。另外,通过混合17ml的溶液和183ml的b溶液获得ph12的缓冲液。用ph计(hm-30r,gst-5741c电极,dkk-toacorporation)确认ph值。流动相的线性速度(流速)为1.8±0.1mm/s,以uv254nm进行了检测。
结果如图18所示。通过将ph从3(图18a)改变为12(图18b),可以分离甲酸和罗丹明b。即使ph从3变更至12,中空毛细管内壁也保持有负电荷,羧基解离,具有负电荷,所以可以被分离。该结果表明,中空毛细管柱的内壁与待分离的物质之间存在相互作用。
实施例6使用磷酸盐缓冲生理盐水(pbs)作为流动相分析蛋白质
使用内径为25μm、柱长为60m的由熔融二氧化硅制成的中空毛细管,用nacl溶液作为流动相,对白蛋白(pi4.5,分子量9.9×104)、过氧化氢酶(pi5.6,分子量4.9×104)和α胰凝乳蛋白酶(pi8.8,分子量2.3×104)进行了分离。
结果如图19所示。如图19所示,可以分离三种蛋白质。
此外,使用相同的系统检验含有各种pi的蛋白质的相对保留时间和pi的关系(甲状腺球蛋白pi4.5,白蛋白pi4.7,过氧化氢酶pi5.6,伴刀豆蛋白api8.4,α胰凝乳蛋白酶pi8.8,溶菌酶pi11)。结果示于图20。如图20所示,确认了蛋白质的相对保留时间、等电点(pi)和理论塔板数之间的关联。如果蛋白质的pi高,相对保留时间和峰的宽度增加。其结果显示了蛋白质和柱内壁的相互作用。
实施例7分析时间效率的改善
使用内径为25微米、柱长度为60m的熔融二氧化硅制的中空毛细管,使用纯水作为流动相。将分析时间变长,并连续注入待分离材料,其结果,在一次的分析中能够分析多个样本。结果示于图21。在图21中所示的研究结果中,一次的分析时间为约650分钟,在60分钟时,先注入一次样本,然后,连续注入四次样本,进行分析。在650分钟的分析时间中,可以同时分析四种样本,缩短了分析时间,实现了有效的分析。
实施例8双电层的厚度和负电荷物质从管内壁排除的距离
使用柱长度为60m的由熔融二氧化硅制的中空毛细管,作为样本使用fitc-葡聚糖(平均分子量为5×10-5m,电荷-83),比较研究了双电层的厚度和负电荷物质从管内壁排除的距离。图22示出了对双电层的厚度与负电荷物质从管内壁排除的距离的比较。改变盐nacl的浓度,对所注入的样本从内壁排除的距离与双电层的厚度进行比较。通过两种方法计算双电层的厚度。由比较结果可知,当盐的浓度为5×10-5m以下时,样本从内壁排除的距离比双电层厚度更小。这暗示,当盐浓度低时,双电层变厚,物质分布在双电层中。当双电层变薄并变得比待分离物质的粒径小时,物质从内壁排除的距离受待分离物质的粒径的影响变大。
实施例9在长中空毛细管柱和超纯水的分析条件下ftic-葡聚糖的溶出行为
在使用长中空毛细管柱和水流动相的分析条件下,可以推测在毛细管内壁附近存在薄的双电层并且在分离中起很大作用。将以下四个条件更改并验证。
(1)柱长,(2)柱内径,(3)流动相的离子强度,(4)柱温
评估参数:
a.相对保留时间和平均流速的比率rf
由于本实施例中使用的分析系统难以精确控制流速,因此以物质的平均流速作为基准,以相对保留时间和物质的平均流速的比率rf(rf=t(分析)t(平均))评价物质的溶出。假定中性低分子物质没有电荷,与内壁没有相互作用。而且,低分子物质可以忽略其尺寸效应,而且扩散快,因此可以忽略扩散的影响。在该实施例中,选择作为低分子物质的硫脲,使用硫脲获得的流速作为平均流速,根据相对保留时间和各物质的硫脲的平均流速的比率rf,评估各物质的溶出行为。
b.基于层流溶出体积的从管内壁排除的距离x.
中空毛细管柱具有这种特征,即:由于其与内壁之间的相互作用,而分布有管内层流型各异的线性流速。可以认为,溶出时间可以通过物质在层流型截面受到的线性流速来求出。
物质由毛细管内壁排除,可根据由内壁排除的距离求出其所受到的线性流速。可以认为,排除距离受物质尺寸和电荷等影响因子的影响。其是中空毛细管内的层流,在物理层流模型中,可通过积分在理论上准确计算出溶出体积,其结果,可以求出从内壁排除的距离。在本实施例中,将具有负电荷的不同分子量的异硫氰酸荧光素(fitc)-葡聚糖作为实验对象。尝试通过异硫氰酸荧光素(fitc)-葡聚糖的理论计算值来解析中空毛细管柱内的物质溶出行为。
1)柱长的影响
分析条件
毛细管柱:id25μm,9m,16m,60m
流动相:超纯水
温度:室温(25℃)
可变波长uv检测:200nm,254nm,460nm
得以证实:使用存在于柱内壁上的薄双电层并增加毛细管的长度,由此能够提高分离能力。通过柱长为9m、16m和60m进行分析后的结果表明,色谱柱越长,相对保留时间越少。当相对保留时间小于1时,认为物质的移动比流动相的流速快,先被溶出。随着fitc-葡聚糖的分子量按照4kda、40kda、500kda和2000kda增加,负电荷数也按照-0.1、-2.0、-16.7、-66.7。分子量、粒径或负电荷数越大,溶出越快。图26显示了基于分子量计算的粒径(图25)与相对保留时间之间的理论关系。在实验中获得的相对保留时间低于理论值。这意味着好于基于粒径的分离。
图27示出从管内壁排除的距离x和柱长的关系,按照各分子量并根据2.5mm/s附近的流速示出由相对保留时间计算出的从管内壁排除的距离x。分子量或负电荷数越大,从内壁排除的距离越大。因此,可以认为受到的线性流速变快并且溶出变得更快。从内壁排除的距离大于fitc-葡聚糖的粒径1.6nm、6.3nm、27.6nm、62.4nm。这表明从内壁排除的现象不能仅通过分子量的差异来解释,还要受电荷排除效果的影响。
在实施例1中,显示:当毛细管变长时,dna的分离得到改善。柱越长,分离越得到改进,如图27所示,被认为是因为物质从管内壁排除的距离增加。此外,物质从管内的内壁排除并远离内壁,所接受的线性流速变大也是其原因。
2)柱内径的影响
分析条件:
毛细管柱:id25μm、50μm、75μm,60m
流动相:超纯水
温度:室温(25℃)
可变波长uv检测:200nm、254nm、460nm
在毛细管内径为25μm的情况下,内壁层起了很大分离作用,基于此,使用内径为25μm、50μm和75μm的柱进行了研究。
随着内径变大,相对保留时间增加,四种不同分子量的fitc-葡聚糖的移动速度发生差异,从而可以实现良好的分离。
图28显示了基于粒径的尺寸排除的理论相对保留时间和fitc-葡聚糖的粒径与柱内径之比的关系。另外,采用内径25μm、50μm、75μm的柱进行实验所获得的相对保留时间比率要优于尺寸排除效果的结果。
图29示出了从管内部排除的距离x与柱内径之间的关系。从图29可以看出,在内径为25μm、50μm、75μm的柱内,分子量为40kda的情况下,从内壁排除的距离多少会受到内径的影响。然而,在500kda、2000kda的fitc-葡聚糖的情况下,却没有什么变化,由此可知,内壁的层厚度并不依赖于柱的内径。不过,可以预计,当柱的内径增加时,内壁的层厚为一定厚度,如图23所示,样本分布区域和柱的截面比r/a增加,因此,相对保留时间也会增加。
3)流动相离子强度的影响
分析条件
毛细管柱:id25μm、50μm,60m
流动相:超纯水,0.000005、0.00005、0.0005、0.001、0.005、0.05、0.25mol/lnacl
5.0×10-6mol/l、5.0×10-5mol/l、5.0×10-4mol/l、5.0×10-3mol/l、5.0×10-2mol/l、2.5×10-1mol/l
流速:2.5mm/s附近
温度:室温(25℃)
可变波长uv检测:200nm、254nm、460nm
使用内径为25μm的毛细管柱研究盐浓度(nacl)的影响。nacl在流动相中的浓度为0.000005、0.00005、0.0005、0.001、0.005、0.05或0.25mol/l(图30-1至30-4)。图30-1、30-2、30-3和30-4分别示出了在不同盐浓度条件下分析4kda、40kda、500kda、2000kda的fitc-葡聚糖所得的色谱图,a~h分别表示h2o(超纯水)、0.000005、0.00005、0.0005、0.001、0.005、0.05、0.25mol/lnacl的结果。图中右侧(后方)尖锐的峰是标准物质硫脲的峰,表示为流动相的平均流速。图中左侧(前方)的宽峰是fitc-葡聚糖的峰。随着nacl浓度的增加,fitc-葡聚糖的峰接近标准物质硫脲的峰。此外,fitc-葡聚糖的峰形变得尖锐。
以下,对这两个变化进行研究。
1.随着盐浓度的增加,fitc-葡聚糖的峰接近标准物质硫脲的峰
基于相对保留时间比率评估该现象的结果显示在图31中。如图所示,相对保留时间比率随着nacl浓度的增加而降低。其理由为如下三点
(1)毛细管柱内壁上的双电层变薄。
(2)fitc-葡聚糖的结构或保持电荷发生了变化。
(3)毛细管柱内壁对fitc-葡聚糖的排除效果减弱。
2.fitc-葡聚糖的峰形锐化
通常,认为峰形是物质分子量的分布。然而,当nacl浓度增加时,物质分子量的分布不太可能发生变化。但是,最近,有报告称,核酸的折叠状态根据盐浓度发生变化,色谱的峰形状发生了变化(friedrich,sm等,journaloftheamericanchemicalsociety2016,138(1),319-327)。)。在本实施例中也推断:因nacl浓度的差异,fitc-葡聚糖已从长拉伸结构变为球形结构。即,具有长拉伸结构的物质在毛细管柱中比球形结构更容易移动并且可以快速溶出。
edl(双电层)计算公式:
为了验证柱内壁上的薄层排除是否为双电层排除,调查和双电层的厚度密切相关的流动相的离子强度与由管内壁排除的距离x之间的关系是有效的。将超纯水的离子强度设在1.0×10-7mol/l范围内、nacl浓度设在0.0000017mol/l-0.25mol/l范围内进行研究,根据研究结果(图31),求出从内壁排除的距离(图32)。如图所示,从内壁排除的距离与双电层的厚度相关。因此,认为双电层的电荷排除效应对物质分离具有影响。
在内径为50μm的柱中,已确认:相对保留时间和盐浓度之间存在关联。
与内径为25μm的柱同样地,盐浓度增加,双电层的厚度减小,其结果,样本分布区域和柱的截面比r/a变大,因此,相对保留时间增加。在相同nacl浓度的情况下,使用内径为50μm的柱时,其相对保留时间均高于使用内径为25μm的柱时的相对保留时间。该结果与研究内径的影响时的结果一致(图28)。
另一方面,在nacl浓度为0.0005mol/l以上时,双电层变得非常薄,从内壁排除的距离比fitc-葡聚糖的粒径小。这种现象尺寸排除而不是电荷排除。图33显示了0.005、0.05、0.25mol/l浓度的nacl的情况下fitc-葡聚糖的粒径与相对保留时间比率之间的关系的理论曲线。
当nacl浓度为0.005mol/l时,小于理论值,因此,受电荷排除效应的影响。而当nacl浓度为0.05mol/l、0.25mol/l时,相对保留时间比率小于理论值。其结果,这是因为基于盐浓度的fitc-葡聚糖的结构发生变化,粒径变小,相对保留时间比率降低。即,得以证实:发生了基于分子量的移动速度差异。
4)柱温的影响
分析条件
毛细管柱:id25μm,60m
流动相:超纯水
温度:冰水(0℃),室温(25℃),40℃、50℃、,60℃
可变波长uv检测:200nm、254nm、460nm
关于温度的影响,有报告指出,通过使用纳米柱进行分析发现,其对流速有影响,但对相对移动没有影响(李,r.等人,;化学快报2012,41(11),1506-1508)。在本实施例中,在0至60℃的温度范围内进行了研究。其结果,在流速一定的情况下,其对相对保留时间存在影响(图34)。温度较高在25℃以上时,物质的布朗运动变强,在柱内向柱内壁靠近的扩散运动变强,从内壁排除的距离变小(图35)。此外,得以证实:在0℃下相对保留时间增加。这表明,0℃下的现象不受布朗运动的影响,而是受温度引起的层流流速分布变化的影响。
结论
在长中空毛细管柱和水流动相的分析条件下,验证了下述四个条件,即,(1)柱的长度,(2)柱的内径,(3)流动相的离子强度,(4)柱温。结果发现,在毛细管内壁附近存在薄层,在分离中起很大作用。根据层流计算模型,可获得柱内的物质分布信息。
实施例10在使用长中空毛细管柱和磷酸盐缓冲生理盐水的分析条件下蛋白质的溶出行为
通过使用毛细管柱和磷酸盐缓冲生理盐水对蛋白质进行分析,显示:蛋白质的等电点增加,相对保留时间增加,理论塔板数减少(实施例6)。本实施例中,研究在伴刀豆蛋白a和过氧化氢酶这两种蛋白质与罗丹明b共存的情况下表面电荷是否因罗丹明b的浓度而发生变化、以及溶出行为是否发生变化。
分析条件
毛细管柱:id25μm,60m
流动相:磷酸盐缓冲生理盐水
温度:室温(25℃)
可变波长uv检测:220nm、280nm、546nm
图36和图37表示将伴刀豆蛋白a或过氧化氢酶与0.05(a)、0.1(b)、0.5(c)及2.5mg/ml(d)的罗丹明b混合后分离的结果。使用伴刀豆蛋白a时的色谱图如图36所示,使用过氧化氢酶时的色谱图如图37所示。色谱图左侧的尖峰是罗丹明b的峰,右侧的宽峰是伴刀豆蛋白a或过氧化氢酶的峰。伴刀豆蛋白a和过氧化氢酶各自被检测为两个峰,当罗丹明b的浓度增加时第二峰变大。这是因为,当罗丹明b的浓度增加时,吸附在蛋白质上的罗丹明b增加,表面电荷增加,或者,结构发生改变,其与内壁间的相互作用变强。
可以认为,在使用中空毛细管柱和磷酸盐缓冲生理盐水对蛋白质进行分析时,伴刀豆蛋白a和过氧化氢酶这两种蛋白质共存的条件下,峰形因罗丹明b的浓度而发生变化,保留时间变慢。
- 还没有人留言评论。精彩留言会获得点赞!