一种氯霉素免疫检测试剂及其制备和检测方法与流程
本发明涉及医学检验领域,具体是一种氯霉素免疫检测试剂及其制备和检测方法。
背景技术
氯霉素(chloramphenicol,cap)是一种应用比较广泛的抗生素,对家禽、家畜、水产养殖动物传染病的预防、控制和治疗起着相当重要的作用。氯霉素因其抗菌消炎作用,对皮肤炎症有一定疗效,因此常被添加在祛痘除螨类化妆品中。但由于人体脸部皮肤柔嫩,黏膜血管丰富,对药物吸收非常快,从而破坏皮肤表面的正常菌群,导致皮疹、速发性过敏等不良反应。同时氯霉素存在严重的副作用,会造成人的再生障碍性贫血、粒细胞缺乏症等疾病。其在动物性食品中的残留也危害着人类的健康,我国和世界上多数国家禁止cap用于食品动物。
目前检测氯霉素的常用方法有:微生物检测法、色谱分析法、免疫检测法。微生物检测法灵敏度较低;色谱分析法样品前处理麻烦,分析速度慢,费用高;免疫分析法具有快速、灵敏度高、高通量的特点。其中免疫分析方法有酶联免疫法、胶体金免疫层析技术等。其中酶联免疫分析法操作相对繁琐,对操作人员的专业知识要求较高;胶体金免疫层析技术稳定性较差、灵敏度较低等。
本发明采用的方法为均相酶免疫检测法,其优点为:操作简便、快速、灵敏度高、准确性好、适合于自动化,应用广泛,并且用全自动生化分析仪对小分子物质和大分子物质都能高通量快速测定。
技术实现要素:
本发明的目的在于解决现有技术中氯霉素检测过程操作复杂、以及测定准确度低的问题,本发明提供了一种快速、灵敏度高、准确检测出待测样本中氯霉素含量的氯霉素均相酶免疫检测试剂及其制备方法。
为实现上述目的,本发明提供如下技术方案:
一种氯霉素免疫检测试剂及其制备和检测方法,其特征在于:酶标氯霉素、用于检测氯霉素抗体-酶标氯霉素复合物的指示试剂;上述酶标氯霉素由氯霉素和葡萄糖脱氢酶偶联而成。
作为本发明进一步的方案,所述指示试剂选自酶试剂,包括:酶标偶联物和酶的底物;上述酶标偶联物包括葡萄糖脱氢酶-氯霉素偶联物;上述酶的底物为葡萄糖。
作为本发明进一步的方案,所述的一种氯霉素免疫检测试剂及其制备方法,其特征在于,包括如下步骤:
(1)葡萄糖脱氢酶-氯霉素偶联物的制备:氯霉素(cap)半抗原的制备,葡萄糖脱氢酶(gdh)与氯霉素半抗原偶联,纯化偶联的酶标抗原。
(2)氯霉素均相酶免疫检测试剂的制备:
试剂1的制备:由氯霉素抗体和均相酶底物混合而成;
试剂2的制备:由葡萄糖脱氢酶-抗原偶联物与磷酸盐缓冲液混合而成。
作为本发明进一步的方案,所述的一种氯霉素免疫检测试剂的制备方法,其特征在于,所述的步骤(1)具体过程为:
1)氯霉素(cap)半抗原的制备
a.称取cap500-1500mg和琥珀酸酐200-800mg加入圆底烧瓶中,加入无水吡啶5-15ml减压蒸馏,收集115℃馏分;
b.然后55~60℃冷凝回流10-16h,反应液用旋转蒸发仪蒸去吡啶,得红色糖浆状物a;
c.加入乙酸乙酯20-100ml和盐酸5-20ml,充分振荡,再分离酸层;
d.反应物用na2co35-20ml溶解,加入baac,80℃搅拌反应0.5-2h,室温过滤得钡盐粗品b;
e.用双蒸水加热溶解钡盐b并用盐酸调ph值为2-4,滤出沉淀,真空干燥得单酯粗品c;
f.用乙醇溶解单酯粗品c,sephadexg-25过柱纯化,真空干燥得单酯纯品,即目标产物氯霉素半琥珀酸酯(cap-hs)。
2)葡萄糖脱氢酶(gdh)与氯霉素的偶联
a.称取cap-hs100-300mg溶于5-25mldmf和1,4-二氧六环混合液中,加入三丁胺50-200ml,冰浴条件下搅拌反应5-20min;
b.加入氯甲酸异丁酯20-100ml,室温搅拌反应0.5-2h,此为a液;
c.称取gdh100-500mg溶于50%dmf水溶液10-50ml中,冰浴条件下用naoh调ph值为8-9,此为b液;
d.冰浴搅拌条件下将b液逐滴加入到a液中,维持ph值为8-9,4℃搅拌反应8-16h。
3)纯化偶联的酶标抗原
通过g-25凝胶层析柱纯化偶联的酶标抗原,得到葡萄糖脱氢酶-氯霉素偶联物,于2-8℃下储存。
作为本发明进一步的方案,所述的一种氯霉素免疫检测试剂的制备方法,其特征在于,步骤(2)的具体过程如下:
试剂1的制备:将2-5g氧化态的烟酰胺腺嘌呤二核苷酸nad、0.5-3g葡萄糖用0.5-2l磷酸盐缓冲液溶解制成均相酶底物;将氯霉素抗体加到上述均相酶底物中,抗体与均相酶底物的体积比为1:100~1:10000;
试剂2的制备:将制备的葡萄糖脱氢酶-氯霉素偶联物加到磷酸盐缓冲液中,上述偶联物与磷酸盐缓冲液的体积比为1:100~1:10000。
作为本发明进一步的方案,所述的氯霉素免疫检测试剂的检测方法,其特征在于,包括以下步骤:
1)将待测样本与氯霉素抗体接触;
2)根据待测样本中酶标氯霉素与氯霉素抗体的结合情况,利用指示试剂判断样本中氯霉素的含量;所述待测样本为血清、血浆、唾液或尿液。
本发明的原理是抗原与酶结合成酶标抗原,保留抗原和酶的生物活性,当酶标抗原与抗体结合后,抗原分子上的酶蛋白与抗体密切接触,使酶的活性中心受到影响,酶的活性受到抑制。测定时样本中的抗原、酶标抗原与抗体竞争性结合,样本中的抗原含量越高,加底物后其od值越高。
本发明的优点在于:本发明的氯霉素免疫检测试剂可以精确快速地确定人体血液等样品中氯霉素含量。与市场上现有的检测试剂相比,本发明检测试剂具有方便快速、灵敏度高、特异性强、定量准确等优点,有利于临床的推广使用。
附图说明
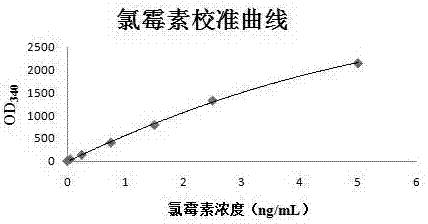
图1是氯霉素均相酶免疫反应校准曲线图。
图2是氯霉素均相酶免疫线性范围图。
具体实施方式
本发明提供了一种氯霉素免疫检测试剂及其制备和检测方法,为使本发明目的、技术方案及效果更加清楚、明确,以下对本发明进行详细说明。
本发明提供了一种氯霉素免疫检测试剂及其制备和检测方法。包括:酶标氯霉素、用于检测氯霉素抗体-酶标氯霉素复合物的指示试剂;上述酶标氯霉素由氯霉素和葡萄糖脱氢酶偶联而成。
本发明中所指的“氯霉素”不仅仅指完整的氯霉素分子,也包括保留完整抗原特异性结合能力的氯霉素片断或者衍生物。
一种氯霉素均相酶免疫检测试剂,包括:酶标氯霉素、用于检测氯霉素抗体-酶标氯霉素复合物的指示试剂。指示试剂选自酶试剂、放射性同位素试剂、荧光试剂和化学发光试剂。优选的,指示试剂为酶试剂,包括:酶标偶联物和酶的底物。其中,酶标偶联物包括葡萄糖脱氢酶-抗原偶联物,其可通过化学合成方法得到。
上述的氯霉素免疫检测试剂的使用方法,包括以下步骤:
1)将待测样本与氯霉素抗体接触;
2)根据待测样本中酶标氯霉素与氯霉素抗体的结合情况,利用指示试剂判断样本中氯霉素的含量;所述待测样本为血清、血浆、唾液或尿液等。优选的,待测样本为血清或血浆。
下面通过具体的实施例对本发明进行详细说明。
实施例一:葡萄糖脱氢酶-抗原偶联物的制备
1)氯霉素(cap)半抗原的制备
a.称取cap966mg和琥珀酸酐600mg加入圆底烧瓶中,加入无水吡啶10ml减压蒸馏,收集115℃馏分;
b.然后55~60℃冷凝回流12h,反应液用旋转蒸发仪蒸去吡啶,得红色糖浆状物a;
c.加入乙酸乙酯50ml和0.1mol/l盐酸10ml,充分振荡,再分离酸层;
d.反应物用10%na2co310ml溶解,加入baac,80℃搅拌反应1h,室温过滤得钡盐粗品b;
e.用双蒸水加热溶解钡盐b并用盐酸调ph值为3,滤出沉淀,真空干燥得单酯粗品c;
f.用乙醇溶解单酯粗品c,sephadexg-25过柱纯化,真空干燥得单酯纯品,即目标产物氯霉素半琥珀酸酯(cap-hs)。
2)葡萄糖脱氢酶(gdh)与氯霉素的偶联
a.称取cap-hs127mg溶于12mldmf和1,4-二氧六环混合液中,加入三丁胺78.6ml,冰浴条件下搅拌反应10min;
b.加入氯甲酸异丁酯45ml,室温搅拌反应1h,此为a液;
c.称取gdh300mg溶于50%dmf水溶液20ml中,冰浴条件下用1mol/lnaoh调ph值为8.5,此为b液;
d.冰浴搅拌条件下将b液逐滴加入到a液中,维持ph值为8.5,4℃搅拌反应12h。
3)纯化偶联的酶标抗原
通过g-25凝胶层析柱纯化偶联的酶标抗原,得到葡萄糖脱氢酶-氯霉素偶联物,于2-8℃下储存。
实施例二:氯霉素均相酶免疫检测试剂的制备
氯霉素均相酶免疫检测试剂,包括:酶标氯霉素、用于检测氯霉素抗体-酶标氯霉素复合物的指示试剂。指示试剂选自酶试剂、放射性同位素试剂、荧光试剂和化学发光试剂。优选的,指示试剂为酶试剂,包括:酶标偶联物和酶的底物。其中,酶标偶联物包括葡萄糖脱氢酶-抗原偶联物,其可通过化学合成方法得到。
氯霉素均相酶免疫检测试剂在使用之前,为了避免指示试剂中的酶标偶联物和酶的底物发生反应,酶标偶联物和酶的底物是分开放置的,因此氯霉素均相酶免疫检测试剂包括两种分开设置的试剂,具体如下:
1.试剂1的制备:将3.588g(10mm)氧化态的烟酰胺腺嘌呤二核苷酸nad、1.802g(10mm)葡萄糖用1l50mm、ph8.0的磷酸盐缓冲液溶解制成均相酶底物;将氯霉素抗体加到上述均相酶底物中,抗体与均相酶底物的体积比为1:100~1:10000,在本实施例中具体的比例为1:650。
2.试剂2的制备:将制备的葡萄糖脱氢酶-氯霉素偶联物加到50mm、ph8.0的磷酸盐缓冲液中,上述偶联物与磷酸盐缓冲液的体积比为1:100~1:10000,在本实施例中具体的比例为1:1800。
上述氯霉素均相酶免疫检测试剂的使用方法,包括以下步骤:
1)将待测样本与氯霉素抗体接触;
2)根据待测样本中酶标氯霉素与氯霉素抗体的结合情况,利用指示试剂判断样本中氯霉素的含量;
具体的,检测时将待测样本加到试剂1中,待测样本中的氯霉素与试剂1中的氯霉素抗体发生特异性结合,生成抗氯霉素抗体-氯霉素复合物;再加入试剂2,此时试剂2中的葡萄糖脱氢酶-氯霉素偶联物与试剂1中的酶的底物混合、接触,发生酶促反应,构成检测氯霉素抗体-酶标氯霉素复合物的指示试剂,指示试剂根据待测样本中氯霉素与上述氯霉素抗体的结合情况判断待测样本中氯霉素的含量。
由于葡萄糖脱氢酶-抗原偶联物与待测样本中的氯霉素竞争性结合氯霉素抗体,所以,待测样本中氯霉素的量越多,均相酶溶液中游离的葡萄糖脱氢酶-抗原偶联物的量越多,酶促反应越快,导致od340上升。
上述待测样本为生理样本,例如血清、血浆、尿液、唾液等,作为一种优选的方案,上述待测样本为血清或血浆。
实施例三:氯霉素均相酶免疫检测试剂反应校准曲线。
1)校准品配制:将市售人氯霉素重组蛋白溶于类似人血清基质的溶液(nacl0.9%,bsa0.2%,nan30.1%,tris-hclph7.4)中,制成不同浓度的校准品。以北京望尔生物科技有限公司氯霉素校准品为原始标准,采用其氯霉素试剂盒对不同浓度的校准品分别检测10次,求出均值,得到氯霉素校准品的浓度:0.05,0.25,0.75,1.5,2.5,5ng/ml。
2)生化分析仪检测:以日立7170操作为例:测定波长为340nm,分别取不同浓度的校准品溶液(15μl),加入氯霉素r1试剂(160μl),混匀,再加入氯霉素r2试剂(40μl),混匀后,测定不同时间点的od340吸光值,算出不同校准品浓度时的反应速率,实际操作过程中需不断调整试剂1和试剂2的体积比例,同时调整测光点,最后得出较理想的反应标准曲线图,每管重复测定3次,以各校准管3次测得的吸光度差值δa的平均值为纵坐标,对应的校准品浓度为横坐标,绘制“浓度-吸光度差值”校准曲线(见图1)。
取待测血清或血浆样本,同法测定样本的吸光度差值,代入校准曲线,即可计算出待测样本中氯霉素的含量。如果血清或血浆中氯霉素的浓度超出校准曲线范围,需对样本进行稀释后再检测以保证检测结果的准确性。
本检测试剂不仅适用于日立7170,还适用于其它品牌和型号的半自动、全自动生化分析仪,具体参数可根据仪器进行调整。
实施例四:线性范围确定
用接近线性范围上限的氯霉素高浓度样本(4.86ng/ml),用上述类似人血清基质的溶液将其按1/2,1/4,1/8,1/16,1/32,1/64稀释,共配制成6个稀释浓度(xi)的溶液,用所述生化分析仪检测方法测定各稀释样本浓度。每个稀释浓度测试3次,分别求出每个稀释浓度检测结果的均值(yi)。以稀释浓度(xi)为自变量,以测定均值(yi)为因变量求出线性回归方程,根据公式(1)计算线性回归的相关系数r,结果显示回归方程为y=0.9469x+0.0319,相关系数r=0.9997,表明本发明试剂在0.08ng/ml-4.86ng/ml线性范围内相关性较好(见图2)。
由于本发明的检测过程是由仪器全自动化完成,所以对检测人员的要求不高,易于实现和推广使用。
需要说明的是,显然本发明不限于上述示范性实施例的细节,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明的专利保护范围内。
此外,以上所述的仅是本发明的优选实施方案,并非因此限制本发明的专利范围,对于本技术领城的技术人员来说,在不脱离本发明原理的前提下,还可以做若干的改进和调整,这些改进的调整均同理包括在本发明的专利保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!