网织红细胞模拟物及其制备方法与应用与流程
本发明属于血液质控物技术领域,具体涉及一种网织红细胞模拟物及其制备方法与应用。
背景技术:
由单一或多组分的血细胞或血细胞模拟物组成的血液质控品,具备如同血液一样的可检测的特性,可以用于血液分析仪的准确性和精确性的日常监控。
网织红细胞是红细胞成熟过程中的过渡阶段的细胞,是未成熟的红细胞,其特征是刚脱去细胞核、胞质内尚残留有少量rna。网织红细胞的总数或百分比对于临床上对贫血及其相关疾病的诊断具有重要的临床意义。网织红细胞计数是反映骨髓造血功能的重要指标,主要表现在以下几个方面。
1、评价骨髓增生能力,判断贫血类型:①网织红增多,表示骨髓造血功能旺盛,常见于各种增生性贫血如缺铁性贫血、巨幼细胞性(缺乏叶酸、维生素b12)贫血、失血性贫血,尤以溶血性贫血时增加最为显著,常>10%。造血恢复期可见ret短暂和迅速增高,是骨髓功能恢复较敏感的指标。②网织红减少:常见于再生障碍贫血,网织红细胞计数常低于0.005,网织红细胞绝对值低于15×109/l。
2、评价疗效:①观察贫血疗效,ret是贫血患者随访检查的项目之一;②骨髓移植后监测骨髓造血恢复。
3、放疗和化疗的监测:网织红细胞的动态观察可指导临床适时调整治疗方案,避免造成严重的骨髓抑制。
综上所述,网织红细胞的各项指标在贫血性疾病的诊断和治疗效果的评估方面具有重要的临床意义,近年的研究发现,网织红细胞参数在检测肝硬化过程中也具有重要的临床意义。
目前中高端的血细胞分析仪都将网织红细胞作为分析和检测的指标,对血液样本中网织红细胞的分析已成为血液分析的重要组成部分,使用质控物对网织红细胞计数进行质量控制是保证血细胞分析仪测定结果准确性的前提,因此开发出准确的可用于全自动血细胞分析仪的网织红细胞质控物是十分必要的。
当前对于网织红细胞质控物的制备主要有以下几种方式:
1、以猪血的网织红细胞为原料,通过离心分离等方法分离出网织红细胞,制备网织红细胞质控品(us5736402,us5858789,us5945340,us6444471),这种制备方法原料的处理量大,产率不好,血小板的分离可能不彻底,所需成本较高。
2、将哺乳动物的红细胞膜进行处理后,注入核酸物质,模拟网织红细胞,制备网织红细胞质控品(us6399388,us6406915,us5432089),该方法制得的产物是红细胞和网织红细胞的混合物,网织红细胞的产率取决于核酸注入的比例多少,并且操作过程繁琐。
3、通过核酸等物质与红细胞膜表面共价结合的方式制备网织红细胞模拟物(us7195919),该方法制备的网织红细胞质控品的储存效期取决于核酸与细胞表面连接的强度,在长期储存时难以保证效期,并且操作繁琐。
4、分离纯化哺乳动物无核红细胞,通过加入细胞处理液和固定液制备网织红细胞质控品(cncn101881778),该制备方法操作过程相对简单,但是其制备过程中利用蛋白质变性剂使细胞内的分子结构发生改变以达到与染料的吸附作用,蛋白变性剂的作用程度会影响网织红细胞模拟物的产率。
技术实现要素:
有鉴于此,本发明的目的是提供一种操作简单、产率更高、稳定性更好的网织红细胞模拟物及其制备方法与应用。
本发明的网织红细胞模拟物的制备方法,步骤如下:
步骤一、分离洗涤红细胞,得到纯化红细胞;
步骤二、用稀释液稀释纯化红细胞,加入加载剂,在脉冲电磁场的作用下将加载剂引入到纯化红细胞内;
所述稀释液由体积比为1:(30-50)的稀释液i和稀释液ii组成;稀释液i由atp、mgcl2和水组成,atp的浓度为10%-40%,mgcl2的浓度为5%-28%;稀释液ii由kh2po4、nahco3、葡萄糖和水组成,稀释液ii的ph值为7.0-7.5,kh2po4浓度为0.5%-2.0%,nahco3浓度为0.05%-0.2%,葡萄糖的浓度0.01%-0.1%;
步骤三、向引入加载体后的细胞中加入固定液,18-28℃固定,洗涤细胞,用细胞保存液保存,得到网织红细胞模拟物。
优选的是,所述红细胞为人红细胞或者mcv与人红细胞类似的哺乳动物红细胞。
优选的是,用稀释液稀释纯化红细胞至1012-1014个/l。
优选的是,所述加载体为人工合成100bp-2000bp的dna片段或人工合成的rna片段,加载体的用量为1.0-1.5μg/l。
优选的是,将脉冲电磁场的作用下将加载剂引入到纯化红细胞内的过程为:电穿孔仪器90-120v电压刺激4-8秒钟。
优选的是,所述细胞固定液为甲醛、戊二醛、丙酮、乙醇中的一种或多种,固定时间为3-5小时。
优选的是,步骤一和步骤三中洗涤采用的洗涤液为pbs缓冲液、d-hanks缓冲液、hepes缓冲液、柠檬酸缓冲液、氯化钠缓冲液或硼酸缓冲液。
优选的是,所述细胞保存液包括缓冲液、营养成分和防腐剂。
本发明还提供上述网织红细胞模拟物的制备方法制备的网织红细胞模拟物。
本发明还提供上述网织红细胞模拟物作为全自动血细胞分析仪检测网织红细胞的质量控制物的应用。
与现有技术相比,本发明的有益效果为:
本发明的网织红细胞模拟物的制备方法,运用电脉冲刺激细胞的方式将核酸物质引入成熟红细胞内制备出网织红细胞模拟物,该模拟物制备步骤简单,适合大批量生产。
本发明的网织红细胞模拟物,由人或者哺乳动物的红细胞,通过脉冲处理引入核酸或其类似物后对细胞进行固定处理,进而模拟网织红细胞的状态,制备出网织红细胞模拟物。
附图说明
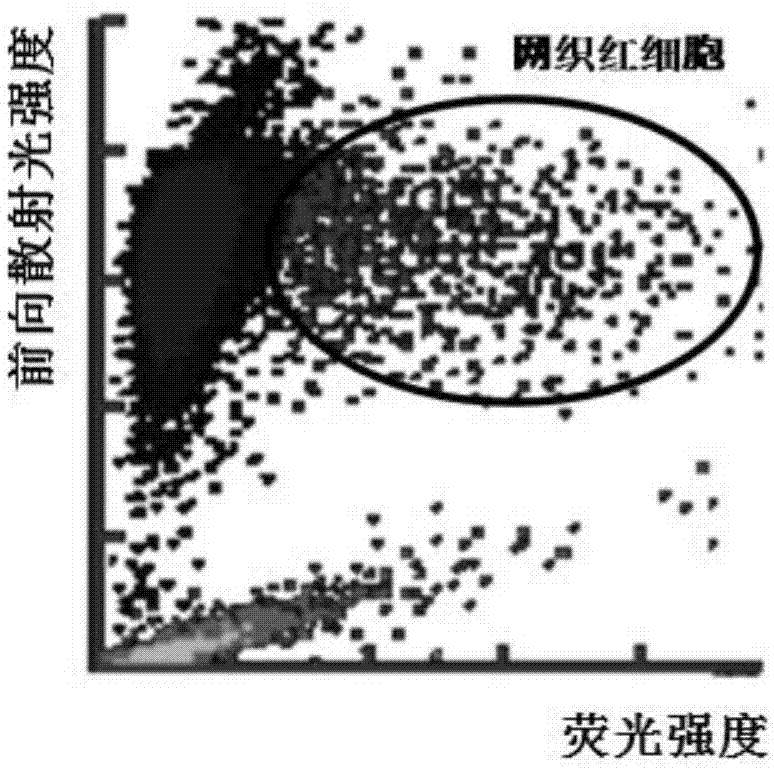
图1为实施例1所制备的网织红细胞模拟物,在以核酸荧光染色为检测原理的血液细胞分析仪上测试图片(仅提供ret通道)。
图2为实施例2所制备的网织红细胞模拟物,在以核酸荧光染色为检测原理的血液细胞分析仪上测试图片(仅ret通道)。
图3为实施例3所制备的网织红细胞模拟物,在以核酸荧光染色为检测原理的血液细胞分析仪上测试图片(仅ret通道)。
图4为实施例4所制备的网织红细胞模拟物,在以核酸荧光染色为检测原理的血液细胞分析仪上测试图片(仅ret通道)。
具体实施方式
为了进一步理解本发明,下面对本发明优选实施方案进行描述,但是应当理解,这些描述只是为进一步说明本发明的特征和优点,而不是对本发明权利要求的限制。
本发明的网织红细胞模拟物的制备方法:先分离洗涤红细胞,得到纯化红细胞;然后将纯化红细胞加入稀释液中,加入加载剂,经脉冲电场的作用将加载剂导入到纯化红细胞内,最后向引入加载体后的细胞中加入固定液,18-28℃固定,洗涤细胞,用细胞保存液保存,得到网织红细胞模拟物。
上述技术方案中,红细胞可以是人的红细胞,也可以是mcv值与人接近的哺乳动物的红细胞,以新鲜血液制备本发明中的模拟物效果更佳。分离方法是通过离心、洗涤、过滤的方式去除血液样本中的白细胞和血小板,其中,过滤可以用白细胞滤器去除白细胞。
上述技术方案中,稀释液为稀释液i和稀释液ii组成,稀释液i和稀释液ii的体积比为1:(30-50),优选为1:(32-42),最优选为1:40。其中,稀释液i由atp、mgcl2和水组成;atp的浓度为10%-40%,优选为15%-35%,更优选为20%-30%;mgcl2的浓度为5%-28%,优选为8%-20%,更优选为10%-15%。稀释液ii由kh2po4、nahco3、葡萄糖和水组成;稀释液ii的ph值为7.0-7.5,优选为7.2-7.4;kh2po4的浓度为0.5%-2.0%,优选为0.8%-1.8%,更优选为1.0%-1.4%;nahco3的浓度为0.05%-0.2%,优选为0.08%-0.18%,更优选为0.1%-0.14%;葡萄糖的浓度为0.01%-0.1%,优选为0.04%-0.08%。一般稀释液稀释纯化红细胞至1012-1014个/l。
上述技术方案中,加载剂是可以和染料分子结合的物质,如人工合成的dna片段,但不仅限于dna片段,也可以是人工合成的rna片段,加载体的用量为1.0-1.5μg/l。人工合成的dna片段没有特殊限制,可以是任意序列的100bp-2000bp的dna,优选200-1500bp,最优选500-800bp。dna分子经人工合成至表达载体中,表达载体可以是puc57载体,但不仅限于puc57载体,可以是其他可以在大肠杆菌中表达扩增的载体;克隆至载体中的dna分子经大肠杆菌扩增,可以得到大量的含dna片段的产物,产物经酶切纯化得到用于加载剂的dna片段。
上述技术方案中,将脉冲电磁场的作用下将加载剂引入到纯化红细胞内的过程为:电穿孔仪器90-120v电压刺激4-8秒钟。
上述技术方案中,细胞固定液为甲醛、戊二醛、丙酮、乙醇等常规固定剂中的一种或多种的混合。固定时间为3-5小时。
上述技术方案中,对红细胞和产物进行洗涤处理时,洗涤液为常规的等渗溶液,例如pbs缓冲液、d-hanks缓冲液、hepes缓冲液、柠檬酸缓冲液、氯化钠缓冲液、硼酸缓冲液等均可使用,并没有严格的限定。
上述技术方案中,细胞保存液为本领域常用物质,没有特殊限制,细胞保存液包括缓冲液、营养成分以及防腐剂组成。
以下结合实施例进一步说明本发明,实施例中所采用的化学试剂为分析纯,可通过商购获得。实施例中所涉及到的试剂包括以下几种。
洗涤液:每升蒸馏水中含nacl5.5g,na2hpo420.3g,nah2po43.1g。用hcl或naoh调节ph至7.0±0.1,用nacl调节渗透压至300±10mosm/kgh2o。
稀释液a:稀释液i:每100ml蒸馏水中含atp20g,mgcl212g。稀释液ii:每升蒸馏水中含kh2po412g,nahco31.2g,葡萄糖0.4g,ph值7.2。稀释液i:稀释液ii的体积比为1:40。
稀释液b:稀释液i:每100ml蒸馏水中含atp30g,mgcl215g。稀释液ii:每升蒸馏水中含kh2po410g,nahco31g,葡萄糖0.5g,ph值7.3。稀释液i:稀释液ii的体积比1:30。
稀释液c:稀释液i:每100ml蒸馏水中含atp25g,mgcl210g。稀释液ii:每升蒸馏水中含kh2po414g,nahco31.4g,葡萄糖0.8g,ph值7.4。稀释液i:稀释液ii的体积比1:50。
固定液:每升固定液中含有甲醛溶液100ml,戊二醛溶液20ml,乙二胺四乙酸二钠0.6g,nah2po40.15g。
保存液:每升蒸馏水中含柠檬酸0.2g,柠檬酸钠1.5g,nah2po41g,葡萄糖8g,甘露醇12g,甘氨酸7g,腺嘌呤0.2g,庆大霉素20万单位,混匀后用hcl或naoh调节ph值至7.0±0.1,用nacl调节渗透压至300±10mosm/kgh2o。
加载剂1:如序列表中序列1所示的dna经人工合成后克隆到puc57载体,经大肠杆菌内扩增,提取分离纯化表达载体,经酶切纯化后得到大量dna片段,得到加载剂1。
加载剂2:如序列表中序列2所示的dna经人工合成后克隆到pcdna3.1载体,经大肠杆菌内扩增,提取分离纯化表达载体,经酶切纯化后得到大量dna片段,得到加载剂2。
实施例1
将以edta-2k作为抗凝剂的抗凝全血放置离心机中,3000rpm离心5min,弃去上清液,用洗涤液清洗沉淀细胞,3000rpm离心5min,弃去上清液,重复洗涤1-2次,用白细胞滤器除去白细胞,用稀释液a将红细胞稀释至1012个/l,按1.5μg/l加入加载剂1,电穿孔仪器100v电压刺激5秒钟,将电刺激后的样品中加入固定剂室温下固定4小时。用洗涤液重复洗涤反应产物3-4次,用适量保存液对产物进行悬浮,用以核酸荧光染色为检测原理的血液细胞分析仪对上述质控物检测,结果参见图1(仅提供ret通道图像)。
实施例2
将以edta-2k作为抗凝剂的抗凝全血放置离心机中,3000rpm离心5min,弃去上清液,用洗涤液清洗沉淀细胞,3000rpm离心5min,弃去上清液,重复洗涤1-2次,用白细胞滤器除去白细胞,稀释液b将红细胞稀释至1013个/l,按1.2μg/l的加入加载剂2,电穿孔仪器90v电压刺激8秒钟,将电刺激后的样品中加入固定剂室温下固定4小时。用洗涤液重复洗涤反应产物3-4次,用适量保存液对产物进行悬浮,用以核酸荧光染色为检测原理的血液细胞分析仪对上述质控物检测,结果参见图2(仅提供ret通道图像)。
实施例3
将以edta-2k作为抗凝剂的抗凝全血放置离心机中,3000rpm离心5min,弃去上清液,用洗涤液清洗沉淀细胞,3000rpm离心5min,弃去上清液,重复洗涤1-2次,用白细胞滤器除去白细胞,稀释液b将红细胞稀释至1014个/l,按1.0μg/l的加入加载剂2,电穿孔仪器120v电压刺激4秒钟,将电刺激后的样品中加入固定剂室温下固定3小时。用洗涤液重复洗涤反应产物3-4次,用适量保存液对产物进行悬浮,用以核酸荧光染色为检测原理的血液细胞分析仪对上述质控物检测,结果参见图3(仅提供ret通道图像)。
实施例4
将以edta-2k作为抗凝剂的抗凝全血放置离心机中,3000rpm离心5min,弃去上清液,用洗涤液清洗沉淀细胞,3000rpm离心5min,弃去上清液,重复洗涤1-2次,用白细胞滤器除去白细胞,稀释液b将红细胞稀释至1012个/l,按1.3μg/l的加入加载剂2,电穿孔仪器100v电压刺激5秒钟,将电刺激后的样品中加入固定剂室温下固定5小时。用洗涤液重复洗涤反应产物3-4次,用适量保存液对产物进行悬浮,用以核酸荧光染色为检测原理的血液细胞分析仪对上述质控物检测,结果参见图4(仅提供ret通道图像)。
由附图1-4可见,本发明各实施例制得的血液质控物在血液分析仪中检测分析,得到与成熟红细胞区具有明显界限的网织红细胞区。因此,本发明方法得到的网织红细胞模拟物能够实现以核酸荧光染色为原理的网织红细胞的质量控制。本发明所得到的网织红细胞模拟物可以单独使用,完成对网织红细胞检测的质量控制,同时也可以与其他血液质控物,白细胞模拟粒子,血小板模拟粒子按比例制备成全血质控物,完成对血细胞分析仪的质量控制。本发明中涉及到的网织红细胞模拟粒子包含红细胞模拟粒子,其与红细胞模拟粒子的比例可以进行有效的调整。本发明中所设计的网织红细胞模拟物制备过程简单,所用试剂成分较单一,制得的产物产率较高,适合大量的生产。
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
序列表
<110>迪瑞医疗科技股份有限公司
<120>网织红细胞模拟物及其制备方法与应用
<160>2
<170>siposequencelisting1.0
<210>1
<211>600
<212>dna
<213>人工序列(artificialsequence)
<400>1
aggtgaaggtcggagtcaacggatttggtcgtattgggcgcctggtcaccagggctgctt60
ttaactctggtaaagtggatattgttgccatcaatgaccccttcattgacctcaactaca120
tggtttacatgttccaatatgattccacccatggcaaattccatggcaccgtcaaggctg180
agaacgggaagcttgtcatcaatggaaatcccatcaccatcttccaggagcgagatccct240
ccaaaatcaagtggggcgatgctggcgctgagtacgtcgtggagtccactggcgtcttca300
ccaccatggagaaggctggggctcatttgcaggggggagccaaaagggtcatcatctctg360
ccccctctgctgatgcccccatgttcgtcatgggtgtgaaccatgagaagtatgacaaca420
gcctcaagatcatcagcaatgcctcctgcaccaccaactgcttagcacccctggccaagg480
tcatccatgacaactttggtatcgtggaaggactcatgaccacagtccatgccatcactg540
ccacccagaagactgtggatggcccctccgggaaactgtggcgtgatggccgcggggctc600
<210>2
<211>480
<212>dna
<213>人工序列(artificialsequence)
<400>2
tcatccatgacaactttggtatcgtggaaggactcatgaccacagtccatgccatcactg60
ccacccagaagactgtggatggcccctccgggaaactgtggcgtgatggccgcggggctc120
tccagaacatcatccctgcctctactggcgctgccaaggctgtgggcaaggtcatccctg180
agctgaacgggaagctcactggcatggccttccgtgtccccactgccaacgtgtcagtgg240
tggacctgacctgccgtctagaaaaacctgccaaatatgatgacatcaagaaggtggtga300
agcaggcgtcggagggccccctcaagggcatcctgggctacactgagcaccaggtggtct360
cctctgacttcaacagcgacacccactcctccacctttgacgctggggctggcattgccc420
tcaacgaccactttgtcaagctcatttcctggtatgacaacgaatttggctacagcaaca480
- 还没有人留言评论。精彩留言会获得点赞!