细胞分析方法、细胞信息提供装置和系统、控制程序、记录介质与流程
本发明涉及细胞分析方法、细胞信息提供装置、及细胞信息提供系统等。
背景技术:
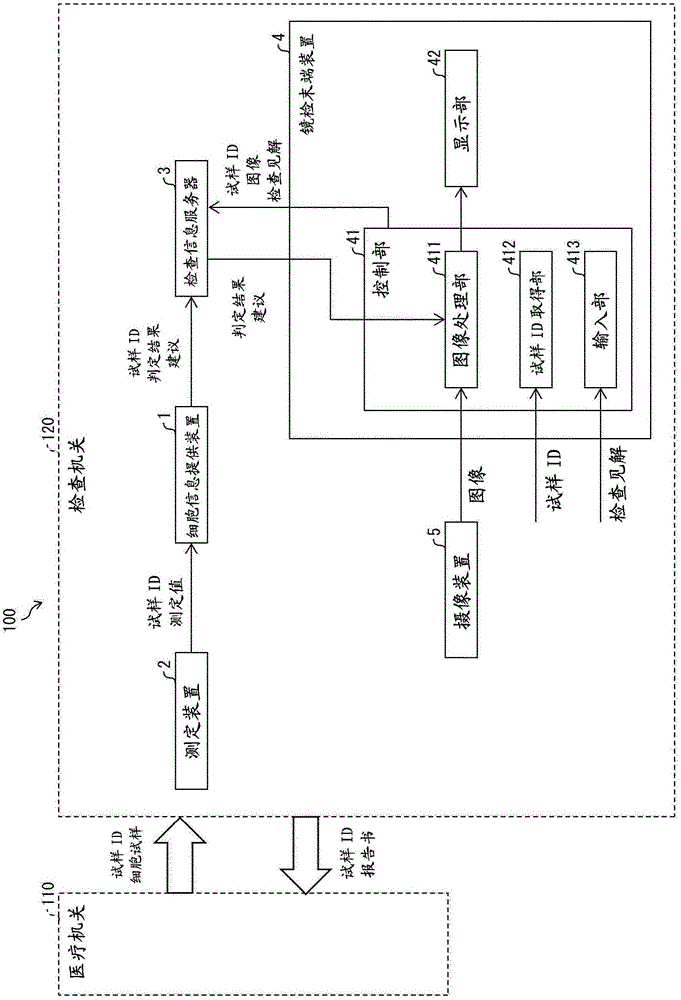
:已知自动分析从受试者的上皮组织采集的细胞,提供关于上皮组织的癌化的信息的分析装置(参照例如专利文献1)。子宫颈部、口腔等的上皮组织由基底层、副基底层、中层、表层形成。在专利文献1中记载的分析装置对于从受试者采集的细胞,取得含表示细胞的大小的数据、表示细胞核的大小的数据、及表示细胞所具有的dna量的数据的测定数据,基于细胞核的大小和作为细胞的大小的比的n/c比而确定作为解析对象接近基底膜的细胞的测定数据。此分析装置基于确定的测定数据中所含的dna量的数据而算出有g0期或g1期的dna量的细胞的数和有s期以上的dna量的细胞的数的比,基于算出的比超阈值与否而判断再检查必要(阳性)与否。【现有技术文献】【专利文献】【专利文献1】特开2013-24768号公报【发明的概要】【发明要解决的课题】例如,在子宫颈部的组织学诊断中,如图15的“组织学诊断的判断”所示,从正常的状态至癌的过程从正常的状态顺序地区分为“正常”、“cin1”、“cin2”、“cin3”、及“癌”的多个阶段。在上述专利文献1中记载的分析装置中,以易出现异形化为癌的初期阶段的细胞的基底膜侧的细胞的测定数据作为解析对象。所以,可区别受试者是处于如“cin2”至“cin3”一样的癌的初期阶段,还是处于被判断为不需要治疗的“cin1”以前的阶段。但是,在例如处于“cin1”以前的阶段时,优选可更详细地掌握将来发展到“cin2”阶段的可能性的程度、处于“cin2”往后的阶段时的癌化的进行程度等受试者的细胞的状态。【用于解决课题的手段】为了解决上述的课题,本发明的一实施方式涉及的细胞分析方法包括:在试样中所含的细胞之中,对如下第1细胞数及第2细胞数各自进行计数的计数步骤:基于细胞的大小和细胞核的大小而分类为第1组,表示有比阈值多的dna量的细胞的数的第1细胞数、及,基于细胞的大小和细胞核的大小而分类为与上述第1组不同的第2组,表示有比上述阈值多的dna量的细胞的数的第2细胞数;及对上述第1细胞数和上述第2细胞数进行比较的比较步骤。根据上述的构成,可取得表示在基于细胞的大小和细胞核的大小而分类的不同的组各自中的dna量多的细胞的存在状态的信息,可提供用于更详细地掌握受试者处于至达到癌的哪个状态等、受试者的细胞的状态的信息。在上述计数步骤中,也可基于细胞的大小和细胞核的大小而对上述试样中所含的细胞进行分类至上述第1组含表层侧的细胞、而上述第2组含基底侧的细胞。由此,可取得表示在表层侧和基底侧各自中的dna量多的细胞的存在状态的信息,不仅是基底侧的状态,也考虑表层侧的状态,可提供用于更详细地掌握受试者的细胞的状态的信息。在上述计数步骤中,也可基于细胞的大小和细胞核的大小的比率而将上述试样中所含的细胞分类为上述第1组和上述第2组。在上述计数步骤中,也可通过将上述比率与第2阈值比较,将上述细胞分类为上述第1组和上述第2组。在上述计数步骤中,也可基于从细胞核得到的荧光量而对有比上述阈值多的dna量的细胞进行计数。再者,荧光量是指反映细胞核中的dna量的荧光信息,含从细胞核得到的荧光的信号波形的脉冲面积、峰强度等。上述阈值也可为设定在显示二倍体细胞的dna量的值和显示比二倍体细胞多的dna量的值之间的值。试样中所含的细胞也可为从组织剥离的细胞。上述组织也可为上皮组织。在上述输出步骤中,也可根据上述第1细胞数比上述第2细胞数多与否,输出关于上述组织的表层及中层中的发育异常有无的信息。也可还具备在上述试样中所含的细胞之中,对如下第3细胞数及第4细胞数各自进行计数的第2计数步骤:表示细胞所具有的dna量在上述阈值以下的细胞的数的第3细胞数、及表示细胞所具有的dna量比上述阈值多的细胞的数的第4细胞数,在上述输出步骤中,基于上述第1细胞数和上述第2细胞数的比较结果,及上述第3细胞数和上述第4细胞数的比较结果而输出上述组织的状态。根据上述的构成,通过还利用关于上皮组织的细胞之中有比二倍体细胞多的dna量的细胞数多或少的信息,可进一步提升输出的信息的可靠性。为了解决上述的课题,本发明的一实施方式涉及的细胞分析方法包括:对于试样中所含的细胞,取得表示细胞的大小的第1数据、表示细胞核的大小的第2数据、及表示细胞的dna量的第3数据的数据取得步骤;对如下第1细胞数及第2细胞数各自进行计数的计数步骤:在基于上述第1数据及上述第2数据而分类为第1组的细胞之中,表示基于上述第3数据确定的细胞的数的第1细胞数、及在基于上述第1数据及上述第2数据而分类为与上述第1组不同的第2组的细胞之中,表示基于上述第3数据确定的细胞的数的第2细胞数;及对上述第1细胞数和上述第2细胞数进行比较的比较步骤。根据上述的构成,发挥与上述细胞分析方法同样的效果。在上述计数步骤中,也可基于从上述第1数据及上述第2数据求出的细胞的大小和细胞核的大小的比率而将上述试样中所含的细胞分类为上述第1组和上述第2组。在上述计数步骤中,也可通过将上述细胞的大小和细胞核的大小的比率与阈值比较,将上述试样中所含的细胞分类为上述第1组和上述第2组。上述阈值也可为设定在中层细胞的大小和该中层细胞的细胞核的大小的比率与副基底层细胞的大小和该副基底层细胞的细胞核的大小的比率之间的值。上述第1数据可为从上述细胞发生的散射光信号的脉宽,上述第2数据可为从上述细胞的细胞核发生的荧光信号的脉宽,上述第3数据可为上述荧光信号的脉冲面积。为了解决上述的课题,本发明的一实施方式涉及的细胞信息提供装置具备:在上述试样中所含的细胞之中,对如下第1细胞数及第2细胞数各自进行计数的计数部:基于细胞的大小和细胞核的大小而分类为第1组,表示有比阈值多的dna量的细胞的数的第1细胞数、及,基于细胞的大小和细胞核的大小而分类为与上述第1组不同的第2组,表示有比上述阈值多的dna量的细胞的数的第2细胞数;及对上述第1细胞数和上述第2细胞数进行比较的比较部。根据上述的构成,发挥与上述细胞分析方法同样的效果。为了解决上述的课题,本发明的一实施方式涉及的细胞信息提供装置具备:试样中所含的细胞之中,取得表示细胞的大小的第1数据、表示细胞核的大小的第2数据、及,表示细胞的dna量的第3数据的数据取得部;对如下第1细胞数及第2细胞数各自进行计数的计数部:基于上述第1数据及上述第2数据而分类为第1组,表示上述第3数据的值比阈值大的细胞的数的第1细胞数、及,基于上述第1数据及上述第2数据而分类为与上述第1组不同的第2组,表示上述第3数据的值比上述阈值大的细胞的数的第2细胞数;及对上述第1细胞数和上述第2细胞数进行比较的比较部。根据上述的构成,发挥与上述细胞分析方法同样的效果。也可还具备基于由上述比较部的比较结果而判断上述组织的状态的判断部。还具备在上述试样中所含的细胞之中,对如下第3细胞数及第4细胞数各自进行计数的第2计数部:表示细胞所具有的dna量在上述阈值以下的细胞的数的第3细胞数、及表示细胞所具有的dna量比上述阈值多的细胞的数的第4细胞数,上述判断部也可基于上述第1细胞数和上述第2细胞数的比较结果,及上述第3细胞数和上述第4细胞数的比较结果而判断上述组织的状态。通过具备这样的构成,可进一步提升判断结果的可靠性。上述数据取得部也可从含流式细胞仪的测定装置取得上述第1数据、上述第2数据、及上述第3数据。测定装置通过含流式细胞仪,测定装置可输出表示试样中所含的细胞的大小的第1数据、表示细胞的细胞核的大小的第2数据、及表示细胞所具有的dna量的第3数据。所以,细胞信息提供装置可利用能从流式细胞仪取得的适宜的测定数据。为了解决上述的课题,本发明的一实施方式涉及的细胞信息提供系统含:上述细胞信息提供装置,将由上述细胞信息提供装置给出的判断结果与试样的识别信息对应而存储的存储装置,及取得对被赋予与上述试样的识别信息相同的识别信息的试样进行摄像的图像,从上述存储装置读取对应于该识别信息的上述判断结果,显示上述图像和上述判断结果的镜检终端装置。根据上述的构成,发挥与上述细胞分析方法及上述细胞信息提供装置同样的效果。例如,当将关于组织的细胞的发育异常的信息提供于进行细胞学诊断及组织学诊断等的病理诊断的细胞检查员时,能高效且适合地进行病理诊断,再者诊断结果的可靠性也提升。本发明的各实施方式涉及的细胞信息提供装置可由计算机实现,此时,通过以计算机作为上述细胞信息提供装置所具备的各部(软件要素)运行而使上述细胞信息提供装置用计算机实现的细胞信息提供装置的控制程序、及记录其的计算机能读取的记录介质也在本发明的范畴内。【发明的效果】根据本发明的一实施方式,可提供用于更详细地掌握受试者的细胞的状态的信息。【附图的简单的说明】【图1】是显示本发明的一实施方式涉及的细胞信息提供系统的构成例的图。【图2】是对构成上皮组织的细胞层进行说明的模式图。【图3】是对dna量的直方图和细胞周期的关联进行说明的图。【图4】是显示测定装置的构成例的框图。【图5】是显示测定装置所具备的光学检测部及摄像部的构成例的框图。【图6】是对于从由测定装置测定的测定数据算出各种数据的方法进行说明的图。【图7】是例示作为细胞信息提供装置能利用的计算机的构成的框图。【图8】是显示本发明的一实施方式涉及的细胞信息提供装置的构成例的框图。【图9】是显示细胞信息提供装置进行的处理的流程的一例的流程图。【图10】是对于第1计数部计数的细胞数进行说明的模式图。【图11】是显示细胞信息提供装置进行的处理的流程的别的例的流程图。【图12】是对于第2计数部计数的细胞数进行说明的模式图。【图13】是显示分类表的一例的图。【图14】是显示评论对应表的一例的图。【图15】是对上皮组织中的前癌病变和细胞学诊断断中的分类的关系进行说明的图。【图16】是显示镜检终端装置显示镜检图像、及由细胞信息提供装置给出的判断结果的画面显示的一例的图。【图17】是在验证由细胞信息提供装置给出的判断结果的一实施例中的结果。【具体实施方式】首先,使用图1对利用本发明的一实施方式涉及的细胞信息提供装置1的细胞信息提供系统100的概略构成进行说明。图1是显示本发明的一实施方式涉及的利用细胞信息提供系统100的检查机关120的构成例的图。如图1所示,细胞信息提供系统100是能适宜地应用于对从医疗机关110提供的细胞试样中所含的细胞进行分析的检查机关120的系统。(医疗机关110)图1中所示的医疗机关110是进行患者等的受试体的诊察的机关,可根据需要,采集受试体的细胞。在医疗机关110,可进行对于依赖于检查机关120的分析及检查必要的预处理,此时,实施预处理的细胞作为细胞试样被提供于检查机关120。再者,向每个细胞试样赋予试样id,与成为细胞的来源的受试体的信息等对应。在本说明书中,举对子宫颈部等的上皮组织的细胞进行分析的情况作为例进行说明。再者,本发明的一实施方式涉及的细胞信息提供系统100,作为主要的分析对象的细胞,例如,在子宫颈部以外,可举出从口腔、食道、或者支气管等的上皮组织剥离的细胞。另外,从子宫内膜剥离的细胞、及从泌尿器剥离的尿中的细胞、及体腔液内的细胞等也可成为细胞信息提供系统100的分析对象。<上皮组织的构成、及上皮组织中所含的细胞的特征>其中,使用图2及图3对于上皮组织的构成、及上皮组织中所含的细胞的特征进行说明。首先,将成为细胞信息提供装置1进行判断的对象的上皮组织的构成、及上皮组织中所含的细胞的特征的概略使用图2进行说明。图2是对构成上皮组织的细胞层进行说明的模式图。多种细胞从基底膜顺序地各自成层状存在于这些组织中的上皮中。再者,在本说明书中,在以基底膜作为下层时,将位于上层的表层及中层称为表层侧。一方面,将副基底层及基底层称为基底层侧或深层系。例如,在子宫颈部及口腔粘膜中,与外界邻接的侧对应于表层侧。在子宫颈部中,如图2所示,从基底膜侧顺序地形成了由基底细胞形成的层(基底层)、由副基底细胞形成的层(副基底层)、由中层细胞形成的层(中层)、及由表层细胞形成的层(表层)。基底膜附近的基底细胞向副基底细胞、副基底细胞向中层细胞、中层细胞向表层细胞分化。另外,在口腔粘膜中,从基底膜侧顺序地形成了基底细胞的层、鳞状细胞的层、颗粒细胞的层、及角质层。将这些综合在以下的表1。【表1】在构成上皮的多种细胞之中,涉及癌化的细胞是基底细胞。在发展到癌的过程中,基底细胞异形化而成为异型细胞(获得发育异常而成为异型细胞的细胞)。异型细胞获得增殖能,变得从基底层侧占表层侧。因此,在发展到癌的初期阶段,存在于子宫颈部的上皮组织的基底层、副基底层、及中层的细胞中大量存在癌化细胞。另外,口腔粘膜的上皮组织的情况,存在于基底细胞的层及鳞状细胞的层的细胞中大量存在癌化细胞。相反,在发展到癌的初期阶段,在存在于子宫颈部的上皮组织的表层及口腔粘膜的上皮组织的角质层等的上皮组织的表层侧的层的细胞中,癌化细胞极其少。另外已知,在前述的上皮组织中,随着从表层侧的层向基底膜侧的层,细胞的大小逐渐变小,而细胞核的大小逐渐变大。从而,细胞核的大小和细胞的大小的比率(后述的n/c比)也随着从表层侧的层向基底膜侧的层而逐渐变大。构成子宫颈部的上皮组织的各细胞的形态、细胞质的大小(即,细胞的大小)、及细胞核的大小示于以下的表2。【表2】名称细胞形态细胞质的大小核的大小表层细胞多边形50~60μm5μm中层细胞多边形~类圆形30~50μm8μm副基底细胞类圆形20μm9μm基底细胞圆形~类圆形12~14μm8~10μm根据表2,子宫颈部的上皮组织的情况,基底细胞的n/c比是0.57~0.83,副基底细胞的n/c比是0.45,中层细胞的n/c比是0.16~0.27,表层细胞的n/c比是0.08~0.1。从而,例如,n/c比在0.3以上的细胞是含副基底细胞及基底细胞的深层系细胞,n/c比不足0.3的细胞是表-中层细胞。这样,在子宫颈部、口腔、食道、或者支气管等的发生扁平上皮化生的组织中,能基于n/c比的值而区别细胞是深层系细胞,还是表-中层细胞。接下来,使用图3对于细胞的dna量的变化及异形化的细胞的dna量进行说明。图3是对dna量的直方图和细胞周期的关联进行说明的图。细胞如图3所示,根据一定的循环(细胞周期)而经dna复制、染色体的分配、核分裂、及细胞质分裂等的事件而分裂为二个细胞,增殖。分裂后的细胞回到出发点。细胞周期可对应于其阶段(阶段)而分为以下的4期。g1期:为了进入到s期的准备和检查的时期s期:dna合成期g2期:为了进入到m期的准备和检查的时期m期:分裂期即,细胞处于向上述的4期加细胞增殖休止的休止期(g0期)的5期之中之任一者的阶段。在根据细胞周期而增殖的过程中,细胞核的染色体也增加。所以,通过对细胞的dna量进行测定,可推定细胞处于细胞周期的何阶段。在正常的细胞的情况中,在g1期的dna量一定,在随后的s期dna量缓慢地增加,其后进入到g2期则成为一定的值,此值在m期也维持。对于关于从由正常的细胞构成的上皮等的组织采集的细胞的dna量的直方图,例如,成为如图3所示的直方图。有最高的峰的山对应于dna量最少的处于g0期或g1期的细胞,有次高的峰的山对应于dna量最多的处于g2期或m期的细胞,它们之间对应于处于s期的细胞。当分析对象的细胞均为正常的细胞时,处于s期、g2期、或者m期之任一者的阶段的细胞的数和处于g0期、或者g1期的细胞的数的比呈现大致一定的范围内的值。但是,在含癌化的细胞或癌化的过程中异形化的细胞时,与正常细胞比染色体的数异常多而dna量也多的异常细胞的存在频度升高。例如,推定分析对象的细胞中含癌化细胞或在癌化的过程中异形化的细胞与否时,以正常的处于g0期或g1期的细胞的数与有比正常的处于g0期或g1期的细胞所具有的dna量多的dna量的细胞的数的比作为判断基准即可。具体而言,在图3中所示的dna量直方图中,最左侧的山对应于有相当于处于g0期或g1期的正常细胞所具有的dna量的dna量的细胞,其右侧的3个山对应于有比处于g0期或g1期的正常细胞的dna量多的dna量的细胞。将与处于g0期或g1期的正常细胞有同等的dna量的细胞在以下记为“相当于二倍体细胞的dna量的细胞”。另外,将有比处于g0期或g1期的正常细胞所具有的dna量多的dna的细胞记为“比二倍体细胞dna量多的细胞”等。再者,在图3中,将显示正常的dna量的范围表述为“2c”,将表示g2期及m期的细胞所具有的dna量的范围表述为“4c”。这些右侧的3个山被认为含对应于图3中所示的处于s期的细胞(正中的2个山)、或者处于g2/m期的细胞(最右侧的山),及癌化细胞及在癌化的过程中异形化的细胞。进而认为,癌化细胞的数变得越多,右侧的3个山变得越大。再者,在图3中,为了使易于理解,显示有3个山的例,但在实际制成从受试者采集的子宫颈部的上皮组织中所含的细胞的dna量直方图时,可识别为山的数根据受试者的状态来决定。(检查机关120)回到图1,检查机关120是对从医疗机关110送到的细胞试样进行分析或检查的机关。在检查机关120,不限定于其,但设置有测定装置2、细胞信息提供装置1、检查信息服务器3、及镜检终端装置4等。在检查机关120,对应于来自医疗机关110的分析依赖,细胞试样被分析-检查,基于分析结果及检查结果而制成报告书。该报告书提供于作为分析依赖源的医疗机关110。(细胞信息提供系统100的构成)在以下,对于检查机关120具备的细胞信息提供系统100的构成进行说明。细胞信息提供系统100如图1所示,测定装置2、细胞信息提供装置1、检查信息服务器3、及含由进行细胞试样的细胞学诊断、及组织学诊断等的细胞检查员使用的镜检终端装置4。测定装置2、细胞信息提供装置1、及镜检终端装置4的构成的详细在下文说明。检查信息服务器3将由细胞信息提供装置1的判断结果与分析试样固有的试样id(识别信息)对应而存储。镜检终端装置4取得对赋予试样id的涂抹标本(试样)进行摄像的图像,从检查信息服务器3读取对应于与该涂抹标本相同的试样id的判断结果,图像和判断结果一同显示于显示部42。再者,试样id也可使用与针对每个受试体赋予的id(例如,患者编号等)相同的。在医疗机关110,使用从受试体的组织剥离(采集)的成为分析对象的细胞而制作的细胞试样在实施指定的预处理的状态下被送到检查机关120。在送到检查机关120的细胞试样中,可含供于测定装置2的测定试样(试样)、及供于镜检等的细胞学诊断及组织学诊断的涂抹标本。向细胞试样赋予固有的试样id,在检查机关120进行的全部的检查的结果,分析的结果,及观察结果等对应于试样id而存储到检查信息服务器3中。即,在检查机关120,从检查信息服务器3读取对应于每个试样id的摄像图像、及检查观察结果等,使用这些制成报告书。制成的报告书与试样id对应而提供于医疗机关110。一般而言,由于由测定装置2的分析在涂抹标本的细胞学诊断之前进行,来自细胞信息提供装置1的判断结果在赋予相同的试样id的涂抹标本的细胞学诊断之前提供。如果应用这样的系统,使用镜检终端装置4而进行细胞学诊断的者可在参照从细胞信息提供装置1提供的关于细胞试样的判断结果及评论的基础上,有效且适合地进行镜检等的病理诊断。(测定装置2的构成)接下来,对于测定装置2的构成而使用图4进行说明。图4是显示测定装置2的构成例的框图。如图4所示,测定装置2向细胞信息提供装置1提供测定数据。测定装置2具备由从测定试样中所含的细胞检测前方散射光信号波形数据fs及荧光信号波形数据fl等的流式细胞仪构成的光学检测部30,信号处理电路50,测定控制部16,电机、运作器、及阀等的驱动部17,含各种传感器的传感器18和对细胞的图像进行摄像的摄像部26。信号处理电路50具备对将光学检测部30的输出由前置放大器(未图示)扩增的进行扩增处理或过滤处理等的模拟信号处理电路,将模拟信号处理电路的输出变换为数字信号的a/d转换器和对数字信号进行指定的波形处理的数字信号处理电路。另外,测定控制部16通过对传感器18的信号进行处理的同时控制驱动部17的动作,进行测定试样的抽吸或测定。作为测定试样,可使用对受试体的上皮组织的细胞(例如,从子宫颈部采集的细胞)实施离心分离、稀释(悬浮)、搅拌、pi染色等的处理而调制的。这样调制的测定试样被赋予试样id,在收容在试管的状态下配置在试样设置部(未图示)的指定位置,接下来搬送到测定装置2的移液器(未图示)下方位置,由所述移液器抽吸与鞘液一同供给到流动池,在流动池形成试样流。pi染色是使用作为通过嵌入到dna的双螺旋而与dna结合的荧光染料的碘化丙啶(pi)而对dna进行染色的处理。由于在pi染色中对细胞核选择性地实施染色,变得能检测来自细胞核的红色荧光。pi染色使用含红色的染料的荧光染色液进行。测定控制部16具备微处理器20、存储部21、i/o控制器22、传感器信号处理部23、驱动部控制驱动器24、及外部通信控制器25等。存储部21由rom、ram等构成,在rom中储存,对于用于控制驱动部17的控制程序及所述控制程序的执行必要的数据。微处理器20能向ram加载控制程序,或者从rom直接执行。在微处理器20中,来自传感器18的信号通过传感器信号处理部23及i/o控制器22传递。微处理器20通过执行控制程序,可对应于来自传感器18的信号,经i/o控制器22及驱动部控制驱动器24而控制驱动部17。微处理器20使用fs及fl等的测定数据,对于各细胞而算出细胞的大小(第1数据)、细胞核的大小(第2数据)、及dna量(第3数据)。第1数据、第2数据、及第3数据经外部通信控制器25而发送到细胞信息提供装置1等的外部机器。接下来,使用图5对于光学检测部30及摄像部26的构成进行说明。图5是显示测定装置所具备的光学检测部30及摄像部26的构成例的框图。在其中所示的例中,光学检测部30由流式细胞仪构成,具备由半导体激光构成的光源53,从此光源53放射的激光经透镜系统52而聚光到流经流动池51的测定试样。由此激光而从测定试样中的细胞发生的前方散射光经物镜54及滤镜57而被光电二极管(光接收部)55检测。再者,透镜系统52由含准直管透镜、柱面透镜、聚光透镜等的透镜组构成。再者,从细胞发生的荧光及侧方散射光经配置在流动池51的侧方的物镜56而入射到二向色镜61。进而,反射此二向色镜61的荧光及侧方散射光入射到二向色镜62。透过二向色镜62的荧光经滤镜63而由光电倍增管59检测。另外,反射二向色镜62的侧方散射光经滤镜64而由光电倍增管58检测。光电二极管55、光电倍增管58及光电倍增管59将检测的光变换为电信号,各自输出前方散射光信号(fsc)、侧方散射光信号(ssc)及荧光信号(sfc)。这些信号由未图示的前置放大器扩增之后,传送到前述的信号处理电路50(参照图4)。如图4所示,在信号处理电路50中实施过滤处理或a/d变换处理等的信号处理而得到的前方散射光波形数据(fs)、侧方散射光波形数据(ss)及荧光波形数据(fl)在微处理器20中在第1数据、第2数据、及第3数据的算出中利用。算出的第1数据、第2数据、及第3数据经外部通信控制器25而传送到前述的细胞信息提供装置1。再者,作为光源53,也可代替上述半导体激光而使用气体激光,但从低成本、小型、并且低消费电力的方面考虑,优选采用半导体激光。可由半导体激光的采用降低制品成本的同时,谋求装置的小型化及省电力化。在本实施方式中,使用对于使光束窄聚有利的波长短的蓝色半导体激光。蓝色半导体激光对于pi等的荧光激发波长也有效。再者,在半导体激光之中,也可使用低成本并且长寿命,且自厂商的供给稳定的红色半导体激光。另外,在图4中所示的测定装置2中,除了光学检测部30之外,设有摄像部26。此摄像部26如图5所示,具备由脉冲激光构成的光源66和ccd摄像机65,来自光源66的激光经透镜系统60而入射到流动池51,进一步透过物镜56及二向色镜61而在ccd摄像机65成像。光源66在指定的时机发光而使由ccd摄像机65的摄像变得可能。如图4所示,由ccd摄像机65摄像的细胞的图像也可为由微处理器20,经外部通信控制器25而传送到细胞信息提供装置1的构成。此时,细胞的图像在细胞信息提供装置1中,对应于所述细胞涉及的第1数据、第2数据、及第3数据而存储在存储部12。(第1~第3数据的算出方法)接下来,对于测定装置2的微处理器20算出第1数据、第2数据、及第3数据的方法而使用图6进行说明。图6是对于从由测定装置2测定的测定数据算出各种数据的方法进行说明的图。在图6中显示含细胞质及细胞核的细胞的模式图和从此细胞得到的前方散射光信号波形及荧光信号波形。在图6中,坐标图的纵轴表示前方散射光及荧光的强度。前方散射光信号波形的宽度表示细胞质的宽度、即表示细胞的大小(c)的值,荧光信号波形的宽度表示表示细胞核的大小(n)的值。微处理器20基于从各细胞发生的前方散射光信号波形的宽度(前方散射光信号的脉宽)、及从各细胞的细胞核发生的荧光信号波形的宽度(荧光信号的脉宽)而算出第1数据、及第2数据。再者,也可代替前方散射光信号波形的宽度及荧光信号波形的宽度而使用各自前方散射光信号波形的信号强度及光信号波形的信号强度。另外,微处理器20算出表示在图6中所示的坐标图(指定的坐标面)中被荧光信号波形(荧光信号)和相对于荧光信号波形的指定的基线包围的区(在图6中实施阴影的部分)的面积(荧光信号的脉冲面积)的第3数据。再者,也可代替由荧光信号波形和指定的基线包围的区域的面积而使用荧光信号波形的高度算出第3数据。在图4中所示的例中,显示微处理器20算出第1数据、第2数据、及第3数据的构成,但不限于此。例如,也可为从信号处理电路50将第1数据、第2数据、及第3数据输出到微处理器20的构成。(细胞信息提供装置1的构成)细胞信息提供装置1是在试样中所含的细胞之中,基于细胞的大小和细胞核的大小而分类为第1组,表示有比阈值多的dna量的细胞的数的第1细胞数和基于细胞的大小和细胞核的大小而被分类为与上述第1组不同的第2组、且基于显示有比上述阈值多的dna量的细胞的数的第2细胞数的比较结果而得到关于异形化的细胞的存在状况、及异型细胞的增加的倾向的信息的装置。接下来,使用图7对于细胞信息提供装置1的构成进行说明。图7是例示能作为细胞信息提供装置1利用的计算机910的构成的框图。计算机910具备经总线911互相连接的计算装置912、主存储装置913、辅助存储装置914、输入输出接口915和通信接口916。输入输出接口915连接着使用者用于向计算机910输入各种信息的输入装置920、使用者用于向计算机910输出各种信息的输出装置930,通信接口916连接着外部机器940。外部机器940,例如,含图1中所示的测定装置2及检查信息服务器3等。<细胞信息提供装置1的硬件构成的详细>在这里,使用图7对于细胞信息提供装置1的硬件构成的细节进行说明。细胞信息提供装置1的各块可由形成在集成电路(ic芯片)等的逻辑电路(硬件)实现,也可由软件实现。在后者的情况中,可使用如图7所示的计算机(电子计算机)构成细胞信息提供装置1。图7是例示能作为细胞信息提供装置1利用的计算机910的构成的框图。计算机910具备经总线911互相连接的计算装置912、主存储装置913、辅助存储装置914、输入输出接口915和通信接口916。计算装置912、主存储装置913、及辅助存储装置914也可各自为例如处理器(例如cpu:中央处理器,centralprocessingunit等)、ram(随机访问存储器,randomaccessmemory)、硬盘驱动器。输入输出接口915连接着使用者用于向计算机910输入各种信息的输入装置920、使用者用于向计算机910输出各种信息的输出装置930、及测定装置2及检查信息服务器3等的外部机器940。输入装置920及输出装置930可内藏于计算机910中,也可与计算机910连接(外设)。例如,输入装置920可为键盘、鼠标、触摸传感器等,输出装置930可为显示器、打印机、扬声器等。另外,也可应用如触摸传感器和显示器一体化的触控面板一样的,有输入装置920及输出装置930的双方的功能的装置。进而,通信接口916是用于计算机910与外部的装置通信的接口。在辅助存储装置914中,储存用于以计算机910作为细胞信息提供装置1运行的各种程序。进而,计算装置912通过在主存储装置913上展开储存到辅助存储装置914的上述程序而执行该程序中所含的命令,以计算机910作为细胞信息提供装置1所具备的各部发挥功能。再者,辅助存储装置914所具备的记录程序等的信息的记录介质是计算机能读取的“非暂时性的有形的介质”即可,例如,也可为带、盘、卡、半导体存储器、可编程逻辑电路等。另外,只要是能将记录介质中记录的程序不在主存储装置913上展开而执行的计算机,就也可省略主存储装置913。再者,上述各装置(计算装置912、主存储装置913、辅助存储装置914、输入输出接口915、通信接口916、输入装置920、输出装置930、及外部机器940)可为各自1个,也可为多个。另外,上述程序可从计算机910的外部取得,此时,也可经任意的传送介质(通信网络或放送波等)而取得。进而,本发明以上述程序由电子传送具现化的、埋入到搬送波的数据信号的形态也可实现。图8是对细胞信息提供装置1的软件构成进行说明的功能块图。细胞信息提供装置1具备数据取得部13、控制部11、存储控制部11使用的各种数据的存储部12、及输出部14。控制部11统括细胞信息提供装置1具备的各部而进行控制。控制部11具备n/c算出部111、第1计数部112(计数部)、第2计数部113、发育异常度判断部114。发育异常度判断部114具备第1比较部1141(比较部)、第2比较部1142、及判断部1143。存储部12存储分类表121及评论对应表122。再者,图7中所示的通信接口916作为数据取得部13及输出部14发挥功能。即,细胞信息提供装置1经通信接口916而从含流式细胞仪等的光学检测部的测定装置2取得显示细胞的大小的第1数据、显示细胞核的大小的第2数据、显示dna量的第3数据、及试样id。另外,细胞信息提供装置1经通信接口916而向检查信息服务器3输出试样id、判断结果,及评论。计算装置912作为控制部11的各功能块发挥功能,辅助存储装置914作为存储部12发挥功能。(细胞信息提供装置进行的处理的流程)其中,参照图8中所示的功能块,使用图9对于细胞信息提供装置1进行的处理流程进行说明。图9是显示细胞信息提供装置1进行的处理的流程的一例的流程图。数据取得部13从测定装置2取得关于从受试体的上皮组织采集的细胞的显示细胞的大小的第1数据、显示细胞核的大小的第2数据、及显示dna量的第3数据(步骤s1:数据取得步骤)。再者,数据取得部13也可为从测定装置2取得从分析试样(试样)中所含的各细胞得到的前方散射光信号波形数据、及各细胞的荧光信号波形数据等的测定数据的构成。此时,细胞信息提供装置1还具备使用前方散射光信号波形数据及荧光信号波形数据而算出第1数据、第2数据、及第3数据的数据算出部(未图示)即可。再者,在进行上述的处理的数据取得部13向每个含从每个受试体、或者受试体的组织采集的细胞的分析试样赋予个别的试样id(识别信息)时,数据取得部13也可为与测定数据一同取得试样id的构成。数据取得部13对除去显示细胞无法有的大小的数据等的有效数据数进行计数。当有效数据数不足设定为对于细胞信息提供装置1输出担保一定的可靠性的判断结果必要的测定数据数的目标值(例如,5000)时(在步骤s2中no),输出部14有效数据数不足,输出称为不能判断的信息(步骤s15)。再者,前述的“5000”的目标值是作为判断细胞学诊断的检查的适当性的指标一般使用的数字,在本实施方式中,也作为用于保证分析精度的目标值采用。有效数据数在目标值以上时(在步骤s2中yes)、n/c算出部111对于各细胞而算出细胞的大小和其细胞的细胞核的大小的比(n/c比)(步骤s3)。再者,n/c算出部111制成如图10所示的散点图(步骤s4)。制成的散点图也可为与判断结果一同从输出部14输出到显示装置(未图示)而显示的构成。即,n/c算出部111对于各细胞算出细胞的大小和细胞核的大小的比率作为从第1数据及第2数据算出的关于细胞的形态的特征值。在以下,举n/c算出部111算出细胞的大小(c)和该细胞的细胞核的大小(n)的比率(以下,记为“n/c比”)的情况作为例进行说明。但是,不限定于其,例如,n/c算出部111算出的值只要是关于细胞的形态的值即可。即,n/c算出部111也可以相对于细胞核的大小的细胞的大小(c/n比)作为特征值算出。或者,n/c算出部111也可使用指定的关系式,从细胞核和细胞的大小的关系算出表示各细胞的形态的值。再者,采用与n/c比不同的特征值时,后述的第2阈值可对应于采用的特征值而适宜设定。第1计数部112取得各细胞的n/c比、及各细胞的dna量。另外,第1计数部112设定第2阈值(例如,n/c=0.3)。例如,在图10中,以一点划线表示第2阈值。第1计数部112对n/c比在第2阈值以下的区域(图10的区域l)的dna量多的细胞数p(第1细胞数)和比第2阈值大的区域(图10的区域h)的dna量多的细胞数q(第2细胞数)进行计数(步骤s5:第1计数步骤(计数步骤))。即,细胞数p是基于细胞的大小和细胞核的大小而属于区域l(分类为第1组)细胞之中,有比第1阈值(阈值)多的dna量的细胞的数。一方面,细胞数q是基于细胞的大小和细胞核的大小而属于区域h(分类为第2组)细胞之中,有比第1阈值多的dna量的细胞的数。例如,第1计数部112使用n/c算出部111算出的n/c比、及从数据取得部13取得的表示细胞的dna量的第3数据,对如下细胞数p及细胞数q各自进行计数:n/c比在第2阈值以下的细胞之中,表示第3数据的值比第1阈值大的细胞数的细胞数p、及,n/c比比第2阈值大的细胞之中,表示第3数据的值比第1阈值大的数的细胞数q。即,n/c比相对小的细胞和n/c比相对大的细胞对于n/c比而使用设定的第2阈值进行区别。再者,第2阈值是指为了基于细胞的形态区别含表层及中层的细胞的表-中层细胞(表层侧的细胞)和含副基底层及基底层的细胞(基底侧的细胞)的深层系细胞而设定的值。再者,在这里,举作为第2阈值使用1个值的情况作为例进行说明,但不限定于其,第2阈值也可为有一定的宽度的值。例如,规定用于规定n/c比相对小的细胞的上限的阈值和规定用于规定n/c比相对大的细胞的下限的阈值也可为不同的值。再者,第1计数部112,例如,也可制成对于各细胞的第1数据和n/c比的散点图,对有此散点图中标绘于指定的区域(参照图10的区域l及区域h)内的数据的组的细胞的数进行计数的构成。此时,第2阈值设定为分割为散点图的n/c比的值域不同的2个区域的分界线。第1计数部112对2个区域各自所含的细胞数各自进行计数。一方面,“第1阈值”是指设定在显示二倍体细胞的dna量的值和显示比二倍体细胞多的dna量的值之间的值,是为了区别是相当于二倍体细胞的dna量的细胞,还是比二倍体细胞dna量多的细胞而设定的值。即,第1计数部112对如下细胞数各自进行计数:n/c比在第2阈值以下的细胞之中,细胞所具有的dna量比第1阈值多的细胞数、及,n/c比比第2阈值大的细胞之中,细胞所具有的dna量比第1阈值多的细胞数。再者,第1计数部112,例如,可制成对于细胞的dna量的直方图,第1阈值也可为从此直方图中相当于二倍体细胞的峰的最频值及半值宽度等使用统计学方法算出的值。<在步骤s5中对第1细胞数及第2细胞数进行计数的方法>在这里,使用图10对于第1计数部112对第1细胞数及第2细胞数进行计数的方法进行说明。图10是对于第1计数部112计数的细胞数进行说明的模式图。如图10所示,在以n/c比作为横轴,以第1数据作为纵轴的散点图中,对应于测定试样中的细胞的数据的各标绘点显示呈右下降的新月形状的分布。在步骤s5中,第1计数部112基于从各细胞的细胞核得到的荧光信号的脉冲面积、即荧光量而对有比第1阈值多的dna量的细胞进行计数。具体而言,第1计数部112取得n/c算出部111算出的各细胞的n/c比、及对应于从各细胞的细胞核得到的荧光量的各细胞的dna量。进而,第1计数部112对n/c比在第2阈值(例如,0.3)以下的区域l的dna量多的细胞数p、及比第2阈值大的区域h的dna量多的细胞数q各自进行计数。再者,图10是模式图,方便地将对应于有相当于二倍体细胞的dna量的细胞的标绘点用“×”表示,将对应于有比二倍体细胞少的dna量的细胞的标绘点用黑色圆点表示,将对应于有比二倍体细胞多的dna量的细胞的标绘点用“白色圆点”表示。第1计数部112计数的细胞数p是在图10中区域l的白色圆点的数,细胞数q是区域h的白色圆点的数。回到图11的流程图,第1比较部1141对第1计数部112计数的细胞数p和细胞数q进行比较。判断部1143基于此比较结果而判断细胞的状态。例如,判断部1143在比较结果是细胞数p/细胞数q≥0.6时(在步骤s9中yes:比较步骤),判断为有出与在上皮组织的表层及中层发育异常关联的观察结果的可能性(步骤s21:判断步骤)。一方面,判断部1143在比较结果是细胞数p/细胞数q<0.6时(在步骤s9中no:比较步骤),判断为有出与在上皮组织的深层系细胞中发育异常关联的观察结果的可能性(步骤s22:判断步骤)。再者,也可为将如上所述的比较结果,及含关于含试样中所含的细胞的组织的状态的信息的判断结果的至少任一方从输出部14输出到显示装置等的外部机器(参照图7)(输出步骤)的构成。(细胞信息提供装置进行的处理的流程的变形例)接下来,以下使用图11对于控制部11具备第2计数部113,并且发育异常度判断部114具备第2比较部1142,判断部1143还使用有dna量在第1阈值以下的dna量的细胞数和有dna量比第1阈值多的dna量的细胞数的比(cpix值)而进行判断的处理流程进行说明。图11是显示细胞信息提供装置1进行的处理的流程的别的例的流程图。再者,为了说明的便利,对于进行与上述实施方式中说明的步骤同样的处理的步骤而付记相同的符号,省略其说明。第2计数部113使用在步骤s3中n/c算出部111算出的n/c比而确定关于基底侧的细胞的测定数据,使用确定的测定数据中所含的dna量的数据而制成直方图(步骤s6)。关于基底侧的细胞的测定数据的特定,例如,通过提取n/c比在0.3以上的细胞的测定数据来进行。进而,第2计数部113各自算出在此直方图中有第1阈值以下的dna量的细胞数d(第3细胞数)、有比及第1阈值多的dna量的细胞数m(第4细胞数)(步骤s7:第2计数步骤)。<在步骤s8中对细胞数d及细胞数m进行计数的方法>在这里,使用图12对于第2计数部113对细胞数d及细胞数m进行计数的方法进行说明。图12的纵轴表示细胞的数、横轴表示细胞的dna量。属于图12中所示的a以上b以下的范围的细胞是有相当于二倍体细胞的dna量的dna量(在参照图3中的“2c”)的细胞。第2计数部113将属于图12中所示的a以上b以下的范围的细胞数作为细胞数d进行计数。一方面,属于大于b且c以下的范围的细胞是有比二倍体细胞的dna量多的dna量(在图3中的“4c”等)的细胞。第2计数部113将属于图12所示的大于b且c以下的范围的细胞数作为细胞数m进行计数。即,在作为细胞数d计数的细胞中,含处于g0期及g1期的正常的细胞,在作为细胞数m计数的细胞中,含处于s期、g2期、及m期的细胞,癌化的细胞及异形化的细胞。再者,图12中所示的b的值(第1阈值)是为了分有比二倍体细胞多的dna量的细胞与否而设定的值即可,例如,也可为以二倍体细胞所具有的dna量作为基准而预先设定的值。例如,在分析对象的细胞中,考虑分析的精度或可靠性,由各种实验或验证等选定正常的dna量的范围(图12的a-b间)及异常的dna量的范围(图12的b-c间)即可。回到图11的流程图,继续对细胞信息提供装置1进行的处理的流程进行说明。再者,在以下,对于第2比较部1142对cpix值和作为成为基准的指定的值的0.2进行比较的情况进行说明。第2比较部1142使用第2计数部113算出(步骤s7)的细胞数d和细胞数m而算出cpix值(细胞数m/细胞数d)(步骤s8),对cpix值和0.2进行比较。一方面,第1比较部1141进行与前述的步骤s9同样的处理(步骤s9及步骤s12:比较步骤)。判断部1143参照分类表121,如下所述判断。·在cpix值不足0.2(在步骤s8中no),并且,细胞数p/细胞数q不足0.6(在步骤s9中no)时,判断为分类1(步骤s10)。·在cpix值不足0.2(在步骤s8中no),并且,细胞数p/细胞数q在0.6以上(在步骤s9中yes)时,判断为分类2(步骤s11)。·在cpix值在0.2以上(在步骤s8中yes),并且,细胞数p/细胞数q在0.6以上(在步骤s12中yes)时,判断为分类3(步骤s13)。·在cpix值在0.2以上(在步骤s8中yes),并且,细胞数p/细胞数q不足0.6(在步骤s12中no)时,判断为分类4(步骤s14)。<分类表121的详细内容>其中,使用图13对于分类表121进行说明。图13中所示的分类表121规定在判断部1143判断分析试样中所含的细胞的发育异常度时参照的第1基准、及第2基准的一例。图13中所示的分类表的“cpix值”的栏是关于第2基准的规定,“区域l的dna量多的细胞数/区域h的dna量多的细胞数”(参照图10)的栏是关于第1基准的规定。其中,cpix值是指作为细胞数d和细胞数m的比算出,表示有比二倍体细胞的dna量多的dna量的细胞的比率的值。在cpix值高的情况中,可作为显示以何种程度怀疑癌化的细胞及异形化的细胞的存在的值活用。在图13中所示的例中,以“区域l的dna量多的细胞数”和“区域h的dna量多的细胞数”的比在0.6以上与否作为基准,但不限于此。例如,也可将“区域l的dna量多的细胞数”和“区域h的dna量多的细胞数”的比在1.0以上与否设定为基准。同样地,在图13中所示的例中,以cpix值在0.2以上与否作为基准,但不限于此。判断部1143,例如,也可进行对应于以下的分类的判断。·(分类1)在细胞数d和细胞数m的比不足0.2,并且,细胞数p和细胞数q的比不足0.6时,判断为无观察结果。·(分类2)在细胞数d和细胞数m的比不足0.2,并且,细胞数p和细胞数q的比在0.6以上时,判断为有在上皮组织的表层及中层见到发育异常的可能性。·(分类3)在细胞数d和细胞数m的比在0.2以上,并且,细胞数p和细胞数q的比在0.6以上时,判断为进展到需要治疗的阶段,并且,在上皮组织的表层及中层见到发育异常的可能性高。·(分类4)在细胞数d和细胞数m的比在0.2以上,并且,细胞数p和细胞数q的比不足0.6时,判断为进展到需要治疗的阶段,并且,见到上皮组织的副基底层及基底层中的发育异常的可能性高。再者,也可为将如上所述的判断结果从输出部14输出到显示装置等的外部机器(未图示)的构成。另外,也可为输出部14基于评论对应表122而将判断结果应的评论与判断结果一同输出的构成。图11中所示的处理的流仅为一例,不限定于其。例如,可为并行步骤s3~步骤s5的处理和步骤s6~步骤s7的处理而进行的构成,也可为在步骤s3~步骤s5的处理之前进行步骤s6~步骤s7的处理的构成。同样地,步骤s8的处理和步骤9及步骤12的处理的顺序可逆。即,也可作为对于步骤9的处理中yes及no的各自的情况而进行步骤s8的处理的构成。<评论对应表122的详细内容>判断部1143也可为参照图14中所示的评论对应表122,选择对应于判断结果(例如,上述的分类1~4)的评论的构成(未图示)。如图14所示,在评论对应表122中针对每个分类,对应关于要关注的部位的信息及备注。在备注中,也可含关于判断结果的解说、及关于使用细胞数p、细胞数q、细胞数d、及细胞数m算出的各种值的信息等。例如,对应于图14的分类2的备注的“在表-中层细胞见到dna量多的细胞”是关于判断结果的解说。一方面,在被判断为分类1时,例如,要关注的部位被设为“无”,在备注中,含关于称为“无观察结果(再者,在深层系细胞中见到dna量多的细胞)”的判断结果的解说。另外,也可对应于如图14的分类3及分类4的备注所示,含称为“cpix值高”的基于细胞数d和细胞数m的比较的信息。输出部14对应赋予每个试样的试样id和从判断部1143取得的判断结果及评论,输出到显示装置等的外部机器(未图示)(输出步骤)。具体而言,输出部14,除了从判断部1143取得的判断结果之外,也可输出对细胞数p和细胞数q进行比较的结果,及对细胞数d和细胞数m进行比较的结果的至少任一方。再者,外部机器只要是具备对于使用者而提示判断结果的功能即可,例如,可为医师及看护师等使用的个人计算机(未图示),也可为后述的细胞检查员等使用的镜检终端装置4等。或者,细胞信息提供装置1也可为具备显示装置的构成。另外,输出部14也可为将第1计数部112制成的散点图、及第2计数部113制成的直方图的至少任何一方与判断结果及评论对应而输出的构成。再者,在图6中显示输出部14从测定装置2取得试样id的构成例,但不限于此。例如,数据取得部13与各种数据一同取得试样id,输出部14也可经数据取得部13而取得试样id。再者,细胞信息提供装置1也可为与多个测定装置2经局域网络(lan)等的网络连接,取得来自多个测定装置2的测定数据的构成。或者,也可为使测定装置2和细胞信息提供装置1一体化的构成。<分类1~4和组织学诊断及细胞学诊断的判断结果的关系>其中,将从细胞信息提供装置1输出的判断结果的“分类1”~“分类4”与组织学诊断及细胞学诊断中的分类有何对应关系使用图15进行说明。图15是对上皮组织中的前癌病变和细胞学诊断断中的分类的关系进行说明的图。例如,在子宫颈部的组织学诊断中,从正常的状态至癌的过程从正常的状态顺序地,有称为“正常(normal)”、“cin1”、“cin2”、“cin3”、及“癌(cancer)”的多个阶段。图15的上部所示的5个模式图显示此5个阶段的细胞的样式。在这之中,对应于称为子宫颈部上皮内肿瘤(cin)的阶段的是“cin1”、“cin2”、及“cin3”的阶段。“cin1”是异常细胞从基底层向表层之间的3分之1增殖的状态,是自然消退的可能性高的状态。因此,在“cin1”中,判断为尚不需要治疗。在图15中,显示在副基底层确认到异常细胞的样式,和表层及中层细胞之中确认到因hpv增殖的细胞变化的细胞。“cin2”是异常细胞从基底层向表层之间的3分之2增殖的状态,是在“cin2”中判断为需要治疗的状态。“cin3”是异常细胞经从基底层向表层之间的几乎全部而增殖的状态,在“cin3”中判断为需要治疗。为了早期开始癌的治疗,优选可在癌的进行情况从达到“cancer”之前的“cin2”至如“cin3”一样的癌的初期阶段检测有癌的担忧的。一方面,子宫颈癌检诊的情况,首先进行细胞学诊断检查。此检查的结果应用称为bethesda分类的分类方法。在bethesda分类中,使用正常(nilm)、推定轻度的异常的“lowsil(lsil)”、推定高度的异常的“highsil(hsil)”、及疑似子宫癌的称为“scc”的多个阶段。再者,“sil”是指扁平上皮内病变的英语的简称。在组织学诊断中的“cin1”、“cin2”、及“cin3”和bethesda分类的“lsil”及“hsil”可认为是如图15所示的关系。从细胞信息提供装置1输出的判断结果的“分类1”相当于组织学诊断的“正常”的阶段及细胞学诊断的“正常(nilm)”的阶段。“分类2”在组织学诊断的“cin1”之中,相当于更接近正常的阶段,相当于细胞学诊断的“lsil”的阶段。“分类3”相当于从组织学诊断的“cin1”至“cin2”之中接近“cin1”的阶段,相当于从细胞学诊断的“lsil”至“lsil”和“hsil”拮抗的阶段。“分类4”相当于从组织学诊断的“cin2”之中接近“cin3”的阶段至“cancer”的阶段,相当于从细胞学诊断的“lsil”和“hsil”拮抗的阶段至“scc”的阶段。(检查信息服务器3)检查信息服务器3是将细胞信息提供装置1输出的判断结果,及评论等与试样id对应存储的存储装置。检查信息服务器3将在细胞学诊断中对涂抹标本进行摄像的图像、及由进行细胞学诊断的细胞检查员输入的观察结果等与试样id对应存储。基于存储到检查信息服务器3中的信息而制成报告书,该报告书从检查机关120交付(提供)于医疗机关110。(镜检终端装置4的构成)其中,参照图1而对于镜检终端装置4的构成进行说明。镜检终端装置4具备总地控制镜检终端装置4的各功能的控制部41和显示图像等的显示部42。再者,控制部41具备图像处理部411、试样id取得部412、及输入部413。图像处理部411生成将由摄像装置5摄像的图像、由进行细胞学诊断的细胞检查员输入的检查观察结果、及从检查信息服务器3读取的判断结果等组合的画面显示而显示于显示部42(参照图16)。试样id取得部412取得赋予涂抹标本的试样id。取得的试样id在从检查信息服务器3读取关于细胞试样的判断结果及评论,或将对涂抹标本进行摄像的图像及细胞学诊断的观察结果等登记到检查信息服务器3上时利用。输入部413取得由进行细胞学诊断的细胞检查员输入的检查观察结果。(细胞信息提供系统100提供的细胞信息)接下来,举在细胞信息提供系统100中由细胞信息提供装置给出的判断结果在镜检终端装置4中利用的场面作为例,使用图16进行说明。图16是显示镜检终端装置显示镜检图像、及由细胞信息提供装置给出的判断结果的画面显示的一例的图。在栏w4中,记载“患者编号”、“接收日”、“生年月日”、“年龄”、“设施名”、及“既往史”。“设施名”是医疗机关110的名称,是从患者采集细胞试样的医疗机关。“患者编号”虽然也能作为试样id利用,但也可向每个细胞试样、或者每个患者赋予试样id。此时,试样id与患者编号对应。在图16中所示的例中,栏w1的“xxxxxx”是赋予每个细胞试样的试样id。在栏w2中,显示从细胞信息提供装置1提供的cpix值“0.50”、及判断结果“分类4”,在栏w3中,显示与判断结果“分类4”对应的评论(参照图14)。在栏w5中,显示由细胞检查员等进行镜检的细胞检查员输入的“标本精度”、“检查结果”、及观察结果。在栏w6中,显示在镜检中摄像的图像。在栏w7设记入“综合判断”的栏,例如,在制成报告书的阶段,显示作为最终的判断输入的判断结果。本发明不限定于上述的各实施方式,在权利要求中所示的范围内各种变更是可能的,对于将各自在不同的实施方式中公开的技术手段适宜组合而得到的实施方式而也包括在本发明的技术性范围内。【实施例】以下使用图17对于验证由本发明的细胞信息提供装置1的判断结果的一实施例进行说明。图17是在验证由细胞信息提供装置1的判断结果的一实施例中的结果。图17的(a)是对于cpix值不足0.2、并且在细胞学诊断中有关于异形化的细胞的出现场所的观察结果的14试样而进行由细胞信息提供装置1的判断时的结果。细胞信息提供装置1成功地将在细胞学诊断中有关于表层及中层细胞的发育异常的观察结果的12试样之中的11试样判断为“分类2”,其判断的精度是91.6%。图17的(b)是对于cpix值在0.2以上、并且在细胞学诊断中有关于异形化的细胞的出现场所的观察结果的45试样而进行由细胞信息提供装置1的判断时的结果。细胞信息提供装置1成功地将在细胞学诊断中有关于表层及中层细胞的发育异常的观察结果的31试样之中的20试样判断为“分类3”,其判断的精度是90.9%。另外,细胞信息提供装置1成功地将在细胞学诊断中有关于从中层至基底层细胞的发育异常的观察结果的9试样之中的7试样判断为“分类4”,其判断的精度是77.8%。这样,证实细胞信息提供装置1可关于试样中所含的细胞的发育异常而以高的精度进行判断。【符号的说明】1:细胞信息提供装置2:测定装置3:检查信息服务器(存储装置)4:镜检终端装置13:数据取得部14:输出部100:细胞信息提供系统112:第1计数部(计数部)113:第2计数部1141:第1比较部(比较部)1143:判断部s1:数据取得步骤s5:第1计数步骤(计数步骤)s7:第2计数步骤s9,s12:比较步骤当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1