DBN1蛋白在制备神经变性疾病诊断药物中的应用的制作方法
本发明涉及医药生物技术领域,具体涉及到dbn1蛋白在制备神经变性疾病诊断药物中的应用。
背景技术:
神经变性病(neurodegenerativediseases)是指由于神经元变性、凋亡所导致的神经系统退行性疾病。根据临床症状和病理解剖分为以下几组:
1、姿势和运动异常综合征,如帕金森病,多系统萎缩
2、进行性痴呆综合征,如阿尔茨海默病,额颞叶痴呆
3、进行性痴呆伴其他神经性异常,如huntington舞蹈病,皮质基底节变性
4、进行性共济失调综合征,如脊髓小脑共济失调
5、缓慢进展的肌无力和肌萎缩综合征,如运动神经元病
6、感觉和运动障碍,如遗传性运动感觉神经病(cmt)
7、进行性失明或眼外肌麻痹,如青光眼,遗传性视神经病
8、以神经感觉性耳聋为特点的综合征,如遗传性听力丧失伴神经系统萎缩
有研究发现tau蛋白通过调节神经元微管的动态稳定性在轴突传导过程中发挥重要作用,tau蛋白病变在视网膜疾病以及阿尔茨海默病(ad)等神经变性疾病中已有广泛研究,但也都局限于视网膜组织以及脑脊髓液等中的研究。其在神经变性疾病患者脑或视网膜组织中以及在脑脊髓液(csf)中的表达量显著上升。检测在脑或视网膜组织中的表达需要病理标本,而脑脊髓液也需要腰穿来获取,对患者造成负担,临床应用存在困难。
另一方面青光眼作为视网膜神经变性疾病,只能临床检查发现和评估视神经损伤程度,目前尚无有效生物标志物用于诊断与评估。但是,也有些患者因为屈光介质浑浊等原因,无法精确的观察眼底并准确的评估神经损伤程度。更为严重的是,因为早期没有任何症状,很多患者被医院诊断为青光眼时已有30-50%视网膜神经节细胞已丢失。能开发一个可应用于早期诊断和评估神经损伤的生化学标记物,对临床的意义重大。
研究发现脑发育调节蛋白drebrin(亦称dbn1)作为神经骨架蛋白actin调节蛋白,在中枢神经系统中发挥重要的作用,并与神经变性疾病的发生发展相关。因此,本领域中存在人群中诊断与神经变性疾病风险的需要,即存在对患有所述疾病的风险的评估和指导精准的治疗方案。所述疾病严重程度的评估和/或所述疾病预估风险的需要,提供一种在检测手段上方便检测,不会对患者造成二次伤害的检测方法的需要。这对相关疾病的预测、预防具有重要的临床意义和社会经济效益。
技术实现要素:
针对现有技术存在的不足,本发明的目的在于提供dbn1蛋白的新用途,以提供一种方便快捷的诊断神经变性的方法以及药物。
为实现上述目的,本发明提供了dbn1蛋白在诊断神经变性疾病的药物的制备中的用途,所述诊断中的应用包括神经变性疾病的早期诊断和神经损伤严重程度的评估,所述诊断通过测定外周血血浆中dbn1蛋白的含量进行。
在本发明的实施方案中,其中神经变性疾病包括姿势和运动异常综合征,其中包括帕金森病,多系统萎缩;进行性痴呆综合征,其中包括阿尔茨海默病,额颞叶痴呆;进行性痴呆伴其他神经性异常,其中包括亨廷顿舞蹈病,皮质基底节变性;进行性共济失调综合征,其中包括脊髓小脑共济失调;缓慢进展的肌无力和肌萎缩综合征,其中包括运动神经元病;感觉和运动障碍,其中包括遗传性运动感觉神经病(cmt);进行性失明或眼外肌麻痹,其中包括青光眼,遗传性视神经病;以神经感觉性耳聋为特点的综合征,其中包括遗传性听力丧失伴神经系统萎缩;以及其他神经变性疾病。
在本发明的实施方案中,其中进行性失明特别包括青光眼疾病中的原发性闭角型青光眼和原发性开角型青光眼。
在本发明的实施方案中,其中所述诊断通过酶联免疫定量检测试剂盒进行检测。
在本发明的实施方案中,其中所述药物包括试剂盒。
在本发明的实施方案中,其中所述试剂盒为酶联免疫试剂盒。
在本发明的实施方案中,其中所述试剂盒中包含所述dbn1蛋白的抗体。
在本发明的实施方案中,其中所述抗体中包含捕获抗体a和/或酶标检测抗体b。
在本发明的实施方案中,其中所述试剂盒还包括预包被板、标准品、包被缓冲液、样品稀释液、封闭液、辣根过氧化物酶、洗脱液,显色剂。
本发明在研究基础上发现dbn1蛋白在中枢神经系统中发挥重要的作用,在神经系统发生变性,血液中的dbn1蛋白的表达会增加,以此基础,通过实验论证,神经变性疾病的患者的dbn1蛋白均有明显的增加表达情况,将dbn1蛋白作为神经变性疾病标志蛋白,通过酶联免疫定量检测试剂盒检测患者血液中的dbn1蛋白含量,来诊断患者是否患有神经变性疾病,整体上检测手段方便检测,不会对患者造成二次伤害,这对相关疾病的预测、预防具有重要的临床意义和社会经济效益。
附图说明
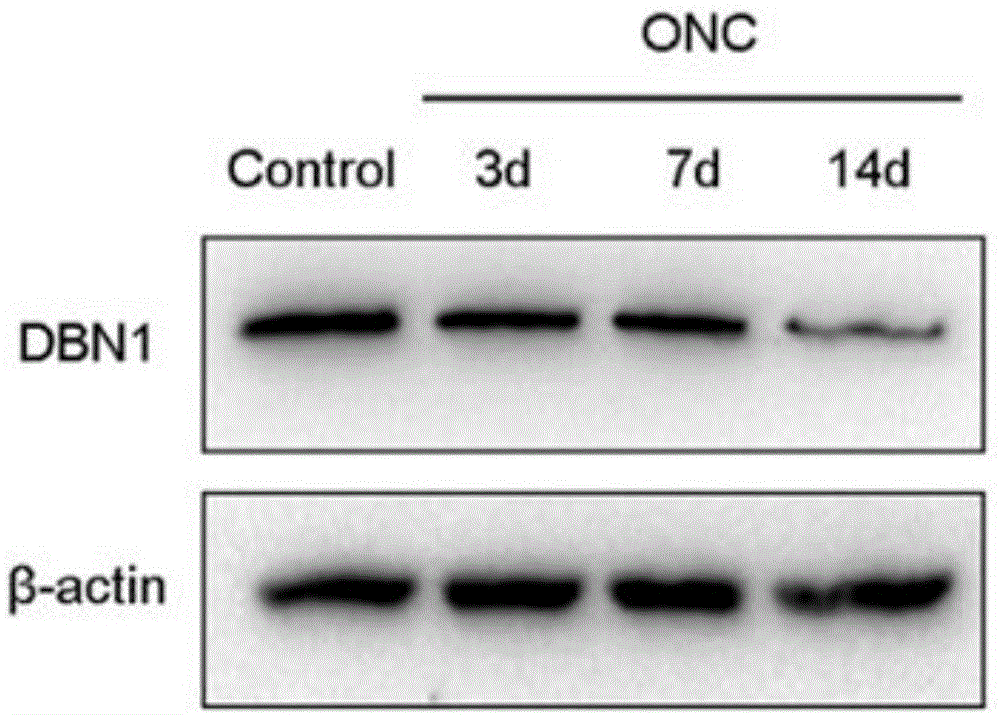
图1为动物模型视神经夹闭损伤3d,7d,14d及对照组视网膜的westernblot实验结果;
图2为动物模型视神经夹闭损伤3d,7d,14d及对照组视网膜的westernblot实验定量分析结果;
图3为视神经夹闭损伤动物模型的血清中dbn1蛋白表达量变化图;
图4为经细胞毒性试剂nmda处理的neuro-2a细胞及对照组dbn1蛋白的免疫荧光染色的定量分析结果;
图5为开青、闭青、青睫患者在将视神经纤维层厚度分为八个象限后在每个象限的厚度;
图6为青光眼患者及对照组血浆dbn1蛋白表达水平;
图7为青光眼患者及对照组血浆tau表达水平;
图8为dbn1蛋白阳性及阴性患者视神经纤维层厚度的八个象限中,正常范围、临界值及明显变薄的占比;
图9为dbn1蛋白表达量与视神经纤维层厚度的logistic回归分析图。
具体实施方式
下面将结合实施例对本发明做进一步的详述。
本发明涉及一种新发现,即dbn1蛋白在神经变性疾病中高表达,并经细胞分泌,进入血液循环,使神经变性疾病患者血清中该蛋白水平升高。因此dbn1蛋白可以作为新的神经变性疾病血清标记物,可用于神经变性疾病的筛查、追踪、早期诊断、治疗指导和预后判断。
dbn1蛋白的氨基酸序列如序列表seqidno:1所示。
本发明提供的检测神经变性疾病的试剂盒,包括特异性识别dbn1蛋白的捕获抗体a,该捕获抗体a被包被在预包被板上。
本发明基于抗dbn1蛋白特异性抗体,开发出利用elisa检测技术检测血清dbn1蛋白抗原的试剂盒,此试剂盒适用于神经变性疾病的筛查、追踪、早期诊断和指导治疗与判断预后。
本发明提供的检测dbn1蛋白抗原的elisa试剂盒特征是,主要包括有:包被有捕获dbn1蛋白特异性抗体的预包被板、酶标检测抗体、标准品、包被缓冲液、样品稀释液、封闭液、辣根过氧化物酶、洗脱液,显色剂。捕获抗体与检测抗体均可与dbn1蛋白抗原结合。
实施例1公开抗原的纯化以及抗体的制备过程;
1.表达、纯化及鉴定dbn1蛋白:
dbn1蛋白是从前期研究中的经过基因工程改造过的酿酒酵母,利用半乳糖诱导过量表达,琼脂糖亲和介质(谷胱甘肽)分离纯化,并经过western-blotting鉴定。
2.血清样品的准备:
全血标本于室温放置2小时或4℃过夜后于1000g离心20分钟左右,取上清即可立即检测;或进行分装,并将标本放于-20℃或-80℃保存,但应避免反复冻融。解冻后的样品应再次离心,然后检测。所检测样品中不能含有nan3,因为nan3抑制辣根过氧化物酶(hrp)的活性。
3.elisa法各种缓冲液及试剂的配制方法:
(1)包被缓冲液:0.05mph9.6的na2co3-nahco3
(2)样品稀释液:ph7.4pbs溶液
(3)洗脱液:ph7.4的pbst溶液
(4)封闭液:0.5%bsa的ph7.4pbs溶液
(5)显色剂:显色剂a和显色剂b(现配现用)
(6)终止液:2mol/lh2so4溶液(配时将浓硫酸缓慢滴入蒸馏水中,边加边混匀)
4.elisa法测定血清中抗dbn1蛋白的igg抗体的浓度,以辅助早期诊断胃癌:具体操作步骤如下:
(1)包被:将纯化的人dbn1蛋白溶液用包被缓冲液稀释至1μg/ml,加入到96孔酶标板中,每孔100μl,37℃包被2小时或4℃过夜;洗涤液洗板3次,甩干;
(2)封闭:加入封闭液200μl,室温保温2小时;洗涤液洗板3次,甩干;
(3)标准品与样品的稀释与加样:将标准品与待测血清样品1∶100用样品缓冲液稀释至100μl,加入到各自的抗原测定孔板中。注意不要有气泡,加样将样品加于梅标板孔底部,尽量不触及孔壁,轻轻晃动混匀,酶标板上加盖或覆膜。若待测血清样品较多,建议使用多管微量加液器加样。标准品及待检测样品临用前15分钟内配制,用完丢弃,下次检测使用新鲜配制的标准品。
(4)温育:酶标板置于37℃反应120分钟,甩净孔中液体,不用洗涤。
(5)加酶:每孔加辣根过氧化物酶标记的dbn1蛋白igg抗体100μl,37℃,60分钟。甩净孔中液体,同上洗板5次拍干。
(6)显色:拍干后各孔先滴加显色剂a50μl,再加入显色剂b50μl,轻轻震荡混匀,37℃避光显色15分钟。
(7)终止:依序每孔加终止液50μl,终止反应。终止液的加入顺序应尽量与底物液的加入顺序相同。底物反应时间到后应尽快加入终止液。
(8)结果判定:
i.用酶联仪在450nm波长依序测量各孔的光密度(od值)。
*a450是450nm处吸光度的缩写。
目前dbn1蛋白抗体尚无国际通行的参考标准,因此本检测结果校准时采用了相对单位。
ii.血清中抗dbn1蛋白值的判定
iii.质量控制
每个检测结果必须符合以下标准:
标准血清1的a450:≤0.100
标准血清2的a450:≥0.700
如不符合上述标准,则结果视为无效,必须重新检测。
实施例2实验模型的制备以及结果的验证
大鼠视神经损伤动物模型:大鼠眼球颞侧剪开球结膜,钝性分离眼周组织,于眼球正后方2mm处用5号手术钳夹闭视神经5秒,制作视神经损伤动物模型。
大鼠视神经夹闭后取视网膜组织经免疫印迹法及免疫荧光染色,检测视网膜dbn1蛋白表达情况,采用imagej软件进行量化。
用100umnmda处理neuro-2a细胞24小时,免疫荧光试验检测其drebrin水平。
dbn1蛋白大部分主要分布于视网膜神经节细胞层和内丛状层,视神经夹闭3d,7d,14d及对照组视网膜的westernblot实验结果表明,其结果如图1-2所示:视网膜组织内的dbn1蛋白表达量逐步减少。通过大鼠模型取心脏血,于冰箱放置2小时后经2000g,4℃离心10分钟后转移上清至1.5mlep管,-80℃保存,elisa技术检验视神经夹闭动物模型的血清中dbn1蛋白表达量变化,如图3所示,至夹闭第7天,dbn1蛋白表达量显著上升,并夹闭14天后,表达量回落。这个动物模型研究,明确了视神经损伤时血液中dbn1蛋白的表达量显著升高,神经损伤与血中dbn1蛋白表达量之间存在相关性。
经细胞毒性试剂nmda处理的neuro-2a细胞及对照组dbn1蛋白的免疫荧光染色结果表明如图4所示:在正常neuro-2a细胞中,dbn1蛋白主要分布于胞膜边缘,经过nmda处理后,dbn1蛋白表达量显著下调(p<0.01),分布有改变。这个实验结果也明确了,与在体研究一样,在神经细胞损伤时dbn1蛋白表达量降低,通过被释放到细胞外,进而血液中的dbn1蛋白表达量增加。
实施例3:根据本发明的诊断试剂盒示例性诊断应用
我们自2016年10月至2017年12月于温州医科大学眼视光医院收集了232名青光眼患者,其中包括164名原发性闭角型青光眼(闭青,pacg)、46名原发性开角型青光眼(开青,poag)和22名青光眼睫状体炎综合症(青睫,ps)患者,以及50名对照组。
通过本发明提供的诊断试剂盒对利用酶联免疫吸附测定(elisa)试剂盒检测血浆drebrin表达量,并收集和分析患者眼压、oct及视野等临床检查结果,其结果如表1所示:
表1中的视野指数中接近100为正常值,数值越小表明视野损伤严重;视野指数平均变异接近0为正常,负值越大,说明视野损伤越大;模型标准变异接近0为正常值,偏离越大,说明视野损伤越大。与对照组相比,青睫患者视野指数无明显改变,闭青及开青患者则明显降低,与正常值的偏差较大,其受到的视野损伤更为严重;与对照组相比,青睫患者视神经纤维层厚度无明显改变,闭青及开青患者则明显降低(p<0.0001);杯/盘比的正常值在0.3-0.5左右,一般在大于0.6时认为是青光眼,与正常值相比,青睫患者杯/盘比属于正常值,闭青患者的杯/盘比均高于0.5,及开青患者的杯/盘比则均高于0.7,可以另外佐证得出青睫、闭青、开青的视神经损伤依次递增。图5表示将视神经纤维层厚度进一步分为八个象限,每个象限厚度基本呈现开青最薄、闭青次之、青睫再次的趋势。视神经纤维层厚度越薄,说明视神经损伤程度越严重。
通过比对青光眼患者dbn1蛋白阳性及阴性患者视神经纤维层厚度的八个象限中,正常范围(上段)、临界值(中段)及明显变薄(下段)的占比,如图8所示,在it象限,dbn1蛋白阳性患者厚度变薄的百分率高于dbn1蛋白阴性组,具有显著性差异。st象限亦有厚度变薄的百分率高于dbn1蛋白阴性组趋势,通过各个象限中dbn1蛋白表达量与视神经纤维层厚度的logistic回归分析,如图9所示,表明在in、it及st象限,p值<0.05,代表血浆dbn1蛋白表达量上升与视神经纤维层厚度变薄,即与神经损伤程度相关。
上述的232名青光眼患者以及50名对照组的血清dbn1蛋白表达量结果如图6所示,与对照组相比,青睫患者dbn1蛋白表达量未见明显差异,闭青患者表达量显著升高(p<0.05),开青患者表达水平升高最为显著(p<0.01);
同时检测上述的232名青光眼患者以及对照组的血清tau表达水平如图7所示,相对于dbn1蛋白表达水平,tau含量在所有青睫、闭青及开青患者血浆中均显著升高(分别为p<0.001,p<0.0001,p<0.0001);
以上结果表明通过检查血清dbn1蛋白表达量来鉴定青光眼患者,能够鉴定青光眼视神经损伤程度。相反,检测血清tau表达水平,未能正确反映视神经损伤严重程度。
由上述可知,dbn1蛋白在原发性闭角型青光眼患者和原发性开角型青光眼患者中存在明显的差异表达,显然与青光眼的发生发展有着密切的相关性,相应的,特异性抗dbn1蛋白的抗体,包括各种单克隆抗体和多克隆抗体,由于其能够用于检测dbn1蛋白的表达量,因而可以用于检测原发性闭角型青光眼患者和原发性开角型青光眼,或者用于制备检测原发性闭角型青光眼患者和原发性开角型青光眼的试剂或试剂盒,这对本领域人员来说是显而易见的。
以上仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
sequencelisting
<110>温州医科大学
<120>dbn1蛋白在制备神经变性疾病诊断药物中的应用
<141>2018-10-24
<160>1
<170>siposequencelisting1.0
<210>1
<211>649
<212>prt
<213>artificialsequence
<400>1
metalaglyvalserpheserglyhisargleugluleuleualaala
151015
tyrglugluvalileargglugluseralaalaasptrpalaleutyr
202530
thrtyrgluaspglyseraspaspleulysleualaalaserglyglu
354045
glyglyleuglngluleuserglyhisphegluasnglnlysvalmet
505560
tyrglyphecysservallysaspserglnalaalaleuprolystyr
65707580
valleuileasntrpvalglygluaspvalproaspalaarglyscys
859095
alacysalaserhisvalalalysvalalagluphepheglnglyval
100105110
aspvalilevalasnalaserservalgluaspileaspalaglyala
115120125
ileglyglnargleuserasnglyleualaargleuserserproval
130135140
leuhisargleuargleuarggluaspgluasnalagluprovalgly
145150155160
thrthrtyrglnlysthraspalaalavalglumetlysargileasn
165170175
arggluglnphetrpgluglnalalyslysgluglugluleuarglys
180185190
gluglugluarglyslysalaleuaspgluargleuargpheglugln
195200205
gluargmetgluglngluargglngluglnglugluarggluargarg
210215220
tyrarggluarggluglnglnileglugluhisargarglysglngln
225230235240
thrleuglualagluglualalysargargleulysgluglnserile
245250255
pheglyasphisargaspglugluglugluthrhismetlyslysser
260265270
glusergluvalgluglualaalaalaileilealaglnargproasp
275280285
asnproarggluphephelysglnglngluargvalalaseralaser
290295300
alaglysercysaspvalproserpropheasnhisargproglyser
305310315320
hisleuaspserhisargargmetalaprothrproileprothrarg
325330335
serproseraspserserthralaserthrprovalalagluglnile
340345350
gluargalaleuaspgluvalthrserserglnproproproleupro
355360365
proproproproproalaglngluthrglngluproserproileleu
370375380
aspserglugluthrargalaalaalaproglnalatrpalaglypro
385390395400
metglugluproproglnalaglnalaproproargglyproglyser
405410415
proalagluaspleumetphemetgluseralagluglnalavalleu
420425430
alaalaprovalgluproalathralaaspalathrgluilehisasp
435440445
alaalaaspthrilegluthraspthralathralaaspthrthrval
450455460
alaasnasnvalproproalaalathrserleuileaspleutrppro
465470475480
glyasnglygluglyalaserthrleuglnglygluproargalapro
485490495
thrproproserglythrgluvalthrleualagluvalproleuleu
500505510
aspgluvalalaprogluproleuleuproalaglygluglycysala
515520525
thrleuleuasnpheaspgluleuprogluproproalathrphecys
530535540
aspproglugluvalgluglygluserleualaalaproglnthrpro
545550555560
thrleuproseralaleuglugluleugluglngluglngluproglu
565570575
prohisleuleuthrasnglygluthrthrglnlysgluglythrgln
580585590
alasergluglytyrpheserglnserglngluglugluphealagln
595600605
serglugluleucysalalysalaproproprovalphetyrasnlys
610615620
proprogluileaspilethrcystrpaspalaaspprovalproglu
625630635640
gluglugluglyphegluglyglyasp
645
- 还没有人留言评论。精彩留言会获得点赞!