用于单细胞处理的系统和方法与流程
交叉引用
本申请要求提交于2017年12月12日的美国临时专利申请62/597,578的权益,所述申请以引用方式全文并入本文。
背景技术:
可出于各种目的处理样品,如鉴定样品内部分或分析物的类型。样品可以是生物样品。可出于各种目的处理生物样品,如检测疾病(例如癌症)或鉴定特定物质。存在各种处理样品的方法,如聚合酶链反应(pcr)和测序。
可在各种反应环境(如分配区(partition))内处理生物样品。分配区可以是孔或液滴。可采用液滴或孔以使生物样品能够被分配和独立处理的方式处理生物样品。例如,此类液滴可与其他液滴在流体上隔离,从而能够精确控制液滴中的各个环境。
分配区中的生物样品可经受各种过程,如化学过程或物理过程。分配区中的样品可经受加热或冷却,或化学反应,如以产生可定性或定量处理的物质。
技术实现要素:
在处理过程中,可能难以鉴定分离的分析物(例如,蛋白质、代谢物、核酸分子等)的来源(例如,细胞)。本文认识到需要在单细胞水平上有效且准确地测量一种或多种分析物的处理系统和方法。所述系统和方法可鉴定一种或多种分析物的一个或多个来源。例如,分析物可以是蛋白质(例如,表面结合蛋白、内部蛋白等)。分析物可以是代谢物(例如,醇、氨基酸、核苷酸、抗氧化剂、有机酸、多元醇、维生素、辅因子等)。分析物可以是细胞的任何成分。分析物可以是特异性捕获和分析的靶向分析物,如对抗体具有结合特异性。分析物可以是非特异性捕获和分析的非靶向分析物。
在一个方面,提供了一种用于在含有或怀疑含有蛋白质的细胞内鉴定所述蛋白质的方法,包括:(a)使由细胞产生的细胞珠与对蛋白质具有结合特异性的抗体接触,其条件足以允许抗体流入细胞珠中并与蛋白质偶合,其中抗体与包含第一核酸序列的第一核酸条形码分子偶合;(b)将细胞珠和珠粒共分配在分配区中,其中珠粒包括包含第二核酸序列的第二核酸条形码分子;(c)使用第一核酸条形码分子和第二核酸条形码分子产生包含第一核酸序列和第二核酸序列的核酸分子;(d)对核酸分子或其衍生物进行测序以鉴定第一核酸序列和第二核酸序列,其中第一核酸序列鉴定蛋白质并且第二核酸序列鉴定细胞珠;以及(e)确定蛋白质源自细胞内。
在一些实施方案中,所述方法还包括,在(a)之后,从细胞珠中洗出未结合的抗体。
在一些实施方案中,在细胞珠中裂解细胞。
在一些实施方案中,珠粒是凝胶珠粒。
在一些实施方案中,分配区是乳液中的液滴。
在一些实施方案中,第二核酸分子与珠粒可释放地偶合。在一些实施方案中,所述方法还包括从珠粒中释放第二核酸条形码分子。
在一些实施方案中,珠粒包含多个核酸条形码分子,多个核酸条形码分子中的每一个包含第二核酸序列。在一些实施方案中,多个核酸条形码分子中的每一个包含对多个核酸条形码分子中的每一个而言唯一的唯一核酸序列。
在一些实施方案中,(a)包括使细胞珠与各自对不同蛋白质具有结合特异性的多种不同抗体接触,其中多种不同抗体中的给定抗体与包含鉴定给定抗体的核酸序列的核酸条形码分子偶合。在一些实施方案中,细胞珠包含来自细胞的多种不同蛋白质,其中(d)包括鉴定不同蛋白质,并且其中(e)包括确定不同蛋白质源自细胞内。
在一些实施方案中,所述确定包括确定蛋白质源自细胞内的可能性。
在另一方面,提供了一种用于从含有或怀疑含有蛋白质的细胞中鉴定蛋白质的方法,包括:(a)将细胞和珠粒共分配在第一分配区中,其中珠粒包含被构造成与蛋白质偶合的多种抗体,其中多种抗体中的每种抗体与包含第一核酸序列的第一核酸条形码分子偶合;(b)使细胞经受足以允许多种抗体中的抗体与蛋白质偶合的条件,以产生包含第一核酸条形码分子的蛋白质-抗体复合物;(c)将蛋白质-抗体复合物与包含第二核酸序列的第二核酸条形码分子共分配在第二分配区中,其条件足以允许蛋白质-抗体复合物的第一核酸条形码分子和第二核酸条形码分子产生包含第一核酸序列和第二核酸序列的核酸分子;(d)对核酸分子或其衍生物进行测序以鉴定第一核酸序列和第二核酸序列,其中第一核酸序列鉴定细胞并且第二核酸序列鉴定蛋白质;以及(e)确定蛋白质源自细胞。
在一些实施方案中,多种抗体被构造成与蛋白质非特异性地偶合。
在一些实施方案中,第一分配区是液滴。
在一些实施方案中,第二分配区是孔。
在一些实施方案中,(b)包括裂解第一分配区中的细胞。
在一些实施方案中,使多种抗体中的给定抗体与包含对给定抗体而言唯一的核酸序列的核酸条形码分子偶合。
在一些实施方案中,珠粒是凝胶珠粒。
在一些实施方案中,多种抗体与珠粒可释放地偶合。在一些实施方案中,所述方法还包括从珠粒中释放多种抗体。
在一些实施方案中,所述方法还包括,在(b)之后,将包含一种类型的蛋白质的第一组蛋白质-抗体复合物与包含其他类型的蛋白质的其他蛋白质-抗体复合物分离,其中第一组蛋白质-抗体复合物包含所述蛋白质-抗体复合物。在一些实施方案中,第一组蛋白质-抗体复合物包含来自多个细胞的蛋白质,其中多个细胞包括所述细胞。
在一些实施方案中,蛋白质来自细胞内。
在一些实施方案中,蛋白质是表面结合蛋白。
在一些实施方案中,所述确定包括确定蛋白质源自细胞内的可能性。
在另一方面,提供了一种用于在含有或怀疑含有代谢物的细胞内鉴定代谢物的方法,包括:(a)使由细胞产生的细胞珠与对代谢物具有结合特异性的抗体接触,其条件足以允许抗体流入细胞珠中并与代谢物偶合,其中抗体与包含第一核酸序列的第一核酸条形码分子偶合;(b)将细胞珠和珠粒共分配在分配区中,其中珠粒包括包含第二核酸的第二核酸条形码分子;(c)使用第一核酸条形码分子和第二核酸条形码分子产生包含第一核酸序列和第二核酸序列的核酸分子;(d)对核酸分子进行测序以鉴定第一核酸序列和第二核酸序列,其中第一核酸序列鉴定代谢物并且第二核酸序列鉴定细胞珠;以及(e)确定代谢物源自细胞内。
在一些实施方案中,代谢物包含对抗体具有结合特异性的结构单元。
在一些实施方案中,代谢物选自由以下组成的组:醇、氨基酸、核苷酸、抗氧化剂、有机酸、多元醇和维生素。
在一些实施方案中,代谢物来自一类代谢物。
在一些实施方案中,代谢物是辅因子。
在一些实施方案中,所述方法还包括,在(a)之后,从细胞珠中洗出未结合的抗体。
在一些实施方案中,在细胞珠中裂解细胞。
在一些实施方案中,珠粒是凝胶珠粒。
在一些实施方案中,分配区是乳液中的液滴。
在一些实施方案中,第二核酸分子与珠粒可释放地偶合。在一些实施方案中,所述方法还包括从珠粒中释放第二核酸条形码分子。
在一些实施方案中,珠粒包含多个核酸条形码分子,多个核酸条形码分子中的每一个包含第二核酸序列。在一些实施方案中,多个核酸条形码分子中的每一个包含对多个核酸条形码分子中的每一个而言唯一的唯一核酸序列。
在一些实施方案中,所述确定包括确定代谢物源自细胞内的可能性。
在另一方面,提供了一种用于确定第一分析物和第二分析物源自细胞的方法,其中第一分析物来自细胞的表面并且第二分析物来自细胞内,包括:(a)用第一抗体处理细胞或细胞衍生物,其条件足以允许第一抗体与第一分析物偶合,其中第一抗体包括包含第一核酸序列的第一核酸条形码分子;(b)用第二抗体处理细胞或细胞衍生物,其条件足以允许第二抗体与第二分析物偶合,其中第二抗体包括包含第二核酸序列的第二核酸条形码分子;(c)使用第一核酸条形码分子和第二核酸条形码分子分别产生第一核酸分子和第二核酸分子,其中第一核酸分子包含第一核酸序列和共有条形码序列,并且第二核酸分子包含第二核酸序列和共有条形码序列,其中共有条形码序列鉴定细胞或细胞衍生物;(d)对第一核酸分子和第二核酸分子或其衍生物进行测序,以鉴定第一核酸序列、第二核酸序列和共有条形码序列,其中第一核酸序列鉴定第一分析物,第二核酸序列鉴定第二分析物,并且共有条形码序列鉴定细胞或细胞衍生物;以及(e)确定第一分析物和第二分析物源自细胞。
在一些实施方案中,第一分析物和第二分析物是不同类型的分析物。
在一些实施方案中,第一分析物和第二分析物是相同类型的分析物。
在一些实施方案中,第一分析物和/或第二分析物是蛋白质。
在一些实施方案中,第二分析物是代谢物。
在一些实施方案中,(a)包括处理细胞,并且(b)包括处理细胞衍生物。在一些实施方案中,细胞衍生物是细胞珠。
在一些实施方案中,(c)通过将细胞或细胞衍生物与各自包含共有条形码序列的多个条形码分子共分配来执行。在一些实施方案中,多个条形码分子与珠粒偶合。
在一些实施方案中,所述确定包括确定第一分析物或第二分析物源自细胞的可能性。
在一些实施方案中,所述确定包括确定第一分析物源自细胞的第一可能性和确定第二分析物源自细胞内的第二可能性。
本公开的另外的方面和优点从以下具体实施方式变得为本领域技术人员显而易知,其中仅示出并描述本公开的例示性实施方案。应当认识到的是,本公开能够具有其他以及不同的实施方案,并且其若干细节能够在各种不同方面做出修改,所有均不脱离公开内容。因此,附图和说明书应被视为在本质上是说明性的而不是限制性的。
以引用的方式并入
在本说明书中提及的所有公布、专利和专利申请以引用的方式并入本文,其引用程度就如同每个单独的公布、专利或专利申请被具体和单独地指出以引用的方式并入一般。如果通过引用并入的出版物和专利或专利申请与说明书中包含的公开内容相矛盾,则说明书旨在取代和/或优先于任何这样的矛盾材料。
附图说明
本发明的新型特征在随附权利要求中具体阐述。通过参考对其中利用本发明的原理的例示性实施方案作出阐述的以下详细描述以及附图(在本文中还有“图(figure和fig.)”)获得对本发明的特征和优点的更好理解,在附图中:
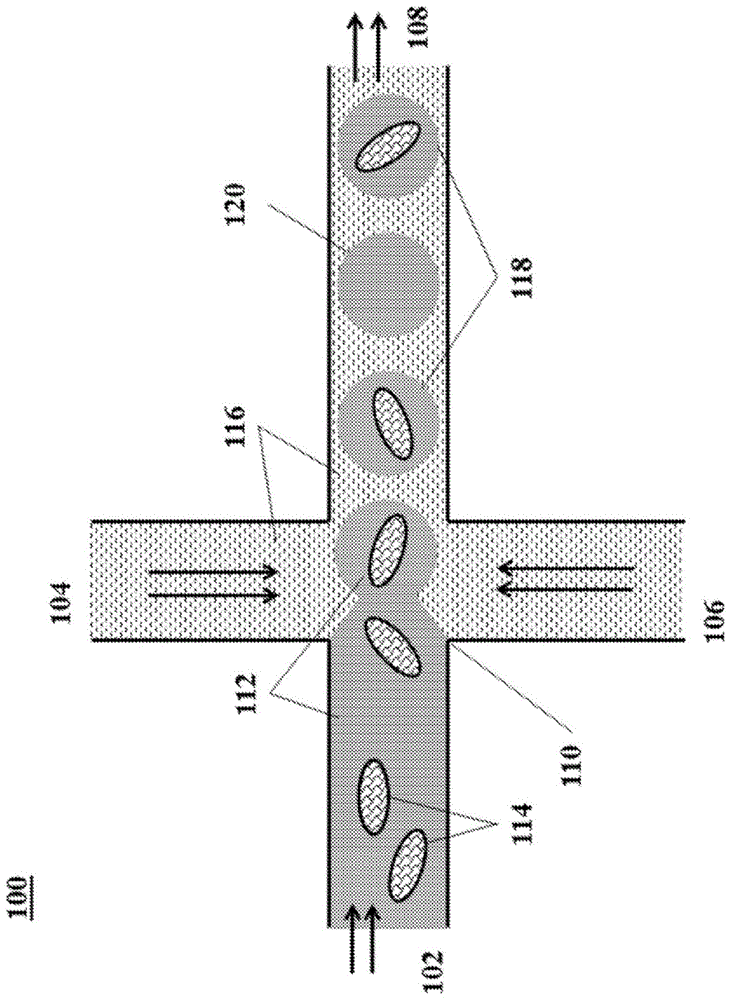
图1示出用于分配单个生物颗粒的微流体通道结构的实例。
图2示出用于将携带条形码的珠粒递送至液滴的微流体通道结构的实例。
图3示出用于共分配生物颗粒和试剂的微流体通道结构的实例。
图4示出用于将珠粒受控地分配到离散液滴中的微流体通道结构的实例。
图5示出用于增加液滴产生通量的微流体通道结构的实例。
图6示出用于增加液滴产生通量的微流体通道结构的另一实例。
图7a示出具有用于受控分配的几何特征的微流体通道结构的另一实例的横截面视图。图7b示出图7a的通道结构的透视图。
图8示出携带条形码的珠粒的实例。
图9示出用于鉴定和测量细胞中的分析物的方法。
图10示出用于鉴定和测量细胞中的分析物的另一方法。
图11示出已编程或以其他方式配置成实施本文提供的方法的计算机系统。
具体实施方式
虽然本文已经示出并描述本发明的各种实施方案,但是本领域技术人员显而易知此类实施方案仅作为举例来提供。许多改变、变化和取代可由本领域技术人员想到而不脱离本发明。应理解,可使用本文所述的本发明的实施方案的各种替代方案。
在将值描述为范围的情况下,应理解,此类公开内容包括公开在此范围内的所有可能子范围,以及落入此范围内的特定数值,而不管特定数值或特定子范围是否明确说明。
如本文所用,术语“条形码”通常是指传达或能够传达关于分析物的信息的标记或标识符。条形码可以是分析物的一部分。条形码可以独立于分析物。除了分析物的内源特征(例如,分析物的大小或一个或多个末端序列)之外,条形码可以是附接于分析物(例如,核酸分子)的标签或标签的组合。条形码可包含多个条形码单元或元件。条形码可以是唯一的。条形码可以有多种不同的格式。例如,条形码可包括:多核苷酸条形码;随机核酸和/或氨基酸序列;和合成核酸和/或氨基酸序列。条形码可以以可逆或不可逆的方式附接于分析物。在样品测序之前、期间和/或之后,可以将条形码添加到例如脱氧核糖核酸(dna)或核糖核酸(rna)样品的片段中。条形码可以允许各个测序读长的鉴定和/或定量。
如本文所用,术语“实时”可以指小于约1秒、十分之一秒、百分之一秒、毫秒或更小的响应时间。响应时间可能大于1秒。在一些情况下,实时可以指同时或基本上同时的处理、检测或鉴定。
如本文所用,术语“受试者”通常是指动物,如哺乳动物(例如人)或禽类(例如鸟),或其他生物(如植物)。例如,受试者可以是脊椎动物、哺乳动物、啮齿动物(例如,小鼠)、灵长类动物、猿猴或人。动物可包括但不限于农场动物、运动型动物和宠物。受试者可以是健康的或无症状的个体、患有或疑似患有疾病(例如,癌症)或易患疾病的个体和/或需要治疗或疑似需要治疗的个体。受试者可以是患者。受试者可以是微生物(microorganism)或微生物(microbe)(例如,细菌、真菌、古细菌、病毒)。
如本文所用,术语“基因组”通常是指来自受试者的基因组信息,其可以是例如受试者遗传信息的至少一部分或全部。基因组可以dna或rna形式编码。基因组可以包含编码区(例如,蛋白质的编码区)以及非编码区。基因组可以包括生物体中所有染色体一起的序列。例如,人类基因组普通具有共计46条染色体。所有这些的序列可共同构成人基因组。
术语“一个或多个衔接子”、“一个或多个接头”和“一个或多个标签”可以同义地使用。接头或标签可以通过任何方法包括连接、杂交或其他方法与待“标记”的多核苷酸序列偶合。
如本文所用,术语“测序”通常是指用于确定一种或多种多核苷酸中的核苷酸碱基的序列的方法和技术。多核苷酸可以是,例如,核酸分子如脱氧核糖核酸(dna)或核糖核酸(rna),包括其变体或衍生物(例如,单链dna)。测序可以通过目前可用的各种系统执行,诸如但不限于通过
如本文所用,术语“珠粒”通常是指颗粒。珠粒可以是固体或半固体颗粒。珠粒可以是凝胶珠粒。凝胶珠粒可包括聚合物基体(例如,通过聚合或交联形成的基体)。聚合物基体可包括一种或多种聚合物(例如,具有不同官能团或重复单元的聚合物)。聚合物基体中的聚合物可以无规排列,如在无规共聚物中,和/或具有有序结构,如在嵌段共聚物中。交联可以通过共价、离子或感应相互作用或物理缠结进行。珠粒可以是大分子。珠粒可由结合在一起的核酸分子形成。珠粒可以通过分子(例如大分子)的共价或非共价组装形成,如单体或聚合物。此类聚合物或单体可以是天然的或合成的。此类聚合物或单体可以是或包括,例如,核酸分子(例如,dna或rna)。珠粒可由聚合物材料形成。珠粒可以是磁性的或非磁性的。珠粒可以是刚性的。珠粒可以是柔性的和/或可压缩的。珠粒可以是可破坏的或可溶解的。珠粒可以是覆盖有包含一种或多种聚合物的涂层的固体颗粒(例如,金属基颗粒,包括但不限于氧化铁、金或银)。这种涂层可以是可破坏或可溶解的。
如本文所用,术语“样品”通常是指受试者的生物样品。生物样品可包含任何数量的大分子,例如细胞大分子。样品可以是细胞样品。样品可以是细胞系或细胞培养物样品。样品可以包括一个或多个细胞。样品可以包括一种或多种微生物。生物样品可以是核酸样品或蛋白质样品。生物样品也可以是碳水化合物样品或脂质样品。生物样品可以来源于另一样品。样品可以是组织样品,例如活组织检查、核心活组织检查(corebiopsy)、针吸出物或细针吸出物。样品可以是流体样品,如血液样品、尿液样品或唾液样品。样品可以是皮肤样品。样品可以是面颊拭子(cheekswab)。样品可以是血浆或血清样品。样品可以是无细胞(cell-free或cellfree)样品。无细胞样品可包括细胞外多核苷酸。细胞外多核苷酸可以从身体样品中分离,所述身体样品可选自由血液、血浆、血清、尿液、唾液、粘膜分泌物、痰液、粪便和泪液组成的组。
如本文所用,术语“生物颗粒”通常是指来源于生物样品的离散生物系统。生物颗粒可以是大分子。生物颗粒可以是小分子。生物颗粒可以是病毒。生物颗粒可以是细胞或细胞的衍生物。生物颗粒可以是细胞器。生物颗粒可以是来自细胞群的稀有细胞。生物颗粒可以是任何类型的细胞,包括但不限于原核细胞、真核细胞、细菌、真菌、植物、哺乳动物或其他动物细胞类型、支原体、正常组织细胞、肿瘤细胞或任何其他细胞类型,无论是来源于单细胞还是多细胞生物体。生物颗粒可以是细胞的成分。生物颗粒可以是或可包括dna、rna、细胞器、蛋白质、代谢物或其任何组合。生物颗粒可以是或可包括基体(例如,凝胶或聚合物基体),其包含细胞或来自细胞的一种或多种成分(例如,细胞珠),如来自细胞的dna、rna、细胞器、蛋白质、代谢物或其任何组合。生物颗粒可以从受试者的组织获得。生物颗粒可以是硬化细胞。这种硬化细胞可以包括或不包括细胞壁或细胞膜。生物颗粒可包括细胞的一种或多种成分,但可不包括细胞的其他成分。此类成分的一个实例是细胞核或细胞器。细胞可以是活细胞。活细胞可以能够被培养,例如,当被包封在凝胶或聚合物基体中时被培养,或者当包含凝胶或聚合物基体时被培养。
如本文所用,术语“大分子组分”通常是指包含在生物颗粒内或来自生物颗粒的大分子。大分子成分可包含核酸。在一些情况下,生物颗粒可以是大分子。大分子成分可包含dna。大分子成分可包含rna。rna可以是编码或非编码的。rna可以是例如信使rna(mrna)、核糖体rna(rrna)或转移rna(trna)。rna可以是转录物。rna可以是长度小于200个核酸碱基的小rna,或长度大于200个核酸碱基的大rna。小rna可包括5.8s核糖体rna(rrna)、5srrna、转移rna(trna)、微rna(mirna)、小干扰rna(sirna)、核仁小rna(snorna)、piwi相互作用rna(pirna)、trna衍生的小rna(tsrna)和小rdna衍生的rna(srrna)。rna可以是双链rna或单链rna。rna可以是环状rna。大分子成分可包含蛋白质。大分子成分可包含肽。大分子成分可包含多肽。
如本文所用,术语“分子标签”通常是指能够结合大分子成分的分子。分子标签可以以高亲和力结合大分子成分。分子标签可以高特异性结合大分子成分。分子标签可包含核苷酸序列。分子标签可包含核酸序列。核酸序列可以是分子标签的至少一部分或全部。分子标签可以是核酸分子或可以是核酸分子的一部分。分子标签可以是寡核苷酸或多肽。分子标签可包含dna适体。分子标签可以是或包含引物。分子标签可以是或包含蛋白质。分子标签可包含多肽。分子标签可以是条形码。
如本文所用,术语“分配区”通常是指可适于包含一种或多种物质或进行一种或多种反应的空间或体积。分配区可以是物理区室,如液滴或孔。分配区可将一个空间或体积与另一个空间或体积隔离。液滴可以是与第一相不混溶的第二相(例如,油)中的第一相(例如,水相)。液滴可以是不与第一相相分离的第二相中的第一相,例如水相中的胶囊或脂质体。分配区可包括一个或多个其他(内部)分配区。在一些情况下,分配区可以是可由跨多个和/或远程物理区室的索引(例如,索引库)定义和标识的虚拟区室。例如,物理区室可包括多个虚拟区室。
本文提供了在单细胞水平上有效且准确地测量一种或多种分析物的处理系统和方法。所述系统和方法可鉴定一种或多种分析物所源自的细胞。分析物可以是蛋白质(例如,表面结合蛋白、内部蛋白等)。分析物可以是代谢物(例如,醇、氨基酸、核苷酸、抗氧化剂、有机酸、多元醇、维生素、辅因子等)。分析物可以是细胞的任何成分,如小的分子、大的分子或大分子。分析物可以是生物颗粒。分析物可以是特异性捕获和分析的靶向分析物,如对抗体具有结合特异性。分析物可以是非特异性捕获和分析的非靶向分析物。
在单细胞水平上鉴定和测量分析物
用于在细胞内鉴定靶向分析物的方法可包括由细胞产生细胞珠,以及将抗体洗入细胞珠中。抗体可对靶向分析物具有结合特异性,并与第一条形码分子偶合。第一条形码分子可包含第一条形码序列。在细胞珠内部,抗体可以结合或以其他方式偶合至靶向分析物,从而形成分析物-抗体复合物,并用第一条形码序列标记靶向分析物。可将细胞珠与珠粒共分配在分配区中,其中珠粒与第二条形码分子偶合。分配区可以是乳液(例如,油包水、水包油等)中的液滴。第二条形码分子可包含第二条形码序列。在分配区中,第二条形码分子可从珠粒中释放并附接于分析物-抗体复合物,从而用第一条形码序列和第二条形码序列标记靶向分析物。第一条形码分子和第二条形码分子可形成包含复合序列的复合条形码分子,所述复合序列包含第一条形码序列和第二条形码序列。第一条形码序列可指示靶向分析物并且第二条形码序列可指示细胞。可对复合条形码分子进行测序以鉴定靶向分析物和细胞,并确定靶向分析物源自细胞内。
第一条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。第一条形码序列可唯一鉴定对通过第一条形码序列标记的抗体具有结合特异性的分析物类型。例如,可以用不同的条形码序列标记对第一类型的分析物具有结合特异性的第一抗体和对第二类型的分析物具有结合特异性的第二抗体。各自对相同类型的分析物(例如,第一类型的蛋白质)具有结合特异性的多种抗体可各自用相同的条形码序列标记。
第二条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。第二条形码序列可唯一鉴定第二条形码分子所偶合的珠粒。例如,第一珠粒和第二珠粒可以与包含不同条形码序列的条形码分子偶合。各自与相同珠粒偶合的多个条形码分子可包含相同的条形码序列。与唯一条形码序列(例如,第二条形码序列)缔合的珠粒可以与细胞共分配。珠粒的唯一条形码序列可用于唯一鉴定与珠粒共分配的细胞。
复合条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。复合条形码序列可包含第一条形码序列和第二条形码序列。在一些情况下,复合条形码序列可包含在本文其他地方描述的一个或多个另外的条形码序列(例如,唯一分子标识符、锚定元件等)。
在一些情况下,可对复合条形码分子进行测序以确定靶向分析物源自细胞内的可能性。例如,在一些情况下,多个珠粒中的两个或更多个珠粒可具有相同的条形码序列(例如,第二条形码序列),这可以是或可以不是有意的。在此类情况下,鉴定第二条形码序列可指示靶向分析物源自两个或更多个细胞(各自与不同的珠粒共分配)中的一个。例如,在五个珠粒具有相同的第二条形码序列的情况下,鉴定第二条形码序列可指示靶向分析物源自五个细胞(各自与不同的珠粒共分配)中的一个。在一些情况下,靶向分析物源自细胞的可能性可至少部分地基于系统中的不同珠粒包含唯一的第二条形码序列的可能性(例如,如果在多个其他珠粒中第一珠粒具有唯一的第二条形码序列的可能性基本上是100%,那么鉴定第二条形码序列可指示靶向分析物源自与第一珠粒共分配的细胞的可能性基本上是100%)。在一些情况下,靶向分析物源自细胞内的可能性可以是至少约50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或100%。可替代地,所述可能性可小于约50%。
靶向分析物可以是内部蛋白,并且接触细胞珠的抗体可对内部蛋白具有结合特异性。在另一个实例中,靶向分析物可以是代谢物,并且接触细胞珠的抗体可对代谢物具有结合特异性。在一些情况下,代谢物可以是醇、氨基酸、核苷酸、抗氧化剂、有机酸、多元醇或维生素。代谢物可以是辅因子。靶向分析物可以是细胞的任何成分,如任何小的分子、大的分子或大分子(例如,大分子成分)。在另一个实例中,靶向分析物可以来自共享结构相似性或同源性(例如,部分、官能团等)的一类、组或亚组的分析物(例如,蛋白质、代谢物、小分子等),并且接触细胞珠的抗体可通过结构相似性而对该类、组或亚组的分析物具有结合特异性。在此类情况下,第一条形码序列可唯一鉴定该类、组或亚组的分析物。在与抗体结合(或以其他方式偶合)后,可通过第一条形码序列将靶向分析物分类为该类、组或亚组的分析物的成员。
用于分配和使用细胞珠和条形码偶合珠粒的系统和方法在本文其他地方更详细地描述,如参考图1-8。
图9示出用于鉴定和测量细胞中的分析物的方法。可对细胞902进行处理,以产生细胞珠904。这可通过将细胞902提供于分配区(如液滴)中来执行。本文其他地方描述了用于产生细胞珠的系统和方法,如通过包封和聚合细胞。可将细胞裂解以释放细胞珠904中的一种或多种分析物,如第一分析物906、第二分析物908和第三分析物910。可替代地,可在形成细胞珠904之前裂解细胞902,然后用裂解的内容物产生细胞珠。例如,将细胞以液滴形式提供并裂解,随后使液滴聚合以产生细胞珠904。可将多种抗体洗入细胞珠中。多种抗体可包含包括第一类型的抗体914的第一组抗体和包括第二类型的抗体918的第二组抗体。第一类型的抗体可以对第一分析物906具有结合特异性并且已经偶合了包含第一条形码序列912的第一条形码分子。第二类型的抗体918可以对第二分析物908具有结合特异性并且已经偶合了包含第二条形码序列916的第二条形码分子。对不同类型的分析物具有结合特异性的抗体可各自具有不同的条形码序列。条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。
洗入细胞珠904中的多种抗体可根据各自的结合特异性结合或以其他方式偶合于一种或多种分析物。例如,第一类型的抗体914的第一抗体可结合(或以其他方式偶合)第一分析物906,从而形成第一分析物-抗体复合物920,并用第一条形码序列912标记第一分析物906。第二类型的抗体918的第二抗体可结合(或以其他方式偶合)第二分析物908,从而形成第二分析物-抗体复合物922,并用第二条形码序列916标记第二分析物908。可将未结合的抗体,如对不存在的分析物具有结合特异性或无法找到游离分析物的那些抗体从细胞珠中洗出。
可替代地或另外地,在将多种类型的抗体批量洗入细胞珠904中时,可将抗体每次一种类型地(例如,顺序地)洗入细胞珠904中。在一些情况下,未结合的抗体可在各洗入之间被洗出。在一些情况下,一种或多种类型的未结合抗体可以一起被洗出。
细胞珠904可与珠粒926共分配在分配区924中。分配区924可以是乳液中的液滴。珠粒926可偶合于多个条形码分子,所述条形码分子各自包含共有的第三条形码序列928。例如,图8示出与多个条形码分子偶合的珠粒。第三条形码序列928对于珠粒926而言可以是唯一的。如本文其他地方所述,多个条形码分子可通过可释放的键与珠粒926偶合。在分配区924中,可以用多个条形码分子标记来自细胞珠904的分析物(例如,在从珠粒926中释放之后)。
在一些情况下,只有偶合于另一条形码分子(例如,偶合于第一类型的抗体914的第一条形码分子、偶合于第二类型的抗体916的第二条形码分子)的抗体所结合(或偶合)的分析物可通过第三条形码序列928标记。例如,偶合于珠粒926的多个条形码分子可包含被构造成偶合于另一条形码分子的特异性引发序列。可替代地或另外地,其他分析物(例如,未结合的分析物)可通过第三条形码序列928标记。
因此,可通过复合条形码序列标记分析物,复合条形码序列包含第三条形码序列928和通过抗体标记的另一条形码序列(例如,第一条形码序列912、第二条形码序列914)。例如,第一分析物906可通过包含第一条形码序列912和第三条形码序列930的第一复合条形码序列930标记。第二分析物908可通过包含第二条形码序列916和第三条形码序列932的第二复合条形码序列932标记。在将如来自不同分配区(例如,包含不同的细胞和珠粒)的复合序列汇集后,可对复合序列进行测序,以通过将一种或多种分析物归属于细胞来测量细胞中的一种或多种分析物。
例如,由第一复合条形码序列930,第一条形码序列912的鉴定可指示第一类型的分析物906,并且第三条形码序列928的鉴定可指示细胞904,从而允许确定第一类型的分析物906源自细胞904。在另一个实例中,由第二复合条形码序列932,第二条形码序列916的鉴定可指示第二类型的分析物908,并且第三条形码序列928的鉴定可指示细胞904,从而允许确定第二类型的分析物906源自细胞904。可替代地或另外地,如当存在两个或更多个珠粒可共享其共有条形码序列(例如,第三条形码序列932)的可能性时,第三条形码序列928的鉴定可指示特定分析物源自细胞904的可能性。在一些情况下,可确定多种分析物源自细胞的相应可能性。
虽然在图9中未示出,在共分配不同细胞与包含不同共有条形码序列的不同珠粒的其他分配区中,复合条形码序列中的不同共有条形码序列的鉴定可指示不同细胞,从而允许将一种或多种分析物归属于(例如,来源、来源的可能性)不同细胞。
有利地,所述系统和方法可将内部蛋白(例如,不是表面结合的)和代谢物归属于单个细胞,并允许其准确而有效的测量。
本公开的方法可允许鉴定表面结合分析物和内部分析物(例如,蛋白质)。例如,参考图9,可在裂解之前,如在将细胞提供于分配区中以产生细胞珠904之前,使细胞902与第一组抗体接触。在一些情况下,细胞902处于可与第一组抗体批量接触的细胞的集合中。第一组抗体中的每种抗体可包含具有指示表面结合分析物的第一条形码序列的条形码分子。在一些情况下,第一组抗体中的抗体可对给定分析物或给定类型的分析物具有结合特异性。对于此类情况,在一些情况下,抗体上的条形码分子可包含一个或多个另外的条形码序列,其经过选择对给定分析物或给定类型的分析物(例如,给定类型的蛋白质)具有特异性并指示所述给定分析物或给定类型的分析物。例如,在第一组抗体中各自对不同类型的分析物具有结合特异性的两种抗体之间,两种抗体可包含相同的第一条形码序列(指示表面结合分析物),但是一个或多个不同的另外序列(指示不同类型的分析物)。当使细胞902(在裂解之前)与第一组抗体接触时,第一组抗体中的抗体可偶合于细胞902的表面结合分析物(例如,表面结合蛋白)以形成抗体-分析物复合物,从而用第一条形码序列(指示表面结合分析物)标记每个抗体结合的表面结合分析物。
在用第一组抗体处理细胞902之后,细胞902可用于产生细胞珠904,如以上在图9的上下文中所述。可在细胞珠904产生之前或之后裂解细胞。然后可通过洗入第二组抗体用第二组抗体(例如,用于蛋白质、代谢物等的测定的抗体914和抗体918)处理来自细胞902内的分析物。第二组抗体中的每种抗体可包含具有指示内部分析物的第二条形码序列的条形码分子。在一些情况下,第二组抗体中的抗体可对给定分析物或给定类型的分析物具有结合特异性。对于此类情况,在一些情况下,抗体上的条形码分子可包含一个或多个另外的条形码序列,其经过选择对给定分析物或给定类型的分析物具有特异性并指示所述给定分析物或给定类型的分析物。例如,在第二组抗体中各自对不同类型的分析物具有结合特异性的两种抗体之间,两种抗体可包含相同的第二条形码序列(指示内部分析物),但是具有一个或多个不同的另外序列(指示不同类型的分析物)。当使来自细胞902内的分析物与第二组抗体接触时,第二组抗体中的抗体可偶合于内部分析物(来自细胞902内)以形成抗体-分析物复合物,从而用第二条码序列(指示内部分析物)标记每个抗体结合的内部分析物。
在一些情况下,如以上在图9的上下文中所述,可将细胞珠(通过第一组和第二组抗体处理过的)与包含多个包含第三条形码序列(指示细胞)的条形码分子的珠粒共分配,并且每种分析物,包括表面结合分析物(通过第一条形码序列标记)和内部分析物(通过第二条形码序列标记),可通过第三条形码序列标记,诸如以形成复合条形码序列。例如,第一复合序列可包含第一条形码序列和第三条形码序列。在另一个实例中,第二复合序列可包含第二条形码序列和第三条形码序列。
在将如来自不同分配区(例如,包含不同的细胞和珠粒)的复合序列汇集后,可对复合序列进行测序,以通过将一种或多种分析物归属于细胞来测量细胞中的一种或多种分析物。测序之后,第一条形码序列和第二条形码序列可分别鉴定表面结合分析物和内部分析物,并且第三条形码序列可鉴定细胞(例如,902)。在一些情况下,一个或多个另外的序列可鉴定给定分析物或给定类型的分析物。有利地,对于所鉴定的分析物,本公开的系统和方法不仅可鉴定来源细胞,而且可鉴定在细胞中的来源位置(例如,表面结合、内部等)。
用于测量细胞中的分析物的另一种方法可包括将细胞和珠粒共分配在第一分配区中。第一分配区可以是乳液中的液滴。珠粒可包含被构造成偶合于分析物(例如,蛋白质)的多种抗体。多种抗体可以可释放地附接于珠粒,诸如本文其他地方所述。在一些情况下,多种抗体中的给定抗体可具有非结合特异性,如能够结合或以其他方式偶合于不同的分析物。可替代地或另外地,给定抗体可对特定类型的分析物(例如,特定类型的蛋白质)具有结合特异性。可替代地或另外地,给定抗体可对特定类、组或亚组的分析物具有结合特异性。多种抗体中的每种抗体可与包含共有的第一条形码序列的共有的第一条形码分子偶合。共有的第一条形码序列对于珠粒而言可以是唯一的。可使细胞经受足以允许给定抗体与分析物偶合的条件,以产生第一分析物-抗体复合物,从而用第一条形码序列标记分析物。例如,可将细胞裂解并且从珠粒中释放抗体。
可将第一分析物-抗体复合物与如来自相同分配区和/或不同分配区(例如,不同液滴)的其他分析物-抗体复合物汇集。可通过每种分析物-抗体复合物中分析物的类型将分析物-抗体复合物的汇集物分选到不同的分配区中。例如,分配区可以是孔。第一分析物-抗体复合物可和与第一分析物-抗体复合物相同类型的其他分析物-抗体复合物(如果存在的话)一起共分配在第二分配区(例如,孔)中。第一分析物-抗体复合物可与包含第二条形码序列的第二条形码分子共分配,其条件足以允许第一分析物-抗体复合物的第一条形码分子和第二条形码分子产生包含包括第一条形码序列和第二条形码序列的复合条形码序列的复合条形码分子,从而用第一条形码序列和第二条形码序列标记分析物。可在将第一分析物-抗体复合物分配在第二分配区中之前、期间或之后,将第二条形码分子递送至第二分配区。可将第二条形码分子递送到如珠粒的载体上。第二条形码分子可作为各自包含第二条形码序列的多个条形码分子的一部分被递送。第二条形码序列对于第二分配区而言可以是唯一的。每个孔(各自包含不同类型的分析物-抗体复合物)可包含对于每个孔而言唯一的不同条形码序列。例如,包含相同类型的分析物-抗体复合物的两个或更多个孔可包含相同的共有条形码序列(例如,第二条形码序列)。分配区可以是非孔分配区。
可对复合条形码分子或其衍生物进行测序,以由复合条形码序列中的第一条形码序列鉴定细胞,并由复合条形码序列中的第二条形码序列鉴定分析物,并且确定分析物源自细胞。
第一条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。第一条形码序列可以是核酸序列。第一条形码序列可唯一地鉴定第一条形码分子所偶合的珠粒。例如,第一珠粒和第二珠粒可以与包含不同条形码序列的条形码分子偶合。各自与相同珠粒偶合的多个条形码分子可包含相同的条形码序列。与唯一条形码序列(例如,第一条形码序列)缔合的珠粒可与细胞共分配。珠粒的唯一条形码序列可用于唯一鉴定与珠粒共分配的细胞。
第二条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。第二条形码序列可唯一地鉴定第二条形码序列被递送的分配区。例如,不同的分配区可各自被递送不同的条形码序列。分配区可包含第一常见类型的分析物。分配区的唯一条形码序列(例如,第二条形码序列)可用于唯一地鉴定在分配区中共分配的第一常见类型的分析物。可替代地,第二条形码序列可唯一地鉴定一种类型的分析物。例如,在第一常见类型的分析物被分配在两个或更多个分配区(例如,一半在第一分配区,另一半在第二分配区)的情况下,第二条形码序列可被递送到两个或更多个分配区中的每一个中,并且可将不同的唯一条形码序列递送到包含不同类型分析物的其他分配区中。
复合条形码分子可以是核酸分子,如寡核苷酸或多核苷酸。复合条形码序列可包含第一条形码序列和第二条形码序列。在一些情况下,复合条形码序列可包含在本文其他地方描述的一个或多个另外的条形码序列(例如,唯一分子标识符、锚定元件等)。
在一些情况下,可对复合条形码分子进行测序以确定分析物源自细胞的可能性。例如,在一些情况下,多个珠粒中的两个或更多个珠粒可具有相同的条形码序列(例如,第一条形码序列),这可以是或可以不是有意的。在此类情况下,鉴定第一条形码序列可指示分析物源自两个或更多个细胞(各自与不同的珠粒共分配)中的一个。例如,在五个珠粒具有相同的第一条形码序列的情况下,鉴定第一条形码序列可指示分析物源自五个细胞(各自与不同的珠粒共分配)中的一个。在一些情况下,分析物源自细胞的可能性可至少部分地基于系统中的不同珠粒包含唯一的第一条形码序列的可能性(例如,如果在多个其他珠粒中第一珠粒具有唯一的第一条形码序列的可能性基本上是100%,那么鉴定第一条形码序列可指示分析物源自与第一珠粒共分配的细胞的可能性基本上是100%)。在一些情况下,分析物源自细胞的可能性可以是至少约50%、55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或100%。可替代地,所述可能性可小于约50%。
分析物可以是内部蛋白。在另一个实例中,分析物可以是代谢物。分析物可以是细胞的任何成分,如任何小的分子、大的分子或大分子(例如,大分子成分)。在另一个实例中,分析物可以来自共享结构相似性或同源性(例如,部分、官能团等)的一类、组或亚组的分析物(例如,蛋白质、代谢物、小分子等)。分析物可以是靶向分析物或来自靶向类别的分析物,如通过采用对靶向分析物或靶向类别的分析物具有结合特异性的抗体。分析物可以是非靶向分析物。
图10示出用于鉴定和测量细胞中的分析物的另一方法。细胞1002和珠粒1004可共分配在第一分配区1006中。第一分配区1006可以是乳液中的液滴。珠粒1004可在将细胞1002分配在第一分配区1006中之前、期间或之后递送到第一分配区1006中。用于分配的系统和方法在本文其他地方描述。珠粒1004可偶合于多种抗体1010,所述抗体可以或可以不对细胞1002中或怀疑处于其中的分析物或一类分析物具有结合特异性。多种抗体1010中的每种抗体可包含共有的第一条形码序列1008。珠粒1004可经由一个或多个条形码分子(例如,包含共有的第一条形码序列1008)偶合于多种抗体1010。珠粒1004可以与一个或多个条形码分子可释放地偶合,如本文其他地方所述。例如,图8示出与多个条形码分子偶合的珠粒。第一条形码序列1008对于珠粒1004而言可以是唯一的。
可将细胞1002裂解以将一种或多种分析物释放在第一分配区1006中,如第一分析物1012、第二分析物1014和第三分析物1016,所述分析物各自为不同类型的分析物(例如,不同类型的蛋白质)。多种抗体1010可以从珠粒1004中释放,如本文其他地方所述(例如,施加一种或多种刺激)。在第一分配区1006中,来自细胞1002的给定分析物(例如,1012、1014、1016)可与给定抗体(例如,1010)结合(或以其他方式偶合),以形成给定的分析物-抗体复合物,从而用第一条形码序列1008标记给定分析物。在第一分配区1006中形成的各分析物-抗体复合物可用第一条形码序列1008标记,与分析物的类型无关。例如,为不同类型分析物的第一分析物1012、第二分析物1014和第三分析物1016中的每一种可用第一条形码序列1008标记。
可将给定的分析物-抗体复合物与如来自相同分配区(第一分配区1006)和/或不同分配区(例如,不同液滴)的其他分析物-抗体复合物汇集。可通过每种分析物-抗体复合物中分析物的类型将分析物-抗体复合物的汇集物分选到不同的分配区中。例如,分配区可以是孔。例如,可将包含第一分析物1012的第一分析物-抗体复合物与来自第一分配区1006或包含与第一分析物1012相同类型的分析物的其他分配区的其他分析物-抗体复合物一起分配到第一孔中。可将包含第二分析物1014的第二分析物-抗体复合物与来自第一分配区1006或包含与第二分析物1014相同类型的分析物的其他分配区的其他分析物-抗体复合物一起分配到第二孔中。可将包含第三分析物1016的第三分析物-抗体复合物与来自第一分配区1006或包含与第三分析物1016相同类型的分析物的其他分配区的其他分析物-抗体复合物一起分配到第三孔中。
在图10中,例如,第一孔包含来自第一分配区1006的第一分析物-抗体复合物,以及来自共分配第二细胞和包含第二条形码序列1018的第二珠粒的第一其他分配区的与第一分析物1012相同类型的另一分析物-抗体复合物,从而用第二条形码序列1018进行标记。第二孔包含来自第一分配区1006的第二分析物-抗体复合物,以及来自第一其他分配区的与第二分析物1014相同类型的另一分析物-抗体复合物,从而用第二条形码序列1018进行标记,以及来自共分配第三细胞和包含第三条形码序列1020的第三珠粒的第二其他分配区的与第二分析物1014相同类型的另一分析物-抗体复合物,从而用第三条形码序列1020进行标记。第三孔包含来自第一分配区1006的第三分析物-抗体复合物。
在一些情况下,可将一种类型的分析物分选到多于一个孔中。例如,各自包含相同的第一类型分析物的多个分析物-抗体复合物可分布在两个或更多个孔中,前提条件是每个孔仅包含一种类型的分析物。
可将包含对于每个孔而言唯一的条形码序列的条形码分子递送至每个孔。例如,可将包含第四条形码序列1022的条形码分子递送至第一孔,可将包含第五条形码序列1024的条形码分子递送至第二孔,并且可将包含第六条形码序列1026的条形码分子递送至第三孔。在一些情况下,条形码分子可经由珠粒递送至每个孔。在一些情况下,条形码分子可作为各自包含相同的唯一条形码序列的多个条形码分子的一部分递送。例如,第四条形码序列1022对于第一孔而言可以是唯一的,第五条形码序列1024对于第二孔而言可以是唯一的,并且第六条形码序列1026对于第三孔而言可以是唯一的。
可替代地或另外地,可将包含对于一种类型的分析物而言唯一的条形码序列的条形码分子递送至每个孔。例如,在两个或更多个孔包含相同类型的分析物的情况下,可将相同的条形码序列递送至两个或更多个孔。
可使孔及其成分经受足以允许将给定条形码分子(例如,包括1022、1024、1026)递送至孔并且分析物-抗体复合物的给定条形码分子产生包含复合条形码序列的给定的复合条形码分子的条件。复合条形码序列可包括递送至孔的条形码分子的条形码序列和标记在分析物-抗体复合物上的条形码序列。
例如,在图10中,在第一孔中,第一复合条形码序列包含来自第一分配区1006的第一条形码序列1008(对于第一分配区而言是唯一的)和第四条形码序列1022(对于第一孔而言是唯一的),并且第二复合条形码序列包含来自第一其他分配区(对于第一其他分配区而言是唯一的)的第二条形码序列1018和第四条形码序列1022(对于第一孔而言是唯一的)。在第二孔中,第三复合条形码序列包含来自第一分配区1006的第一条形码序列1008(对于第一分配区而言是唯一的)和第五条形码序列1024(对于第二孔而言是唯一的),第四复合条形码序列包含来自第一其他分配区的第二条形码1018(对于第一其他分配区而言是唯一的)和第五条形码序列1022(对于第二孔而言是唯一的),并且第五复合条形码序列包含来自第二其他分配区的第三条形码序列1020(对于第二其他分配区而言是唯一的)和第五条形码序列1022(对于第二孔而言是唯一的)。在第三孔中,第六复合条形码序列包含来自第一分配区1006的第一条形码序列1008(对于第一分配区而言是唯一的)和第六条形码序列1026(对于第三孔而言是唯一的)。
在将如来自不同分配区(例如,孔)的复合序列汇集后,可对复合序列进行测序,以通过将一种或多种分析物归属于细胞来测量细胞中的一种或多种分析物。
例如,由第一复合条形码序列,第一条形码序列1008的鉴定可指示细胞1002,并且第四条形码序列1022的鉴定可指示第一分析物1012类型,从而允许确定第一分析物1012类型源自细胞1002。在另一个实例中,由第五复合条形码序列,第三条形码序列1020的鉴定可指示第三细胞(与包含第三条形码序列1020的第三珠粒共分配在第二其他分配区中),并且第五条形码序列1022的鉴定可指示第二分析物1014类型,从而允许确定第二分析物1014类型源自第二细胞。可替代地或另外地,如当存在两个或更多个珠粒可共享其共有条形码序列(例如,第一条形码序列1008)的可能性时,第一条形码序列1008的鉴定可指示特定类型的分析物源自细胞1004的可能性。可确定不同类型的分析物的相应可能性。
虽然图10示出三种不同类型的分析物的鉴定,但是可鉴定任何数量的分析物。虽然图10示出三种不同类型的细胞的鉴定,但是可鉴定任何数量的细胞。
虽然参照图9和图10描述的系统和方法示出通过使用一种或多种可以或可以不具有结合特异性的抗体来捕获一种或多种分析物,但是所述系统和方法可使用被构造成偶合于一种或多种分析物的其他衔接子或分子(例如,肽),如特异性引发序列或随机引物来应用。例如,参考图10,珠粒可偶合于被构造成与一种或多种分析物偶合的多个衔接子或分子。在一些情况下,珠粒可偶合于包含条形码序列的不同衔接子或分子的一个或多个群体,如抗体的第一群体和引发序列的第二群体。
本公开的方法可用于鉴定关于来自细胞的分析物的信息,包括分析物的身份(例如,类型)和分析物的位置(例如,表面结合、内部)。此类分析物可包括,例如,蛋白质、代谢物、核糖核酸(rna)分子和脱氧核糖核酸(dna)分子。在一些实例中,可获得细胞的蛋白质组学信息,并将其与关于细胞的基因组信息(例如,dna或基因组变体)和/或转录组信息(例如,mrna)相结合。这可允许鉴定,例如,转录为mrna的基因和翻译成蛋白质的mrna。
计算机系统,例如参考图11所描述的,可用于实施本公开的系统和方法,如生成和维护一个或多个库,以及执行测序,并分析这种测序的结果以鉴定一种或多种分析物、鉴定一种或多种细胞,和/或将所鉴定的分析物归属于所鉴定的细胞。有利地,本文提供的系统和方法可在单细胞水平上有效且准确地测量一种或多种分析物。
用于样品区室化的系统和方法
在一个方面,本文所述的系统和方法提供将一个或多个颗粒(例如,生物颗粒、生物颗粒的大分子成分、珠粒、试剂等)区室化、沉积或分配到离散区室或分配区(在本文中可互换地称为分配区)中,其中每个分配区保持其自己的内容物与其他分配区的内容物的分离。分配区可以是乳液中的液滴。分配区可包括一个或多个其他分配区。
分配区可包括一个或多个颗粒。分配区可包括一种或多种类型的颗粒。例如,本公开的分配区可包括一个或多个生物颗粒和/或其大分子成分。分配区可包括一个或多个凝胶珠粒。分配区可包括一个或多个细胞珠。分配区可包括单个凝胶珠粒、单个细胞珠,或单个细胞珠和单个凝胶珠粒。分配区可包括一种或多种颗粒。可替代地,分配区可未被占据。例如,分配区可不包括珠粒。细胞珠可以是例如通过含有生物颗粒的液滴和能够被聚合或胶凝的前体的聚合而包裹在凝胶或聚合物基体内的生物颗粒和/或其大分子成分中的一种或多种。可以在液滴产生之前、之后或同时如通过微胶囊(例如珠粒)将唯一标识符(如条形码)注射到液滴中,如本文其他地方所描述。微流体通道网络(例如,在芯片上)可用于产生如本文所述的分配区。在单个生物颗粒的分配中也可以采用替代机制,包括多孔膜,通过多孔膜将细胞的含水混合物挤出到非含水流体中。
分配区可在流体流内流动。分配区可包括例如微囊泡,其具有围绕内部流体中心或核心的外部屏障。在一些情况下,分配区可包括多孔基体,其能够在其基体内夹带和/或保留材料。分配区可以是第二相内的第一相的液滴,其中第一相和第二相是不混溶的。例如,分配区可以是非含水连续相(例如,油相)内的含水流体的液滴。在另一个实例中,分配区可以是水相内的非含水流体的液滴。在一些实例中,分配区可以油包水乳液或水包油乳液的形式提供。在例如美国专利申请公布2014/0155295中描述了多种不同的容器,所述申请出于所有目的以引用方式全文并入本文。用于在非含水或油状连续相中产生稳定液滴的乳液体系描述于例如美国专利申请公布2010/0105112中,所述申请出于所有目的以引用方式全文并入本文。
就乳液中的液滴而言,在一个非限制性实例中,将单个颗粒分配到离散分配区中可以通过将含水流体中的颗粒的流动流引入非含水流体的流动流中,使得在两股流的汇合点处产生液滴来实现。流体特性(例如,流体流速、流体粘度等)、颗粒特性(例如,体积分数、粒度、颗粒浓度等)、微流体架构(例如,通道几何形状等)以及其他参数可调整,以控制所得分配区的占据率(例如,每个分配区的生物颗粒数目、每个分配区的珠粒数目等)。例如,可以通过提供一定颗粒浓度和/或流速的含水流来控制分配区占据率。为了产生单个生物颗粒分配区,可以选择不混溶流体的相对流速,使得平均而言,分配区可以每个分配区包含少于一个生物颗粒,以确保被占据的那些分配区主要被单独占据。在一些情况下,多个分配区中的分配区可包含至多一个生物颗粒(例如,珠粒、dna、细胞或细胞材料)。在一些实施方案中,可选择或调整各种参数(例如,流体特性、颗粒特性、微流体架构等),使得大部分分配区被占据,例如,仅允许小百分比的未占据分配区。可以控制流和通道架构以确保给定数量的单独占据分配区、小于一定水平的未占据分配区和/或小于一定水平的多占据分配区。
图1示出用于分配单个生物颗粒的微流体通道结构100的实例。通道结构100可包括在通道汇合点110处连通的通道区段102、104、106和108。在操作中,包括悬浮生物颗粒(或细胞)114的第一含水流体112可沿通道区段102输送到汇合点110中,同时与含水流体112不混溶的第二流体116从通道区段104和106中的每一个输送到汇合点110,以产生第一含水流体112的离散液滴118、120,离散液滴118、120流入通道区段108并从汇合点110流走。通道区段108可以流体联接到可以储存和/或收集离散液滴的出口贮存器。产生的离散液滴可包括单个生物颗粒114(如液滴118)。产生的离散液滴可包括多于一个单独生物颗粒114(图1中未示出)。离散液滴可以不包含生物颗粒114(例如液滴120)。每个离散分配区可保持其自身内容物(例如,单独的生物颗粒114)与其他分配区的内容物的分离。
第二流体116可包含油,如氟化油,其包括用于稳定所得液滴(例如,抑制所得液滴118、120的后续聚结)的含氟表面活性剂。特别有用的分配流体和含氟表面活性剂的实例描述于例如美国专利申请公布2010/0105112中,所述申请出于所有目的以引用方式全文并入本文。
如将理解的,本文描述的通道区段可以联接到多种不同流体源或接收部件中的任一个,包括其他系统的贮存器、管道、歧管或流体部件。如将理解的,微流体通道结构100可具有其他几何形状。例如,微流体通道结构可具有多于一个通道汇合点。例如,微流体通道结构可以具有2、3、4或5个通道区段,所述通道区段各自承载在通道汇合点处相遇的颗粒(例如,生物颗粒、细胞珠和/或凝胶珠粒)。可以通过一个或多个流体流动单元引导流体沿着一个或多个通道或贮存器流动。流体流动单元可包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等以控制流体的流动。还可以或以其他方式通过施加的压力差、离心力、电动泵送、真空、毛细管或重力流等来控制流体。
产生的液滴可包括两个液滴子集:(1)占据的液滴118,其包含一个或多个生物颗粒114,和(2)未占据的液滴120,其不包含任何生物颗粒114。占据的液滴118可以包括单占液滴(具有一个生物颗粒)和多占液滴(具有多于一个生物颗粒)。如本文其他地方所述,在一些情况下,大多数占据的分配区可以每个占据的分配区包括不多于一个生物颗粒,并且一些产生的分配区可以未被(任何生物颗粒)占据。但是,在一些情况下,一些占据的分配区可能包括多于一个生物颗粒。在一些情况下,可以控制分配过程,使得少于约25%的占据分配区包含多于一个生物颗粒,并且在许多情况下,少于约20%的占据分配区具有多于一个生物颗粒,而在一些情况下,少于约10%或甚至少于约5%的占据分配区包括每个分配区多于一个生物颗粒。
在一些情况下,可能希望最小化过度数量空分配区的产生,例如以降低成本和/或提高效率。尽管这种最小化可以通过在分配汇合点110处提供足够数量的生物颗粒(例如,生物颗粒114)例如以确保至少一个生物颗粒被包封在分配区中来实现,但是泊松分布可以预期地增加包含多个生物颗粒的分配区的数量。因此,在要获得单占分配区的情况下,至多约95%、90%、85%、80%、75%、70%、65%、60%、55%、50%、45%、40%、35%、30%、25%、20%、15%、10%、5%或更少产生的分配区可以是未被占据的。
在一些情况下,可以控制一个或多个生物颗粒(例如,在通道区段102中)的流动,或者引导到分配汇合点中的其他流体(例如,在通道区段104、106中)的流动,使得在许多情况下,不多于约50%产生的分配区、不多于约25%产生的分配区或不多于约10%产生的分配区未被占据。可以控制这些流以便呈现单占分配区的非泊松分布,同时提供较低水平的未占据分配区。可以实现上述范围的未占据分配区,同时仍然提供上述任何单占率。例如,在许多情况下,使用本文所述的系统和方法可以产生具有小于约25%、小于约20%、小于约15%、小于约10%,并且在许多情况下,小于约5%的多占率的所得分配区,同时具有小于约50%、小于约40%、小于约30%、小于约20%、小于约10%、小于约5%或更少的未占据分配区。
如应理解,上述占据率也适用于包括生物颗粒和另外试剂的分配区,包括但不限于携带条形码化核酸分子(例如,寡核苷酸)的微胶囊或珠粒(例如,凝胶珠粒)(参照图2描述)。占据分配区(例如,至少约10%、20%、30%、40%、50%、60%、70%、80%、90%、95%或99%的占据分配区)可包括包含条形码化核酸分子的微胶囊(例如珠粒)和生物颗粒。
在另一方面中,除了基于液滴的分配之外或作为基于液滴的分配的替代方案,生物颗粒可以包封在微胶囊内,所述微胶囊包括其中夹带有一个或多个单独生物颗粒或少量生物颗粒的外壳、层或多孔基体。微胶囊可包括其他试剂。可以通过多种方法执行生物颗粒的包封。此类方法可以将含有生物颗粒的含水流体与聚合物前体材料组合,所述聚合物前体材料在将特定刺激施加到聚合物前体后能够形成凝胶或其他固体或半固体基体。这样的刺激可以包括,例如,热刺激(例如,加热或冷却)、光刺激(例如,通过光固化)、化学刺激(例如,通过交联、前体的聚合引发(例如,通过添加的引发剂))、机械刺激或其组合。
包含生物颗粒的微胶囊的制备可以通过多种方法执行。例如,气刀液滴或气溶胶发生器可用于将前体流体液滴分配到胶凝溶液中,以形成包含单独生物颗粒或少量生物颗粒的微胶囊。同样地,基于膜的包封系统可用于产生包含如本文所述的包封生物颗粒的微胶囊。本公开的微流体系统,如图1所示,可容易地用于包封如本文所述的细胞。特别地,并且参考图1,包含(i)生物颗粒114和(ii)聚合物前体材料(未示出)的含水流体112流入通道汇合点110,在通道汇合点110中含水流体112通过非含水流体116的流动被分配成液滴118、120。就包封方法而言,非含水流体116还可包括引发剂(未示出),以引起聚合物前体的聚合和/或交联,从而形成包含夹带的生物颗粒的微胶囊。聚合物前体/引发剂对的实例包括美国专利申请公布2014/0378345中描述的那些,所述申请出于所有目的以引用方式全文并入本文。
例如,在聚合物前体材料包含线性聚合物材料(例如线性聚丙烯酰胺、peg或其他线性聚合物材料)的情况下,活化剂可包含交联剂或活化在所形成的液滴中的交联剂的化学品。同样,对于包含可聚合单体的聚合物前体,活化剂可包括聚合引发剂。例如,在某些情况下,当聚合物前体包含丙烯酰胺单体与n,n'-双-(丙烯酰基)胱胺(bac)共聚单体的混合物时,可在通道区段104和106中的第二流体流116内提供如四乙基甲二胺(temed)的试剂,其可以引发丙烯酰胺和bac共聚成交联聚合物网络或水凝胶。
在汇合点110处第二流体流116与第一流体流112接触后,在液滴形成期间,temed可以从第二流体116扩散到包含线性聚丙烯酰胺的含水流体112中,这将活化液滴118、120内的聚丙烯酰胺的交联,导致以夹带细胞114的固体或半固体珠粒或颗粒的形式的凝胶(例如,水凝胶)微胶囊的形成。尽管描述了聚丙烯酰胺包封,但是其他“可活化的”包封组合物也可以用于本文所述的方法和组合物的上下文中。例如,形成藻酸盐液滴,然后暴露于二价金属离子(例如,ca2+离子),可以用作使用所述方法的包封方法。同样地,琼脂糖液滴也可以通过基于温度的胶凝(例如,在冷却后等)转化成胶囊。
在一些情况下,包封的生物颗粒可以选择性地从微胶囊中释放,例如通过时间的推移或在施加特定刺激后,所述刺激使微胶囊充分降解以允许生物颗粒(例如,细胞)或其其他内容物从微胶囊中释放,例如进入分配区(例如,液滴)。例如,就上述聚丙烯酰胺聚合物而言,微胶囊的降解可以通过引入适当的还原剂如dtt等以裂解交联聚合物基体的二硫键来完成。参见,例如,美国专利申请公布2014/0378345,所述申请出于所有目的以引用方式全文并入本文。
可以使生物颗粒经受足以聚合或胶凝前体的其他条件。足以聚合或胶凝前体的条件可包括暴露于加热、冷却、电磁辐射和/或光。足以聚合或胶凝前体的条件可包括足以聚合或胶凝前体的任何条件。在聚合或胶凝之后,可以在生物颗粒周围形成聚合物或凝胶。聚合物或凝胶可扩散地渗透到化学或生物化学试剂中。聚合物或凝胶不可扩散地渗透到生物颗粒的大分子成分中。以这种方式,聚合物或凝胶可以起允许生物颗粒经受化学或生物化学操作,同时在空间上将大分子成分限制在由聚合物或凝胶限定的液滴区域的作用。聚合物或凝胶可包括二硫键交联的聚丙烯酰胺、琼脂糖、藻酸盐、聚乙烯醇、聚乙二醇(peg)-二丙烯酸酯、peg-丙烯酸酯、peg-硫醇、peg-叠氮化物、peg-炔烃、其他丙烯酸酯、壳聚糖、透明质酸、胶原蛋白、纤维蛋白、明胶或弹性蛋白中的一种或多种。聚合物或凝胶可包含任何其他聚合物或凝胶。
可以将聚合物或凝胶官能化以结合靶向分析物,例如核酸、蛋白质、碳水化合物、脂质或其他分析物。聚合物或凝胶可通过被动机制聚合或胶凝。聚合物或凝胶在碱性条件下或在升高的温度下可以是稳定的。聚合物或凝胶可具有与珠粒的机械特性类似的机械特性。例如,聚合物或凝胶可具有与珠粒类似的尺寸。聚合物或凝胶可具有与珠粒类似的机械强度(例如拉伸强度)。聚合物或凝胶的密度可以低于油。聚合物或凝胶的密度可以与缓冲液的密度大致类似。聚合物或凝胶可具有可调的孔径。可以选择孔径以例如保留变性的核酸。可以选择孔径以保持对外源性化学物质如氢氧化钠(naoh)和/或内源性化学物质如抑制剂的扩散渗透性。聚合物或凝胶可以是生物相容的。聚合物或凝胶可以保持或增强细胞活力。聚合物或凝胶可以是生物化学相容的。聚合物或凝胶可以以热、化学、酶促和/或光的方式聚合和/或解聚。
聚合物可包含与二硫键交联的聚(丙烯酰胺-共-丙烯酸)。聚合物的制备可包括两步反应。在第一活化步骤中,可以将聚(丙烯酰胺-共-丙烯酸)暴露于酰化剂以将羧酸转化为酯。例如,可以将聚(丙烯酰胺-共-丙烯酸)暴露于4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(dmtmm)。可以将聚丙烯酰胺-共-丙烯酸暴露于4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉的其他盐。在第二交联步骤中,可以将在第一步中形成的酯暴露于二硫化物交联剂。例如,可以将酯暴露于胱胺(2,2'-二硫代双(乙胺))。在这两个步骤之后,生物颗粒可以被通过二硫桥连接在一起的聚丙烯酰胺链包围。以这种方式,生物颗粒可以被包裹在凝胶或基体(例如,聚合物基体)内部或包含凝胶或基体以形成“细胞珠”。细胞珠可以包含生物颗粒(例如,细胞)或生物颗粒的大分子成分(例如,rna、dna、蛋白质等)。细胞珠可包括单个细胞或多个细胞,或单个细胞或多个细胞的衍生物。例如,在裂解和洗涤细胞后,可以从细胞裂解物中洗去抑制组分,并且可以将大分子成分结合为细胞珠。本文公开的系统和方法可适用于含有生物颗粒的细胞珠(和/或液滴或其他分配区)和含有生物颗粒的大分子成分的细胞珠(和/或液滴或其他分配区)。
与基于液滴分配的生物颗粒相比,包封的生物颗粒可以提供更易储存和更便携的某些潜在优点。此外,在一些情况下,希望允许生物颗粒在分析之前温育一段选定时间,例如以便表征在存在或不存在不同刺激的情况下此类生物颗粒随时间的变化。在此类情况下,与在乳液液滴中分配相比,包封可以允许更长时间的温育,但是在一些情况下,液滴分配的生物颗粒也可以温育不同的时间段,例如,至少10秒、至少30秒、至少1分钟、至少5分钟、至少10分钟、至少30分钟、至少1小时、至少2小时、至少5小时、或至少10小时或更长时间。生物颗粒的包封可以构成生物颗粒的分配,其他试剂在其中共分配。可替代地或另外地,包封的生物颗粒可以轻易地沉积到如上文所述的其他分配区(例如,液滴)中。
珠粒
分配区可包含一个或多个唯一标识符,如条形码。条形码可预先、随后或同时递送到保持分室化或分配生物颗粒的分配区。例如,可以在液滴产生之前、之后或同时将条形码注射到液滴中。将条形码递送到特定分配区允许稍后将单独生物颗粒的特征归属于特定分配区。条形码可通过任何合适的机制在例如核酸分子(例如,寡核苷酸)上递送至分配区。条形码化核酸分子可以通过微胶囊递送至分配区。在一些情况下,微胶囊可包含珠粒。珠粒在下面进一步详细描述。
在一些情况下,条形码化核酸分子可以最初与微胶囊缔合,然后从微胶囊释放。条形码化核酸分子的释放可以是被动的(例如,通过从微胶囊中扩散出来)。另外地或可替代地,从微胶囊中释放可以在施加允许条形码化核酸分子从微胶囊中解离或释放的刺激时。这种刺激可破坏微胶囊,是将条形码化核酸分子与微胶囊偶合或在微胶囊内偶合的相互作用,或两者。这种刺激可以包括,例如,热刺激、光刺激、化学刺激(例如,ph的变化或使用一种或多种还原剂)、机械刺激、辐射刺激;生物刺激(例如酶)或其任何组合。
图2示出用于将携带条形码的珠粒递送至液滴的微流体通道结构200的实例。通道结构200可包括在通道汇合点210处连通的通道区段201、202、204、206和208。在操作中,通道区段201可将包含多个珠粒214(例如,具有核酸分子、寡核苷酸、分子标签)的含水流体212沿着通道区段201输送到汇合点210处。多个珠粒214可以源自珠粒的悬浮液。例如,通道区段201可以连接到包含珠粒214的含水悬浮液的贮存器。通道区段202可以将包括多个生物颗粒216的含水流体212沿着通道区段202输送到汇合点210。多个生物颗粒216可以源自生物颗粒的悬浮液。例如,通道区段202可以连接到包含生物颗粒216的含水悬浮液的贮存器。在一些情况下,第一通道区段201或第二通道区段202中或两个区段中的含水流体212可以包括一种或多种试剂,如下面进一步描述的。与含水流体212不混溶的第二流体218(例如,油)可以从通道区段204和206中的每一个被递送到汇合点210。在来自通道区段201和202中的每一个的含水流体212与来自通道区段204和206中的每一个的第二流体218在通道汇合点210处相遇后,含水流体212可以在第二流体218中以离散液滴220的形式被分配并且沿着通道区段208从汇合点210流出。通道区段208可以将离散液滴递送到流体联接到通道区段208的出口贮存器,在所述贮存器中将它们加以收集。
作为替代方案,通道区段201和202可以在汇合点210的上游的另一个汇合点处相遇。在这样的汇合点处,珠粒和生物颗粒可以形成混合物,所述混合物沿着另一个通道被引导到汇合点210以产生液滴220。所述混合物可以以交替的方式提供珠粒和生物颗粒,使得例如液滴包含单个珠粒和单个生物颗粒。
珠粒、生物颗粒和液滴可以基本上常规的流动模式(例如,以常规流速)沿着通道流动。此类常规的流动模式可允许液滴包括单个珠粒和单个生物颗粒。此类常规的流动模式可以允许液滴具有大于5%、10%、20%、30%、40%、50%、60%、70%、80%、90%或95%的占据率(例如,具有珠粒和生物颗粒的液滴)。在例如美国专利公布2015/0292988中提供了此类常规流动模式和可用于提供此类常规流动模式的装置,所述专利以引用方式全文并入本文。
第二流体218可包含油,例如氟化油,其包括用于稳定所得液滴(例如,抑制所得液滴220的后续聚结)的含氟表面活性剂。
产生的离散液滴可包括单独的生物颗粒216。产生的离散液滴可包括携带条形码或其他试剂的珠粒214。产生的离散液滴可包括单个生物颗粒和携带条形码的珠粒,如液滴220。在一些情况下,离散液滴可以包括多于一个单独的生物颗粒或不包括生物颗粒。在一些情况下,离散液滴可包括多于一个珠粒或不包括珠粒。离散液滴可能未被占据(例如,没有珠粒、没有生物颗粒)。
有利地,分配生物颗粒和携带条形码的珠粒的离散液滴可以有效地允许将条形码归属于分配区内的生物颗粒的大分子成分。分配区的内容物可保持与其他分配区的内容物离散。
如将理解的,本文描述的通道区段可以联接到多种不同流体源或接收部件中的任一个,包括其他系统的贮存器、管道、歧管或流体部件。如将理解的,微流体通道结构200可具有其他几何形状。例如,微流体通道结构可具有多于一个通道汇合点。例如,微流体通道结构可以具有2、3、4或5个通道区段,每个通道区段携带在通道汇合点处相遇的珠粒。可以通过一个或多个流体流动单元引导流体沿着一个或多个通道或贮存器流动。流体流动单元可包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等以控制流体的流动。还可以或以其他方式通过施加的压力差、离心力、电动泵送、真空、毛细管或重力流等来控制流体。
珠粒可以是多孔的、无孔的、固体的、半固体的、半流体的、流体的和/或其组合。在一些情况下,珠粒可以是可溶解的、可破坏的和/或可降解的。在一些情况下,珠粒可以是不可降解的。在一些情况下,珠粒可以是凝胶珠粒。凝胶珠粒可以是水凝胶珠粒。凝胶珠粒可以由分子前体形成,例如聚合物或单体物质。半固体珠粒可以是脂质体珠粒。固体珠粒可包含金属,包括氧化铁、金和银。在一些情况下,珠粒可以是二氧化硅珠粒。在一些情况下,珠粒可以是刚性的。在其他情况下,珠粒可以是柔性的和/或可压缩的。
珠粒可具有任何合适的形状。珠粒形状的实例包括但不限于球形、非球形、椭圆形、长圆形、无定形、圆形、圆柱形及其变型形式。
珠粒可具有均匀尺寸或不均匀尺寸。在一些情况下,珠粒的直径可以是至少约10纳米(nm)、100nm、500nm、1微米(μm)、5μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm、100μm、250μm、500μm、1mm或更大。在一些情况下,珠粒的直径可小于约10nm、100nm、500nm、1μm、5μm、10μm、20μm、30μm、40μm、50μm、60μm、70μm、80μm、90μm、100μm、250μm、500μm、1mm或更小。在一些情况下,珠粒的直径可以在约40-75μm、30-75μm、20-75μm、40-85μm、40-95μm、20-100μm、10-100μm、1-100μm、20-250μm、或20-500μm的范围内。
在某些方面中,珠粒可以以具有相对单分散尺寸分布的珠粒群体或多个珠粒提供。在需要在分配区内提供相对一致量的试剂的情况下,保持相对一致的珠粒特征(如尺寸)可有助于总体一致性。特别地,本文所述的珠粒可具有其横截面尺寸的变异系数小于50%、小于40%、小于30%、小于20%,并且在一些情况下小于15%、小于10%、小于5%或更小的尺寸分布。
珠粒可包含天然和/或合成材料。例如,珠粒可包含天然聚合物、合成聚合物或天然和合成聚合物。天然聚合物的实例包括蛋白质和糖,例如脱氧核糖核酸、橡胶、纤维素、淀粉(例如,直链淀粉、支链淀粉)、蛋白质、酶、多糖、丝、聚羟基链烷酸酯、壳聚糖、葡聚糖、胶原、角叉菜胶、卵叶车前子、阿拉伯胶、琼脂、明胶、虫胶、梧桐树胶、黄原胶、玉米糖胶、瓜尔胶、刺梧桐树胶、琼脂糖、海藻酸、藻酸盐或其天然聚合物。合成聚合物的实例包括丙烯酸类、尼龙、硅氧烷、氨纶、粘胶人造丝、多元羧酸、聚乙酸乙烯酯、聚丙烯酰胺、聚丙烯酸酯、聚乙二醇、聚氨酯、聚乳酸、二氧化硅、聚苯乙烯、聚丙烯腈、聚丁二烯、聚碳酸酯、聚乙烯、聚对苯二甲酸乙二醇酯、聚(三氟氯乙烯)、聚(环氧乙烷)、聚(对苯二甲酸乙二醇酯)、聚乙烯、聚异丁烯、聚(甲基丙烯酸甲酯)、聚(甲醛)、聚甲醛、聚丙烯、聚苯乙烯、聚(四氟乙烯)、聚(乙酸乙烯酯)、聚(乙烯醇)、聚(氯乙烯)、聚(偏二氯乙烯)、聚(偏二氟乙烯)、聚(氟乙烯)和/或其组合(例如,共聚物)。珠粒也可以由除聚合物之外的材料形成,包括脂质、胶束、陶瓷、玻璃陶瓷、材料复合物、金属、其他无机材料等。
在一些情况下,珠粒可含有分子前体(例如,单体或聚合物),其可通过分子前体的聚合形成聚合物网络。在一些情况下,前体可以是已经聚合的物质,其能够通过例如化学交联进行进一步聚合。在一些情况下,前体可包含丙烯酰胺或甲基丙烯酰胺单体、低聚物或聚合物中的一种或多种。在一些情况下,珠粒可包含预聚物,其是能够进一步聚合的低聚物。例如,可以使用预聚物制备聚氨酯珠粒。在一些情况下,珠粒可含有可进一步聚合在一起的单个聚合物。在一些情况下,可以通过不同前体的聚合生成珠粒,使得它们包含混合聚合物、共聚物和/或嵌段共聚物。在一些情况下,珠粒可在聚合物前体(例如,单体、低聚物、线性聚合物)、核酸分子(例如,寡核苷酸)、引物和其他实体之间包含共价键或离子键。在一些情况下,共价键可以是碳-碳键、硫醚键或碳-杂原子键。
交联可以是永久的或可逆的,这取决于所用的特定交联剂。可逆交联可允许聚合物在适当条件下线性化或解离。在一些情况下,可逆交联还可以允许结合至珠粒表面的材料的可逆附接。在一些情况下,交联剂可形成二硫键。在一些情况下,形成二硫键的化学交联剂可以是胱胺或改性胱胺。
在一些情况下,二硫键可以在掺入珠粒的分子前体单元(例如,单体、低聚物或线性聚合物)或前体与核酸分子(例如,寡核苷酸)之间形成。例如,胱胺(包括改性胱胺)是包含二硫键的有机试剂,其可以用作珠粒的单个单体或聚合物前体之间的交联剂。聚丙烯酰胺可以在胱胺或包含胱胺的物质(例如,改性胱胺)的存在下聚合,以生成包含二硫键的聚丙烯酰胺凝胶珠粒(例如,包含可化学还原交联剂的可化学降解珠粒)。二硫键可以使珠粒在珠粒暴露于还原剂后被降解(或溶解)。
在一些情况下,壳聚糖(线性多糖聚合物)可以通过亲水链与戊二醛交联以形成珠粒。壳聚糖聚合物的交联可以通过由热、压力、ph变化和/或辐射引发的化学反应来实现。
在一些情况下,珠粒可包含acrydite部分,其在某些方面可用于将一个或多个核酸分子(例如,条形码序列、条形码化核酸分子、条形码化寡核苷酸、引物或其他寡核苷酸)附接于珠粒。在一些情况下,丙烯酰胺亚磷酰胺部分可以指由丙烯酰胺亚磷酰胺与一种或多种物质反应例如丙烯酰胺亚磷酰胺与其他单体和交联剂在聚合反应期间的反应所生成的丙烯酰胺亚磷酰胺类似物。可以修饰acrydite部分以与待附接的物质形成化学键,例如核酸分子(例如条形码序列、条形码化核酸分子、条形码化寡核苷酸、引物或其他寡核苷酸)。丙烯酰胺亚磷酰胺部分可以用能够形成二硫键的硫醇基团修饰,或者可以用已经包含二硫键的基团修饰。硫醇或二硫化物(通过二硫化物交换)可以用作待附接的物质的锚点,或者丙烯酰胺亚磷酰胺部分的另一部分可以用于附接。在一些情况下,附接可以是可逆的,使得当二硫键断裂时(例如,在还原剂存在下),附接的物质从珠粒中释放出来。在其他情况下,acrydite部分可包含可用于附接的反应性羟基。
用于附接核酸分子(例如,寡核苷酸)的珠粒的官能化可以通过多种不同方法实现,包括活化聚合物内的化学基团、将活性或可活化的官能团掺入聚合物结构中或者在珠粒生产中的预聚物或单体阶段进行附接。
例如,聚合形成珠粒的前体(例如,单体,交联剂)可包含丙烯酰胺亚磷酰胺部分,使得当生成珠粒时,珠粒还包含丙烯酰胺亚磷酰胺部分。所述acrydite部分可以附接于核酸分子(例如,寡核苷酸),其可以包括引发序列(例如,用于扩增靶核酸的引物、随机引物、用于信使rna的引物序列)和/或一个或多个条形码序列。一个或多个条形码序列可包括对于与给定珠粒偶合的所有核酸分子相同的序列和/或对于与给定珠粒偶合的所有核酸分子不同的序列。核酸分子可被掺入珠粒中。
在一些情况下,核酸分子可以包含例如用于附接于测序流动池的功能序列,例如用于
图8示出携带条形码的珠粒的实例。核酸分子802(如寡核苷酸)可以通过可释放键806(例如二硫化物接头)与珠粒804偶合。相同的珠粒804可偶合(例如,经由可释放键)至一个或多个其他核酸分子818、820。核酸分子802可以是或包含条形码。如本文其他地方所述,条形码的结构可包含多个序列元件。核酸分子802可包含可用于后续处理的功能序列808。例如,功能序列808可包括测序仪特异性流动池附接序列(例如,用于
核酸分子802可包含唯一分子标识序列816(例如,唯一分子标识符(umi))。在一些情况下,唯一分子标识序列816可包含约5至约8个核苷酸。可替代地,唯一分子标识序列816可包含少于约5个或多于约8个核苷酸。唯一分子标识序列816可以是在偶合于单个珠粒(例如,珠粒804)的各个核酸分子(例如,802、818、820等)之间变化的唯一序列。在一些情况下,唯一分子标识序列816可以是随机序列(例如,随机n聚体序列)。例如,umi可提供被捕获的起始mrna分子的唯一标识符,以便允许原始表达的rna数量的定量。如将认识到的,虽然图8示出与珠粒804的表面偶合的三个核酸分子802、818、820,但是单个珠粒可偶合于任何数量的单个核酸分子,例如一个至数万至数十万个或甚至上百万个单个核酸分子。单个核酸分子的相应条形码可以包含共有序列区段或相对共有序列区段(例如,808、810、812等)和偶合于相同珠粒的不同的单个核酸分子之间的可变或唯一序列区段(例如,816)。
在操作中,生物颗粒(例如,细胞、dna、rna等)可以与携带条形码的珠粒804共分配。条形码化核酸分子802、818、820可以从珠粒804释放到分配区中。举例来说,在分析样品rna的上下文中,所释放的核酸分子中的一个(例如,802)的poly-t区段(例如,812)可以与mrna分子的poly-a尾杂交。逆转录可产生mrna的cdna转录物,但是所述转录物包括核酸分子802的序列区段808、810、816中的每一个。因为核酸分子802包含锚定序列814,所以它更可能与mrna的poly-a尾的序列末端杂交并在该处引发逆转录。在任何给定的分配区内,单个mrna分子的所有cdna转录物可包括共有条形码序列区段810。然而,由给定分配区内的不同mrna分子制成的转录物可在唯一分子标识序列812区段(例如,umi区段)上变化。有利地,即使在给定分配区的内容物的任何后续扩增之后,不同umi的数量也可以指示源自给定分配区并因此源自生物颗粒(例如,细胞)的mrna的量。如上所述,可以对转录物进行扩增、净化和测序,以鉴定mrna的cdna转录物的序列,并且对条形码区段和umi区段进行测序。尽管描述了poly-t引物序列,但其他靶向或随机引发序列也可用于引发逆转录反应。同样,尽管描述为将条形码化寡核苷酸释放到分配区中,但是在一些情况下,与珠粒(例如,凝胶珠粒)结合的核酸分子可用于杂交和捕获珠粒固相上的mrna,例如,以便促进rna与其他细胞内容物的分离。
在一些情况下,包含具有反应性或能够被活化以使得变得具有反应性的官能团的前体可以与其他前体聚合以产生包含活化或可活化官能团的凝胶珠粒。然后官能团可用于将另外的物质(例如,二硫化物接头、引物、其他寡核苷酸等)附接于凝胶珠粒。例如,包含羧酸(cooh)基团的一些前体可与其他前体共聚合以形成也包含cooh官能团的凝胶珠粒。在一些情况下,丙烯酸(包含游离cooh基团的物质)、丙烯酰胺和双(丙烯酰基)胱胺可以共聚合在一起以生成包含游离cooh基团的凝胶珠粒。可以将凝胶珠粒的cooh基团活化(例如,通过1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(edc)和n-羟基琥珀酰亚胺(nhs)或4-(4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉氯化物(dmtmm))使得它们具有反应性(例如,具有与胺官能团的反应性,其中edc/nhs或dmtmm用于活化)。然后,活化的cooh基团可以与适当的物质(例如,包含胺官能团的物质,其中羧酸基团被活化以具有与胺官能团的反应性)反应,所述物质包含与珠粒连接的部分。
在聚合物网络中包含二硫键的珠粒可以通过将一些二硫键还原成游离硫醇来用另外的物质官能化。二硫键可以通过例如还原剂(例如dtt,tcep等)的作用被还原,以生成游离硫醇基团,而不会溶解珠粒。然后,珠粒的游离硫醇可以与物质的游离硫醇或包含另一个二硫键的物质(例如,通过硫醇-二硫化物交换)反应,使得物质可以与珠粒连接(例如,通过生成的二硫键)。在一些情况下,珠粒的游离硫醇可与任何其他合适的基团反应。例如,珠粒的游离硫醇可与包含丙烯酰胺亚磷酰胺部分的物质反应。珠粒的游离硫醇基团可通过迈克尔加成化学与丙烯酰胺亚磷酰胺反应,使得包含丙烯酰胺亚磷酰胺的物质与珠粒连接。在一些情况下,可以通过包含硫醇加帽剂如n-乙基马来酰胺或碘乙酸酯来防止不受控制的反应。
可以控制珠粒内二硫键的活化,使得仅少量二硫键被活化。例如,可以通过控制用于生成游离硫醇基团的还原剂的浓度和/或用于在珠粒聚合中形成二硫键的试剂的浓度来进行控制。在一些情况下,低浓度(例如,还原剂分子:凝胶珠粒比率小于或等于约1:100,000,000,000、小于或等于约1:10,000,000,000、小于或等于约1:1,000,000,000、小于或等于约1:100,000,000、小于或等于约1:10,000,000、小于或等于约1:1,000,000、小于或等于约1:100,000、小于或等于约1:10,000)还原剂可用于还原。控制还原成游离硫醇的二硫键的数量可用于确保官能化期间的珠粒结构完整性。在一些情况下,光学活性剂(例如荧光染料)可以通过珠粒的游离硫醇基团与珠粒偶合,并用于定量珠粒中存在的游离硫醇的数量和/或追踪珠粒。
在一些情况下,在凝胶珠粒形成之后向凝胶珠粒中添加各部分可能是有利的。例如,在凝胶珠粒形成之后添加寡核苷酸(例如,条形码化寡核苷酸)可以避免在聚合期间可能发生的链转移终止期间物质的损失。此外,较小的前体(例如,不包含侧链基团和连接部分的单体或交联剂)可以用于聚合,并且由于粘性效应而可以最小程度地阻碍链末端生长。在一些情况下,在凝胶珠粒合成之后的官能化可以在潜在的破坏剂(例如,自由基)和/或化学环境的情况下使待负载的物质(例如,寡核苷酸)的暴露最小化。在一些情况下,所生成的凝胶可具有上限临界溶液温度(ucst),其可允许温度驱动的珠粒溶胀和塌陷。在随后用寡核苷酸官能化珠粒期间,这种官能团可有助于寡核苷酸(例如,引物)渗入珠粒中。产生后官能化也可用于控制珠粒中物质的负载比率,使得例如负载比率的可变性最小化。物质负载也可以在分批过程中进行,使得多个珠粒可以在单批次中用物质官能化。
注射或以其他方式引入到分配区中的珠粒可包括可释放、可裂解或可逆附接的条形码。注射或以其他方式引入到分配区中的珠粒可包括可活化的条形码。注射或以其他方式引入到分配区中的珠粒可以是可降解的、可破坏的或可溶解的珠粒。
条形码可以可释放地、可裂解地或可逆地附接到珠粒,使得条形码可以通过裂解条形码分子与珠粒之间的连接而释放或为可释放的,或者通过下面的珠粒自身的降解释放,从而允许条形码被其他试剂接近或可被其他试剂接近,或两者兼而有之。在非限制性实例中,可以通过还原二硫键、使用限制酶、光活化裂解或通过其他类型的刺激(例如,化学、热、ph、酶等)和/或反应进行裂解来实现,例如本文其他地方所述。可释放条形码有时可被称为可活化的,因为它们一旦释放就可用于反应。因此,例如,可通过从珠粒(或本文所述的其他合适类型的分配区)释放条形码来活化可活化的条形码。在所描述的方法和系统的上下文中还设想了其他可活化配置。
除了珠粒与缔合分子(例如含有条形码的核酸分子(例如条形码化寡核苷酸))之间的可裂解键之外或作为其替代,珠粒可以在自发地或在暴露于一种或多种刺激(例如,温度变化、ph变化、暴露于特定化学物质或相、暴露于光、还原剂等)后为可降解、可破坏或可溶解的。在一些情况下,珠粒可以是可溶解的,使得珠粒的材料组分在暴露于特定化学物质或环境变化(例如变化温度或ph变化)时溶解。在一些情况下,凝胶珠粒可以在升高的温度和/或碱性条件下降解或溶解。在一些情况下,珠粒可以是可热降解的,使得当珠粒暴露于适当的温度变化(例如,加热)时,珠粒降解。与物质(例如,核酸分子,例如条形码化寡核苷酸)结合的珠粒的降解或溶解可导致物质从珠粒中释放。
从以上公开内容可以理解,珠粒的降解可以指在使物理珠粒本身的结构发生和不发生降解的情况下结合或夹带的物质从珠粒中解离。例如,珠粒的降解可以涉及通过本文其他地方描述的一种或多种物质和/或方法裂解可裂解键。在另一个实例中,可以通过例如由改变化学环境引起的渗透压差从珠粒中释放夹带的物质。举例来说,由渗透压差引起的珠粒孔径的改变通常可以在珠粒本身的结构没有降解的情况下发生。在一些情况下,由珠粒的渗透溶胀引起的孔径增加可以允许珠粒内的夹带物质的释放。在其他情况下,由于孔径收缩,珠粒的渗透收缩可能使珠粒更好地保留夹带物质。
可以将可降解的珠粒引入到分配区(例如乳液中的液滴或孔)中,使得珠粒在分配区内降解,并且当施加适当的刺激时,任何缔合的物质(例如,寡核苷酸)在液滴内释放。游离物质(例如,寡核苷酸、核酸分子)可以与分配区中包含的其他试剂相互作用。例如,包含胱胺并通过二硫键与条形码序列连接的聚丙烯酰胺珠粒可以与油包水乳液的液滴中的还原剂组合。在液滴内,还原剂可以破坏各种二硫键,导致珠粒降解并将条形码序列释放到液滴的含水内部环境中。在另一个实例中,加热在碱性溶液中包含结合珠粒的条形码序列的液滴也可导致珠粒降解并将附接的条形码序列释放到液滴的含水内部环境中。
任何合适数量的分子标签分子(例如,引物、条形码化寡核苷酸)可以与珠粒缔合,使得在从珠粒中释放后,分子标签分子(例如,引物,例如,条形码化寡核苷酸)以预先定义的浓度存在于分配区中。可以选择这种预定义浓度以促进用于在分配区内生成测序文库的某些反应(例如扩增)。在一些情况下,引物的预先定义的浓度可以通过产生携带核酸分子(例如,寡核苷酸)的珠粒的过程来限制。
在一些情况下,珠粒可以非共价地负载有一种或多种试剂。珠粒可以通过例如使珠粒经受足以使珠粒溶胀的条件,使试剂有足够的时间扩散到珠粒的内部,并使珠粒经受足以使珠粒去溶胀的条件来非共价负载。例如,可以通过将珠粒置于热力学上有利的溶剂中,使珠粒经受较高或较低的温度,使珠粒经受较高或较低的离子浓度,和/或使珠粒经受电场来实现珠粒的溶胀。珠粒的溶胀可以通过各种溶胀方法来实现。珠粒的去溶胀可以通过例如将珠粒转移到热力学上不利的溶剂中,使珠粒经受较低或较高温度,使珠粒经受较低或较高的离子浓度,和/或除去电场来实现。珠粒的去溶胀可以通过各种去溶胀方法来实现。转移珠粒可能导致珠粒中的孔收缩。然后收缩可能阻碍珠粒内的试剂从珠粒的内部扩散出来。阻碍可能是由于试剂与珠粒内部之间的空间相互作用。转移可以以微流体方式完成。例如,转移可以通过将珠粒从一种共流动的溶剂流移动到不同的共流动的溶剂流中来实现。珠粒的溶胀性和/或孔径可通过改变珠粒的聚合物组成来调节。
在一些情况下,与前体连接的acrydite部分、与前体连接的另一种物质或前体本身可包含不稳定键,例如化学、热或光敏感键,例如二硫键、uv敏感键等。一旦丙烯酰胺亚磷酰胺部分或包含不稳定键的其他部分被掺入珠粒中,珠粒也可包含不稳定键。例如,不稳定键可用于将物质(例如,条形码、引物等)可逆地连接(例如,共价连接)到珠粒。在一些情况下,例如,在寡核苷酸与附接于珠粒的互补序列杂交时,热不稳定键可包括基于核酸杂交的附接,使得杂合体的热解链将寡核苷酸(例如含有条形码的序列)从珠粒或微胶囊释放。
向凝胶珠粒中添加多种类型的不稳定键可导致生成能够对不同刺激有反应的珠粒。每种类型的不稳定键可能对相关联的刺激(例如,化学刺激、光、温度、酶等)敏感,使得通过每个不稳定键附接到珠粒上的物质的释放可以通过施加适当的刺激来控制。这种官能团可用于从凝胶珠粒受控地释放物质。在一些情况下,包含不稳定键的另一物质可以在凝胶珠粒形成之后通过例如如上所述的凝胶珠粒的活化官能团与凝胶珠粒连接。如应当理解的,可释放地、可裂解地或可逆地附接到本文所述的珠粒的条形码包括通过条形码分子与珠粒之间的键联的裂解来释放或可释放的条形码,或通过下面的珠粒本身的降解来释放的条形码,允许条形码被其他试剂接近或可被其他试剂接近,或两者兼而有之。
如本文所述可释放的条形码有时可被称为可活化的,因为它们一旦释放就可用于反应。因此,例如,可通过从珠粒(或本文所述的其他合适类型的分配区)释放条形码来活化可活化的条形码。在所描述的方法和系统的上下文中还设想了其他可活化配置。
除了可热裂解的键、二硫键和uv敏感键之外,可以与前体或珠粒偶合的不稳定键的其他非限制性实例包括酯键(例如,可用酸、碱或羟胺裂解)、邻位二醇键(例如,可通过高碘酸钠裂解)、狄尔斯-阿尔德(diels-alder)键(例如,可通过热裂解)、砜键(例如,可通过碱裂解)、甲硅烷基醚键(例如,可通过酸裂解)、糖苷键(例如,可通过淀粉酶裂解)、肽键(例如,可通过蛋白酶裂解)或磷酸二酯键(例如,可通过核酸酶(例如,dna酶)裂解))。键可以通过其他核酸分子靶向酶裂解,例如限制酶(例如限制性内切核酸酶),如下文进一步描述的。
在珠粒产生期间(例如,在前体聚合期间),可以将物质包封在珠粒中。此类物质可能参与或可能不参与聚合。此类物质可以进入聚合反应混合物中,使得生成的珠粒在珠粒形成后包含各物质。在一些情况下,可在形成之后将此类物质加入凝胶珠粒中。此类物质可包括,例如,核酸分子(例如,寡核苷酸)、用于核酸扩增反应的试剂(例如,引物、聚合酶、dntp、辅因子(例如,离子辅因子)、缓冲液)包括文中所述的那些、用于酶促反应的试剂(例如,酶、辅因子、底物、缓冲液)、用于核酸修饰反应的试剂(例如聚合、连接或消化)和/或用于一种或多种测序平台的模板制备(例如,标记)的试剂(例如,用于
可降解珠粒可包含一种或多种具有不稳定键的物质,使得当珠粒/物质暴露于适当的刺激时,键断裂并且珠粒降解。不稳定键可以是化学键(例如,共价键、离子键)或可以是另一种类型的物理相互作用(例如,范德华相互作用、偶极-偶极相互作用等)。在一些情况下,用于产生珠粒的交联剂可包含不稳定键。在暴露于适当的条件后,不稳定键可以断裂并且珠粒降解。例如,当将包含胱胺交联剂的聚丙烯酰胺凝胶珠粒暴露于还原剂后,胱胺的二硫键可以断裂并且珠粒降解。
与不降解的珠粒相比,当将适当的刺激施加到珠粒上时,可降解的珠粒可用于更快地从珠粒释放附接的物质(例如,核酸分子、条形码序列、引物等)。例如,对于与多孔珠粒的内表面结合的物质或在包封物质的情况下,该物质在珠粒降解后可具有较大迁移率并且可被溶液中的其他物质接近。在一些情况下,物质也可以通过可降解的接头(例如,二硫化物接头)附接于可降解的珠粒。可降解的接头可以对与可降解珠粒相同的刺激有反应,或者两种可降解物质可以对不同的刺激有反应。例如,条形码序列可以通过二硫键附接到包含胱胺的聚丙烯酰胺珠粒上。在条形码化珠粒暴露于还原剂后,珠粒降解并且条形码序列在条形码序列与珠粒之间的二硫键断裂以及珠粒中胱胺的二硫键断裂后释放。
从以上公开内容可以理解,虽然被称为珠粒的降解,但在如上所述的许多情况下,所述降解可以指在使物理珠粒本身的结构发生和不发生降解的情况下结合或夹带的物质从珠粒中解离。例如,可以通过例如由改变化学环境引起的渗透压差从珠粒中释放夹带的物质。举例来说,由渗透压差引起的珠粒孔径的改变通常可以在珠粒本身的结构没有降解的情况下发生。在一些情况下,由珠粒的渗透溶胀引起的孔径增加可以允许珠粒内的夹带物质的释放。在其他情况下,由于孔径收缩,珠粒的渗透收缩可能使珠粒更好地保留夹带物质。
在提供可降解珠粒的情况下,避免将此类珠粒在给定时间之前暴露于引起这种降解的一个或多个刺激可能是有益的,以便例如避免过早的珠粒降解和由这种降解引起的问题,包括例如不良的流动特性和聚集。举例来说,在珠粒包含可还原的交联基团例如二硫化物基团的情况下,希望避免使此类珠粒与还原剂例如dtt或其他二硫化物裂解试剂接触。在此类情况下,对本文所述珠粒的处理将在一些情况下不提供还原剂,例如dtt。因为还原剂通常在商业酶制剂中提供,所以可能需要在处理本文所述的珠粒时提供不含还原剂(或不含dtt)的酶制剂。此类酶的实例包括例如聚合酶制剂、逆转录酶制剂、连接酶制剂、以及可用于处理本文所述珠粒的许多其他酶制剂。术语“不含还原剂”或“不含dtt”的制剂可以指对于用于降解这些珠粒的此类材料而言具有小于约1/10、小于约1/50、或甚至小于约1/100的较低范围的制剂。例如,对于dtt,不含还原剂的制剂可具有小于约0.01毫摩尔(mm)、0.005mm、0.001mmdtt、0.0005mmdtt、或甚至小于约0.0001mmdtt。在许多情况下,dtt的量可能无法检测到。
可以使用许多化学触发剂来触发珠粒的降解。这些化学变化的实例可包括但不限于ph介导的珠粒内组分完整性的改变、通过交联键的裂解的珠粒组分的降解以及珠粒组分的解聚。
在一些实施方案中,珠粒可以由包含可降解的化学交联剂(例如bac或胱胺)的材料形成。此类可降解交联剂的降解可通过许多机制完成。在一些实例中,可以将珠粒与化学降解剂接触,所述化学降解剂可以诱导氧化、还原或其他化学变化。例如,化学降解剂可以是还原剂,例如二硫苏糖醇(dtt)。还原剂的其他实例可包括β-巯基乙醇、(2s)-2-氨基-1,4-二巯基丁烷(二硫代丁胺或dtba)、三(2-羧乙基)膦(tcep)或其组合。还原剂可降解在形成珠粒的凝胶前体之间形成的二硫键,并且因此降解珠粒。在其他情况下,溶液的ph变化(例如ph增加)可触发珠粒的降解。在其他情况下,暴露于水溶液(例如水)可触发水解降解,并且因此触发珠粒的降解。在一些情况下,刺激的任何组合可触发珠粒的降解。例如,ph的变化可使得化学试剂(例如,dtt)变成有效的还原剂。
在施加热刺激后,还可以诱导珠粒释放其内容物。温度的变化可导致珠粒的各种变化。例如,热可导致固体珠粒液化。热的变化可导致珠粒的熔化,使得珠粒的一部分降解。在其他情况下,热可增加珠粒组分的内压,使得珠粒破裂或爆炸。热还可以作用于用作构建珠粒的材料的热敏聚合物。
任何合适的试剂可使珠粒降解。在一些实施方案中,温度或ph的变化可用于降解珠粒内的热敏性或ph敏感性键。在一些实施方案中,化学降解剂可用于通过氧化、还原或其他化学变化降解珠粒内的化学键。例如,化学降解剂可以是还原剂,例如dtt,其中dtt可以降解在交联剂与凝胶前体之间形成的二硫键,因此降解珠粒。在一些实施方案中,可以添加还原剂以使珠粒降解,所述还原剂可以使珠粒释放或不释放其内容物。还原剂的实例可包括二硫苏糖醇(dtt)、β-巯基乙醇、(2s)-2-氨基-1,4-二巯基丁烷(二硫代丁胺或dtba)、三(2-羧乙基)膦(tcep)或其组合。还原剂可以以约0.1mm、0.5mm、1mm、5mm、10mm的浓度存在。还原剂可以以至少约0.1mm、0.5mm、1mm、5mm、10mm或大于10mm的浓度存在。还原剂可以以至多约10mm、5mm、1mm、0.5mm、0.1mm或更低的浓度存在。
任何合适数量的分子标签分子(例如,引物、条形码化寡核苷酸)可以与珠粒缔合,使得在从珠粒中释放后,分子标签分子(例如,引物,例如,条形码化寡核苷酸)以预先定义的浓度存在于分配区中。可以选择这种预定义浓度以促进用于在分配区内生成测序文库的某些反应(例如扩增)。在一些情况下,引物的预先定义的浓度可以通过产生携带寡核苷酸的珠粒的过程来限制。
尽管以上已经就提供基本上单独占据的分配区描述了图1和图2,但在某些情况下,可能希望提供例如包含两个、三个、四个或更多个细胞的多占分配区和/或在单个分配区内包括条形码化核酸分子(例如,寡核苷酸)的微胶囊(例如珠粒)。因此,如上所述,可以控制含有生物颗粒和/或珠粒的流体和分配流体的流动特性,以提供这种多占分配区。特别地,可以控制流动参数以提供大于约50%、大于约75%、并且在一些情况下大于约80%、90%、95%或更高的分配区的给定占据率。
在一些情况下,可以使用另外的微胶囊以将额外的试剂递送到分配区。在这种情况下,从不同的珠粒源(例如,包含不同的缔合试剂)通过不同的通道入口进入公共通道或液滴产生汇合点(例如,汇合点210)将不同的珠粒引入这样的公共通道或液滴产生汇合点可能是有利的。在此类情况下,可以控制不同珠粒进入通道或汇合点的流动和频率,以提供来自每个源的一定比率的微胶囊,同时确保到分配区中的此类珠粒与给定数量的生物颗粒的给定配对或组合(例如,每个分配区一个生物颗粒和一个珠粒)。
本文所述的分配区可包括小体积,例如,小于约10微升(μl)、5μl、1μl、900皮升(pl)、800pl、700pl、600pl、500pl、400pl、300pl、200pl、100pl、50pl、20pl、10pl、1pl、500纳升(nl)、100nl、50nl或更低。
例如,在基于液滴的分配区的情况下,液滴可具有小于约1000pl、900pl、800pl、700pl、600pl、500pl、400pl、300pl、200pl、100pl、50pl、20pl、10pl、1pl或更少的总体积。在与微胶囊共分配的情况下,应当理解,分配区内的样品流体体积(例如包括共分配的生物颗粒和/或珠粒)可小于上述体积的约90%、小于约80%、小于约70%、小于约60%、小于约50%、小于约40%、小于约30%、小于约20%、或小于上述体积的约10%。
如本文其他地方所述,将物质分配可产生分配区群或多个分配区。在此类情况下,可以产生或以其他方式提供任何合适数量的分配区。例如,可以产生或以其他方式提供至少约1,000个分配区、至少约5,000个分配区、至少约10,000个分配区、至少约50,000个分配区、至少约100,000个分配区、至少约500,000个分配区、至少约1,000,000个分配区、至少约5,000,000个分配区、至少约10,000,000个分配区、至少约50,000,000个分配区、至少约100,000,000个分配区、至少约500,000,000个分配区、至少约1,000,000,000个分配区或更多分配区。此外,多个分配区可以包括未占据的分配区(例如,空分配区)和占据的分配区。
试剂
根据某些方面,生物颗粒可以连同裂解试剂一起分配,以释放分配区内的生物颗粒的内容物。在此类情况下,裂解剂可以在将生物颗粒例如通过通道汇合点上游的另外通道或多个通道引入分配汇合点/液滴产生区(例如,汇合点210)的同时或就在其之前与生物颗粒悬浮液接触。根据其他方面,另外地或可替代地,生物颗粒可以连同其他试剂一起分配,如下面将进一步描述的。
图3示出用于共分配生物颗粒和试剂的微流体通道结构300的实例。通道结构300可包括通道区段301、302、304、306和308。通道区段301和302在第一通道汇合点309处连通。通道区段302、304、306和308在第二通道汇合点310处连通。
在示例性操作中,通道区段301可以将包括多个生物颗粒314的含水流体312沿着通道区段301输送到第二汇合点310中。作为替代或除此之外,通道区段301可以运输珠粒(例如,凝胶珠粒)。珠粒可包含条形码分子。
例如,通道区段301可以连接到包括生物颗粒314的含水悬浮液的贮存器。在第二汇合点310的上游和就在达到其之前,通道区段301可以在第一汇合点309处与通道区段302相遇。通道区段302可以将悬浮在含水流体312中的多个试剂315(例如,裂解剂)沿着通道区段302输送到第一汇合点309中。例如,通道区段302可以连接到包含试剂315的贮存器。在第一汇合点309之后,通道区段301中的含水流体312可以将生物颗粒314和试剂315携带到第二汇合点310。在一些情况下,通道区段301中的含水流体312可包括一种或多种试剂,所述一种或多种试剂可以是与试剂315相同或不同的试剂。与含水流体312不混溶的第二流体316(例如,油)可从通道区段304和306中的每一个递送到第二汇合点310。在来自通道区段301的含水流体312与来自通道区段304和306中的每一个的第二流体316在第二通道汇合点310处相遇后,含水流体312可以在第二流体316中以离散液滴318的形式被分配并且沿着通道区段308从第二汇合点310流出。通道区段308可以将离散液滴318递送到流体联接到通道区段308的出口贮存器,在所述贮存器中将它们加以收集。
第二流体316可包含油,例如氟化油,其包括用于稳定所得液滴(例如,抑制所得液滴318的后续聚结)的含氟表面活性剂。
产生的离散液滴可以包括单独的生物颗粒314和/或一种或多种试剂315。在一些情况下,产生的离散液滴可以包括携带条形码的珠粒(未示出),例如通过本文其他地方描述的其他微流体结构。在一些情况下,离散液滴可能未被占据(例如,没有试剂、没有生物颗粒)。
有利地,当裂解试剂和生物颗粒共分配时,裂解试剂可以促进分配区内生物颗粒的内容物的释放。分配区中释放的内容物可能保持与其他分配区的内容物离散。
如将理解的,本文描述的通道区段可以联接到多种不同流体源或接收部件中的任一个,包括其他系统的贮存器、管道、歧管或流体部件。如将理解的,微流体通道结构300可具有其他几何形状。例如,微流体通道结构可具有多于两个通道汇合点。例如,微流体通道结构可以具有2、3、4、5个或更多个通道区段,每个通道区段携带在通道汇合点处相遇的相同或不同类型的珠粒、试剂和/或生物颗粒。可以控制每个通道区段中的流体流动以控制不同元素到液滴中的分配。可以通过一个或多个流体流动单元引导流体沿着一个或多个通道或贮存器流动。流体流动单元可包括压缩机(例如,提供正压)、泵(例如,提供负压)、致动器等以控制流体的流动。还可以或以其他方式通过施加的压力差、离心力、电动泵送、真空、毛细管或重力流等来控制流体。
裂解剂的实例包括生物活性试剂,例如用于裂解不同细胞类型(例如革兰氏阳性或阴性细菌、植物、酵母、哺乳动物等)的裂解酶,例如溶菌酶、无色肽酶、溶葡球菌素、labiase、kitalase、溶细胞酶和可从例如sigma-aldrich公司(stlouis,mo)购得的各种其他裂解酶、以及其他可商购的裂解酶。其他裂解剂可以另外地或可替代地与生物颗粒共分配以引起生物颗粒内容物释放到分配区中。例如,在一些情况下,基于表面活性剂的裂解溶液可用于裂解细胞,但是这些可能不太适用于基于乳液的系统,在基于乳液的系统中表面活性剂可干扰稳定的乳液。在一些情况下,裂解溶液可包括非离子表面活性剂,例如像tritonx-100和tween20。在一些情况下,裂解溶液可包括离子表面活性剂,例如像十二烷基肌氨酸钠和十二烷基硫酸钠(sds)。在某些情况下,也可以使用电穿孔、热、声学或机械细胞破坏,例如,基于非乳液的分配区如生物颗粒的包封可以补充或代替液滴分配区,其中在细胞破坏后,包封物的任何孔径足够小以保留给定大小的核酸片段。
可替代地或除了与上述生物颗粒共分配的裂解剂之外,其他试剂也可以与生物颗粒共分配,包括例如dna酶和rna酶灭活剂或抑制剂(例如蛋白酶k)、螯合剂(例如edta)和用于去除或以其他方式降低不同细胞裂解物组分对核酸后续处理的负面活性或影响的其他试剂。另外,就包封的生物颗粒而言,可以将生物颗粒暴露于适当的刺激以从共分配的微胶囊中释放生物颗粒或其内容物。例如,在一些情况下,化学刺激可以连同包封的生物颗粒一起共分配,以允许微胶囊的降解和细胞或其内容物向更大的分配区中的释放。在一些情况下,所述刺激可以与本文其他地方描述的用于从其各自的微胶囊(例如珠粒)中释放核酸分子(例如,寡核苷酸)的刺激相同。在替代方面中,这可以是不同的且不重叠的刺激,以允许包封的生物颗粒在与核酸分子释放到相同分配区中不同的时间释放到分配区中。
另外的试剂也可以与生物颗粒共分配,例如片段化生物颗粒的dna的内切核酸酶、dna聚合酶和用于扩增生物颗粒的核酸片段并将条形码分子标签附接到扩增片段的dntp。其他酶可共分配,包括但不限于聚合酶、转座酶、连接酶、蛋白酶k、dna酶等。另外的试剂还可以包括逆转录酶,包括具有末端转移酶活性的酶、引物和寡核苷酸、以及可以用于模板转换的转换寡核苷酸(在本文中也称为“转换oligo”或“模板转换寡核苷酸”)。在一些情况下,模板转换可用于增加cdna的长度。在一些情况下,模板转换可用于将预定义的核酸序列附加到cdna。在模板转换的实例中,cdna可以从模板(例如细胞mrna)的逆转录产生,其中具有末端转移酶活性的逆转录酶可以以模板非依赖性方式向cdna添加另外的核苷酸,例如polyc。转换oligo可包括与另外的核苷酸(例如polyg)互补的序列。cdna上的另外核苷酸(例如polyc)可以与转换oligo上的另外核苷酸(例如polyg)杂交,由此转换oligo可以被逆转录酶用作模板以进一步延伸cdna。模板转换寡核苷酸可包含杂交区和模板区。杂交区可包含能够与靶杂交的任何序列。在一些情况下,如前所述,杂交区包含一系列g碱基以与cdna分子3'末端的突出c碱基互补。所述系列g碱基可包含1个g碱基、2个g碱基、3个g碱基、4个g碱基、5个g碱基或多于5个g碱基。模板序列可包含任何掺入cdna的序列。在一些情况下,模板区包含至少1个(例如,至少2、3、4、5个或更多个)标签序列和/或功能序列。转换oligo可包含脱氧核糖核酸;核糖核酸;修饰的核酸包括2-氨基嘌呤、2,6-二氨基嘌呤(2-氨基-da)、反向dt、5-甲基dc、2'-脱氧肌苷、supert(5-羟基丁炔-2'-脱氧尿苷)、superg(8-氮杂-7-脱氮鸟苷)、锁核酸(lna)、解锁核酸(una,例如una-a、una-u、una-c、una-g)、iso-dg、iso-dc、2'氟代碱基(例如,氟代c、氟代u、氟代a和氟代g)或任何组合。
在一些情况下,转换oligo的长度可为至少约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249或250个核苷酸或更长。
在一些情况下,转换oligo的长度可为至多约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79、80、81、82、83、84、85、86、87、88、89、90、91、92、93、94、95、96、97、98、99、100、101、102、103、104、105、106、107、108、109、110、111、112、113、114、115、116、117、118、119、120、121、122、123、124、125、126、127、128、129、130、131、132、133、134、135、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、153、154、155、156、157、158、159、160、161、162、163、164、165、166、167、168、169、170、171、172、173、174、175、176、177、178、179、180、181、182、183、184、185、186、187、188、189、190、191、192、193、194、195、196、197、198、199、200、201、202、203、204、205、206、207、208、209、210、211、212、213、214、215、216、217、218、219、220、221、222、223、224、225、226、227、228、229、230、231、232、233、234、235、236、237、238、239、240、241、242、243、244、245、246、247、248、249或250个核苷酸。
一旦细胞的内容物释放到它们各自的分配区中,其中包含的大分子组分(例如,生物颗粒的大分子成分,例如rna、dna或蛋白质)可以在分配区内进一步处理。根据本文所述的方法和系统,单个生物颗粒的大分子组分内容物可以具有唯一标识符,使得在表征那些大分子组分时,它们可以归属为来源于相同的一个或多个生物颗粒。通过将唯一标识符特定地分配给单独的生物颗粒或生物颗粒群组来提供将特征归属于单独的生物颗粒或生物颗粒群组的能力。唯一标识符(例如,以核酸条形码的形式)可以被指定或与各个生物颗粒或生物颗粒群组缔合,以便用唯一标识符对生物颗粒的大分子组分(并且导致其特征)加标签或进行标记。然后可以使用这些唯一标识符以将生物颗粒的组分和特征归属于单独的生物颗粒或生物颗粒群组。
在一些方面中,这通过将单个生物颗粒或生物颗粒群组与唯一标识符共分配来执行,例如如上所述(参见图2)。在一些方面中,唯一标识符以核酸分子(例如,寡核苷酸)的形式提供,所述核酸分子包含核酸条形码序列,所述核酸条形码序列可以附接于单独的生物颗粒的核酸内容物或以其他方式与单独的生物颗粒的核酸内容物缔合,或附接于生物颗粒的其他组分,特别是那些核酸的片段。核酸分子被分配,使得在给定分配区中的核酸分子之间,其中包含的核酸条形码序列是相同的,但是在不同分配区之间,核酸分子可以并且确实具有不同的条形码序列,或者至少表示在给定分析中所有分配区中的大量不同条形码序列。在一些方面中,只有一个核酸条形码序列可以与给定的分配区缔合,但是在一些情况下,可以存在两个或更多个不同的条形码序列。
核酸条形码序列可以在核酸分子(例如,寡核苷酸)的序列内包括约6至约20个或更多个核苷酸。核酸条形码序列可以包括约6至约20、30、40、50、60、70、80、90、100个或更多个核苷酸。在一些情况下,条形码序列的长度可以是约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更长。在一些情况下,条形码序列的长度可以是至少约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更长。在一些情况下,条形码序列的长度可以是至多约6、7、8、9、10、11、12、13、14、15、16、17、18、19、20个核苷酸或更短。这些核苷酸可以是完全连续的,即在相邻核苷酸的单个区段中,或者它们可以被分成两个或更多个由1个或多个核苷酸分开的单独子序列。在一些情况下,分开的条形码子序列的长度可为约4至约16个核苷酸。在一些情况下,条形码子序列可以是约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更长。在一些情况下,条形码子序列可以是至少约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更长。在一些情况下,条形码子序列可以是至多约4、5、6、7、8、9、10、11、12、13、14、15、16个核苷酸或更短。
共分配的核酸分子还可以包含可用于处理来自共分配的生物颗粒的核酸的其他功能序列。这些序列包括例如靶向或随机/通用扩增引物序列,其用于从分配区内的各个生物颗粒扩增基因组dna,同时附接缔合的条形码序列、测序引物或引物识别位点,杂交或探测序列,例如用于鉴定序列存在或用于下拉条形码化核酸,或许多其他潜在的功能序列中任一种。还可以使用共分配寡核苷酸的其他机制,包括例如两个或更多个液滴的聚结,其中一个液滴包含寡核苷酸,或寡核苷酸微分配到分配区中,例如微流体系统内的液滴。
在一个实例中,提供微胶囊(例如珠粒),其各自包括大量可释放地附接于珠粒的上述条形码化核酸分子(例如,条形码化寡核苷酸),其中附接于特定珠粒的所有核酸分子将包括相同的核酸条形码序列,但是在所使用的珠粒群体中表示大量不同的条形码序列。在一些实施方案中,水凝胶珠粒(例如包含聚丙烯酰胺聚合物基体)用作核酸分子进入分配区的固体支持物和递送载体,因为它们能够携带大量核酸分子,并且可以配置为在暴露于特定刺激后释放那些核酸分子,如本文其他地方所述。在一些情况下,珠粒群体提供各种条形码序列文库,其包括至少约1,000种不同的条形码序列、至少约5,000种不同的条形码序列、至少约10,000种不同的条形码序列、至少约50,000种不同的条形码序列、至少约100,000种不同的条形码序列、至少约1,000,000种不同的条形码序列、至少约5,000,000种不同的条形码序列或至少约10,000,000种不同的条形码序列或更多。另外,每个珠粒可以具有大量附接的核酸(例如寡核苷酸)分子。特别地,在单独的珠粒上包括条形码序列的核酸分子的分子数可以是至少约1,000个核酸分子、至少约5,000个核酸分子、至少约10,000个核酸分子、至少约50,000个核酸分子、至少约100,000个核酸分子、至少约500,000个核酸、至少约1,000,000个核酸分子、至少约5,000,000个核酸分子、至少约10,000,000个核酸分子、至少约50,000,000个核酸分子、至少约100,000,000个核酸分子、至少约250,000,000个核酸分子并且在一些情况下至少约10亿个核酸分子,或更多。给定珠粒的核酸分子可包括相同(或共有)条形码序列、不同条形码序列或两者的组合。给定珠粒的核酸分子可包括多个核酸分子集合。给定集合的核酸分子可包括相同的条形码序列。相同的条形码序列可以与另一集合的核酸分子的条形码序列不同。
此外,当分配珠粒群体时,所得到的分配区群体还可以包括各种条形码文库,其包括至少约1,000种不同的条形码序列、至少约5,000种不同的条形码序列、至少约10,000种不同的条形码序列、至少约50,000种不同的条形码序列、至少约100,000种不同的条形码序列、至少约1,000,000种不同的条形码序列、至少约5,000,000种不同的条形码序列、或至少约10,000,000种不同的条形码序列。另外,群体的每个分配区可以包括至少约1,000个核酸分子、至少约5,000个核酸分子、至少约10,000个核酸分子、至少约50,000个核酸分子、至少约100,000个核酸分子、至少约500,000个核酸、至少约1,000,000个核酸分子、至少约5,000,000个核酸分子、至少约10,000,000个核酸分子、至少约50,000,000个核酸分子、至少约100,000,000个核酸分子、至少约250,000,000个核酸分子并且在一些情况下至少约10亿个核酸分子。
在一些情况下,可能希望将多个不同的条形码掺入给定分配区内,或附接至分配区内的单个或多个珠粒。例如,在一些情况下,混合但已知的条形码序列集合可以在后续处理中提供更大的识别保证,例如,通过向给定分配区提供更强的地址或条形码属性,作为从给定分配区输出的重复或独立确认。
核酸分子(例如,寡核苷酸)在对珠粒施加特定刺激后可从珠粒中释放。在一些情况下,刺激可以是光刺激,例如通过裂解光不稳定键以释放核酸分子。在其他情况下,可以使用热刺激,其中珠粒环境的温度升高将导致键裂解或核酸分子从珠粒中的其他释放。在其他情况下,可以使用化学刺激,其裂解核酸分子与珠粒的键,或者以其他方式导致核酸分子从珠粒中释放。在一种情况下,此类组合物包括上述用于包封生物颗粒的聚丙烯酰胺基体,并且可以通过暴露于还原剂如dtt而降解以释放附接的核酸分子。
在一些方面中,提供了用于受控分配的系统和方法。可以通过调节通道架构(例如,微流体通道架构)中的某些几何特征来控制液滴尺寸。例如,可以调节通道的扩张角、宽度和/或长度来控制液滴尺寸。
图4示出用于将珠粒受控地分配到离散液滴中的微流体通道结构的实例。通道结构400可包括在通道汇合点406(或交叉点)处与贮存器404连通的通道区段402。贮存器404可以是腔室。如本文所用,对“贮存器”的任何提及也可以指“腔室”。在操作中,包括悬浮珠粒412的含水流体408可以沿着通道区段402输送到汇合点406处以相遇与贮存器404中含水流体408不混溶的第二流体410,以产生流入贮存器404的含水流体408的液滴416、418。在含水流体408和第二流体410相遇的汇合点406处,可以基于各种因素形成液滴,如在汇合点406处的流体动力,两种流体408、410的流速,流体特性以及通道结构400的某些几何参数(例如,w、h0、α等)。多个液滴通过连续地从通道区段402注入含水流体408通过汇合点406而收集在贮存器404中。
产生的离散液滴可包括珠粒(例如,如在占据的液滴416中)。可替代地,产生的离散液滴可包括多于一个珠粒。可替代地,产生的离散液滴可以不包括任何珠粒(例如,如在未占据的液滴418中)。在一些情况下,产生的离散液滴可含有一个或多个生物颗粒,如本文其他地方所述。在一些情况下,产生的离散液滴可包含一种或多种试剂,如本文其他地方所述。
在一些情况下,含水流体408可以具有基本均匀浓度或频率的珠粒412。珠粒412可以从单独的通道(图4中未示出)引入到通道区段402中。通道区段402中珠粒412的频率可以通过控制珠粒412被引入通道区段402的频率和/或通道区段402和单独通道中流体的相对流速来控制。在一些情况下,珠粒可以从多个不同的通道引入到通道区段402中,并且相应地控制频率。
在一些情况下,通道区段402中的含水流体408可包括生物颗粒(例如,参见图1和图2描述)。在一些情况下,含水流体408可具有基本均匀浓度或频率的生物颗粒。与珠粒一样,生物颗粒可以从单独通道引入到通道区段402中。可以通过控制生物颗粒被引入到通道区段402的频率和/或通道区段402和单独通道中流体的相对流速来控制通道区段402中的含水流体408中的生物颗粒的频率或浓度。在一些情况下,可以从多个不同的通道将生物颗粒引入到通道区段402中,并相应地控制频率。在一些情况下,第一单独通道可以引入珠粒,并且第二单独通道可以将生物颗粒引入通道区段402中。引入珠粒的第一单独通道可以在引入生物颗粒的第二单独通道的上游或下游。
第二流体410可包含油,例如氟化油,其包括用于稳定所得液滴(例如,抑制所得液滴的后续聚结)的含氟表面活性剂。
在一些情况下,第二流体410可以不经受和/或被引导任何流入或流出贮存器404。例如,第二流体410可以在贮存器404中是基本静止的。在一些情况下,第二流体410可以在贮存器404内流动,但不流入或流出贮存器404,如通过向贮存器404施加压力和/或在汇合点406处受到含水流体408的进入流的影响。可替代地,第二流体410可以经受和/或被引导流入或流出贮存器404。例如,贮存器404可以是将第二流体410从上游引导到下游的通道,从而输送所产生的液滴。
在汇合点406处或附近的通道结构400可具有某些几何特征,其至少部分地确定通过通道结构400形成的液滴的尺寸。通道区段402可在汇合点406处或附近具有高度h0和宽度w。举例来说,通道区段402可包括矩形横截面,其通向具有较宽横截面(例如在宽度或直径方面)的贮存器404。可替代地,通道区段402的横截面可以是其他形状,例如圆形、梯形、多边形或任何其他形状。在汇合点406处或附近的贮存器404的顶壁和底壁可以以扩张角α倾斜。扩散角α允许舌部(在汇合点406处离开通道区段402并在液滴形成之前进入贮存器404的部分含水流体408)增加深度并有助于减小中间形成的液滴的曲率。液滴尺寸可随着扩张角的增加而减小。可以通过针对上述几何参数h0、w和α的以下等式预测所得的液滴半径rd:
举例来说,对于w=21μm,h=21μm和α=3°的通道结构,预测的液滴尺寸为121μm。在另一个实例中,对于w=25μm,h=25μm和α=5°的通道结构,预测的液滴尺寸是123μm。在另一个实例中,对于w=28μm,h=28μm和α=7°的通道结构,预测的液滴尺寸是124μm。
在一些情况下,扩张角α的范围可以在约0.5°至约4°、约0.1°至约10°、或约0°至约90°的范围之间。例如,扩张角可以是至少约0.01°、0.1°、0.2°、0.3°、0.4°、0.5°、0.6°、0.7°、0.8°、0.9°、1°、2°、3°、4°、5°、6°、7°、8°、9°、10°、15°、20°、25°、30°、35°、40°、45°、50°、55°、60°、65°、70°、75°、80°、85°或更高。在一些情况下,扩张角可以是至多约89°、88°、87°、86°、85°、84°、83°、82°、81°、80°、75°、70°、65°、60°、55°、50°、45°、40°、35°、30°、25°、20°、15°、10°、9°、8°、7°、6°、5°、4°、3°、2°、1°、0.1°、0.01°或更小。在一些情况下,宽度w可以在约100微米(μm)至约500μm的范围之间。在一些情况下,宽度w可以在约10μm至约200μm的范围之间。可替代地,宽度可小于约10μm。可替代地,宽度可以大于约500μm。在一些情况下,进入汇合点406的含水流体408的流速可在约0.04微升(μl)/分钟(min)与约40μl/min之间。在一些情况下,进入汇合点406的含水流体408的流速可在约0.01微升(μl)/分钟(min)与约100μl/min之间。可替代地,进入汇合点406的含水流体408的流速可小于约0.01μl/min。可替代地,进入汇合点406的含水流体408的流速可以大于约40μl/min,如45μl/min、50μl/min、55μl/min、60μl/min、65μl/min、70μl/min、75μl/min、80μl/min、85μl/min、90μl/min、95μl/min、100μl/min、110μl/min、120μl/min、130μl/min、140μl/min、150μl/min或更高。在较低的流速下,例如约小于或等于10微升/分钟的流速,液滴半径可能不取决于进入汇合点406的含水流体408的流速。
在一些情况下,至少约50%的产生的液滴可具有一致的尺寸。在一些情况下,至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更高的产生的液滴可以具有一致的尺寸。可替代地,小于约50%的产生的液滴可具有一致的尺寸。
可以通过增加生成点来增加液滴生成的通量,例如增加含水流体408通道区段(例如,通道区段402)与贮存器404之间的汇合点(例如,汇合点406)的数量。可替代地或另外地,可以通过增加通道区段402中的含水流体408的流速来增加液滴产生的通量。
图5示出用于增加液滴产生通量的微流体通道结构的实例。微流体通道结构500可包括多个通道区段502和贮存器504。多个通道区段502中的每一个可与贮存器504流体连通。通道结构500可在多个通道区段502与贮存器504之间包括多个通道汇合点506。每个通道汇合点可以是液滴产生点。来自图4中的通道结构400的通道区段402以及对其部件的任何描述可以对应于通道结构500中的多个通道区段502的给定通道区段以及对其相应部件的任何描述。来自通道结构400的贮存器404以及对其部件的任何描述可以对应于来自通道结构500的贮存器504以及对其相应部件的任何描述。
多个通道区段502中的每个通道区段可包括含水流体508,所述含水流体包括悬浮珠粒512。贮存器504可包括与含水流体508不混溶的第二流体510。在一些情况下,第二流体510可以不经受和/或被引导任何流入或流出贮存器504。例如,第二流体510可以在贮存器504中是基本静止的。在一些情况下,第二流体510可以在贮存器504内流动,但不流入或流出贮存器504,如通过向贮存器504施加压力和/或在汇合点处受到含水流体508的进入流的影响。可替代地,第二流体510可以经受和/或被引导流入或流出贮存器504。例如,贮存器504可以是将第二流体510从上游引导到下游的通道,从而输送所产生的液滴。
在操作中,包括悬浮珠粒512的含水流体508可以沿着多个通道区段502输送到多个汇合点506中以与贮存器504中的第二流体510相遇以产生液滴516、518。从每个通道区段,在与贮存器504的每个相应汇合点处,可形成液滴。在含水流体508和第二流体510相遇的汇合点处,可以基于各种因素形成液滴,例如在汇合点处的流体动力,两种流体508、510的流速,流体特性以及通道结构500的某些几何参数(例如,w、h0、α等),如本文其他地方所述。多个液滴可以通过连续地从多个通道区段502注入含水流体508通过多个汇合点506而收集在贮存器504中。通过通道结构500的平行通道配置,通量可以显著增加。例如,具有五个包括含水流体508的入口通道区段的通道结构可以产生频率是具有一个入口通道区段的通道结构五倍的液滴,条件是通道区段中的流体流速基本上相同。不同入口通道区段中的流体流速可以基本上相同或不同。通道结构可以具有依据实际并且允许贮存器的尺寸那么多的平行通道区段。例如,通道结构可以具有至少约2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100、150、500、250、300、350、400、450、500、600、700、800、900、1000、1500、5000或更多个平行或基本平行的通道区段。
对于多个通道区段502中的每个通道区段,几何参数w、h0和α可以是一致或不一致的。例如,每个通道区段可以在其与贮存器504的各自通道汇合点处或附近具有相同或不同的宽度。例如,每个通道区段可以在其与贮存器504的各自通道汇合点处或附近具有相同或不同的高度。在另一个实例中,贮存器504可以在与多个通道区段502的不同通道汇合点处具有相同或不同的扩张角。当几何参数一致时,有利地,即使增加了通量,也可以控制液滴尺寸为一致的。在一些情况下,当希望具有不同的液滴尺寸分布时,可以相应地改变多个通道区段502的几何参数。
在一些情况下,至少约50%的产生的液滴可具有一致的尺寸。在一些情况下,至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更高的产生的液滴可以具有一致的尺寸。可替代地,小于约50%的产生的液滴可具有一致的尺寸。
图6示出用于增加液滴产生通量的微流体通道结构的另一个实例。微流体通道结构600可包括围绕贮存器604的周边大致圆形布置的多个通道区段602。多个通道区段602中的每一个可与贮存器604流体连通。通道结构600可在多个通道区段602与贮存器604之间包括多个通道汇合点606。每个通道汇合点可以是液滴产生点。来自图2中的通道结构400的通道区段402以及对其部件的任何描述可以对应于通道结构600中的多个通道区段602的给定通道区段以及对其相应部件的任何描述。来自通道结构400的贮存器404以及对其部件的任何描述可以对应于来自通道结构600的贮存器604以及对其相应部件的任何描述。
多个通道区段602中的每个通道区段可包括含水流体608,所述含水流体包括悬浮珠粒612。贮存器604可包括与含水流体608不混溶的第二流体610。在一些情况下,第二流体610可以不经受和/或被引导任何流入或流出贮存器604。例如,第二流体610可以在贮存器604中是基本静止的。在一些情况下,第二流体610可以在贮存器604内流动,但不流入或流出贮存器604,例如通过向贮存器604施加压力和/或在汇合点处受到含水流体608的进入流的影响。可替代地,第二流体610可以经受和/或被引导流入或流出贮存器604。例如,贮存器604可以是将第二流体610从上游引导到下游的通道,从而输送所产生的液滴。
在操作中,包括悬浮珠粒612的含水流体608可以沿着多个通道区段602输送到多个汇合点606中以与贮存器604中的第二流体610相遇以产生多个液滴616。从每个通道区段,在与贮存器604的每个相应汇合点处,可形成液滴。在含水流体608和第二流体610相遇的汇合点处,可基于多种因素形成液滴,例如汇合点处的水动力,两种流体608、610的流速,流体特性以及通道结构600的某些几何参数(例如,通道区段602的宽度和高度、贮存器604的扩张角等),如本文其他地方所述。多个液滴可以通过连续地从多个通道区段602注入含水流体608通过多个汇合点606而收集在贮存器604中。通过通道结构600的基本平行通道配置,通量可以显著增加。通道结构可以具有依据实际并且贮存器的尺寸允许的那么多的基本平行通道区段。例如,通道结构可以具有至少约2、3、4、5、6、7、8、9、10、20、30、40、50、60、70、80、90、100、150、200、250、300、350、400、450、500、600、700、800、900、1000、1500、5000或更多个平行或基本平行的通道区段。多个通道区段可以基本上均匀地间隔开,例如,围绕贮存器的边缘或周边。可替代地,多个通道区段的间隔可以是不均匀的。
贮存器604可以在每个通道汇合点处或附近具有扩张角α(图6中未示出)。多个通道区段602中的每个通道区段可以在通道汇合点处或附近具有宽度w和高度h0。对于多个通道区段602中的每个通道区段,几何参数w、h0和α可以是一致或不一致的。例如,每个通道区段可以在其与贮存器604的各自通道汇合点处或附近具有相同或不同的宽度。例如,每个通道区段可以在其与贮存器604的各自通道汇合点处或附近具有相同或不同的高度。
贮存器604可以在与多个通道区段602的不同通道汇合点处具有相同或不同的扩张角。例如,圆形贮存器(如图6所示)可以具有圆锥形、圆顶状、或者半球形顶板(例如,顶壁)以在多个通道汇合点606处或附近为每个通道区段602提供相同或基本相同的扩张角。当几何参数一致时,有利地,即使增加了通量,也可以控制所得液滴尺寸为一致的。在一些情况下,当希望具有不同的液滴尺寸分布时,可以相应地改变多个通道区段602的几何参数。
在一些情况下,至少约50%的产生的液滴可具有一致的尺寸。在一些情况下,至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更高的产生的液滴可以具有一致的尺寸。可替代地,小于约50%的产生的液滴可具有一致的尺寸。注入液滴中的珠粒和/或生物颗粒可以具有一致或不一致的尺寸。
图7a示出具有用于受控分配的几何特征的微流体通道结构的另一个实例的横截面视图。通道结构700可以包括在通道汇合点706(或交叉点)处与贮存器704连通的通道区段702。在一些情况下,通道结构700及其一个或多个部件可以对应于通道结构100及其一个或多个部件。图7b示出图7a的通道结构700的透视图。
包括多个颗粒716的含水流体712可以沿着通道区段702输送到汇合点706处以相遇与贮存器704中含水流体712不混溶的第二流体714(例如,油等),以产生流入贮存器704的含水流体712的液滴720。在含水流体712和第二流体714相遇的汇合点706处,可以基于各种因素形成液滴,如汇合点706处的流体动力,两种流体712、714的相对流速,流体特性以及通道结构700的某些几何参数(例如,δh等)。多个液滴通过在汇合点706处连续地从通道区段702注入含水流体712而收集在贮存器704中。
产生的离散液滴可包括多个颗粒716中的一个或多个颗粒。如本文其他地方所述,颗粒可以是任何颗粒,如珠粒、细胞珠、凝胶珠粒、生物颗粒、生物颗粒的大分子组分或其他颗粒。可替代地,产生的离散液滴可不包括任何颗粒。
在一些情况下,含水流体712可以具有基本均匀浓度或频率的颗粒716。如本文其他地方所述(例如,参考图4),可以将颗粒716(例如,珠粒)从单独通道(在图7中未示出)引入通道区段702中。通道区段702中颗粒716的频率可通过控制颗粒716被引入通道区段702的频率和/或通道区段702和单独通道中流体的相对流速来控制。在一些情况下,颗粒716可以从多个不同的通道引入到通道区段702中,并且相应地控制频率。在一些情况下,不同的颗粒可通过单独通道引入。例如,第一单独通道可以引入珠粒,并且第二单独通道可以将生物颗粒引入到通道区段702中。引入珠粒的第一单独通道可以在引入生物颗粒的第二单独通道的上游或下游。
在一些情况下,第二流体714可以不经受和/或被引导任何流入或流出贮存器704。例如,第二流体714在贮存器704中可以是基本静止的。在一些情况下,第二流体714可以在贮存器704内流动,但不流入或流出贮存器704,如通过向贮存器704施加压力和/或在汇合点706处受到含水流体712的进入流的影响。可替代地,第二流体714可以经受和/或被引导流入或流出贮存器704。例如,贮存器704可以是将第二流体714从上游引导到下游的通道,从而输送所产生的液滴。
汇合点706处或附近的通道结构700可具有某些几何特征,其至少部分地确定通过通道结构700形成的液滴的尺寸和/或形状。通道区段702可以具有第一横截面高度h1,并且贮存器704可以具有第二横截面高度h2。第一横截面高度h1和第二横截面高度h2可以是不同的,以使在汇合点706处,存在δh的高度差。第二横截面高度h2可大于第一横截面高度h1。在一些情况下,其后可逐渐增加贮存器的横截面高度,例如,离汇合点706更远。在一些情况下,贮存器的横截面高度可根据汇合点706处或附近的扩张角β增大。高度差δh和/或扩张角β可允许舌部(在汇合点706处离开通道区段702并在液滴形成之前进入贮存器704的部分含水流体712)增加深度并有助于减小中间形成的液滴的曲率。例如,液滴尺寸可随着高度差的增加和/或扩张角的增加而减小。
高度差δh可以是至少约1μm。可替代地,高度差可以是至少约1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、25、30、35、40、45、50、60、70、80、90、100、200、300、400、500μm或更多。可替代地,高度差可以是至多约500、400、300、200、100、90、80、70、60、50、45、40、35、30、25、20、19、18、17、16、15、14、13、12、11、10、9、8、7、6、5、4、3、2、1μm或更小。在一些情况下,扩张角β的范围可以在约0.5°至约4°、约0.1°至约10°、或约0°至约90°的范围之间。例如,扩张角可以是至少约0.01°、0.1°、0.2°、0.3°、0.4°、0.5°、0.6°、0.7°、0.8°、0.9°、1°、2°、3°、4°、5°、6°、7°、8°、9°、10°、15°、20°、25°、30°、35°、40°、45°、50°、55°、60°、65°、70°、75°、80°、85°或更高。在一些情况下,扩张角可以是至多约89°、88°、87°、86°、85°、84°、83°、82°、81°、80°、75°、70°、65°、60°、55°、50°、45°、40°、35°、30°、25°、20°、15°、10°、9°、8°、7°、6°、5°、4°、3°、2°、1°、0.1°、0.01°或更小。
在一些情况下,进入汇合点706的含水流体712的流速可在约0.04微升(μl)/分钟(min)与约40μl/min之间。在一些情况下,进入汇合点706的含水流体712的流速可在约0.01微升(μl)/分钟(min)与约100μl/min之间。可替代地,进入汇合点706的含水流体712的流速可小于约0.01μl/min。可替代地,进入汇合点706的含水流体712的流速可以大于约40μl/min,如45μl/min、50μl/min、55μl/min、60μl/min、65μl/min、70μl/min、75μl/min、80μl/min、85μl/min、90μl/min、95μl/min、100μl/min、110μl/min、120μl/min、130μl/min、140μl/min、150μl/min或更大。在较低的流速下,如约小于或等于10微升/分钟的流速,液滴半径可能不取决于进入汇合点706的含水流体712的流速。第二流体714在贮存器704中可以是静止的,或基本上静止的。可替代地,第二流体714可以是流动的,如以上针对含水流体712所述的流速。
在一些情况下,至少约50%的产生的液滴可具有一致的尺寸。在一些情况下,至少约55%、60%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或更高的产生的液滴可以具有一致的尺寸。可替代地,小于约50%的产生的液滴可具有一致的尺寸。
虽然图7a和7b示出高度差δh在汇合点706处突然变化(例如,梯度增加),但是高度差可逐渐增加(例如,从约0μm至最大高度差)。可替代地,高度差可以从最大高度差逐渐减小(例如,渐缩)。如本文所用,高度差的逐渐增加或减小可指高度差的连续增量增加或减小,其中高度剖面的任何一个差别区段与高度剖面的紧邻差别区段之间的角度大于90°。例如,在汇合点706处,通道的底壁和贮存器的底壁可以以大于90°的角度相遇。可替代地或另外地,通道的顶壁(例如,顶板)和贮存器的顶壁(例如,顶板)可以以大于90°的角度相遇。逐渐增加或减小可以是线性或非线性的(例如,指数的、正弦的等)。可替代地或另外地,高度差可以线性地或非线性地可变地增加和/或减小。虽然图7a和7b示出线性扩张的贮存器横截面高度(例如,恒定扩张角β),但是横截面高度可非线性扩张。例如,贮存器可以至少部分地由具有可变扩张角的圆顶状(例如,半球形)形状限定。横截面高度可以任何形状扩张。
例如,如上文或本文其他地方所述的通道网络可以流体地联接到适当的流体部件。例如,入口通道区段流体地联接到它们要递送到通道汇合点的材料的适当来源。这些来源可以包括多种不同的流体部件中的任一种,从在微流体装置的主体结构中限定或与其连接的简易贮存器,到从装置外来源、歧管、流体流动单元(例如,致动器、泵、压缩机)等递送流体的流体管道。同样地,出口通道区段(例如,通道区段208、贮存器604等)可以流体地联接到分配细胞的接收容器或导管以便后续处理。同样,这可以是在微流体设备的主体中限定的储存器,或者其可以是用于将分配细胞递送到随后的过程操作、仪器或部件的流体导管。
本文描述的方法和系统可用于极大地提高单细胞应用和/或接收基于液滴的输入的其他应用的效率。例如,在对占据细胞和/或适当大小的细胞进行分选之后,可以执行的后续操作可以包括产生扩增产物、纯化(例如,通过固相可逆固定化(spri))、进一步处理(例如,剪切、功能序列的连接和随后的扩增(例如,通过pcr))。这些操作可以本体发生(例如,在分配区外)。在分配区是乳液中的液滴的情况下,可以破坏乳液并且将液滴的内容物汇集用于另外的操作。可连同携带条形码的珠粒共分配的其他试剂可包括阻断核糖体rna(rrna)的寡核苷酸和消化细胞中基因组dna的核酸酶。可替代地,可以在另外的处理操作期间应用rrna去除剂。通过这种方法生成的构建体的构型可有助于在测序期间最小化(或避免)poly-t序列的测序和/或对多核苷酸序列的5'末端进行测序。可以对扩增产物(例如,第一扩增产物和/或第二扩增产物)进行测序以进行序列分析。在一些情况下,可以使用测序用部分发夹扩增(partialhairpinamplificationforsequencing;phase)方法执行扩增。
多种应用需要生物颗粒群体内不同生物颗粒或生物体类型的存在的评估和其量化,包括例如微生物菌群分析和表征、环境测试、食品安全测试、流行病学分析,例如,追踪污染等。
计算机系统
本公开提供了被编程用于实施本公开的方法的计算机系统。图11示出计算机系统1101,其被编程或以其他方式被配置用于(i)控制微流体系统(例如,流体流),如用于受控的分配、分选(例如,分析物、分配区、细胞等的分选)、聚合、一种或多种刺激的施加等,(ii)产生和维护条形码的一个或多个文库,(iii)执行测序,和/或(iv)分析和/或输出这种测序的结果。计算机系统1101可以调节本公开的各个方面,例如,调节微流体结构中一个或多个通道中的流体流速,调节分析物、生物颗粒和/或样品的一种或多种反应或相互作用,调节一种或多种分析物的分选,和/或调节一种或多种文库的产生。计算机系统1101可以是用户的电子设备或相对于电子设备远程定位的计算机系统。电子设备可以是移动电子设备。
计算机系统1101包括中央处理单元(cpu,在本文中也称为“处理器”和“计算机处理器”)1105,其可为单一核心或多核心处理器,或用于并行处理的多个处理器。计算机系统1101还包括存储器或存储单元1110(例如,随机存取存储器、只读存储器、闪速存储器),电子存储单元1115(例如,硬盘),与一个或多个其他系统通信的通信接口1120(例如,网络适配器),和外围设备1125,如高速缓冲存储器、其他存储器、数据存储和/或电子显示适配器。存储器1110、存储单元1115、接口1120和外围设备1125经由通信总线(实线)如母板与cpu1105通信。存储单元1115可为用于存储数据的数据存储单元(或数据储存库)。计算机系统1101可借助于通信接口1120来可操作地耦接至计算机网络(“网络”)1130。网络1130可为互联网、互联网和/或外联网或与互联网通信的内部网和/或外联网。网络1130在一些情况下为电信和/或数据网络。网络1130可包括一个或多个计算机服务器,其可实现分布式计算,如云计算。网络1130在一些情况下借助于计算机系统1101,可实施对等网络,其可使得耦接至计算机系统1101的设备能够作为客户端或服务器来运作。
cpu1105可执行序列机器可读指令,所述指令可在程序或软件中具体实现。指令可存储于存储单元,如存储器1110中。指令可被引导至cpu1105,其可随后编程或另外配置cpu1105来实施本公开的方法。由cpu1105执行的操作的实例可包括撷取、解码、执行和写回。
cpu1105可为电路的一部分,如集成电路。系统1101的一个或多个其他部件可包含于电路中。在一些情况下,电路是专用集成电路(asic)。
存储单元1115可存储文件,如驱动程序、文库和保存程序。存储单元1115可存储用户数据,例如,用户偏好和用户程序。计算机系统1101在一些情况下可包括一个或多个另外的数据存储单元,所述单元在计算机系统1101外部,如位于经由内部网或互联网与计算机系统1101通信的远程服务器上。
计算机系统1101可经由网络1130与一个或多个远程计算机系统通信。例如,计算机系统1101可以与用户(例如,运营商)的远程计算机系统通信。远程计算机系统的实例包括个人计算机(例如,便携式pc)、板式pc或平板pc(例如,
如本文描述的方法可经由机器(例如,计算机处理器)可执行代码来实施,所述代码存储于计算机系统1101的电子存储位置上,例如像,存储器1110或电子存储单元1115。机器可执行或机器可读代码可以软件形式提供。在使用期间,代码可由处理器1105执行。在一些情况下,代码可从存储单元1115撷取并且存储在存储器1110上准备由处理器1105访问。在一些情况下,可排除电子存储单元1115,并且机器可执行指令存储于存储器1110上。
代码可预先编译并且被配置来供具有适于执行代码的处理器的机器来使用,或可在执行时间期间加以编译。代码可以程序语言来提供,可选择所述程序语言以使得代码能够以预先编译或原样编译方式来执行。
本文提供的系统和方法,如计算机系统1101的方面可在编程中具体实现。技术的各个方面可被认为是通常呈机器(或处理器)可执行代码和/或相关联数据形式的“产品”或“制品”,所述数据承载或具体实现于一定类型的机器可读介质中。机器可执行代码可存储于电子存储单元,如存储器(例如,只读存储器、随机存取存储器、闪速存储器)或硬盘上。“存储”类型介质可包括计算机、处理器等的任何或所有有形存储器,或其相关联模块,如各种半导体存储器、磁带驱动器、磁盘驱动器等,其可在任何时候提供非暂时性存储用于软件编程。软件的全部或一部分可有时经由互联网或各种其他电信网络来传送。此类通信,例如,可使得将软件从一个计算机或处理器加载至另一个计算机或处理器,例如,从管理服务器或主机计算机加载至应用服务器的计算机平台中。因此,可承载软件元件的另一种类型的介质包括光、电和电磁波,如跨越本地设备之间的物理接口、经由有线和光学陆地线网络和各种空中链路所使用的光、电和电磁波。携带此类波的物理元件,如有线或无线链路、光链路等也可被认为是承载软件的介质。如本文使用,除非限于非暂时性、有形“存储”介质,术语如计算机或机器“可读介质”是指参与提供指令至处理器供执行的任何介质。
因此,机器可读介质,如计算机可执行代码,可采用许多形式,包括但不限于有形存储介质、载波介质或物理传输介质。非易失性存储器介质包括,例如,光盘或磁盘,如任何计算机等中的任何存储设备,如在附图中示出的可用于实施数据库等的存储设备。易失性存储器介质包括动态存储器,如这类计算机平台的主存储器。有形传输介质包括同轴电缆;铜线和光导纤维,包括构成计算机系统中的总线的导线。载波传输介质可采用电或电磁信号,或声或光波的形式如在射频(rf)和红外(ir)数据通信期间产生的信号。常见形式的计算机可读介质因此包括例如:软盘、软磁盘、硬盘、磁带、任何其他磁介质、cd-rom、dvd或dvd-rom、任何其他光学介质、冲孔卡纸带、具有孔图案的任何其他物理存储器介质、ram、rom、prom和eprom、快闪eprom、任何其他存储器芯片或盒、运输数据或指令的载波、运输这类载波的电缆或链路,或计算机可读取编程代码和/或数据的任何其他介质。许多这些形式的计算机可读介质可涉及运送一个或多个指令的一个或多个序列至处理器供执行。
计算机系统1101可包括或与电子显示器1135通信,所述显示器包含用户接口(ui)1140以用于提供例如测序分析的结果。ui的实例包括但不限于图形用户界面(gui)和基于web的用户界面。
本公开的方法和系统可经由一个或多个算法来实施。算法可在由中央处理单元1105执行后经由软件来实施。算法可以例如执行测序和处理文库,如通过访问一个或多个数据库。
本公开的设备、系统、组合物和方法可用于各种应用,比如例如,处理来自单细胞的单一分析物(例如,rna、dna、代谢物、蛋白质等)或多种分析物(例如,dna和rna、dna和蛋白质、rna和蛋白质、或rna、dna和蛋白质等)。例如,将生物颗粒(例如,细胞或细胞珠)分配在分配区(例如,液滴)中,并处理生物颗粒的多种分析物以用于后续处理。多种分析物可以来自单细胞。这可以实现例如对细胞的蛋白质组、转录组和基因组同时分析。
尽管本文已示出和描述了本发明的优选实施方案,但对于本领域技术人员来说将显而易见,此类实施方案仅作为实例提供。本发明不旨在受到本说明书中提供的具体实施例的限制。尽管已经参考上述说明书描述本发明,但本文中的实施方案的描述和说明不意图以限制意义解释。本领域技术人员现在将想到许多变化、改变和替换而不偏离本发明。此外,应当理解,本发明的所有方面均不限于本文所述的具体描述、配置或相对比例,其取决于多种条件和变量。应当理解的是,可以在实践本发明时采用在本文中描述的本发明的实施方案的各种替代方案。因此,预期本发明还应涵盖任何此类替代方案、修改、变型或等同物。所意图的是,以下权利要求限定本发明的范围以及由此涵盖这些权利要求及其等同物范围内的方法和结构。
- 还没有人留言评论。精彩留言会获得点赞!