一种快速时间分辨荧光免疫分析检测试剂盒及其检测方法与流程
本发明属于时间分辨荧光免疫分析
技术领域:
,尤其涉及一种快速时间分辨荧光免疫分析检测试剂盒及其检测方法。
背景技术:
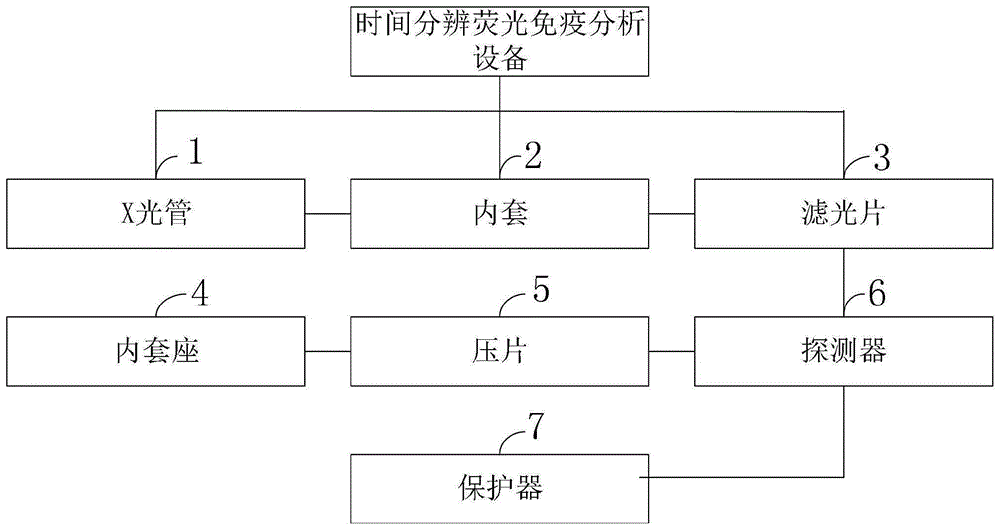
:目前,最接近的现有技术:结核病是由结核分枝杆菌复合群中的结核分枝杆菌(mycobacteriumtuberculosis,mtb)、牛分枝杆菌(mycobacteriumbovis)和非洲分枝杆菌(mycobacteriumafricanum)引起的慢性传染性疾病,可累及全身各个器官,其中尤以肺结核多见。结核分枝杆菌一般是由呼吸道结核病患者通过空气飞沫传染给新宿主。结核病的潜伏期为数周至数月,期间大部分感染者无明显症状。结核病严重危害公共安全,全世界每年有200万人死于结核病。在中国,每年有100万的新增结核病人。结核分枝杆菌的镜检是最常用的诊断结核病的方法,但是该方法的阳性率低。结核分枝杆菌的培养是确定结核病的金标准,但是由于结核分枝杆菌的生长速度慢,试验周期长(2~3周),不能满足临床的要求。另外,结核病还可以通过胸透,核酸检测,体格检查等方法确认。潜伏性结核菌感染是宿主感染结核分枝杆菌后的一种特殊状态,感染者体内的结核分枝杆菌处于持留状态,不能诊断为活动性结核病,但具有发展为活动性结核病的风险。对潜伏性结核菌感染的高危人群进行早期诊断和适当干预,在结核病控制中具有积极意义。结核菌素试验是唯一可以诊断潜伏性结核菌感染的方法,在结核杆菌感染后2~10周内结核菌素试验转为阳性。然而,有些感染者对结核菌素是没有反应的,这些人群中既包括那些各种原因导致免疫抑制者,也包括一些没有免疫抑制的人。此外,接种卡介苗,感染非致病性分枝杆菌,以及其他因素,会导致非结核菌感染者结核菌素试验阳性。结核感染t细胞的γ-干扰素体外释放法(interferon-gammareleaseassays,igras)检测是通过结核分枝杆菌特异抗原所引发的细胞介导免疫(cellmediatedimmunity,cmi)反应来实现的。目前上市的试剂盒使用的抗原或多肽或其类似物主要有早期分泌抗原靶蛋白6(earlysecretingantigentarget6,esat6)、培养滤液蛋白10(culturefiltrateprotein-10,cfp-10)和tb7.7(p4)等中的一种或多种作为特异性刺激抗原,所有的卡介苗菌株及绝大部分的非结核分枝杆菌[堪萨斯分枝杆菌(mycobacteriumkansasii),苏尔加分枝杆菌(mycobacteriumszulgai),海氏分枝杆菌(mycobacteriummarinum)除外]不含有这些蛋白质。感染结核分枝杆菌复合群的患者的血液中通常含有能够识别这些蛋白质和其它分枝杆菌抗原的淋巴细胞,这一识别过程伴随着γ-干扰素的合成和分泌。igras利用结核分枝杆菌特异性抗原或多肽或其类似物刺激人全血标本中的结核分枝杆菌抗原特异性t细胞产生免疫应答,再用免疫测定的方法定量测定人血清中免疫应答产生的γ-干扰素的浓度,从而判断受试者是否具有结核分枝杆菌特异的t细胞免疫反应,即结核感染t细胞检测。γ-干扰素为th1细胞分泌的一种细胞因子,不但能够反映机体结核的th1细胞免疫情况,还与体内结核菌的抗原含量密切相关。被结核分枝杆菌抗原致敏的t细胞再遇到同类抗原时能产生高水平的γ-干扰素,因此被用于结核潜伏感染的诊断。现有的荧光免疫分析设备采用反射的方式,主要有以下几种:反射式的x荧光分析仪,只要测出荧光x射线的波长或者能量,就可以知道元素的种类,这就是荧光x射线定性分析的基础。此外,荧光x射线的强度与相应元素的含量有一定的关系,据此,可以进行元素定量分析。反射式的x荧光分析仪缺点:难于作绝对分析,故定量分析需要标样。对轻元素的灵敏度要低一些。容易受相互元素干扰和叠加峰影响。综上所述,现有技术存在的问题是:现有技术中,常规时间分辨荧光免疫分析技术试剂组分繁多,液态试剂不够稳定,操作繁琐,耗时较长的缺点。以往的结核感染t细胞测定中需要独立的采血管和培养管、操作繁杂、容易出错、自动化程度不高。全血培养过程中不能防止样本在采血管开盖、分装血样过程中的二次污染,减少了此过程中潜在的生物安全风险,不能防止二次标识过程产生的错误。现有技术中,采血过程中耗材高,检测结果准确性差、灵敏度低。传统荧光仪检出限达不到要求;反射角度很小,调试难度大;样品含量少,测量时间长,不适合快速测量。技术实现要素:本发明的目的在于提供一种快速时间分辨荧光免疫分析检测试剂盒及其检测方法,采用了γ-干扰素体外释放法,联合采用了生物素亲和素法,双抗体夹心时间分辨荧光免疫法,实验方法简单快速,可自动化操作,检测系统为开放式操作系统。本发明采用的技术方案为:一种快速时间分辨荧光免疫分析检测试剂盒的检测方法,所述快速时间分辨荧光免疫分析检测试剂盒的检测方法包括:采用时间分辨荧光免疫分析设备进行荧光值计数。所述时间分辨荧光免疫分析设备的探测器利用全反射技术进行最低探测限的测定,测量系统的最低探测限由如下公式计算:mdl=3(ib/t)1/2m/i。mdl是本底计数率,t为测量计数时间,m为被测量元素质量,l代表被测量元素产生的特征峰净计数率,s=i/m就是系统灵敏度。进一步,所述时间分辨荧光免疫分析设备包括x光管、内套、滤光片、内套座、压片、探测器、保护器。所述x光管一端镶嵌在内套座上,内套座与探测器通过导线连接,保护器通过导线连接探测器。内套镶嵌在内套座内部,滤光片固定在内套上,压片位于内套和探测器之间并固定在内套上。被测样品设置在内套上。所述内套底部设置有方孔,方孔设置为准直器。内套与内套座设置有通孔。所述的探测器具体采用x射线检测器和固定夹子组合,x射线检测器设置光纤和导光单元,导光单元由固定材料固定于探测器主体内,固定材料形成于导光单元的周围的至少一部分,导光单元的至少一部分由玻璃形成,固定材料是氟系树脂材料、四氟乙烯-全氟间二氧环戊烯聚合物和氟硅橡胶或折射率比导光单元的折射率低的低折射率硅酮树脂或甲基系硅酮树脂,导光单元的光出射端由固定材料覆盖。保护器包括拼合件、保护器主体和遮挡盖,拼合件具有基本管形,以对至少部分覆盖被保持于拼合件之间的电线的至少一个波纹管进行保持,拼合件包括一个或两个肋、波纹管,一对肋包括竖立端,竖立端被弯曲以沿着波纹管的凹槽彼此靠近,设置轴线沿着拼合件的纵向方向延伸的一个或多个支承轴部分,设置在肋的竖立端的基端处或附近,和/或肋通过支承轴部分与一个或两个拼合件的外围壁相连续,拼合件能够与安装在线束上的至少一个波纹管相接合,拼合件设置安装凹槽、膨胀板、接合支腿和弹性板,膨胀板具有基本正方形,接合支腿包括至少一个突出部分,当膨胀板至少部分插入容纳部分中时,能够与膨胀板相协作而夹入导引板,多个突出部分与膨胀板相协作而夹入导引板,弹性板在拼合件的内部位置处基本沿着拼合件的周向表面延伸,弹性板的表面设置有突出的表面和支线部分的外表面基本彼此齐平保护器主体具有拼合件、底壁、间隔壁和从该底壁竖立成为彼此相对的一对竖立壁,底壁的内表面和一对竖立壁的内表面形成收纳槽,在收纳槽中收纳有一根或多根电缆,遮挡盖与保护器主体接合以便覆盖收纳槽。进一步,导光单元包括对从光源出射的光进行传导的第一导光构件和使由第一导光构件传导的光扩散并传导至x射线检测器附近的第二导光构件,第二导光构件在光从第一导光构件入射的光入射侧包括使入射光扩散的光扩散构件,第一导光构件和第二导光构件中至少第二导光构件由固定材料固定,第一导光构件和第二导光构件中仅第二导光构件由固定材料固定,固定夹子包括具有远端和近端的长形构件,固定夹子还包括至少一个安装在长形构件的远端处的相对构件和壳体,相对构件被布置为在长形构件与相对构件之间夹紧探测器的一部分,相对构件从长形构件的远端朝向长形构件的近端延伸,相对构件通过横贯构件连接至长形构件,横贯构件被布置为在使用中接合探测器的一部分的上部边缘,相对构件被朝向长形构件而弹性地偏置,壳体在长形构件的与相对构件相反的一侧被安装至长形构件,所述壳体被围绕横向于长形构件的纵向方向的轴线而枢转地安装至长形构件,壳体相对于长形构件可滑动地安装,用于阻止壳体与长形构件的相对滑动的制动装置,制动装置包括齿条和棘爪。进一步,保护器主体还具有突起条,突起条从底壁的内表面朝遮挡盖突出,形成在所述一对竖立壁之间以便沿与一对竖立壁相交的方向延伸,在突起条中的每一个与一对竖立壁之间的边界部分中,突起条在排出方向上延伸横跨底壁的内表面,排出方向与一根或多根电缆的布设方向和垂直于布设方向的方向中的每一个方向相交,间隔壁从底壁竖立,并布置在所述一对竖立壁之间,与一对竖立壁相对,突起条具有形成在一对竖立壁中的一个竖立壁与间隔壁之间的第一突起条和形成在一对竖立壁中的另一个竖立壁与间隔壁之间的第二突起条,在第一突起条中的每一个与一个竖立壁相邻的边界部分和第一突起条与间隔壁相邻的边界部分中。进一步,干燥为50~70℃热风下干燥30~40s。进一步,采用时间分辨荧光免疫分析设备进行荧光值计数前需进行:第一步,分别向空白对照培养管、测试培养管和阳性对照培养管三种培养管中加入样本,并颠倒数次使样本与三种培养管中的内容物混匀。第二步,将加有样本的三种培养管置于35~38℃下直立培养16~24小时。第三步,培养结束后,通过离心将三种培养管的样本的组织分离。第四步,向校准品反应杯中预设的含有不同浓度的校准品的孔内分别加入实验缓冲液,并将第三步中分离的样本中的组织及实验缓冲液加入测试反应杯中。第五步,将校准品反应杯和测试反应杯在30~40℃下,振荡孵育5~20min。进一步,所述第三步中,3000~5000r/min转速下离心10~20min。本发明的另一目的在于提供一种快速时间分辨荧光免疫分析检测试剂盒包括:测试反应杯,内包被有链霉亲和素以及结合在链霉亲和素上的生物素化γ-干扰素单克隆抗体,并含有镧系元素标记的γ-干扰素单克隆抗体。校准品反应杯,内包被有链霉亲和素以及结合在链霉亲和素上的生物素化γ-干扰素单克隆抗体,并含有铕标记γ-干扰素单克隆抗体及不同浓度的校准品。空白对照培养管,内含有抗凝血物质。测试培养管,内含有抗凝血物质和能够刺激结核分枝杆菌抗原特异性t细胞产生γ-干扰素的刺激物,刺激物为结核分枝杆菌的抗原及其衍生的抗原表位肽和它们的类似物中的至少一种。阳性对照培养管,内含有抗凝血物质和细胞凝集素。实验缓冲液。浓缩洗液。进一步,所述刺激物为结核分枝杆菌rv0733、rv1978、rv1980c、rv1981c、rv1984c、rv1985c、rv2654c、rv3425、rv3429、rv3615c、rv3873、rv3874、rv3875、rv3878、rv3879c抗原、它们的衍生抗原表位肽、嵌合重组抗原及类似物中的至少一种。所述抗凝血物质为肝素钠和/或肝素锂。所述细胞凝集素为植物血细胞凝集素和/或刀豆凝集素。所述实验缓冲液为含有0.15mol/l的氯化钠、0.6ml/l的吐温-20、30ppm的防腐剂、100μmol/l的乙二胺四乙酸的5mmol/l,ph7.8的4-羟乙基哌嗪乙磺酸缓冲液。所述浓缩洗液为含有1.125g/l的氯化钠、0.2ml/l的吐温-20、30ppm的防腐剂的50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸缓冲液。所述隔离层使用的隔离层溶液为含有0.12mol/l的氯化钠、0.38g/l的叠氮钠、10g/l的牛γ球蛋白、50g/l的牛血清白蛋白、50g/l的海藻糖、0.8g/l原生鼠igg、0.05g/l的变性小鼠igg、2g/l酪蛋白、37.5u/ml的肝素钠的50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸。进一步,所述刺激物为rv3874和rv3875的组合。测试反应杯的制备方法为:将所述链霉亲和素稀释至浓度0.1~10μg/ml,加入到空白测试反应杯中,2~8℃下孵育20~24h,洗涤。将所述生物素化γ-干扰素单克隆抗体稀释至浓度0.1~10μg/ml,加入到包被有链霉亲和素的测试反应杯中,2~8℃下孵育20~24h,洗涤。然后每个杯中加入隔离层溶液,干燥后形成隔离层以防止镧系元素标记的γ-干扰素单克隆抗体吸附到测试反应杯上,最后在隔离层上加入工作浓度为100~400ng/ml的所述镧系元素标记的γ-干扰素单克隆抗体,干燥后即得所述测试反应杯。综上所述,本发明的优点及积极效果为:本发明采用干试剂快速时间分辨荧光免疫分析技术,解决了以往的常规时间分辨荧光免疫分析技术试剂组分繁多,液态试剂不够稳定,操作繁琐,耗时较长的缺点。并且本发明解决了以往的结核感染t细胞测定中需要独立的采血管和培养管、操作繁杂、容易出错、自动化程度不高等缺点。本发明实现了采血管和培养管一体化,真空负压精确采血。3种培养管采用不同颜色标签和帽盖进行区分。全血培养过程中避免了采血管开盖、分装血样、二次标识等过程,防止了样本在采血管开盖、分装血样过程中的二次污染,减少了此过程中潜在的生物安全风险,也防止了二次标识过程产生的错误,并且全血培养后只要按常规离心后即可放置在全自动系统上进行取样检测,降低了工作强度和提高了工作效率。本发明的培养管具有采血管和培养管一体化、采血过程中减少了耗材使用、真空精确采血、适于自动化操作等特点。本发明的试剂盒具有检测结果准确性、灵敏度高、特异性强、稳定性好、检测方法简便、高效等特点,适合于即时检验(point-of-caretesting,poct)。本发明的时间分辨荧光免疫分析设备能够降低最低检出限。并且能实现实时快速测量。可以实现实时测量、制样方便、检出限低,本发明的时间分辨荧光免疫分析设备利用全反射技;使样品荧光的杂散本底降低约四个量级,从而大大提高了能量分辨率和灵敏率,避免了xrf和wxrf测量中通常遇到的本底增强或减背效应,大大缩减了定量分析的工作量和工作时间,同时提高了测量的精确度。附图说明图1是本发明实施例提供的时间分辨荧光免疫分析设备结构示意图。图中:1、x光管;2、内套;3、滤光片;4、内套座;5、压片;6、探测器;7、保护器。图2是本发明实施例提供的时间分辨荧光免疫分析设备测量原理图。图3是本发明实施例提供的试剂盒的γ-干扰素定量检测剂量-反应曲线。具体实施方式为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。以下实施例中的链霉亲和素购于深圳菲鹏股份有限公司;生物素标记γ-干扰素单克隆抗体购于荷兰mabtech公司;标记用γ-干扰素单克隆抗体购于厦门万泰凯瑞生物技术有限公司;rv0733、rv1978、rv1980c(mpt64)、rv1981c、rv1984c(cfp-21)、rv1985c、rv2654c(tb7.7)、rv3425、rv3429、rv3615c(espc)、rv3873、rv3874(cfp-10)、rv3875(esat-6)、rv3878、rv3879c抗原或多肽或其类似物或其嵌合重组抗原购于美国sigma公司;植物血凝素l(phytohaemagglutinin-l,pha-l)购于美国sigma公司;铕的4-[2-(4-异硫氰基苯基)乙炔基]-2,6双{[n,n双(羧甲基)-氨基]甲基}吡啶试剂购于美国perkinelmer公司;空白反应杯购于丹麦nunc公司;编号87/586的γ-干扰素生物参考标准品购于英国国家生物制品检定所;琼脂糖凝胶sepharosecl-6b购于瑞典pharmacia公司;洗液、实验缓冲液、fwz-ⅰ型微量振荡仪、dem-ⅲ型全自动酶标洗板均由广州市丰华生物工程有限公司提供;victortm2d1420型trfia仪购于美国perkinelmer公司;aqt90flex快速免疫分析仪购于丹麦radiometer公司。其他试剂为国产分析纯;结核感染t细胞检测试剂盒(体外释放酶联免疫法)购于北京万泰生物药业股份有限公司。现有技术中,常规时间分辨荧光免疫分析技术试剂组分繁多,液态试剂不够稳定,操作繁琐,耗时较长的缺点。以往的结核感染t细胞测定中需要独立的采血管和培养管、操作繁杂、容易出错、自动化程度不高。全血培养过程中不能防止样本在采血管开盖、分装血样过程中的二次污染,减少了此过程中潜在的生物安全风险,不能防止二次标识过程产生的错误。现有技术中,采血过程中耗材高,检测结果准确性差、灵敏度低。为解决上述问题,下面结合具体方案对本发明作详细描述。本发明实施例提供的快速时间分辨荧光免疫分析检测试剂盒的检测方法,包括:采用时间分辨荧光免疫分析设备进行荧光值计数。所述时间分辨荧光免疫分析设备(如图1-图2)的探测器利用全反射技术进行最低探测限的测定,测量系统的最低探测限由如下公式计算:mdl=3(ib/t)1/2m/i。mdl是本底计数率,t为测量计数时间,m为被测量元素质量,l代表被测量元素产生的特征峰净计数率,s=i/m就是系统灵敏度。如图1所示,本发明实施例提供的时间分辨荧光免疫分析设备包括x光管1、内套2、滤光片3、内套座4、压片5、探测器6、保护器7。所述x光管1一端镶嵌在内套座上,内套座与探测器6通过导线连接,保护器7通过导线连接探测器。内套镶嵌在内套座内部,滤光片3固定在内套上,压片5位于内套和探测器之间并固定在内套上。被测样品设置在内套上。所述内套底部设置有方孔,方孔设置为准直器。内套与内套座设置有通孔。所述的探测器具体采用x射线检测器和固定夹子组合,x射线检测器设置光纤和导光单元,导光单元由固定材料固定于探测器主体内,固定材料形成于导光单元的周围的至少一部分,导光单元的至少一部分由玻璃形成,固定材料是氟系树脂材料、四氟乙烯-全氟间二氧环戊烯聚合物和氟硅橡胶或折射率比导光单元的折射率低的低折射率硅酮树脂或甲基系硅酮树脂,导光单元的光出射端由固定材料覆盖。保护器包括拼合件、保护器主体和遮挡盖,拼合件具有基本管形,以对至少部分覆盖被保持于拼合件之间的电线的至少一个波纹管进行保持,拼合件包括一个或两个肋、波纹管,一对肋包括竖立端,竖立端被弯曲以沿着波纹管的凹槽彼此靠近,设置轴线沿着拼合件的纵向方向延伸的一个或多个支承轴部分,设置在肋的竖立端的基端处或附近,和/或肋通过支承轴部分与一个或两个拼合件的外围壁相连续,拼合件能够与安装在线束上的至少一个波纹管相接合,拼合件设置安装凹槽、膨胀板、接合支腿和弹性板,膨胀板具有基本正方形,接合支腿包括至少一个突出部分,当膨胀板至少部分插入容纳部分中时,能够与膨胀板相协作而夹入导引板,多个突出部分与膨胀板相协作而夹入导引板,弹性板在拼合件的内部位置处基本沿着拼合件的周向表面延伸,弹性板的表面设置有突出的表面和支线部分的外表面基本彼此齐平保护器主体具有拼合件、底壁、间隔壁和从该底壁竖立成为彼此相对的一对竖立壁,底壁的内表面和一对竖立壁的内表面形成收纳槽,在收纳槽中收纳有一根或多根电缆,遮挡盖与保护器主体接合以便覆盖收纳槽。导光单元包括对从光源出射的光进行传导的第一导光构件和使由第一导光构件传导的光扩散并传导至x射线检测器附近的第二导光构件,第二导光构件在光从第一导光构件入射的光入射侧包括使入射光扩散的光扩散构件,第一导光构件和第二导光构件中至少第二导光构件由固定材料固定,第一导光构件和第二导光构件中仅第二导光构件由固定材料固定,固定夹子包括具有远端和近端的长形构件,固定夹子还包括至少一个安装在长形构件的远端处的相对构件和壳体,相对构件被布置为在长形构件与相对构件之间夹紧探测器的一部分,相对构件从长形构件的远端朝向长形构件的近端延伸,相对构件通过横贯构件连接至长形构件,横贯构件被布置为在使用中接合探测器的一部分的上部边缘,相对构件被朝向长形构件而弹性地偏置,壳体在长形构件的与相对构件相反的一侧被安装至长形构件,所述壳体被围绕横向于长形构件的纵向方向的轴线而枢转地安装至长形构件,壳体相对于长形构件可滑动地安装,用于阻止壳体与长形构件的相对滑动的制动装置,制动装置包括齿条和棘爪。保护器主体还具有突起条,突起条从底壁的内表面朝遮挡盖突出,形成在所述一对竖立壁之间以便沿与一对竖立壁相交的方向延伸,在突起条中的每一个与一对竖立壁之间的边界部分中,突起条在排出方向上延伸横跨底壁的内表面,排出方向与一根或多根电缆的布设方向和垂直于布设方向的方向中的每一个方向相交,间隔壁从底壁竖立,并布置在所述一对竖立壁之间,与一对竖立壁相对,突起条具有形成在一对竖立壁中的一个竖立壁与间隔壁之间的第一突起条和形成在一对竖立壁中的另一个竖立壁与间隔壁之间的第二突起条,在第一突起条中的每一个与一个竖立壁相邻的边界部分和第一突起条与间隔壁相邻的边界部分中。如图2当光入射到透明或半透明材料表面时,一部分被反射,一部分被吸收,还有一部分可以透射过去。透射是入射光经过折射穿过物体后的出射现象。被透射的物体为透明体或半透明体,如玻璃,滤色片。本发明实施例提供的快速时间分辨荧光免疫分析检测试剂盒,包括:测试反应杯,内包被有链霉亲和素以及结合在链霉亲和素上的生物素化γ-干扰素单克隆抗体,并含有镧系元素标记的γ-干扰素单克隆抗体。校准品反应杯,内包被有链霉亲和素以及结合在链霉亲和素上的生物素化γ-干扰素单克隆抗体,并含有铕标记γ-干扰素单克隆抗体及不同浓度的校准品。空白对照培养管,内含有抗凝血物质。测试培养管,内含有抗凝血物质和能够刺激结核分枝杆菌抗原特异性t细胞产生γ-干扰素的刺激物,刺激物为结核分枝杆菌的抗原及其衍生的抗原表位肽和它们的类似物中的至少一种。阳性对照培养管,内含有抗凝血物质和细胞凝集素。实验缓冲液。浓缩洗液。刺激物为结核分枝杆菌rv0733、rv1978、rv1980c、rv1981c、rv1984c、rv1985c、rv2654c、rv3425、rv3429、rv3615c、rv3873、rv3874、rv3875、rv3878、rv3879c抗原、它们的衍生抗原表位肽、嵌合重组抗原及类似物中的至少一种。所述刺激物为rv3874和rv3875的组合。图3是本发明实施例提供的试剂盒的γ-干扰素定量检测剂量-反应曲线图。下面结合具体实施例对本发明的技术方案作进一步描述。实施例1本发明实施例提供的结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒包括:1)测试反应杯,其内包被有链霉亲和素、联接有生物素化γ-干扰素单克隆抗体,并含有铕标记γ-干扰素单克隆抗体。2)校准品反应杯,其内包被有链霉亲和素、联接有生物素化γ-干扰素单克隆抗体,并含有铕标记γ-干扰素单克隆抗体及不同浓度的校准品。校准品含0,6,300,15000pg/ml的γ-干扰素抗原。3)空白对照培养管,其内含有15iu/ml血的肝素钠,且内部为真空负压状态。4)测试培养管,其内含有15iu/ml血的肝素钠和5μg/ml的rv3874(cfp-10)和rv3875(esat-6)的组合,且内部为真空负压状态。5)阳性对照培养管,其内含有15iu/ml血的肝素钠,以及10μg/ml植物血凝素l,且内部为真空负压状态。6)实验缓冲液,其内含有0.15mol/l的氯化钠、0.6ml/l的吐温-20、30ppm的防腐剂、100μmol/l的乙二胺四乙酸的5mmol/l,ph7.8的4-羟乙基哌嗪乙磺酸缓冲液。7)浓缩洗液,其内含有1.125g/l的氯化钠、0.2ml/l的吐温-20、30ppm的防腐剂的50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸缓冲液。所述测试反应杯的制备方法为:将链霉亲和素用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度5μg/ml,取50μl加入到空白反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤1次。生物素化γ-干扰素单克隆抗体用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度5μg/ml,取50μl加入到包被有链霉亲和素的反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤2次。然后每个杯中小心加入50μl隔离层溶液,在(36±1)℃、5%湿度条件下过夜干燥,然后在隔离层上小心加入1μl最适工作浓度200ng/ml的铕标记γ-干扰素单克隆抗体,立即在60℃的热风下吹干,并真空过塑包装,2~8℃保存备用。所述隔离层使用的隔离层溶液为含有0.12mol/l的氯化钠、0.38g/l的叠氮钠、10g/l的牛γ球蛋白、50g/l的牛血清白蛋白、50g/l的海藻糖、0.8g/l原生鼠igg、0.05g/l的变性小鼠igg、2g/l酪蛋白、37.5u/ml的肝素钠的50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸。其中的稀释铕标记γ-干扰素单克隆抗体的溶液为含有150mmol/l的氯化钠、0.5g/l的叠氮钠、2g/l的去离子牛血清白蛋白、125g/l的海藻糖的50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸。其中的铕标记γ-干扰素单克隆抗体制备方法为,标记用γ-干扰素单克隆抗体中的液体用nap-10柱置换成50mmol/l,ph9.0的碳酸盐缓冲液,并使标记抗体的浓度达到2~5mg/ml,并与3倍质量的铕的4-[2-(4-异硫氰基苯基)乙炔基]-2,6双{[n,n双(羧甲基)-氨基]甲基}吡啶试剂混合在2~8℃下振荡孵育(22±2)h,反应液用50mmol/l,ph7.80三羟甲基氨基甲烷-盐酸缓冲液平衡的sepharosecl-6b柱(1cm×40cm)层析,分别a280监测收集蛋白洗脱峰。其中,空白对照培养管的外安全帽颜色为绿色。测试培养管的外安全帽颜色为黄色。阳性对照培养管的外安全帽颜色为红色。在本发明实施例,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的制备方法包括:本实施例的试剂盒制备方法,包括以下步骤:1)制备测试反应杯:使用本实施例结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒中的测试反应杯的制备方法进行制备。2)制备校准品的反应杯:以英国国家生物制品检定所(nationalinstituteforbiologicalstandardsandcontrol,nibsc)编号87/586的γ-干扰素生物参考标准品(1iu/ml≈50pg/ml)为对照,将重组γ-干扰素抗原用步骤1)中的隔离层溶液稀释成0,6,300,15000pg/ml的校准品,在步骤1)的基础上的测试反应杯中的铕标记γ-干扰素单克隆抗体层上小心加入10μl的校准品,立即在60℃的热风下吹干,校准品每浓度设置2孔,并真空过塑包装,2~8℃保存备用。3)制备空白对照培养管:在洁净的试管(塑料或玻璃)中加入15iu/ml血的肝素钠。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,空白对照培养管的外安全帽颜色采用绿色。4)制备测试培养管:在洁净的试管(塑料或玻璃)中加入15iu/ml血的肝素钠,以及5μg/ml的rv3874(cfp-10)和rv3875(esat-6)的组合。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,外安全帽颜色采用黄色。5)制备阳性对照培养管:在洁净的试管(塑料或玻璃)中加入15iu/ml血的肝素钠,以及10μg/ml的植物血凝素l。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,阳性对照培养管的外安全帽颜色采用红色。6)制备实验缓冲液:5mmol/l,ph7.8的4-羟乙基哌嗪乙磺酸缓冲液中含有0.15mol/l的氯化钠、0.6ml/l的吐温-20、30ppm的防腐剂、100μmol/l的乙二胺四乙酸。分装成半成品。7)制备浓缩洗液:50mmol/l,ph7.8的三羟甲基氨基甲烷-盐酸缓冲液中含有1.125g/l的氯化钠、0.2ml/l的吐温-20、30ppm的防腐剂。分装成半成品。8)分装实验缓冲液和浓缩洗液。9)贴标签。10)成品组装。上述步骤所得产品分装即为半成品。抽出3份经过特异性、精密性、灵敏度及稳定性检定合格才能组装成结核感染t细胞检测试剂盒(体外释放免疫荧光法)。组装完成后还需抽检合格后才能出厂。在本发明实施例,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的检测方法包括以下步骤:1)人γ-干扰素的体外释放:①按空白对照管n,测试管t和阳性对照管p的顺序,在3种培养管中分别抽取或加入1ml全血样本(肝素钠或肝素钾抗凝),立刻颠倒混匀6次以上,使3种培养管中的内容物与血液充分混匀。②将以上加有全血的3种培养管在血液采集后4小时内放入37(±1)℃恒温培养箱中培养16~24小时。培养过程中保持培养管直立。③培养结束后,将培养管以3000~5000r/min的转速离心10min,取血浆以用于检测各培养管中γ-干扰素的浓度。在吸取血浆样本时必须特别注意不要扰动血细胞。如不能及时检测,必须将上清血浆从培养管取出,置于1.5ml的洁净离心管中,2~8℃存放7天,长期储存应在至少-20℃条件下保存,冻融次数应不高于3次。2)人γ-干扰素的定量检测:(1)试剂准备将试剂及所需数量的测试反应杯和校准品反应杯平衡至室温(20~25℃)。余下的反应杯及时置入自封袋密闭并于2~8℃保存。(2)试验操作①每浓度的校准品预设2孔,在校准品反应杯中加入30μl实验缓冲液(校准品浓度成为0,2,100,5000pg/ml),吸取10μl样本以及吸取20μl的实验缓冲液依次加入测试反应杯中。②反应杯在37℃下,振荡孵育10min。③孵育结束后,用洗涤液洗涤4次。④在60℃热风下干燥35s。⑤采用时间分辨荧光免疫分析仪进行荧光值计数分析。图1为本发明试剂盒的γ-干扰素定量检测剂量-反应曲线。实施例2本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒包括:1)测试反应杯,其内包被有链霉亲和素、生物素化γ-干扰素单克隆抗体及铕标记γ-干扰素单克隆抗体。2)校准品反应杯,同实施例1。3)空白对照培养管,其内含有9.8iu/ml血的肝素钾,且内部为真空负压状态。4)测试培养管,其内含有9.8iu/ml血的肝素钾和1μg/ml的rv3874(cfp-10)和rv3875(esat-6)的嵌合重组抗体,且内部为真空负压状态。5)阳性对照培养管,其内含有9.8iu/ml血的肝素钾,以及1μg/ml刀豆凝集素(cona),且内部为真空负压状态。6)实验缓冲液,同实施例1。7)浓缩洗液,同实施例1。所述测试反应杯的制备方法为:将链霉亲和素用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度0.1μg/ml,取50μl加入到空白反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤1次。生物素化γ-干扰素单克隆抗体用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度0.1μg/ml,取50μl加入到包被有链霉亲和素的反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤2次。然后每个杯中小心加入50μl隔离层溶液,在(36±1)℃、5%湿度条件下过夜干燥,然后在隔离层上小心加入1μl最适工作浓度100ng/ml的铕标记γ-干扰素单克隆抗体,立即在60℃的热风下吹干,并真空过塑包装,2~8℃保存备用。所述隔离层使用的隔离层溶液同实施例1。其中的稀释铕标记γ-干扰素单克隆抗体的溶液同实施例1。其中的铕标记γ-干扰素单克隆抗体制备方法同实施例1。其中,空白对照培养管的外安全帽颜色为绿色。测试培养管的外安全帽颜色为黄色。阳性对照培养管的外安全帽颜色为红色。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的制备方法包括以下步骤:1)制备测试反应杯:使用本实施例结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒中的测试反应杯的制备方法进行制备。2)制备校准品的反应杯:同实施例1。3)制备空白对照培养管:在洁净的试管(塑料或玻璃)中加入9.8iu/ml血的肝素钾。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,空白对照培养管的外安全帽颜色采用绿色。4)制备测试培养管:在洁净的试管(塑料或玻璃)中加入9.8iu/ml血的肝素钾,以及1μg/ml的rv3874(cfp-10)和rv3875(esat-6)的嵌合重组抗体。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,外安全帽颜色采用黄色。5)制备阳性对照培养管:在洁净的试管(塑料或玻璃)中加入9.8iu/ml血的肝素钾,以及1μg/ml的刀豆凝集素(cona)。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,阳性对照培养管的外安全帽颜色采用红色。6)制备实验缓冲液:同实施例1。7)制备浓缩洗液:同实施例1。8)分装实验缓冲液和浓缩洗液。9)贴标签。10)成品组装。上述步骤所得产品分装即为半成品。抽出3份经过特异性、精密性、灵敏度及稳定性检定合格才能组装成结核感染t细胞检测试剂盒(体外释放免疫荧光法)。组装完成后还需抽检合格后才能出厂。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的检测方法包括:本实施例的试剂盒的检测方法同实施例1。实施例3本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒包括:1)测试反应杯,其内包被有链霉亲和素、生物素化γ-干扰素单克隆抗体及铕标记γ-干扰素单克隆抗体。2)校准品反应杯,同实施例1。3)空白对照培养管,其内含有28iu/ml血的肝素钠,且内部为真空负压状态。4)测试培养管,其内含有28iu/ml血的肝素钠和10μg/ml的rv0733,且内部为真空负压状态。5)阳性对照培养管,其内含有28iu/ml血的肝素钠,以及20μg/ml刀豆凝集素(cona),且内部为真空负压状态。6)实验缓冲液,同实施例1。7)浓缩洗液,同实施例1。所述测试反应杯的制备方法为:将链霉亲和素用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度10μg/ml,取50μl加入到空白反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤1次。生物素化γ-干扰素单克隆抗体用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度10μg/ml,取50μl加入到包被有链霉亲和素的反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤2次。然后每个杯中小心加入50μl隔离层溶液,在(36±1)℃、5%湿度条件下过夜干燥,然后在隔离层上小心加入1μl最适工作浓度400ng/ml的铕标记γ-干扰素单克隆抗体,立即在60℃的热风下吹干,并真空过塑包装,2~8℃保存备用。所述隔离层使用的隔离层溶液同实施例1。其中的稀释铕标记γ-干扰素单克隆抗体的溶液同实施例1。其中的铕标记γ-干扰素单克隆抗体制备方法同实施例1。其中,空白对照培养管的外安全帽颜色为绿色。测试培养管的外安全帽颜色为黄色。阳性对照培养管的外安全帽颜色为红色。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的制备方法包括:1)制备测试反应杯:使用本实施例结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒中的测试反应杯的制备方法进行制备。2)制备校准品的反应杯:同实施例1。3)制备空白对照培养管:在洁净的试管(塑料或玻璃)中加入28iu/ml血的肝素钠。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,空白对照培养管的外安全帽颜色采用绿色。4)制备测试培养管:在洁净的试管(塑料或玻璃)中加入28iu/ml血的肝素钠,以及10μg/ml的rv0733。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,外安全帽颜色采用黄色。5)制备阳性对照培养管:在洁净的试管(塑料或玻璃)中加入28iu/ml血的肝素钠,以及20μg/ml的刀豆凝集素(cona)。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,阳性对照培养管的外安全帽颜色采用红色。6)制备实验缓冲液:同实施例1。7)制备浓缩洗液:同实施例1。8)分装实验缓冲液和浓缩洗液。9)贴标签。10)成品组装。上述步骤所得产品分装即为半成品。抽出3份经过特异性、精密性、灵敏度及稳定性检定合格才能组装成结核感染t细胞检测试剂盒(体外释放免疫荧光法)。组装完成后还需抽检合格后才能出厂。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的检测方法包括:本实施例的试剂盒的检测方法同实施例1。实施例4本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒包括:1)测试反应杯,其内包被有链霉亲和素、生物素化γ-干扰素单克隆抗体及铕标记γ-干扰素单克隆抗体。2)校准品反应杯,同实施例1。3)空白对照培养管,其内含有20iu/ml血的肝素钾,且内部为真空负压状态。4)测试培养管,其内含有20iu/ml血的肝素钾和6μg/ml的rv1978、rv1980、rv1981c、rv1984、rv1985c和rv2654c的组合物,且内部为真空负压状态。5)阳性对照培养管,其内含有20iu/ml血的肝素钾,以及12μg/ml刀豆凝集素(cona),且内部为真空负压状态。6)实验缓冲液,同实施例1。7)浓缩洗液,同实施例1。所述测试反应杯的制备方法为:将链霉亲和素用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度6μg/ml,取50μl加入到空白反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤1次。生物素化γ-干扰素单克隆抗体用50mmol/l,ph7.8的磷酸缓冲液稀释成最适浓度6μg/ml,取50μl加入到包被有链霉亲和素的反应杯中,2~8℃冰箱中孵育(22±2)h,洗涤2次。然后每个杯中小心加入50μl隔离层溶液,在(36±1)℃、5%湿度条件下过夜干燥,然后在隔离层上小心加入1μl最适工作浓度300ng/ml的铕标记γ-干扰素单克隆抗体,立即在60℃的热风下吹干,并真空过塑包装,2~8℃保存备用。所述隔离层使用的隔离层溶液同实施例1。其中的稀释铕标记γ-干扰素单克隆抗体的溶液同实施例1。其中的铕标记γ-干扰素单克隆抗体制备方法同实施例1。其中,空白对照培养管的外安全帽颜色为绿色。测试培养管的外安全帽颜色为黄色。阳性对照培养管的外安全帽颜色为红色。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的制备方法包括以下步骤:1)制备测试反应杯:使用本实施例结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒中的测试反应杯的制备方法进行制备。2)制备校准品的反应杯:同实施例1。3)制备空白对照培养管:在洁净的试管(塑料或玻璃)中加入20iu/ml血的肝素钠。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,空白对照培养管的外安全帽颜色采用绿色。4)制备测试培养管:在洁净的试管(塑料或玻璃)中加入20iu/ml血的肝素钠,以及6μg/ml的rv1978、rv1980c、rv1981c、rv1984c、rv1985c和rv2654c的组合物。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,外安全帽颜色采用黄色。5)制备阳性对照培养管:在洁净的试管(塑料或玻璃)中加入20iu/ml血的肝素钠,以及12μg/ml的刀豆凝集素(cona)。试管直立放入全自动抽真空压盖机中,使试管内真空负压为1ml/管。培养管的盖子含有内塞和其匹配外安全帽,阳性对照培养管的外安全帽颜色采用红色。6)制备实验缓冲液:同实施例1。7)制备浓缩洗液:同实施例1。8)分装实验缓冲液和浓缩洗液。9)贴标签。10)成品组装。上述步骤所得产品分装即为半成品。抽出3份经过特异性、精密性、灵敏度及稳定性检定合格才能组装成结核感染t细胞检测试剂盒(体外释放免疫荧光法)。组装完成后还需抽检合格后才能出厂。本发明实施例中,结核感染t细胞检测的干试剂快速时间分辨荧光免疫分析试剂盒的检测方法包括:本实施例的试剂盒的检测方法同实施例1。实施例5本发明实施例中,本发明的试剂盒的阳性判断值或参考区间的验证包括:本发明制备的结核感染t细胞检测试剂盒(体外释放免疫荧光法)的阳性判断值,参考中华人民共和国出入境检验检疫行业标准—sn/t3312-2012结核分枝杆菌γ-干扰素体外检测方法中的结果判定方法进行判读,其判读方法如表1。表1结核分枝杆菌γ-干扰素体外检测方法中的结果判定方法注:表中n为空白对照管n中γ-干扰素的浓度,p为阳性对照管p中γ-干扰素的浓度,t为测试管t中γ-干扰素的浓度。验证试验:采集到全血样本共448例。其中样本类型如下:(1)通过痰液涂片或者痰液培养确定为活动性结核病的受试者的静脉血,77例。(2)痰液涂片和痰液培养阴性,但是通过其他方式(诊断性治疗前后两张胸片显示有效。支气管灌洗液、胸部x射线检查,病理学检查,ppd强阳性者中有两项阳性者)确认为结核分枝杆菌感染者的静脉血,80份。(3)按中华医学会临床诊疗指南结核病分册中要求临床确诊的肺外结核的受试者的静脉血,25例。(4)肺癌、非结核呼吸道疾病及确诊其他疾病患者114例。衣原体感染5例,妊娠7例。(5)经问卷调查来自结核杆菌低暴露风险人群,均无临床症状,无结核病接触史,胸部x线检查正常,结核菌素试验阴性的查体健康人群134例。(5)门诊待诊病例7例。结果如表2~表3。按照以上行业标准的结果判读方法,以临床诊断为“金标准”,结核病组的阳性符合率为99.45%,非结核病组的阴性符合率为96.54%,符合报道的结核感染t细胞的γ-干扰素体外释放法的质量控制方法的要求:阳性参考品符合率不低于75%,阴性参考品符合率为不低于75%。可以按照行业标准的结核分枝杆菌γ-干扰素体外检测方法中的结果判定方法进行判读结果。表2448例样本的结果分布情况表3448例样本的结果符合性实施例6本发明的试剂盒的分析性能评价指标包括:本发明的结核感染t细胞检测试剂盒(体外释放免疫荧光法)的性能评价指标如下:1)空白限:平行检测校准品a10孔,计算其检测荧光值的均值和标准差(s),利用剂量-反应曲线计算出对应的浓度值为空白限,空白限优于2pg/ml。2)阴性参考品符合率:检测20份无结核病临床症状的健康志愿者的新鲜外周抗凝血样本,其阴性参考品符合率应不低于80%。具体要求:无结核病临床症状的健康志愿者应包含不同等级的结核菌素皮试人群,即应包含结核菌素皮试强阳性者(72h硬结或红晕直径≥15mm或伴有水泡)、结核菌素皮试阳性者(72h硬结或红晕直径≥5mm)和结核菌素皮试阴性者(72h硬结或红晕直径<5mm)这3种类型。3)阳性参考品符合率:检测10份结核分枝杆菌涂片和(或)培养阳性的结核病患者(菌阳)的新鲜外周抗凝血样本和10份结核分枝杆菌涂片和(或)培养阴性的临床确诊结核病患者(菌阴)的新鲜外周抗凝血样本,其阳性参考品符合率应不低于80%。4)精密度:应用阳性刺激后血浆或者企业精密性参考品作为样品进行检测,平行测试10孔,计算浓度值的变异系数(cv)值,批内cv值应不高于10.0%。连续生产的3个批次试剂盒间的批间cv值应不高于20.0%。5)线性:在2~5000pg/ml线性范围内,线性相关系数r应不低于0.9900。6)准确性:在试剂盒校准品b~f范围内,用定标后的试剂盒配套校准品检测国际参考品或企业参考品,参考品的实测值与标示值的相对偏差应在±20.0%范围内。7)稳定性:在实际储存条件下保存至成品有效期后2个月内的样品对空白限、阴性参考品符合率、阳性参考品符合率、批内精密度、线性和准确性等指标进行检测,检测结果符合以上要求。实施例7本发明的试剂盒的干扰试验评价包括:本发明的结核感染t细胞检测试剂盒(体外释放免疫荧光法)的分析特异性评价如下:检测以下干扰样本,均无出现假阳性或假阴性结果。胆红素818μmol/l、血红蛋白180g/l、甘油三酯21.54mmol/l对本试剂盒的检测结果无干扰作用。表4干扰样本例数干扰样本例数妊娠10衣原体感染10克隆病5老年痴呆5三环类抗抑郁症药物5非甾体类抗炎药物15t细胞活化抑制剂5非结核分枝杆菌感染5过敏15糖尿病10细菌感染10烧伤5糖皮质激素10hiv5既往肿瘤患者10既往免疫系统疾病10微生物污染5溶血10脂血10黄疸10卡介苗15实施例8本发明的试剂盒与参比试剂盒的等效性评价包括:本发明制备的结核感染t细胞检测试剂盒(体外释放免疫荧光法)的等效性评价如下:340例临床试验样本中,包括了165例经本临床试验规定的结核诊断标准确诊的住院结核患者样本,25例门诊样本,70例肺癌及非结核呼吸道疾病患者样本,40例查体健康人样本,40例高危人群样本。以临床诊断为金标准,待评价试剂在结核组的灵敏度可达85.71%,在非结核及健康人群中的特异性可达84.43%,粗一致率可达85.19%。以北京万泰生物药业股份有限公司生产的结核感染t细胞检测试剂盒(体外释放酶联免疫法)为对照试剂,结果详见表5和表6。表5样本类型及检出率表6待评价试剂和对照试剂检测结果比较待评价试剂盒与对照试剂盒检测临床样本结果具有正关联性(rp=0.70)。阳性符合率达100%。阴性符合率达98.11%。总符合率p0为99.12%。kappa指数为0.9824,为高度一致(κ>0.75),认为两系统等效。待评价试剂与对照试剂的阳性检出率结果差异无统计学意义(χ2=1.33<3.84,p>0.05),可以认为两种方法的检验结果一致。3例待评价试剂与对照试剂不符的样本,1例待评价试剂阳性而对照试剂阴性的标本为住院菌阴肺结核组患者样本,2例待评价试剂阴性而对照试剂阳性的标本为高危人群者样本,待评价试剂双孔复检结果与第一次试验结果符合,且ppd皮试为强阳性,但痰菌涂片检测结果为阴性,胸部x线检查未见异常,可能为潜伏性结核分枝杆菌感染者。根据临床试验结果建立四方格表,如表7。表7340份临床试验样本的对比试验评价结果本发明采用干试剂快速时间分辨荧光免疫分析技术,解决了以往的常规时间分辨荧光免疫分析技术试剂组分繁多,液态试剂不够稳定,操作繁琐,耗时较长的缺点。并且本发明解决了以往的结核感染t细胞测定中需要独立的采血管和培养管、操作繁杂、容易出错、自动化程度不高等缺点。本发明实现了采血管和培养管一体化,真空负压精确采血。3种培养管采用不同颜色标签和帽盖进行区分。全血培养过程中避免了采血管开盖、分装血样、二次标识等过程,防止了样本在采血管开盖、分装血样过程中的二次污染,减少了此过程中潜在的生物安全风险,也防止了二次标识过程产生的错误,并且全血培养后只要按常规离心后即可放置在全自动系统上进行取样检测,降低了工作强度和提高了工作效率。本发明的培养管具有采血管和培养管一体化、采血过程中减少了耗材使用、真空精确采血、适于自动化操作等特点。本发明的试剂盒具有检测结果准确性、灵敏度高、特异性强、稳定性好、检测方法简便、高效等特点,适合于即时检验(point-of-caretesting,poct)。以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1