一种快速同时检测苯乳酸、苯甲酸以及山梨酸的方法与流程
本发明属于食品检测领域,具体涉及一种快速同时检测苯乳酸、苯甲酸以及山梨酸的方法。
背景技术:
在食品生产过程中,为延长食品的保质期,往往会在加工过程中加入一些食品防腐剂。苯甲酸和山梨酸是最常用的人工合成食品防腐剂,但过多食用苯甲酸和山梨酸会影响人体对维生素和钙的吸收,加重人体肝脏负担,并引起毒症反应或诱发癌症。因此国家标准对苯甲酸、山梨酸的使用范围与限量做了严格规定。
除人工合成的食品防腐剂外,某些植物、动物、微生物本身或其代谢物中含有抗菌防腐的物质—天然防腐剂。1998年首次被发现的苯乳酸(pla),是一种广谱的杀菌剂、天然新型防腐剂,可以有效的防止食物腐败变质,而且对多种食源性致病菌都有很强的抑菌作用。苯乳酸可以由乳酸菌以苯丙氨酸为原料发酵产生,而苯丙氨酸作为一种常用氨基酸,广泛存在于动植物体内,故由发酵工艺生产的食品很可能含有苯乳酸。有研究者发现,苯乳酸与防腐剂联合作用,可以有效的减少食品中人工合成防腐剂的添加量。在未来天然防腐剂苯乳酸复合其他人工合成防腐剂使用可能会成为一种食品防腐的趋势。
目前,已报道的苯甲酸、山梨酸检测方法主要有色谱法和光谱法,如气相色谱法(gc)、毛细管电泳法(ce)、高效液相色谱法(hplc)、液相色谱-质谱联用法(lc-ms)、液相色谱-三重四极杆质谱法(lc-ms/ms)、时间飞行质谱法(lc-tof/ms)和表面增强拉曼光谱法(sers)等。但以上的检测方法都是针对常用防腐剂的检测,同时检测新型防腐剂——苯乳酸和其他食品防腐剂还未报道。因此建立一种快速的、同时检测苯乳酸、苯甲酸、山梨酸的方法是很有必要的。
本研究旨在建立一种同时检测发酵食品中天然防腐剂苯乳酸与人工合成防腐剂苯甲酸、山梨酸简便、快捷的高效液相色谱的分析方法,并将该方法运用于多种发酵食品检测,建立发酵食品中苯乳酸的本底数据库。
技术实现要素:
本发明目的在于建立一种同时检测发酵食品中天然防腐剂苯乳酸与人工合成防腐剂苯甲酸、山梨酸简便、快捷的高效液相色谱的分析方法。
本发明具体技术方案为:
1、一种快速同时检测苯乳酸、苯甲酸以及山梨酸的方法,所述方法包括如下步骤:
1)制备混合标准溶液:分别称取苯乳酸、苯甲酸、山梨酸的标准品,配制成具有浓度梯度的混合标准液;
2)制备待测样品溶液:
含有蛋白质的样品,称取2.5g样品于25ml比色管中,分别加入0.25mol/l亚铁氰化钾溶液和0.5mol/l乙酸锌溶液各1ml,用10%甲醇-水溶液定容,震荡2min,混匀,取10ml溶液4000rpm离心5min,取上层清液过0.22um聚醚砜滤膜得滤液备用;
不含蛋白质的样品:称取2.5g样品于25ml比色管中,用10%甲醇-水定容至10ml,涡旋震荡2min,混匀,取上层清液过0.22um聚醚砜滤膜得滤液备用;
3)检测仪器及检测条件:
仪器:高效液相色谱仪;检测器:uv检测器;色谱柱:c18柱,流动相:0.02mol/l乙酸铵和甲醇按体积比80:20混合而成;流速:1ml/min;进样量:20μl;进样方式:满环进样;检测波长:220nm;色谱柱温度:25℃;
4)绘制标准曲线:
将步骤1)配制的系列混合标准溶液注入高效液相色谱仪中,在步骤3)的色谱条件下进行洗脱和检测,以保留时间定性,根据各浓度所测峰面积的大小与其浓度的对应关系绘制标准曲线,并评估标准曲线线性度;
5)待测样品检测:
取步骤2)中待测样品溶液注入高效液相色谱仪中,在步骤3)的色谱条件下进行检测,测得滤液中各目标物的峰面积,以保留时间定性,根据4)中制作的标准曲线定量,计算出待测样品中苯乳酸、苯甲酸、山梨酸的含量。
优选的,步骤1)所述混合标准溶液所用稀释溶剂为蒸馏水。
优选的,步骤1)所述混合标准溶液中苯乳酸、苯甲酸、山梨酸浓度分别呈2mg/l,5mg/l,10mg/l,20mg/l,30mg/l,40mg/l,50mg/l的梯度系列。
优选的,步骤3)所述c18色谱柱的规格为250mm×4.6mm内径,颗粒粒径为5μm。
优选的,调节步骤3)所述流动相中0.02mol/l乙酸铵的ph为6.44,所述甲醇为含量大于99.8%的色谱纯。
优选的,通过以下方法验证检测准确度、精密度及回收率:将混合标准溶液不断稀释至信噪比s/n=3,以此进样浓度为检出限(lod),以10倍信噪比对应的浓度为定量下限(loq)。以原生醋做加标回收实验,通过计算回收率考察方法的准确度,以回收率的相对标准偏差(rsd)考察方法的精密度,在原生醋样品中添加混合标准溶液,加标水平分别为5,10,20mg/l,每个添加水平平行测定6次,并用下面的公式计算加标回收率;
其中,csm表示加标检测值;cm表示样品检测值;cs表示加标浓度。
优选的,本方法苯甲酸线性范围为0.01-50mg/l,苯乳酸为0.075-50mg/l,山梨酸为0.05-50mg/l,且线性相关性均大于0.998,检出限在0.01至0.05mg/l之间,定量限在0.025至0.25mg/l之间。
本发明有益效果在于:本发明公开的检测方法实现了在c18柱上同时快速地检测出苯乳酸、苯甲酸以及山梨酸,在优化的色谱条件下,实现11min内完成分离检测,且质量浓度在0.25-50mg/l范围内具有良好的线性关系,r2>0.998。该方法的检出限在0.01-0.05mg/l之间,定量限在0.025-0.25mg/l之间,回收率达到96.93-118.42%,精密度为0.93%-6.21%。表明该方法有较高的回收率和较好的精密度,完全能够满足日常发酵食品中苯乳酸、苯甲酸、山梨酸的分析检测。并且该方法无需复杂的样品前处理。
说明书附图
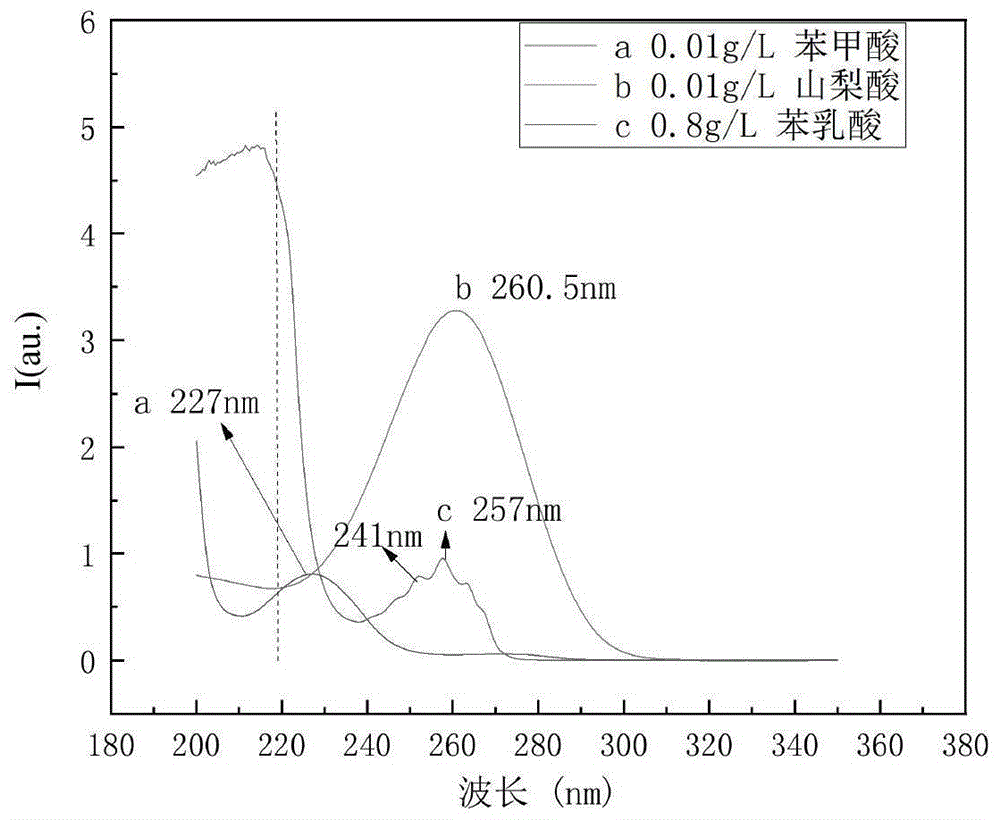
图1为在不同波长条件下苯乳酸、苯甲酸、山梨酸的紫外谱图;
图2为在不同流动相条件下,20mg/l混合标准液中苯乳酸、苯甲酸、山梨酸的色谱流出曲线。
具体实施方式
下面将结合说明书附图和具体实施例对本发明所述技术方案做进一步描述:
以下实施例所使用的色谱柱采用sapphiresiltmc18柱(5μm粒径,4.6mmi.d×250mm),检测器为uv检测器。
制备混合标准溶液:
分别称取苯乳酸、苯甲酸、山梨酸的标准品,配制成具有浓度梯度的混合标准液;所述混合标准溶液中苯乳酸、苯甲酸、山梨酸浓度分别呈2mg/l,5mg/l,10mg/l,20mg/l,30mg/l,40mg/l,50mg/l的梯度系列备用。
列举一种混合溶液的具体配制方法:分别取100mg/l苯乳酸0.1ml、100mg/l苯甲酸0.1ml、100mg/l山梨酸酸0.1ml于2ml离心管中,加入0.7ml蒸馏水,配置成10mg/l混合标准溶液。
样品前处理:
1)含蛋白质的样品
准确称取2.5g样品于25ml比色管中,分别加入0.25m亚铁氰化钾溶液和0.5m乙酸锌溶液各1ml,用10%甲醇-水定容,震荡2min,混匀,取10ml溶液4000rpm离心5min,取上层清液过0.22um聚醚砜滤膜,待上机。
2)其他样品
准确称取2.5g样品于25ml比色管中,用10%甲醇-水定容至10ml,涡旋震荡2min,混匀,取上层清液过0.22um聚醚砜滤膜,待上机。
色谱条件的优化
1)确定检测波长
分别使用0.01g/l苯甲酸、0.01g/l山梨酸、0.8g/l苯乳酸的混合溶液在不同检测波长下进行检测,图1为苯乳酸、苯甲酸、山梨酸的紫外吸收谱图。从图中可以看出待测组分都有紫外吸收,且各组分的最大吸收波长不同,但三种防腐剂在220nm处均有较强紫外吸收,为均衡三种防腐剂的检测灵敏度,故选择220nm作为检测波长。
2)确定流动相
以20mg/l的混合标准液作为实验对象,考察不同流动相对苯乳酸、苯甲酸、山梨酸分离效果的影响,以磷酸盐-甲醇、三氟乙酸-甲醇作流动相,三种防腐剂分离不完全;以0.02mol/l乙酸铵-甲醇作为流动相,通过优化乙酸铵ph为6.44与两相的体积配比为80:20时,苯乳酸、苯甲酸、山梨酸获得了较好的分离度且获得了合适的保留时间与较好的峰形,如图2所示。
3)确定流速
研究流动相流速对三种防腐剂分离的影响,发现1.0ml/min的流速是合适的分离速度。相比之下,将流速增加到1.2ml/min可以加速待分离化合物的洗脱速率,但压力会接近报警值;而将流速降低至0.5ml/min后,可以获得更好的分离参数,但分析运行时间长,不能实现快速分离。故选择1.0ml/min的流速进行后续实验。
4)确定色谱箱温度
考察22℃、25℃、30℃、35℃、40℃分别作为色谱柱箱温度对分离效果和保留时间的影响。随着色谱柱温度的升高,三种防腐剂物保留时间均前移。但22℃与40℃保留时间减少小于2min,同时考虑到能耗的问题,故选择25℃作为最佳色谱柱箱温度。
5)确定滤膜
考察不同滤膜对苯乳酸、苯甲酸、山梨酸的吸附作用的影响。以10mg/l的混合标样作为待过滤液,使用不同类型的滤膜过滤后上机检测,检测结果见表1。以上结果显示使用聚醚砜膜过滤的混合标样浓度的检测浓度与没有过膜的原液浓度更为接近,0.22um尼龙滤膜对苯乳酸、苯甲酸、山梨酸等有增强作用,其原因在于提取剂对尼龙滤膜有溶出作用。故选择聚醚砜滤膜作为样品过滤的滤膜。
表1不同滤膜的检测结果
方法验证
在以上确定的色谱条件下,以苯乳酸、苯甲酸、山梨酸的浓度为横轴(x),峰面积为纵轴(y),配制2,5,10,20,30,40,50mg/l的混合标准溶液并绘制标准曲线,从而评估方法的线性度。将混合标准溶液不断稀释至信噪比s/n=3,以此进样浓度为检出限(lod),以10倍信噪比对应的浓度为定量下限(loq)。通过以上方法验证,得到如表2所示的线性范围、相关系数、回归方程、检出限、定量限:
表2线性范围、相关系数、回归方程、检出限、定量限
由表2显示,通过检测条件的优化,本方法苯甲酸线性范围为0.01-50mg/l,苯乳酸为0.075-50mg/l,山梨酸为0.05-50mg/l,且线性相关性均大于0.998,检出限在0.01至0.05mg/l之间,定量限在0.025至0.25mg/l之间,该方法实现提供具有宽线性范围的灵敏检测。
样品加标回收试验
以原生醋做加标回收实验,通过计算回收率考察方法的准确度,以回收率的相对标准偏差(rsd)考察方法的精密度。在原生醋样品中添加混合标准溶液,加标水平分别为5,10,20mg/l,每个添加水平平行测定6次,并用下面的公式计算加标回收率。
其中,csm表示加标检测值;cm表示样品检测值;cs表示加标浓度。
本研究选取某原生醋作为加标回收试验。分别向样品中加入5、10、20mg/l不同浓度的苯乳酸、苯甲酸、山梨酸的混合标样,混匀,经过样品前处理后测定其回收率。每个添加水平平行测定6次,其结果见表3所示。
表3加标回收率(n=6)
由表3表明,本方法回收率达到96.93-118.42%,精密度达到0.93%-6.21%。表明该方法有较高的回收率和较好的精密度。
实际样品的检测
应用以上所建立的方法对购买自永辉超市和京东的样品进行检测,检测结果见表4。从表4中可以看出,许多食品并没有像生产厂商所承诺的那样,不含任何添加剂,大多数这样的食品里都含有不同程度的防腐剂。根据gb7718-94食品标签通用标准,样品中存在检出与样品标签不符的情况(2-3,5,11-17,19号),但对比国家食品添加剂的相关标准发现苯甲酸与山梨酸检出值均未超过添加限(1g/kg)。11到16号样品标签上都写着“三不加”,但是11-14号样品均有苯甲酸、山梨酸检出,15-16号样品有苯甲酸检出,且11,14,15号样品中检出的苯甲酸浓度较高。而4,6,18号样品与标签相符合。
表4实际样品的检测结果
nd——未检出
以上表明,本发明建立了hplc-uv快速检测食品中苯乳酸、苯甲酸、山梨酸,以分析标准品与样品的保留时间对应定性。在优化的色谱条件下,三种防腐剂在11分钟之内完成分离检测,检出限在0.01-0.05mg/l之间,定量限在0.025-0.25mg/l之间,回收率为96.93-118.42mg/l,精密度为0.93%-6.21%。并且本发明的优势在于样品前处理简单,无需复杂的样品前处理。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,尽管参照实施例对本发明进行了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的宗旨和范围,其均应涵盖在本发明的权利要求范围当中。
- 还没有人留言评论。精彩留言会获得点赞!