利用酶标仪及纳米金颗粒增强的SPR传感器来测定分子结合量的方法与流程
本发明实施例涉及检测技术领域,以c型反应性蛋白(crp)为例利用酶标仪及纳米金颗粒增强的spr传感器来测定分子结合量的方法。
背景技术:
分子相互作用动力学的测量在药物发现,遗传筛查和临床诊断中越来越重要,因为动态结合信息可以提高对疾病的认识和可以为治疗提供新思路。表面等离子体共振(spr)传感器,如商业biacorespr生物传感器系统,能够实时监测动力学生物分子相互作用,无需标记,不受大量背景的影响。由于商业biacorespr生物传感器系统属于传统spr设备,所以其需要特制的设备,专人的操作,使得购买或使用该生物传感器系统需要大量的金钱。
技术实现要素:
本发明所要解决的技术问题是针对现有技术中存在上述缺陷,提供一种以crp为例利用酶标仪及纳米金颗粒增强的spr传感器来测定分子结合量的方法,以解决商业biacorespr生物传感器系统检测成本较高的问题。
根据本发明,提供了一种利用酶标仪及纳米金颗粒增强的spr传感器来测定分子结合量的方法包括:
第一步骤:准备无底孔板以及特异性检测芯片;
第二步骤:制备用于放大检测信号的纳米金颗粒;
第三步骤:在无底孔板中,将特异性检测芯片覆盖待测样品捕获抗体;
第四步骤:配制待测样品浓度标准样品;
第五步骤:利用待测样品标记抗体标记纳米金颗粒,上述待测样品捕获抗体与该标记抗体互为配对抗体;
第六步骤:向标记好的纳米金颗粒中加入待测样品浓度标准样品,制备成混合溶液;
第七步骤:在向孔板中加入混合溶液之前,检测特异性检测芯片在特定波长下的光学密度;
第八步骤:向孔板中加入混合溶液,完成待测样品与标记纳米金颗粒复合物的捕获;
第九步骤:检测加入混合溶液后特异性检测芯片在特定波长下的光学密度,并比较该光学密度与第七步骤获得的光学密度之间的差值,实现待测样品定量检测。
优选地,用加入混合溶液前与加入混合溶液后的测试的od差值来表征crp与crp抗体间的接合量。
优选地,所述待测样品是c型反应性蛋白。
优选地,特定波长是580nm波长。
优选地,特异性检测芯片采用复制成形工艺制作,其中,利用激光干涉光刻在石英基板上制作锥形纳米柱图案,然后将紫外光固化聚合物均匀散布在模具上,顶部以聚对苯二甲酸乙二醇酯支撑;用紫外光进行固化处理,然后将聚对苯二甲酸乙二醇酯基板连同周期性纳米孔道图案从模具上剥除;通过电子束蒸发沉积形成一个钛粘附层和一个黄金层,以实现等离激元器件成形;然后利用射频等离子体溅射沉积二氧化钛谐振腔层,而后通过钛粘附层和顶部黄金层的电子束蒸发形成纳米谐振腔。
优选地,制备用于放大检测信号的纳米金颗粒包括:在去离子水中加入氯金酸溶液,加热至沸腾,然后再加入柠檬酸三钠溶液,继续加热并采用磁力搅拌器进行搅拌,溶液颜色由黑色变至橙红色,待溶液颜色恒定,再加热预定时间后停止加热并静置冷却至室温,得到au纳米颗粒分散溶液,即最终的纳米金颗粒。
优选地,纳米金颗粒的粒径为13~15nm。
优选地,将特异性检测芯片覆盖待测样品捕获抗体包括:在室温条件下将特异性检测芯片置于11-巯基十一烷酸溶液中,用乙醇清洗后吹干;加入1-乙烷基-3-3-二甲基氨丙基碳化二亚胺和n-羟基丁二酰亚胺的1:1混合液中孵育;孵育结束后立即放入单克隆抗crp捕获抗体内于冰箱中孵育,清洗后用吹干;加入牛血清白蛋白阻断液中室温孵育,去除牛血清白蛋白阻断液并加入乙醇胺溶液室温孵育,以覆盖未反应的nhs酯;去离子水清洗,吹干后放置于干燥环境中。
优选地,利用待测样品标记抗体标记纳米金颗粒包括:用k2co3溶液调节纳米金颗粒溶液ph至crp标记抗体的蛋白等电点,加入终浓度为6μg/ml的单克隆抗crp标记抗体,混匀后在室温孵育,然后加入终浓度为1%的牛血清白蛋白阻断液,室温孵育;利用离心机离心去除上清,复溶至原溶液体积的1/4。
优选地,第七步骤包括:取出覆盖了crp捕获抗体的芯片孔板,在待测试孔中加入去离子水,用酶标仪检测待测试孔在580nm波长下的od值;待孔中加入样品混合液并且反应完毕后,吸去样品混合液,并用去离子水清洗测试孔,再向测试孔中加入去离子水,检测测试孔在580nm波长下的od值。
本发明至少具有如下优点:利用普通酶标仪与纳米金颗粒实现生物分子之间定量测定,可最大限度减少特殊仪器系统需求;本发明具有选择性好、敏感度高等优点,而且由于被特定抗体标记后的纳米金颗粒可特异性结合crp蛋白,因此能进一步放大检测信号,且无需额外的检测标记物质,简化了检测过程,降低了检测成本;特别地,芯片在580nm段透射光强度的改变而对表面折射率的变化有极高的敏感性。
附图说明
结合附图,并通过参考下面的详细描述,将会更容易地对本发明有更完整的理解并且更容易地理解其伴随的优点和特征,其中:
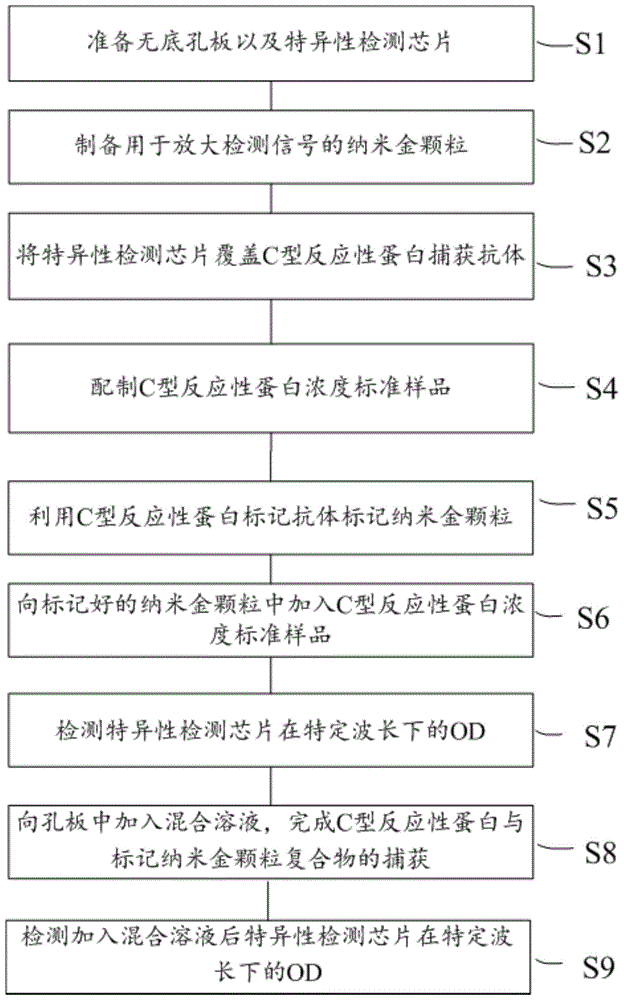
图1示意性地示出了根据本发明优选实施例的利用酶标仪及纳米金颗粒增强的spr传感器来测定分子结合量的方法的流程图。
图2示意性地示出了检测不同浓度的crp的od差值结果图。
图3示意性地示出了检测不同浓度的crp的光强变化率结果图。
需要说明的是,附图用于说明本发明,而非限制本发明。注意,表示结构的附图可能并非按比例绘制。并且,附图中,相同或者类似的元件标有相同或者类似的标号。
具体实施方式
为了使本发明的内容更加清楚和易懂,下面结合具体实施例和附图对本发明的内容进行详细描述。
本发明实施例提供的一种以crp为例利用酶标仪测定分子间动力学参数的方法。
以cpr作为示例蛋白是因为crp是机体受到微生物入侵或组织损伤等炎症性刺激时肝细胞合成的急性相蛋白,crp蛋白是感染或炎症的早期血液信号,可作为多种疾病的生物标记。健康受试者体内血清crp正常水平低于5μg/ml,其浓度在外来抗原出现几个小时后显著提高,随后48小时内甚至高可达300μg/ml2。通过检测crp的血液含量对疾病的诊断有积极的作用。
具体地,图1示意性地示出了根据本发明优选实施例的利用酶标仪及纳米金颗粒来测定分子结合量的方法的流程图。
如图1所示,根据本发明优选实施例的利用酶标仪及纳米金颗粒增强的spr传感器来测定分子结合量的方法包括:
第一步骤s1:准备无底孔板以及特异性检测芯片;
例如,无底孔板是无底96孔板,可通过打印方式制备。
第二步骤s2:制备用于放大检测信号的纳米金颗粒;优选地,纳米金颗粒的粒径为13~15nm。
第三步骤s3:在无底孔板中,将特异性检测芯片覆盖c型反应性蛋白捕获抗体;
第四步骤s4:配制c型反应性蛋白浓度标准样品;
第五步骤s5:利用c型反应性蛋白标记抗体标记纳米金颗粒,上述c型反应性蛋白捕获抗体与该标记抗体互为配对抗体;
第六步骤s6:向标记好的纳米金颗粒中加入c型反应性蛋白浓度标准样品,制备成混合溶液;
第七步骤s7:在向孔板中加入混合溶液之前,检测特异性检测芯片在特定波长(例如,580nm波长)下的od(光学密度);
第八步骤s8:向孔板中加入混合溶液,完成c型反应性蛋白与标记纳米金颗粒复合物的捕获;
第九步骤s9:检测加入混合溶液后特异性检测芯片在特定波长(例如,580nm波长)下的od(光学密度),并比较该od与第七步骤获得的od之间的差值,实现c型反应性蛋白定量检测。具体地,可用加样前后的测试孔od差值来表征crp与crp抗体间的接合量,由此实现crp定量检测。
下面描述本发明优选实施例的具体示例。
作为具体示例,例如,特异性检测芯片采用复制成形工艺。具体地,制备特异性检测芯片方法如下,利用激光干涉光刻在石英基板上制作锥形纳米柱图案,然后将紫外光固化聚合物(例如,noa-61)均匀散布在模具上,顶部以聚对苯二甲酸乙二醇酯支撑;用紫外光进行固化处理,然后将聚对苯二甲酸乙二醇酯基板连同周期性纳米孔道图案从模具上仔细剥除;通过电子束蒸发沉积形成一个钛粘附层和一个黄金层,以实现等离激元器件成形,然后利用射频等离子体溅射沉积二氧化钛谐振腔层,而后通过钛粘附层和顶部黄金层的电子束蒸发形成纳米谐振腔。其中优选地,钛黏附层、黄金层和二氧化钛谐振腔层的厚度分别是16nm、220nm和180nm,固化处理的时间为3分钟。
优选地,制备纳米金颗粒的方法如下,在100ml去离子水中加入1ml1%氯金酸溶液,加热至沸腾,然后再加入4ml1%柠檬酸三钠溶液,继续加热并采用磁力搅拌器进行搅拌,溶液颜色会由黑色变至橙红色,待溶液颜色恒定,再加热15分钟后停止加热。静置,冷却至室温,即可得到澄清透亮的au纳米颗粒分散溶液,即最终的纳米金颗粒。
优选地,将特异性检测芯片覆盖c型反应性蛋白捕获抗体包括:在室温条件下将特异性检测芯片置于1mm11-巯基十一烷酸溶液中12小时,用70%乙醇清洗后以氮气吹干;加入400×10-3m1-乙烷基-3-3-二甲基氨丙基碳化二亚胺和100×10-3mn-羟基丁二酰亚胺的1:1混合液中孵育30分钟;孵育结束后立即放入50μg/ml单克隆抗crp捕获抗体内于4度冰箱中孵育5小时,pbs清洗两次后用氮气吹干;加入30μg/ml牛血清白蛋白阻断液中室温孵育30分钟,去除牛血清白蛋白阻断液并加入10%乙醇胺溶液室温孵育30分钟,以覆盖未反应的nhs酯;去离子水清洗后两次后,氮气吹干后放置于干燥环境中。
进一步的,优选地,配制crp浓度标准样品的方法如下,采用250μg/ml的crp蛋白溶液为母液,稀释配制为不同浓度梯度的crp标准样品溶液(10ng/ml~10μg/ml);稀释底液为pbs缓冲液,现配现用。
优选地,crp标记抗体标记纳米金颗粒的方法如下,用例如0.1mk2co3溶液调节纳米金颗粒溶液ph至crp标记抗体的蛋白等电点,加入终浓度为6μg/ml的单克隆抗crp标记抗体,混匀后在室温孵育30分钟,然后加入终浓度为1%的牛血清白蛋白阻断液,室温孵育10分钟。设置离心机转速为9000rpm/min,离心25分钟,去除上清,复溶至原溶液体积的1/4。
优选地,配制crp浓度标准样品的方法包括采用250μg/ml的crp蛋白溶液为母液,稀释配制为不同浓度梯度的crp标准样品溶液(10ng/ml~10μg/ml);稀释底液为pbs缓冲液。例如,可采用250μg/ml的crp蛋白溶液稀释配制为6种浓度梯度的crp标准样品溶液,分别为10ng/ml、50ng/ml、500ng/ml、1μg/ml、5μg/ml和10μg/ml;稀释底液为pbs缓冲液。
对于检测crp浓度标准样品信号的测定,例如,采用等离光子谐振技术及光敏传感的方法检测crp标准样品浓度;将crp标准样品加入到crp标记抗体标记过的纳米金颗粒复溶液中,混匀后,将混合物加入到覆盖了crp捕获抗体的芯片孔板中,再将孔板放入酶标仪中震荡反应30分钟,记录反应前后od差值,进一步转化为光强变化值,依据所得数据计算标准曲线。
检测加样前后580nm波长下的芯片孔od值的方法例如如下:加样前,取出覆盖了crp捕获抗体的芯片孔板,在待测试孔中加入100μl去离子水,用酶标仪检测待测试孔在580nm波长下的od值。待孔中加入样品混合液并且反应完毕后,吸去样品混合液,并用去离子水清洗测试孔2次,再向测试孔中加入100μl去离子水,检测测试孔在580nm波长下的od值。
通过数据检测验证该方法的可行性,通过对不同浓度的crp进行检测,其od差值结果图如图3所示,最终通过算法求得的光强变化率,光强变化率与crp的浓度成正比,证明此方法的可行性。
本发明的上述实施例至少具有如下优点:利用普通酶标仪与纳米金颗粒增强的spr传感器实现生物分子之间定量测定,可最大限度减少特殊仪器系统需求;本发明具有选择性好、敏感度高等优点,而且由于被特定抗体标记后的纳米金颗粒可特异性结合crp蛋白,因此能进一步放大检测信号,且无需额外的检测标记物质,简化了检测过程,降低了检测成本;特别地,芯片在580nm段透射光强度的改变而对表面折射率的变化有极高的敏感性。
需要说明的是,除非特别指出,否则说明书中的术语“第一”、“第二”、“第三”等描述仅仅用于区分说明书中的各个组件、元素、步骤等,而不是用于表示各个组件、元素、步骤之间的逻辑关系或者顺序关系等。
可以理解的是,虽然本发明已以较佳实施例披露如上,然而上述实施例并非用以限定本发明。对于任何熟悉本领域的技术人员而言,在不脱离本发明技术方案范围情况下,都可利用上述揭示的技术内容对本发明技术方案作出许多可能的变动和修饰,或修改为等同变化的等效实施例。因此,凡是未脱离本发明技术方案的内容,依据本发明的技术实质对以上实施例所做的任何简单修改、等同变化及修饰,均仍属于本发明技术方案保护的范围内。
- 还没有人留言评论。精彩留言会获得点赞!