瑞德西韦有关物质及含量测定方法与流程
1.本发明涉及瑞德西韦的制备,尤其涉及瑞德西韦有关物质及含量测定方法。
背景技术:
2.瑞德西韦(remdesivir),是由吉利德科学公司gilead science开发的一种病毒rna依赖的rna聚合酶(rdrp)抑制剂。2020年10月22日,美国食品药品管理局(fda)批准了吉利德科学的抗病毒药物瑞德西韦用于治疗新冠住院患者,成为美国首个正式获批的新冠治疗药物。瑞德西韦的cas登记号为1809249
‑
37
‑
3,分子式为c
27
h
35
n6o8p,分子量为602.58,英文名为2
‑
ethylbutyln
‑
{(s)
‑
[2
‑
c
‑
(4
‑
aminopyrrolo[2,1
‑
f][1,2,4]triazin
‑7‑
yl)
‑
2,5
‑
anhydro
‑
d
‑
altrononitril
‑6‑
o
‑
yl]phenoxyphosphoryl}
‑
l
‑
alaninate,其化学结构为,
[0003][0004]
瑞德西韦作为原料药,在分析化学以及药物分析领域,瑞德西韦的杂质含量及瑞德西韦含量都要求被准确测定,在制备的过程中,一些杂质不能完全去除,需要鉴定成分,高效液相色谱能够精确的分离检测化合物,我们研究了一种借助高效液相色谱检测瑞德西韦成分的方法。
技术实现要素:
[0005]
本发明的目的在于克服现有技术中的不足,提供一种操作简单、检测精度高的瑞德西韦有关物质及含量测定方法。
[0006]
本发明是通过以下技术方案实现的:一种瑞德西韦有关物质及含量测定方法,包括以下步骤,
[0007]
a,配制标准溶液,称取瑞德西韦对照品,制取标准溶液;
[0008]
b,配制样品溶液,称取瑞德西韦供试品,制得高浓度供试品溶液和低浓度供试品溶液;
[0009]
c,进样高浓度供试品溶液,选择面积归一化法计算杂质含量;
[0010]
d,进样标准溶液和低浓度供试品溶液,选择外标法计算瑞德西韦的含量。
[0011]
进一步地,所述标准溶液中瑞德西韦对照品的浓度为2.00
‑
11.98μg/ml。
[0012]
进一步地,所述高浓度供试品溶液中瑞德西韦供试品浓度为0.9
‑
1.1mg/ml。
[0013]
进一步地,所述低浓度供试品溶液中瑞德西韦供试品浓度为2.0
‑
11.98μg/ml。
[0014]
进一步地,步骤a和步骤b中选用的流动相均由0.05%三氟乙酸水溶液和甲醇组成,0.05%三氟乙酸水溶液和甲醇的体积比为2:3。
[0015]
进一步地,反相高效液相色谱中色谱柱柱温为20
‑
25℃。
[0016]
进一步地,反相高效液相色谱中检测器为紫外检测器,检测波长为250
‑
260nm。
[0017]
进一步地,反相高效液相色谱中流速为1.0ml/min,进样量为20μl。
[0018]
进一步地,所述高浓度供试品溶液测定杂质含量分析时间为56
‑
63min。
[0019]
进一步地,所述低浓度供试品溶液及标准溶液测定瑞德西韦含量分析时间为18
‑
23min。
[0020]
本发明的有益效果在于:本发明基于高效液相色谱检测瑞德西韦的杂质含量及瑞德西韦含量,检测精度高、操作简单,无需进行梯度洗脱,即实现瑞德西韦与杂质的完全分离,最小分离度在1.2以上,有效第避免了各杂质之间的干扰。
附图说明
[0021]
图1是实施例1瑞德西韦的杂质测定供试品图谱;
[0022]
图2是实施例1瑞德西韦的含量测定供试品图谱;
[0023]
图3是实施例1瑞德西韦的含量测定线性关系图。
具体实施方式
[0024]
下面将结合发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0025]
以下各实施例中:
[0026]
瑞德西韦对照品为自制所得,瑞德西韦含量>97.0%;
[0027]
甲醇为色谱纯、三氟乙酸为分析纯、水为纯化水;
[0028]
高效液相色谱仪为岛津spd
‑
10avvp型高效液相色谱仪,色谱柱为c18硅烷键合硅胶填充色谱柱,检测器为紫外检测器,检测波长为254nm,色谱柱内径为4.6mm、长度为150mm、填料粒径为5μm;
[0029]
步骤a和步骤b中选用的流动相均由质量浓度为0.05%三氟乙酸水溶液和甲醇组成,0.05%三氟乙酸水溶液和甲醇的体积比为2:3;
[0030]
反相高效液相色谱中流速为1.0ml/min,进样量为20ul;
[0031]
高浓度供试品溶液测定杂质含量分析时间为60min;
[0032]
低浓度供试品溶液及标准溶液测定瑞德西韦含量分析时间为20min。
[0033]
称取瑞德西韦对照品和瑞德西韦供试品均使用分析天平进行称取,具体为梅特勒
‑
托利多ms105du型分析天平。
[0034]
步骤a中,配制标准溶液,称取瑞德西韦对照品,配制标准溶液,具体为,称取瑞德西韦对照品20mg,置20ml量瓶中,加流动相溶解并稀释至刻度,得到待稀标准液,量取待稀释标准液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,得到标准溶液,标准溶液瑞德西韦对照品含量为10μg/ml;
[0035]
步骤b中,高浓度供试品溶液的制备方法为,取瑞德西韦供试品20mg,置20ml量瓶中,加流动相溶解并稀释至刻度,摇匀,得到高浓度供试品溶液,瑞德西韦供试品含量1mg/ml;
[0036]
步骤b中,低浓度供试品溶液的制备方法为,取瑞德西韦供试20mg,置20ml量瓶中,加流动相溶解并稀释至刻度,得到待稀释低浓度供试品溶液,摇匀,得到高浓度供试品溶液,量取待稀释低浓度供试品溶液1ml,置100ml量瓶中,用流动相稀释至刻度,摇匀,得到低浓度供试品溶液,低浓度供试品溶液中瑞德西韦供试品含量为10μg/ml。
[0037]
步骤c
‑
d中,所用色谱柱为agilent zorbax eclipse xdb
‑
c18,尺寸为4.6mm
×
150mm,3.5μm;流动相为0.05%三氟乙酸水
‑
甲醇;检测波长为254nm;流速为1.0ml/min;进样体积为20μl;运行时间为60min,自动进样。
[0038]
申请人研究发现,标准溶液浓度按约10μg/ml配制,配制所得标准溶液的浓度可以有波动,9μg/ml
‑
11μg/ml都适用,通过线性与范围试验可知,瑞德西韦在2.00μg/ml
‑
11.98μg/ml浓度范围内,浓度和峰面积呈现线性关系,即在2.00μg/ml
‑
11.98μg/ml浓度范围内,瑞德西韦含量测定的结果均是可信的。
[0039]
高浓度供试品溶液按约1mg/ml配制,配制所得高浓度供试品溶液浓度可以有波动,0.9mg/ml
‑
1.1mg/ml都可以,在此浓度下,0.003%含量的杂质均能检出来,灵敏度较高。
[0040]
加入三氟乙酸能调节洗脱液的ph,同时作为离子对试剂与瑞德西韦会相互作用,能增强分离效果,样品峰形也较好,比例选择2:3时,瑞德西韦峰的保留时间为9
‑
10min,瑞德西韦峰与杂质峰的分离度也符合要求。
[0041]
尤其在检测的过程中,温度为25℃,选择室温25℃进行试验,经过验证此温度条件下耐用性也较好。
[0042]
实施例1
[0043]
一种瑞德西韦有关物质及含量测定方法,包括以下步骤,
[0044]
a,配制标准溶液,称取瑞德西韦对照品,配制标准溶液;
[0045]
b,配制样品溶液,称取瑞德西韦供试品,制得高浓度供试品溶液和低浓度供试品溶液;
[0046]
c,进样高浓度供试品溶液,按面积归一化法计算杂质含量;
[0047]
d,进样标准溶液和低浓度供试品溶液,按外标法以峰面积计算瑞德西韦的含量。
[0048]
步骤c得到的检测色谱图如图1,步骤d得到的标准溶液检测色谱图如图2,由图1可以看到,瑞德西韦主峰保留时间为9.411min,峰形良好,拖尾因子为1.502,瑞德西韦与杂质能够完全分离,最小分离度在1.2以上;
[0049]
由图2可以看出瑞德西韦主峰保留时间为9.792min,峰形良好,拖尾因子为1.324,理论塔板数为5890。
[0050]
检测时,需注意室温对主峰的保留时间会有影响,当室温较低时,主峰保留时间会靠后,当室温较高时,主峰保留时间会靠前。
[0051]
验证试验,
[0052]
1、验证实施例1提供的瑞德西韦成分检测方法的系统适应性。
[0053]
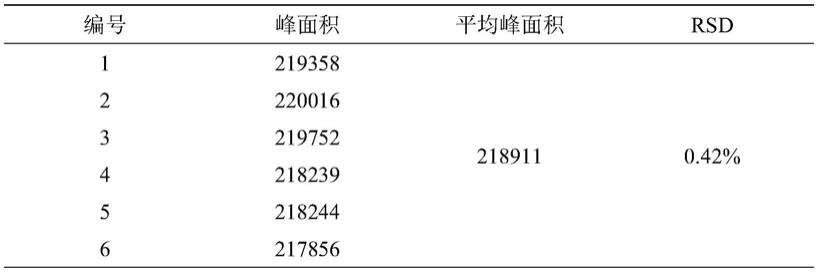
重复步骤d6次,检测结果见附表1。
[0054]
附表1
[0055][0056]
由附表1可以得到,重复进同一瑞德西韦对照品溶液6次,瑞德西韦峰面积rsd%为0.42%,符合药典中rsd%<2.0%的规定,进而说明本发明提供的瑞德西韦成分检测方法系统适用性良好。
[0057]
不同柱温检测结果见附表2。
[0058]
附表2
[0059]
条件未知杂质1未知杂质2未知杂质3瑞德西韦柱温25℃0.03%0.36%0.48%99.8%柱温20℃0.03%0.37%0.47%100.3%柱温30℃0.03%0.37%0.48%99.8%
[0060]
由附表2可以看到,在25℃环境下,检测稳定,可信度高。
[0061]
不同流速测结果见附表3。
[0062]
附表3
[0063]
条件未知杂质1未知杂质2未知杂质3瑞德西韦流速1.0ml/min0.03%0.36%0.48%99.8%流速0.9ml/min0.04%0.36%0.48%100.1%流速1.1ml/min0.03%0.36%0.48%100.0%
[0064]
由附表3可以看到,在0.9
‑
1.1ml/min流速情况下,检测结果变化并不明显,流速对检测的影响不大。
[0065]
杂质含量分析时间为60min,通过典型图谱可知,45.146min出现了杂质峰,后面无杂质峰出现,选择60min较为合适。通过耐用性也可知,60min较为合适,结果见下附表4。
[0066]
附表4
[0067]
条件最后的杂质峰保留试剂原条件45.146min柱温20℃46.914min柱温30℃46.998min流速0.9ml/min50.613min流速1.1ml/min38.141min
[0068]
参数有柱温25℃、流速1.0ml/min、检测波长为254nm、进样体积是20μl,都是选用常用参数,柱温、检测波长的变化对检测无影响,流速的变化会影响主峰的保留时间,进样体积为固定值,杂质含量耐用性结果见附表5。
[0069]
附表5
[0070][0071]
瑞德西韦含量测定耐用性结果如附表6。
[0072]
附表6
[0073][0074]
2、验证实施例1提供的瑞德西韦成分检测方法的线性范围。
[0075]
按照制取低浓度供试品溶液的制备方法,制备供试品含量分别为2.00μg/ml、4.99μg/ml、7.98μg/ml、9.98μg/ml、11.98μg/ml的系列瑞德西韦线性溶液,重复步骤c
‑
e6次,记录色谱图,以瑞德西韦的浓度为横坐标、峰面积为纵坐标,用最小二乘法进行线性回归,测试结果见图3。
[0076]
经标准曲线数据计算,得线性回归方程为y=21500.2979x+2065.1998,线性相关系数r为0.9999,符合药典规定r≥0.999,表明瑞德西韦在2.00
‑
11.98μg/ml范围内线性关
系良好。
[0077]
3、验证实施例1提供的瑞德西韦成分检测方法的重复性。
[0078]
上述已经说明,步骤b中,高浓度供试品溶液的制备方法为,取瑞德西韦供试品20mg,置20ml量瓶中,加流动相溶解并稀释至刻度,摇匀,得到高浓度供试品溶液,瑞德西韦供试品含量1mg/ml,现分别称取瑞德西韦供试品20.00mg、20.04mg、20.13mg、19.88mg、20.06mg、19.96mg配制高浓度供试品溶液,根据实施例1提供的瑞德西韦成分检测方法检测,测得各供试品溶液的含量如附表7所示。
[0079]
附表7
[0080][0081]
结果表明,瑞德西韦原料的平均含量为99.8%,含量rsd%为0.37%,符合药典中的规定,该规定具体为,待测定成分含量100%时,rsd%不大于1.0%,说明瑞德西韦成分检测方法重复性良好。
[0082]
4、验证实施例1提供的瑞德西韦成分检测方法的回收率。
[0083]
用瑞德西韦对照品及瑞德西韦原料配制低、中、高三种不同浓度的考察样,根据本发明提供的方法,平行3次测定,记录色谱图,测定结果所得回收率、平均回收率、rsd值如附表8所示。
[0084]
附表8
[0085][0086][0087]
由附表8可以知道,结果表明,回收率为98.49%
‑
100.29%,rsd%为0.69%,符合药典中的规定,具体为,带测定成分含量100%时,回收率限度98%
‑
101%,rsd%不大于2.0%,说明瑞德西韦成分检测方法准确度良好。
[0088]
5、验证实施例1提供的瑞德西韦成分检测方法的稳定性。
[0089]
配制低浓度供试品溶液,在5℃条件下放置,分别于0、13、19、30小时取样,根据本发明所述方法进样测定,记录色谱图,并根据瑞德西韦峰面积,计算rsd值如附表9所示。
[0090]
附表9
[0091][0092]
结果表明,瑞德西韦峰面积rsd%为0.42%,说明瑞德西韦成分检测方法稳定性良好。
[0093]
6、验证实施例1提供的瑞德西韦成分检测方法的定量限与检测限。
[0094]
以色谱图中瑞德西韦峰高与基线噪声之比(信噪比,s/n)约为3为最低检测限标准,如图2所示,本发明的提供的瑞德西韦成分检测方法检测限为0.03μg/ml;
[0095]
以色谱图中瑞德西韦峰高与基线噪声之比(信噪比,s/n)约为10为定量标准,如图2所示,本发明的提供的瑞德西韦成分检测方法检测限为0.10μg/ml。
[0096]
上述1
‑
6项验证结果表明,本发明提供的瑞德西韦成分检测方法,结果表明检测瑞德西韦含量在2.00
‑
11.98μg/ml范围内呈现良好的线性关系,回归方程为y=21500.2979x+2065.1998,相关系数r为0.9999,精密度、重复性、准确性良好,方法简单,含量测定准确可靠,无干扰峰,检测结果良好,能够用于瑞德西韦供试品的含量测定。
[0097]
最后应说明的是:以上所述仅为本发明的优选实施例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1