痕量微小核糖核酸的电化学检测方法与流程
1.本发明涉及微小核糖核酸检测领域,特别涉及一种痕量微小核糖核酸的电化学检测方法。
背景技术:
2.微小核糖核酸(mirna)是一类具有调控功能的小分子非编码核糖核酸,与人类多种疾病特别是肿瘤的发生发展有关。mirna的稳定性高、是一种极具潜力的肿瘤标志物,发展新型的mirna检测方法对于实现相关疾病的早期诊断具有重要的意义。常规的检测手段如northern blotting、荧光实时定量pcr、mirna芯片等往往具有特定的劣势,包括灵敏度、操作步骤、成本等,因而限制了这些方法的广泛应用。因此,有必要开发一种快速、简单、高灵敏度、低成本的新型mirna检测方法。
技术实现要素:
3.本发明所要解决的技术问题在于针对上述现有技术中的不足,提供一种痕量微小核糖核酸的电化学检测方法。
4.为解决上述技术问题,本发明采用的技术方案是:一种痕量微小核糖核酸的电化学检测方法,包括以下步骤:
5.1)在电极表面修饰dna探针probe a;
6.2)将步骤1)得到的电极置于需检测mirna浓度的样品中;
7.3)向步骤2)的样品中再加入dna探针probe b和probe c;
8.4)将步骤3)得到的电极浸泡到表面修饰有dna探针probe d的金纳米颗粒溶液中;
9.5)对步骤4)得到的电极进行电化学分析,通过电化学信号计算出样品中的待检测的mirna的浓度;
10.其中,probe a、probe b和probe c均为茎环结构dna,probe a的环状部分的序列与待检测的mirna互补配对,待检测的mirna可打开probe a的茎部;probe a的茎部打开后释放的单链dna序列可以依次打开probe b、probe c的茎环结构,发生杂交链式反应;probe b和probe c上暴露有相同序列的单链区域,probe d上具有与该单链区域互补配对的dna序列,使得probe a、probe b和probe c反应形成的长链能够捕获修饰有probe d的金纳米颗粒,从而能够实现通过反应后的电化学信号来表征待检测的mirna的浓度。
11.优选的是,待检测的mirna为mir
‑
21,其核酸序列为:
[0012]5’‑
uagcuuaucagacugauguuga
‑3’
;
[0013]
probe a的序列为:
[0014]5’‑
ataaggtttagcttatcaacatcagtctgataagctaaacctccc c
‑
(ch2)6‑
sh
‑3’
。
[0015]
优选的是,待检测的mirna为mir
‑
141,其核酸序列为:
[0016]5’‑
uaacacugucugguaaagaugg
‑3’
;
[0017]
probe a的序列为:
[0018]5’‑
ataaggtttagcatctttaccagacagtgtgctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0019]
优选的是,待检测的mirna为mir
‑
183,其核酸序列为:
[0020]5’‑
uauggcacugguagaauucacu
‑3’
;
[0021]
probe a的序列为:
[0022]5’‑
ataaggtttagctgaattctaccagtgccagctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0023]
优选的是,待检测的mirna为mir
‑
155,其核酸序列为:
[0024]5’‑
uuaaugcuaaucgugauagggguu
‑3’
;
[0025]
对应的probe a的序列为:
[0026]5’‑
ataaggtttagccctatcacgattagcattgctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0027]
优选的是,probe b的序列为:
[0028]5’‑
taagctaaaccttatgtacatttcgacgaataaggttaaccacct ccgata
‑3’
。
[0029]
优选的是,probe c的序列为:
[0030]5’‑
ataaggtttagcttaaaccttattcgtcgaaggccacctccgata
‑3’
。
[0031]
优选的是,probe d的序列为:5
’‑
sh
‑
(ch2)6‑
tttatcggaggtgg
‑
mb
‑3’
。
[0032]
优选的是,该方法包括以下步骤:
[0033]
1)将电极进行预处理,然后将电极浸泡在probe a溶液中反应,再使用巯基己醇处理,得到表面修饰有probe a的电极;
[0034]
2)将步骤1)得到的电极置于需检测mirna浓度的样品中;
[0035]
3)向步骤2)的样品中再加入dna探针probe b和probe c;
[0036]
4)将probe d和金纳米颗粒混合,充分反应后再加入nacl溶液,然后进行离心纯化后得到表面修饰有dna探针probe d的金纳米颗粒溶液;
[0037]
将步骤3)得到的电极使用双蒸水润洗后浸泡到表面修饰有dna探针probe d的金纳米颗粒溶液中;
[0038]
5)对步骤4)得到的电极进行电化学分析,通过得到的电化学信号与预先建立的表征mirna浓度与电化学信号强度关系的标准曲线计算出样品中的待检测的mirna的浓度。
[0039]
优选的是,该方法包括以下步骤:
[0040]
1)首先使用水虎鱼溶液处理电极5分钟,使用双蒸水清洗电极;然后打磨电极;随后把电极放入乙醇中超声处理5min,再放入双蒸水中超声处理5min;将处理后的电极放入硫酸中,进行循环伏安电化学处理;使用双蒸水清洗后,把电极浸泡在probe a溶液中,反应8小时;之后再将电极使用巯基己醇处理0.5小时,得到表面修饰有probe a的电极;
[0041]
2)将步骤1)得到的电极置于需检测mirna浓度的样品中,浸泡30分钟;
[0042]
3)向步骤2)的样品中再加入dna探针probe b和probe c,反应90分钟;
[0043]
4)将probe d和金纳米颗粒混合,反应16小时后再加入nacl溶液,24小时后进行离心纯化,得到表面修饰有dna探针probe d的金纳米颗粒溶液;
[0044]
将步骤3)得到的电极使用双蒸水润洗后浸泡到表面修饰有dna探针probe d的金纳米颗粒溶液中,反应60分钟;
[0045]
5)对步骤4)得到的电极进行电化学分析,通过得到的电化学信号与预先建立的表征mirna浓度与电化学信号强度关系的标准曲线计算出样品中的待检测的mirna的浓度。
[0046]
本发明的有益效果是:本发明提供的痕量微小核糖核酸的电化学检测方法,利用
目标mirna在电极界面诱导的茎环结构dna开环,释放杂交链式反应的触发链,实现电极表面的原位dna纳米结构生长,同时在产物侧链捕获修饰有互补dna序列的金纳米颗粒,最终通过检测纳米颗粒表面dna末端修饰的电信号分子,能实现对靶mirna浓度的高灵敏检测;且本发明的方法简单、快速、成本低,具有很好的推广应用前景。
附图说明
[0047]
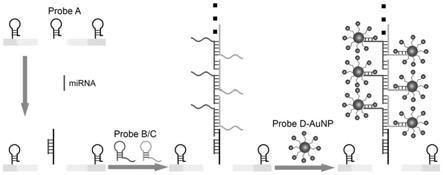
图1为本发明的痕量微小核糖核酸的电化学检测方法的检测原理示意图;
[0048]
图2为本发明的实施例1中建立标准曲线的结果;
[0049]
图3为本发明的实施例1中的反应物及产物的聚丙烯酰胺凝胶电泳表征图和杂链式反应产物与金纳米颗粒结合后的电镜表征图;
[0050]
图4为本发明的实施例1中的基于交流阻抗与方波伏安的mirna检测可行性分析结果;
[0051]
图5为本发明的实施例1中的方波伏安法用于错配mirna分析的结果。
具体实施方式
[0052]
下面结合实施例对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。
[0053]
应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它元件或其组合的存在或添加。
[0054]
本实施例的一种痕量微小核糖核酸的电化学检测方法,包括以下步骤:
[0055]
1)在电极表面修饰dna探针probe a;
[0056]
2)将步骤1)得到的电极置于需检测mirna浓度的样品中;
[0057]
3)向步骤2)的样品中再加入dna探针probe b和probe c;
[0058]
4)将步骤3)得到的电极浸泡到表面修饰有dna探针probe d的金纳米颗粒溶液中;
[0059]
5)对步骤4)得到的电极进行电化学分析,通过电化学信号计算出样品中的待检测的mirna的浓度;
[0060]
参照图1,本发明的方法的检测原理为:
[0061]
其中,probe a、probe b和probe c均为茎环结构dna,probe a的环状部分的序列与待检测的mirna互补配对,所以在待检测的mirna(靶mirna)存在时,电极表面修饰的probe a可以发生构象的改变:靶mirna可打开probe a的茎部;probe a的茎部打开后释放的单链dna序列可打开probe b的茎部,probe b释放出的环状部分与剩余的茎部组成的单链序列可以进一步打开probe c的茎部,同时probe c的环状部分与剩余的茎部组成的单链序列又可以打开另一条probe b的茎部,发生杂交链式反应;同时probe b和probe c预先经过改造,其上均暴露有相同序列的单链区域,且probe d上具有与该单链区域互补配对的dna序列,使得通过probe a、靶mirna的诱发,使probe b和probe c发生杂交链式反应形成的长链侧边暴露出该单链区域,通过该单链区域能够捕获修饰有probe d的金纳米颗粒(probe d
‑
aunp),在电化学检测中会表现出电化学信号的增强,从而能够利用反应后的电化学信号来表征待检测的mirna浓度。
[0062]
以上为本发明的总体构思,以下在其基础上结合更为具体的实施例对本发明作进
一步说明。
[0063]
实施例1
[0064]
本实施例中,待检测的mirna为mir
‑
21,其核酸序列为:
[0065]5’‑
uagcuuaucagacugauguuga
‑3’
。
[0066]
对应设计的dna探针序列具体如下:
[0067]
对应的probe a记为probe a
‑
21,其序列为:
[0068]5’‑
ataaggtttagcttatcaacatcagtctgataagctaaacctccc c
‑
(ch2)6‑
sh
‑3’
。
[0069]
probe b的序列为:
[0070]5’‑
taagctaaaccttatgtacatttcgacgaataaggttaaccacct ccgata
‑3’
。
[0071]
probe c的序列为:
[0072]5’‑
ataaggtttagcttaaaccttattcgtcgaaggccacctccgata
‑3’
。
[0073]
probe d的序列为:5
’‑
sh
‑
(ch2)6‑
tttatcggaggtgg
‑
mb
‑3’
。
[0074]
本实施例中的痕量微小核糖核酸的电化学检测方法包括以下步骤:
[0075]
一、预先制备表征mirna浓度与电化学信号强度关系的标准曲线,具体包括:
[0076]
1)首先使用水虎鱼溶液处理金电极5分钟,使用双蒸水清洗电极;然后在砂纸和氧化铝粉末(1,0.3,0.05μm)上进行电极的打磨;随后把电极放入乙醇中超声处理5min,再放入双蒸水中超声处理5min;将处理后的电极放入0.5m的硫酸中,进行循环伏安电化学处理;使用双蒸水清洗后,把电极浸泡在浓度为0.8μm的probe a溶液中,反应8小时;之后再将电极使用1mm的巯基己醇处理0.5小时,得到表面修饰有probe a的电极;
[0077]
2)配制一系列具有一定浓度梯度的mirna标液,各个浓度的mirna分别进按以下步骤3)
‑
步骤6)操作:
[0078]
3)将步骤1)得到的电极置于mirna标液中,浸泡30分钟;
[0079]
4)向步骤3)的样品中再加入dna探针probe b和probe c,反应90分钟;
[0080]
5)采用柠檬酸还原法制备金纳米颗粒,配制浓度为30μm的probe d,将0.1ml probe d溶液和0.9ml金纳米颗粒溶液混合,反应16小时后再缓慢加入nacl溶液至nacl的终浓度为0.1m,24小时后采用14000g的转速离心纯化,得到表面修饰有dna探针probe d的金纳米颗粒溶液;
[0081]
将步骤4)得到的电极使用双蒸水润洗后浸泡到表面修饰有dna探针probe d的金纳米颗粒溶液中,反应60分钟;
[0082]
6)对步骤5)得到的电极进行电化学分析,得到各个已知浓度的mirna标液的电化学信号,建立得到表征mirna浓度与电化学信号强度关系的标准曲线。
[0083]
本实施例中,使用上海辰华chi660d电化学工作站进行电化学分析,基于三电极系统测试,包括金电极、铂丝对电极、饱和甘汞参比电极。交流阻抗的电解液使用5mm[fe(cn)6]3‑
/4
‑
,参数包括0.1hz
‑
100khz频率范围,5mv振幅;方波伏安法的电解液为20mm tris
‑
hcl,参数包括50mv/s扫描速度,4mv步进,70hz频率及0.1
‑‑
0.4v扫描范围。
[0084]
参照图2a和2b,本实施例中采用了浓度分别为:0.1fm、0.5fm、1fm、5fm、10fm、50fm、100fm、1pm、10pm、100pm的mirna标液进行实验,并采用方波伏安法进行目标mirna的定量分析,最终构建得到了表征mirna浓度与电化学信号强度关系的标准曲线。方波伏安曲线如图2a所示,图中箭头所示处,各曲线代表的浓度由上至下逐渐增大,可以看出,随着
mirna浓度的增加,电流峰逐渐增加。电流峰值与mirna浓度的具体关系如图2b所示(其中的插图显示电流值与mirna对数浓度之间的线性关系),得到的线性区间为0.1fm到0.1pm,标准曲线的方程为:y=33.226+2.002x,(n=3,r2=0.980),其中y为峰电流值,x为mirna浓度的对数值。通过该标准曲线,利用电化学分析得到的峰电流值即可计算出对应的mirna浓度。
[0085]
二、对待测样品进行mirna浓度检测
[0086]
具体步骤与标准曲线建立步骤相同,删去上述步骤2),并将步骤3)中的mirna标液替换为待测样品即可,最后得到的电极进行电化学分析后,将峰电流值带入到标准曲线中即可计算出待测样品中的mirna的浓度。
[0087]
参照图3a,本发明中还进行了反应物及产物的聚丙烯酰胺凝胶电泳表征实验,图3a中从左至右依次显示了mark条带、mirna、probe a、mirna/probea(表示mirna和probe a的混合体系,下同)、mirna/probe a/b/c、probe b、probe c、probe b/d、probe c/d的条带,结果表明相应目标mirna与dna分子之间的有效杂交和杂交链式反应的发生。
[0088]
参照图3b,为本发明中的杂链式反应产物与金纳米颗粒结合后的电镜表征图,图3b显示出在杂交链式反应后,金纳米颗粒沿着反应产物排布的电镜图,其线性对称结构进一步证实了dna
‑
金纳米颗粒复合物的有效形成。
[0089]
参照图4a和图4b,为本发明进行的基于交流阻抗与方波伏安的mirna检测可行性分析结果。本发明中,分别采用交流阻抗与方法伏安对该传感平台的可行性进行了验证,交流阻抗谱的半圆区域的直径与阻抗值呈正相关。图4a中,由左向右代表的曲线(以曲线上端的直线部分作为参考)依次为:blank、probe a、mirna/probe a、mirna/probe a/b/c(表示mirna、probe a、probe b、probe c的混合体系,本文中其他部分采用相同表示方式)、mirna/probe a/b/c/d、mirna/probe a/b/c/d/aunps;图4b中,箭头所示处,由上至下代表的曲线依次为probe a、mirna/probe a、mirna/probe a/b/c、mirna/probe a/b/c/d、mirna/probe a/b/c/d/aunps。从图4a可以看出,裸电极(图中blank)基本不表现出半圆区域,表明金电极具有良好的导电性;修饰probe a后,出现了半圆区域,验证了dna负电的磷酸骨架能够排斥电化学信号分子;当体系中存在mirna时,能够特异性地与probe a杂交,一定程度上增加了半圆区域的直径;进一步引入probe b和c之后,形成的杂交链式反应产物能够极大地提高电极表面的电负性,从而半圆区域的直径进一步加大;由于probe d能够与长链产物杂交,因此,当修饰有大量probe d的金纳米颗粒悬挂在杂交链式反应产物后,其阻抗得到的极大的提高,反映为更大的半圆区域直径。图4b的结果侧面证实了各反应的有序进行,由于亚甲基蓝只修饰在probe d末端,因此只有进行涉及probe d反应的步骤时才出现了明显的电流峰,且金纳米颗粒(aunps)的巨大比表面积能够有效提高其负载量,因此能得到更高的电流峰值。
[0090]
本发明中利用错配序列进行了本方法的选择性实验:采用含有1
‑
2个碱基错配的mirna代替以上的标准样品,按照与上述待测样品相同的步骤进行检测,检测结果如图5所示(图5中,mirna表示错配的序列,mir
‑
21表示无错配的序列,spiked with mir
‑
21表示对应的错配mirna与mir
‑
21的混合物),当体系中只存在错配mirna时,由于其不能够特异性地打开probe a茎环结构,因此无法触发后续的杂交链式反应及金纳米颗粒的固定,因此得到的电化学信号较小,而当体系中加入目标mirna时,有助于电化学信号探针的大量富集,采
集到的电化学信号能够实现明显的增强。
[0091]
错配的mirna包括以下:
[0092]
mismatch 1 5
’‑
uagcaaaucagacugauguuga
‑3’
;
[0093]
mismatch 2 5
’‑
uagcuuaucagacugaucauga
‑3’
;
[0094]
mismatch 3 5
’‑
uagcuaaucagacugagguuga
‑3’
;
[0095]
mismatch 4 5
’‑
uagcuuaucauccugauguuga
‑3’
;
[0096]
mismatch 5 5
’‑
uagauuaucagacugauguuga
‑3’
;
[0097]
mismatch 6 5
’‑
uagcuuaucagacugagguuga
‑3’
;
[0098]
其中下划线处为错配的碱基。
[0099]
以上给出了以靶mirna为mir
‑
21进行检测的详细方法以及相关实验,需要理解的是,按照本发明的上述原理,本发明的方法同样能适用于其他的mirna,只需要根据待测mirna的序列对体系中采用的各dna进行适当修改即可实现,为便于说明,在以下实施例2
‑
4中还针对mir
‑
141、mir
‑
183、mir
‑
155给出了所采用的dna探针的序列,均可实现对应的mirna的检测。
[0100]
实施例2
[0101]
本实施例中,待检测的mirna为mir
‑
141,其核酸序列为:
[0102]5’‑
uaacacugucugguaaagaugg
‑3’
;
[0103]
对应的probe a的序列为:
[0104]5’‑
ataaggtttagcatctttaccagacagtgtgctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0105]
probe b、probe c、probe d与实施例1相同。
[0106]
实施例3
[0107]
本实施例中,待检测的mirna为mir
‑
183,其核酸序列为:
[0108]5’‑
uauggcacugguagaauucacu
‑3’
;
[0109]
probe a的序列为:
[0110]5’‑
ataaggtttagctgaattctaccagtgccagctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0111]
probe b、probe c、probe d与实施例1相同。
[0112]
实施例4
[0113]
本实施例中,待检测的mirna为mir
‑
155,其核酸序列为:
[0114]5’‑
uuaaugcuaaucgugauagggguu
‑3’
;
[0115]
对应的probe a的序列为:
[0116]5’‑
ataaggtttagccctatcacgattagcattgctaaacctcccc
‑
(ch2)6‑
sh
‑3’
。
[0117]
probe b、probe c、probe d与实施例1相同。
[0118]
尽管本发明的实施方案已公开如上,但其并不仅仅限于说明书和实施方式中所列运用,它完全可以被适用于各种适合本发明的领域,对于熟悉本领域的人员而言,可容易地实现另外的修改,因此在不背离权利要求及等同范围所限定的一般概念下,本发明并不限于特定的细节。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1