用于将包含透明质酸的涂层施加到医疗取样装置的表面上的方法以及提供有该涂层的用于捕获循环肿瘤细胞的医疗取样装置与流程
本发明涉及用于捕获生物分析物的涂层,其包含与医疗取样装置的表面端点连接(end-point attached)的透明质酸(hyaluronic acid,ha)。此外,本发明涉及用于捕获用于随后分析的循环肿瘤细胞(circulating tumor cell,ctc)的医疗取样装置。更特别地,本发明涉及提供有引起对ctc的捕获增强的涂层的医疗取样装置,所述ctc随后可被释放以用于分析和诊断。
背景技术:
1、已知装置用于捕获生物分析物,其中待分析对象具有生物活性并选自包含以下的组:大分子、多核苷酸、rna、dna、蛋白质、标志物蛋白质、脂蛋白、多肽、抗体、自身抗体、激素、抗原、细胞、cd44+细胞、病毒、细菌细胞、寄生虫、真菌细胞、肿瘤细胞、来源于妊娠期间胎儿的干细胞和/或细胞、或其部分。特别令人感兴趣的是用于捕获循环肿瘤细胞的装置。
2、在过去的二十年中,化学治疗已变得更加先进。虽然较旧的“通用”化学治疗简单地杀伤体内快速生长的所有细胞(导致对健康组织的损害),但现代靶向化学治疗被设计成仅影响特定(癌症)细胞并使附带损伤最小化。尽管靶向化学治疗在癌症治疗方面已提供了大的改善,但其真正潜力仍未实现。由于癌细胞持续突变,其可适应并变得针对靶向化学治疗具有抗性。这最终导致靶向化学治疗变得无效。考虑到癌症通常是致命的并且靶向化学治疗是昂贵的,因此非常需要允许追踪肿瘤细胞何时以及如何变得具有抗性的工具,使得可相应地调整治疗。
3、目前用于追踪肿瘤突变的最广泛接受的方法是进行活检,即肿瘤的直接组织样品。这是侵入性操作,其固有地是疼痛的,具有局部传播疾病的风险,并且即使当进行良好时也只给出了在特定时间取样的精确位置的反映。由于患者考虑,很少对所有肿瘤进行连续活检。液体活检取样血液而不是肿瘤,并且由于其相对容易且安全,因此是用于持续追踪肿瘤突变的最有前景的工具。有许多不同的液体活检方法,包括分离循环肿瘤细胞(ctc)、肿瘤来源的囊泡(例如外排体)和循环肿瘤dna(circulating tumor dna,ctdna)。在所有这些方法中,ctc提供关于肿瘤抗性的最全面和深入的信息,因为其包含完整的dna、rna和蛋白质的谱。然而,ctc在血液中极为罕见:在数十亿个其他细胞中,典型的血液样品平均少于1ctc/毫升血液。需要多得多的细胞(100+)来可靠地追踪肿瘤抗性,这是需要可有效地将ctc从血液分离的技术的原因。因此,本发明涉及ctc的选择性捕获。
4、将用生物活性分子装饰的基于光纤、导管或线材的装置用于诊断任务的应用是已知的,所述诊断任务例如从生物样品或甚至从活生物体中检测和捕获dna、蛋白质、细胞和其他。
5、wo 2006131400教导用金属岛(metallic island)装饰不锈钢丝,所述金属岛用抗体修饰以用于特异性细胞捕获。通过在金层(gold layer)的沉积步骤期间使用球形单层作为阴影掩模来制造尺寸在100nm范围内的金属岛。将金岛(gold island)用结合特异性抗体的硫醇化接头分子进行修饰。
6、在ep1907848中,描述了诊断性纳米传感器,例如导管或弹簧丝形式的诊断性纳米传感器,其由包含具有检测分子的二维拱形金属纳米结构上的区域的载体组成。诊断性纳米传感器可用于直接检测和分离离开外周血或身体的稀有分子或细胞。这种应用技术能够实现以前不可能的诊断操作:使用母体循环中存在的胎儿滋养层进行染色体畸变的产前诊断;基于体内播散型癌细胞的检测的癌症诊断和癌症治疗监测。
7、ep2344021涉及用于检测分析物的装置,其包含聚合物纤维和捕获分子,其中捕获分子与分析物和/或接头分子结合。捕获分子选自包含以下的组:抗体、抗原、受体、多核苷酸、dna探针、rna探针、多肽、蛋白质和/或细胞。可将如在表面上具有微结构或表面几何形状的本文件中描述的官能化聚合物纤维引入到生物样品(例如血液样品)中或活生物体的静脉中。在至少数秒和数小时的时间期间,纤维通过其生物功能涂层收集相应的靶分析物。在收集过程完成之后,将纤维收回并将所捕获的物质从纤维分离以用于分析。
8、同样地,从ep2547250中,已知具有用于从人体分离分子或细胞的官能化表面的生物检测器。将该生物检测器引入到人体中以用于分离和富集靶分子和靶细胞,并在短时间之后再次从人体中移出。
9、在jinling zhang等人在chem.commun.,2014,50,6722中的“an ensemble ofaptamers and antibodies for multivalent capture of cancer cells”中,可发现经优化的集合作为多价黏附结构域发挥作用以用于捕获和分离癌细胞。所述集合可并入到包含微柱阵列的微流体装置中。使用抗生物素蛋白和生物素反应将抗体和适配体固定到微流体通道上,如sheng w,chen t,katnath r,xiong xl,tan wh,fan zh.anal.chem.2012;84:4199–4206的“aptamer-enabled efficient isolation of cancer cells from wholeblood using a microfluidic device”中所述。据报道,该微流体装置在600nl/秒的流量下产生>95%的捕获效率以及约81%的纯度。这表明了技术可行性,但该流量不足以在临床上应用。更确切地,在该速率下,将需要以100%效率连续运行多于46小时以得到100ctc的假设产率,这完全不切实际。
10、目前在体外以高灵敏度和选择性分离肿瘤细胞,以用于随后筛选临床相关参数。然而,鉴于血液中ctc的出现率非常低,即使可采集最大的血液样品但仍然提供很少的信息。进一步改善灵敏度和选择性将允许替代地在体内进行这些,这将极大地帮助进一步筛选临床相关参数。
11、直接从人静脉中的血流内捕获生物分析物(例如循环肿瘤细胞(ctc))是具有挑战性的。如上所述,捕获生物分析物通常用抗体完成,所述抗体是高度选择性的并提供强且近乎永久的键。然而,抗体仅能够以非常低的相对速度形成这些键,并且它们迅速丧失其以高于1mm/秒的速度捕获生物分析物的能力,而在血流中速度仍然高出多个数量级。此外,现有技术中的问题是经捕获的ctc在捕获之后收回装置时或在释放时经常被损坏或破坏。作为结果,检测或诊断不再可能或不再可信。
12、因此,仍然需要具有改善的灵敏度和选择性以从循环系统(circulatingsystem)、优选地从循环系统(circulatory system)、更优选地直接在血流中分离ctc的医疗取样装置,即允许释放以用于进一步筛选临床相关参数的具有提高的捕获率的经修饰的导丝或导管。
13、在zhi sheng-liang等人的文章“fabrication of carbohydrate microarrayson gold surfaces:direct attachment of nonderivatized oligosaccharides tohydrazide-modified self-assembled monolayers”,analytical chemistry,第78部分,no.14,2006,第4788至4793页中,公开了用于在微阵列的表面上施加包含肝素的涂层的方法,其中肝素与其表面上的胺基端点连接。微阵列可用于对碳水化合物-蛋白质识别事件进行作图。
14、wo2010019189尤其描述了具有表面的医疗装置,其包含基于端点连接的肝素的涂层,所述肝素通过包含1,2,3-三唑的连接与所述表面共价连接。所述肝素用作抗凝剂化合物。所述医疗装置不用作取样装置。虽然提及了支化,但这既不是肝素,也不是提及以改善捕获率。
15、在wo2013188073中,描述了用于通过使身体外的血液与固体接触而从血液中除去有助于癌症发病机制的介质的方法。因此这不是诊断装置。所述方法特别地针对肝素进行描述,因为其他碳水化合物表面可比肝素化表面具有显著更低的血液相容性并且可导致提高的血栓形成。
16、本发明的主要应用是通过提供作为另外的选择机制发挥作用的涂层并提高现有选择机制的灵敏度同时还赋予血液相容性来改进分离ctc的现有方法。所述涂层可施加在体内富集工具上,例如直接在血流中捕获ctc的经修饰的导丝和导管(例如gilupi)。然而,所述涂层也可施加在体外技术上,例如磁珠分离(例如,循环肿瘤细胞试剂盒,其旨在计数全血中上皮来源的ctc(cd45-、epcam+和细胞角蛋白8、18+和/或19+))以及一些微流体流动池(flow cell)。
技术实现思路
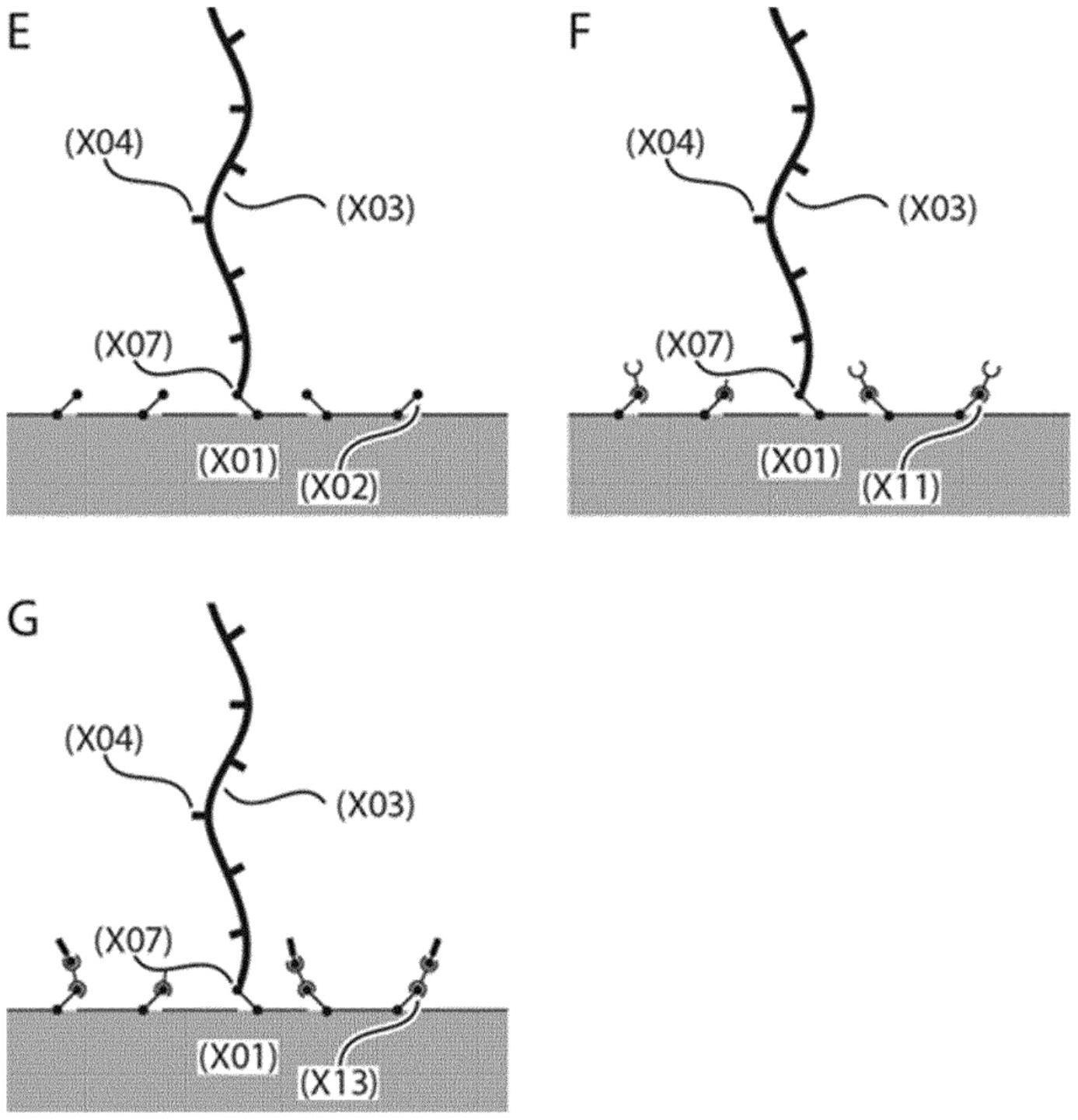
1、本发明提供了包含透明质酸(ha)的涂层,其用于施加在医疗取样装置的表面上,其中所述ha与医疗装置的表面端点连接。此外,本发明提供了用于将包含ha的涂层施加到医疗取样装置的表面上的方法,其中所述ha与医疗装置的表面端点连接,所述方法包括使表面胺化的步骤(a),随后是将ha与表面上的胺基端点连接的步骤(b),任选地随后是封闭表面上任何剩余胺基的步骤(c)。本发明还提供了用于捕获循环肿瘤细胞的医疗取样装置,其具有施加在其上的涂层。
2、本发明还提供了用于捕获循环肿瘤细胞的方法,以及用于释放和分析所捕获的循环肿瘤细胞的方法。
- 还没有人留言评论。精彩留言会获得点赞!