一种塞来昔布中微量硫酸二乙酯的检测方法与流程
1.本
技术实现要素:
属于药物分析技术领域。
背景技术:
2.塞来昔布(celecoxib)是1,5-二芳基取代吡唑类化合物,化学名为4-[5-(4-甲基苯基)-3-(三氟甲基)-1h-吡唑-1-基]苯磺酰胺,pka值为11.1,塞来昔布是新一代非甾体抗炎镇痛药,即特异性抑制cox-2,可通过抑制cox-2阻止炎性前列腺素类物质的产生。相对于传统非选择性的非甾体抗炎药(如萘普生、布洛芬),塞来昔布引起上消化道并发症的几率大大降低。上市以来,塞来昔布一直是风湿性关节炎、骨关节炎及这些疾病引起的疼痛治疗的首选药物之一。
[0003]
近几年基因毒性杂质成为人们关注的焦点,其中硫酸酯具有典型的基因毒性警示结构,从而可能成为引发癌症的诱因。塞来昔布的生产中,因塞来昔布起始物料三氟乙酸乙酯需经三氟乙酸和乙醇在浓硫酸的催化下加热反应得到,而硫酸和乙醇在此条件下可能反应产生硫酸二乙酯,鉴于此,必须开发高灵敏度和准确可靠的方法对塞来昔布中硫酸二乙酯进行检测。
[0004]
欧洲的emea和美国的fda均提出采用“毒理学关注阈值”(threshold of toxicological concern,ttc)作为基因毒性杂质的可接受限度。欧洲药物管理局发布了关于基因毒性杂质(gti)的最大摄取量为1.5 μg/d。参考塞来昔布使用说明书可知,塞来昔布日最大暴露量可达600mg,因此每一类基因毒性杂质限度控制在2.5ppm。故设定硫酸二乙酯的控制限度为2.5 ppm。
发明内容
[0005]
本发明提供了一种塞来昔布中微量硫酸二乙酯的检测方法,该方法采用衍生化-顶空-毛细管气相色谱分离-电子捕获检测的技术,具有较好的专属性,灵敏度高,准确性、重复性好。
[0006]
本发明是通过以下技术方案实现的:(1)顶空参数:顶空瓶温度50~80℃;定量环温度70~100℃;传送带温度100~130℃;顶空瓶加热平衡时间10~40min;进样时间0.5min;定量环定量时间0.2min;定量圈平衡时间0.05min;顶空瓶加压时间0.2min;(2)色谱条件:agilent 7820a型气相色谱仪;agilent 125-1334, db624 (30m
ꢀ×ꢀ
530μm
ꢀ×ꢀ
3μm) 或其他相似色谱柱;电子捕获检测器(μecd)温度220~300℃;载气n2;载气流速1~3ml/min;进样口温度180~230℃,进样量1ml,分流比3:1~8:1;程序升温梯度条件:50℃保持5min,然后以50℃/min的速率升温到200℃,保持2min,分析结束后设置后运行为柱温升到240℃,保持6min;尾吹辅助气流速30ml/min;(3)样品检测:取塞来昔布原料药约40mg,精密称定,置于10ml顶空瓶中,加入乙腈-水(4:1)溶液500μl,适当振摇使样品完全溶解,精密加入内标甲磺酸异丙酯工作溶液
(4.0μg/ml)20μl,振摇混匀后,再加入nai溶液(每1ml约含nai为1.2g的水溶液)500μl,封口,作为塞来昔布样品添加内标的供试品待测溶液。精密吸取乙腈-水(4:1)溶液500μl,置10ml顶空瓶中,精密加入含硫酸二乙酯(2.5μg/ml)和内标甲磺酸异丙酯(4.0μg/ml)的限度浓度的对照标准品溶液20μl于该10ml顶空瓶中,振摇混匀后,再加入nai溶液500μl,封口,作为限度浓度对照品待测溶液;按上述方法操作后,分别进行供试品待测溶液和限度浓度对照品待测溶液顶空进样,gc-ecd测定硫酸二乙酯基因毒性杂质峰(i-ch2ch3)和内标甲磺酸异丙酯(i-ch(ch3)2)面积,记录色谱图。按内标法以峰面积比计算,内标法计算公式如下:校正因子: 供试品浓度:式中:as——对照溶液中内标物质的峰面积;ar——对照溶液中被测物质的峰面积;a
x
——供试品溶液中被测物质的峰面积;——供试品溶液中内标的峰面积;cs——对照溶液中内标物质的浓度(ng /ml);cr——对照溶液中被测物的浓度(ng /ml);——供试品溶液中内标物质的浓度(ng /ml);cx——供试品溶液中被测物质的浓度(ng /ml)。
附图说明
[0007]
附图1:硫酸二乙酯对照测试溶液色谱图(tr=7.38min,c=100ng /ml);附图2:甲磺酸异丙酯对照测试溶液色谱图(tr=8.02min,c=400ng /ml);附图3:混合杂质对照品色谱图(碘乙烷c=100ng /ml,内标2-碘-丙烷c=400ng /ml)。
[0008]
具体实施方式:实施例1专属性:精密吸取乙腈-水(4:1)溶液500μl,置10ml顶空瓶中。精密加入硫酸二乙酯(2.5μg/ml)的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加nai溶液500μl,封口,作为专属性硫酸二乙酯对照测试溶液。精密吸取乙腈-水(4:1)溶液500μl,置10ml顶空瓶中。精密加入内标甲磺酸异丙酯(为4.0μg/ml)的限度浓度的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加nai溶液500μl,封口,作为专属性甲磺酸异丙酯对照测试溶液。精密吸取乙腈-水(4:1)溶液500μl,置10ml顶空瓶中。精密加入含硫酸二乙酯(2.5μg/ml)和内标甲磺酸异丙酯(为4.0μg/ml)的限度浓度的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加nai溶液500μl,封口,作为专属性混合对照测试溶液。分别进样分析,结果见附图1-3。
[0009]
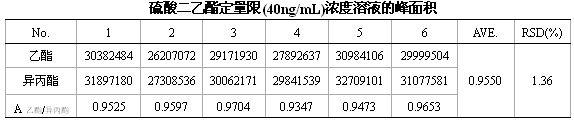
实施例2检测限和定量限:根据chp 2015版通则9101中“响应值标准偏差和标准曲线斜率法”计算,硫酸二乙酯的检测限约为12 ng/ml,定量限约为36 ng/ml。进一步验证,配制硫酸二乙酯浓度分别为20ng/ml和40ng/ml,内标甲磺酸异丙酯浓度为400ng/ml的检测限和定量限供试溶液,检测限供试溶液配制3份、定量限供试溶液配制6份,分别进行hs-gc-ecd进样分析。结果表明硫酸二乙酯的顶空气相色谱ecd测定法检测限为20ng/ml,定量限为40ng/ml,符合测定灵敏度的要求。
[0010]
实施例3线性和范围:精密吸取硫酸二乙酯(200μg/ml) 基因毒性杂质对照品溶液50、75、100、125、200和250μl,置10ml量瓶,分别加入内标工作液(200μg/ml)200μl,并加乙腈-水(4:1)溶液稀释至刻度,摇匀制成每1ml中约含硫酸二乙酯对照品1.0、1.5、2.0、2.5、4.0和5.0μg以及内标甲磺酸异丙酯4μg的6个水平的标准曲线工作溶液。
[0011]
精密吸取硫酸二乙酯6个水平的对照品标准曲线工作溶液各20μl,分别置于已经添加乙腈-水(4:1)溶液500μl的10ml顶空瓶中,振摇混匀后,配制成浓度梯度为40、60、80、100、160和200ng/ml标准曲线待测溶液,再各加入nai溶液500μl,封口,作为标准曲线测试溶液。分别对上述标准曲线测试溶液进行顶空气相色谱-ecd进样分析,记录色谱图。按最小二乘法,以硫酸二乙酯峰(碘乙烷保留时间约为7.4min)面积与内标甲磺酸异丙酯峰(2-碘-丙烷)面积之比(ax/ai),对硫酸二乙酯浓度c(ng/ml),进行线性回归。结果如下:
实施例4准确性:根据该方法的灵敏度设定硫酸二乙酯基因毒性杂质进行限度检查的限度浓度为100 ng/ml。参考基因毒性杂质每日摄入的最大量计算得到的供试品浓度为40mg/ml。对于塞来昔布中添加限度含量低(60%)、中(100%)、高(160%)三个水平浓度作为准确度实验的样品。精密吸取乙腈-水(4:1)溶液500μl,置10ml顶空瓶中,精密加入含硫酸二乙酯(2.5μg/ml)和内标甲磺酸异丙酯(为4.0μg/ml)限度浓度的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加入nai溶液500μl,封口作为回收率对照测试溶液。取塞来昔布原料药约40mg,精密称定,置于10ml顶空瓶中,加入乙腈-水(4:1)溶液500μl,适当振摇使样品完全溶解,分别精密加入含硫酸二乙酯(1.5μg/ml、2.5μg/ml、4.0μg/ml)和内标甲磺酸异丙酯(为4.0μg/ml)的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加入nai溶液500μl,配制成每1ml约含硫酸二乙酯分别为60、100和160ng对照品及内标甲磺酸异丙酯均为400ng/ml的标准品添加溶液,封口作为低(60%)、中(100%)、高(160%)三个水平标准添加供试品待测溶液。每个添加水平平行配制3份,分别进样测定,作为回收率供试溶液。照上述方法试验,根据峰面积比,按内标法计算硫酸二乙酯基因毒性杂质的测得浓度,扣除样品中的本底含量计算回收率。结果如下:
实施例5重复性:称取塞来昔布原料药约40mg,精密称定,置于10ml顶空瓶中,加入乙腈-水(4:1)溶液500μl,适当振摇使样品完全溶解,精密吸取硫酸二乙酯(2.5μg/ml)、内标甲磺酸异丙酯(为4.0μg/ml)的限度浓度的对照标准品溶液20μl于10ml顶空瓶中,振摇混匀后,再加入nai溶液500μl,封口,配制成塞来昔布添加限度浓度基因毒杂质的供试品添加测试溶液,作重复性待测溶液,平行配制6份,分别进样测定。结果如下:
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1