一种检测试剂盒及其制备方法和应用与流程
1.本发明属于生物医药技术领域,具体涉及一种检测试剂盒及其制备方法和应用。
背景技术:
2.肺癌是起源于肺部支气管黏膜或腺体的恶性肿瘤,发病率和死亡率增长最快,对人群健康和生命威胁最大的恶性肿瘤之一。近50年来许多国家都报道肺癌的发病率和死亡率均明显增高,男性肺癌发病率和死亡率均占所有恶性肿瘤的第一位,女性发病率占第二位,死亡率占第二位。肺癌的病因至今尚不完全明确,大量资料表明,长期大量吸烟与肺癌的发生有非常密切的关系。
3.肺癌可分为非小细胞肺癌和小细胞肺癌两大类,非小细胞肺癌可进一步细分为几种组织学亚型,其中鳞状细胞癌和腺癌最多见。晚期非小细胞肺癌常采用含铂化疗和局部放疗相结合的方法治疗,但其患者5年生存率仅为5%~15%,且目前没有得到显著改善;而小细胞肺癌是侵袭性的神经内分泌恶性肿瘤易迅速复发,患者5年生存率不到5%。被批准用于小细胞肺癌的药物只有依托泊苷和拓扑替康,虽然初始反应有60%~80%,但由于癌症干细胞样亚群导致多重耐药性,药效往往非常短暂且极易复发。目前临床上肺癌诊断的金标准是病理穿刺检查,但穿刺活组织检查为有创性操作,患者接受程度较低;影像学检查及糖类抗原19-9、血清癌胚抗原等肺癌相关抗原检测的敏感性与特异性相对较弱,只能作为辅助诊断或筛查指标。而驱动蛋白超家族(kinesin super-family proteins,kifs)在肺癌的发生发展中起重要作用,不仅在肿瘤细胞染色体的运动及异常分裂、侵袭和转移中发挥重要作用,还能影响胞内增殖凋亡信号通路,是非常有潜力的肺癌生物治疗靶点。此外,驱动蛋白还能作为肺癌的诊断和预后标志物,为治疗方案的拟定提供肿瘤分期和预后信息。
4.驱动蛋白于1985年首次被发现,是从乌贼神经轴突和视叶中分离出的一类分子马达,其能够利用腺苷三磷酸酶水解所释放的能量驱动自身及所携带的物质分子沿微管细丝正极做定向运动,进行胞内物质(如信息分子、囊泡、细胞器、染色体、蛋白质复合体)和信使rna的运输,并调节信号通路,从而发挥生物学效应,对细胞的功能和形态至关重要。目前kifs有45个成员,被分为14个亚家族,命名为kinesin1~kinesin14,其中38种表达于神经组织。驱动蛋白分子由两条重链和两条轻链组成,包括马达结构域、ph结构域和fha结构域,其中马达结构域具有腺苷三磷酸结合位点及微管结合位点,并在kifs中高度一致。根据马达结构域在重链上的位置不同,可分为在c端的c-kinesin、n端的n-kinesin以及中间的m-kinesin,大多数的驱动蛋白属于n-kinesin。通常,n-kinesin和c-kinesin分别驱动微管正末端和负末端定向运动,而m-kinesin负责解聚微管。ph结构域参与货物的运输,且能够决定结合货物的特异性,但fha结构域的功能仍然未知。驱动蛋白不能单独发挥作用,了解驱动蛋白的关键是研究其与货物的连接机制,通过将货物与驱动蛋白进行特定配对,可以对其相互作用进行微调。
5.近年来研究表明,驱动蛋白表达水平的变化与肺癌的发生发展有直接关联,驱动
蛋白异常可以通过染色体过度凝集、纺锤体形成异常、细胞分裂缺陷、形成后期桥或非整倍体及有丝分裂阻滞,改变细胞内遗传物质的分布,使细胞周期失控,最终渐进性地导致肿瘤发生。有文献报道,kif23与非小细胞癌密切相关(如:takahashi s,fusaki n,ohta s,et al.downregulation of kif23 suppresses glioma proliferation[j].j neurooncol,2012,106(3):519-529.)。但是,目前还没有kif23检测的相关诊断试剂或试剂盒,因此,有必要开发一种用于kif23检测的试剂或试剂盒。
技术实现要素:
[0006]
为了弥补现有技术的不足,本发明的目的在于提供一种于kif23检测的试剂或试剂盒。
[0007]
因此,本发明一方面提供了一种检测试剂盒,所述检测试剂盒的靶标为人源kif23蛋白,所述的试剂盒包括以下组分:1)有效量的人源kif23重组蛋白,所述人源kif23重组蛋白的氨基酸序列如seq id no.1所示;2)和/或有效量的抗人源kif23蛋白单克隆抗体,所述有效量的抗人源kif23蛋白单克隆抗体为单克隆抗体1和/或单克隆抗体2,所述的单克隆抗体1的重链可变区和轻链可变区序列如seq id no.3和seq id no.4所示,所述的单克隆抗体2的重链可变区和轻链可变区序列如seq id no.5和seq id no.6所示。
[0008]
优选地,本发明所述的kif23重组蛋白密码子优化后的核苷酸序列如seq id no.2所示。
[0009]
优选地,本发明所述的试剂盒为werstern blot检测试剂,所述werstern blot检测试剂中特异性识别kif23蛋白的单克隆抗体1和单克隆抗体2的稀释倍数均为1:1000倍。
[0010]
优选地,本发明所述的试剂盒为免疫荧光检测试剂,所述免疫荧光检测试剂中特异性识别kif23蛋白的单克隆抗体1和单克隆抗体2的稀释倍数均为1:200倍。
[0011]
优选地,本发明所述的试剂盒为双抗体夹心elisa试剂盒,所述双抗体夹心elisa试剂盒包括酶标板、标准品、样品稀释液、洗涤液、酶标抗体、显色液和终止液。
[0012]
优选地,本发明所述试剂盒的标准品为权利要求1所述的人源kif23重组蛋白,所述人源kif23重组蛋白的浓度为1000ng/ml。
[0013]
另一方面,本发明还提供了一种所述的试剂盒在检测人源kif23蛋白中的应用。
[0014]
再一方面,本发明还提供了一种所述的抗人源kif23蛋白单克隆抗体1和单克隆抗体2在检测人源kif23蛋白中的应用。
[0015]
本发明制备的检测人源kif23蛋白的试剂盒(如werstern blot、免疫荧光和双抗体夹心elisa)具有良好的特异性、敏感性和准确度,适合人源kif23蛋白的大量准确的检测。另外,本发明提供的抗人源kif23蛋白单克隆抗体为单克隆抗体1和单克隆抗体2具有良好的特异性,适合人源kif23蛋白的检测和验证。
附图说明
[0016]
图1蛋白质固有无序区域预测结果。分值越高代表该位置为无序区的概率越大,0.5作为是否为无序区的分界线。
[0017]
图2 kif23蛋白werstern blot检测结果。1是单克隆抗体1检测结果,2是单克隆抗体2检测结果。
[0018]
图3免疫荧光检测结果。
[0019]
图4标准曲线图。
具体实施方式
[0020]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”包括一个或多个相关的所列项目的任意的和所有的组合。
[0021]
除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。除非特别说明,以下实施例所用试剂和材料均为市购。
[0022]
实施例1:kif23蛋白的分析和重组蛋白的设计以及制备
[0023]
选择人源kif23蛋白(uniprotkb-q02241(kif23_human)),并对其氨基酸序列进行系统分析。首先对蛋白质motif进行分析,结果显示(表1),该蛋白具有3个motif。其次,对蛋白质固有无序区域预测进行分析,结果显示(图1),aa20以前和aa520以后的区域无序区概率更大。综合考虑,确定kif23重组蛋白的氨基酸序列如seq id no.1所示(aa20~aa520)。
[0024]
使用常规重组蛋白制备方法,对kif23重组蛋白的核苷酸序列进行密码子优化(如seq id no.2所示),通过常规的原核表达体系(参见中国发明专利2020102850203)表达制备kif23重组蛋白,分子量约为61kd,置于-20℃保存备用。当然,本发明人也对不经过优化的人源kif23蛋白按照同样的方法进行表达和制备,发现,不经优化的人源kif23蛋白不好表达,表达量较低(比本发明的kif23重组蛋白的表达量要第2-3倍);分析原因,可能是因为不经过优化的人源kif23蛋白分子量较大(约110kd),导致表达量较低,且不易纯化,进而导致得率较低。
[0025]
表1蛋白质motif分析结果
[0026]
motif类型起始位置终止位置复制序列amidation451454pgrratp_gtp_a112119gvtgsgktkinesin_motor_1331342sqlslvdlagse
[0027]
实施例2:特异性识别kif23重组蛋白单克隆抗体的制备和检验
[0028]
将实施例1制备的kif23重组蛋白免疫小鼠,按照常规的杂交瘤筛选方法制备单克隆抗体(参见中国发明专利cn 106226512 b)。经过筛选和制备,共制备2株杂交瘤细胞和其对应的单克隆抗体,分别命名为杂交瘤细胞1、2和单克隆抗体1、2。
[0029]
我们对单克隆抗体1和单克隆抗体2的可变区序列进行分析(具体分析方法为常规方法,具体可参见cn 111393525 b),其中单克隆抗体1的重链可变区和轻链可变区的序列如seq id no.3和seq id no.4所示;其中单克隆抗体2的重链可变区和轻链可变区的序列如seq id no.5和seq id no.6所示。
[0030]
实施例3:kif23的检测试剂和试剂盒
[0031]
3.1kif23蛋白werstern blot检测:使用制备的单克隆抗体1和单克隆抗体2对阳性样品组织中提取的总蛋白进行kif23的werstern blot检测,检测时,单克隆抗体1和单克隆抗体2(稀释前均调整浓度为1mg/ml)的稀释倍数均为1:1000,二抗(hrp标记羊抗鼠igg)
稀释倍数为1:5000倍。结果显示(图2),单克隆抗体1和单克隆抗体2均能与kif23特异性结合(约在110kd处有特异性条带)。
[0032]
3.2免疫荧光检测:使用单克隆抗体1和单克隆抗体2分别对hela细胞中的kif23蛋白进行免疫荧光分析。结果显示(图3),kif23蛋白与单克隆抗体1和2能特异性结果,图3中绿色所示;细胞核染色为dapi(蓝色)。细胞用多聚甲醛进行固定处理。试验时,单克隆抗体1和2(稀释前均调整浓度为1mg/ml)的稀释倍数均为1:200。
[0033]
3.3双抗体夹心elisa试剂盒
[0034]
3.3.1所述试剂盒包括酶标板、标准品、样品稀释液、洗涤液、酶标抗体、显色液和终止液等组成。其中酶标板包被有一定浓度的单克隆抗体1(一般为1~2μg/ml)或kif23蛋白多克隆抗体(一般为1~5μg/ml)(参见中国发明专利cn 106226512 b进行制备或购买);标准品为本发明制备的不同浓度的kif23重组蛋白;样品稀释液是对检测样品进行稀释,一般为含有一定bsa的pbst缓冲液;酶标抗体为hrp标记的单克隆抗体2(按照hrp标记试剂盒说明书标记,也可以采用改良的高碘酸钠法进行标记);显色液一般为tmb显色液,可以为单组分和双组分;终止液一般为硫酸,浓度一般为2m或1m。
[0035]
3.3.2所述试剂盒检测方法
[0036]
3.3.2.1试剂的准备
[0037]
①
试剂的准备:用前将所有的试剂和样品恢复至室温(15~25℃),试剂应轻轻地旋转或震荡予以混合。
[0038]
②
洗涤液的配制:将1份25
×
浓缩洗涤液加入到24份双蒸水中,混匀;
[0039]
③
配制好的洗涤液,应在3日内用完。
[0040]
3.3.2.2待检样品的稀释:用样品稀释液将待检样品稀释10倍;建议每个样品连续稀释2-3个梯度,如20倍、30倍等。
[0041]
3.3.2.3标准品稀释用样品稀释液将标准品做倍比稀释,具体稀释参考下表。稀释好的标准品2~8℃保存3天。
[0042]
编号样品稀释液体积标准品体积浓度(ng/ml)s8150μl150μl标准品(1000ng/ml)500s7150μl150μl标准品s8250s6150μl150μl标准品s7125s5150μl150μl标准品s662.5s4150μl150μl标准品s531.25s3150μl150μl标准品s415.625s2150μl150μl标准品s37.8125s1150μl150μl标准品s23.90625
[0043]
注:此表为标准品稀释时参考用,具体稀释根据实际使用情况确定。
[0044]
3.3.2.4检验
[0045]
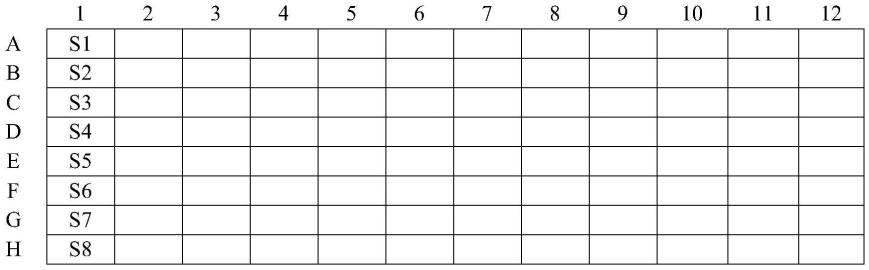
3.3.2.4.1加样根据待检样品数量,取可拆卸包被板,平放桌面,加入稀释好的待检样品100μl/孔,同时加入稀释好的标准品,100μl/孔。包被板上标准品和待检样品添加位置如下表所示:
[0046][0047]
注:“s1-s8”为标准品;其余孔为待检样品。
[0048]
3.3.2.4.2孵育置37℃温箱孵育30分钟。
[0049]
3.3.2.4.3洗涤甩去孔内液体,加入洗涤液,300μl/孔,洗涤3~5次,每次静置30秒,甩去孔内液体,拍干。
[0050]
3.3.2.4.4酶标抗体孵育加入酶标抗体,100μl/孔,置37℃温箱孵育30分钟。
[0051]
3.3.2.4.5洗涤方法同3.3.2.4.3。
[0052]
3.3.2.4.6显色加入tmb底物溶液,100μl/孔,置37℃温箱避光孵育10分钟。
[0053]
3.3.2.4.7终止加入终止液,50μl/孔,轻微震荡混合均匀。
[0054]
3.3.2.4.8读数加入终止液后,立即将包被板置于酶标仪中,在波长为450nm下读取od450nm值。
[0055]
3.3.2.5标准曲线绘制(图4)以s1-s8标准品浓度为横坐标,以对应的标准品od450nm值为纵坐标,拟合标准曲线,并生成标准曲线函数和r2,其中r2应≥0.9。
[0056]
3.3.2.6待测样品浓度计算将稀释后待测样品od450nm值代入标准曲线函数中,计算得到稀释后待测样品浓度,以此浓度*待测样品稀释倍数,即为待测样品的浓度。如样品稀释有2-3个梯度,取所有梯度计算的浓度的平均值作为待测样品的浓度。
[0057]
3.3.3样品检测对3.1中提取的样品进行检测,经过检测,该样品的浓度为105ng/ml。将此样品进行2倍倍比稀释后检测,检测结果如表2所示,在32倍稀释以前(原始结果3.39ng/ml),检测结果均保持准确,但是在64倍稀释后,检测结果不准确,分析可能是因为含量太低,试剂盒灵敏度未达到,导致检测几个偏高。总体来说,本试剂盒具有良好的灵敏度和准确性。
[0058]
表2样品梯度稀释后检测结果
[0059][0060]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1