一种用于测定干扰素-γ的试剂盒及其应用的制作方法
一种用于测定干扰素-γ
的试剂盒及其应用
技术领域
1.本发明涉及化学发光体外诊断技术领域,具体涉及一种用于测定干扰素-γ的试剂盒及其应用。
背景技术:
2.干扰素-γ是机体一类重要的细胞因子,具有广谱抗病毒、抗肿瘤和免疫调节功能,ifn蛋白家族基于它们的基因序列、染色体定位和受体特异性分为3型,即ⅰ型、ⅱ型和ⅲ型干扰素。ifn-γ也叫ⅱ型干扰素,主要由活化t细胞和nk细胞产生,人ifn-γ成熟分子以同源二聚体糖蛋白形式存在。大量研究表明,ifn-γ除具有广谱抗病毒功能外,还具有抗细胞增殖、免疫调节、抗肿瘤、抗寄生虫等方面也发挥着重要作用。有文献报道,covid-19患者中大量细胞因子显著增高,主要有il-6、il-10、il-1β、il-1、il-7、il-8、il-9、粒细胞集落刺激因子(g-csf)、ifn-γ、粒细胞-巨噬细胞集落刺激因子(gm-csf)、干扰素诱导蛋白-10(ip-10)和巨噬细胞炎症蛋白-1α(mip-1α)等。干扰素-γ的检测在临床上主要应用于病毒感染,临床用药后监测以及机体免疫功能评估。
3.cn113702362 a公开了一种使用化学发光方法定量检测ifn-γ浓度的方法,该方法以配体受体结合原理为基础,将包被蛋白、检测物ifn-γ、检测抗体先后结合在固体介质上,然后加入显色底物进行检测。但检测范围较窄,且操作繁琐。
4.即现有采用酶联免疫法检测ifn-γ,具有操作繁琐、耗时长、检测范围窄的缺陷,不利于临床推广应用。
技术实现要素:
5.本发明的目的在于提供一种用于测定干扰素-γ的试剂盒及其应用,解决现有采用酶联免疫法检测ifn-γ检测范围窄的问题,且具有稳定性好、灵敏性高的优点。
6.本发明通过下述技术方案实现:
7.一种用于测定干扰素-γ的试剂盒,包括:
8.试剂1,包括抗人ifn-γ单克隆抗体1包被的磁珠和第一基础缓冲液,所述磁珠上标记有生物素;
9.试剂2,包括含有碱性磷酸酶标记的抗人ifn-γ单克隆抗体2和第二基础缓冲液;
10.试剂3,包括动物血清,所述动物血清包括小牛血清或成牛血清。
11.本发明试剂1、试剂2分别为抗人ifn-γ单克隆抗体1包被的磁珠和酶工作液,抗人ifn-γ单克隆抗体包被的磁珠和酶工作液为检测干扰素-γ提供必要条件;试剂3中的动物血清能够有效的降低样本存在的干扰,提高干扰素-γ检测的准确性。
12.本发明通过试剂1和试剂2与试剂3为相互配合,能提高干扰素-γ检测的特异性和灵敏度,提高ifn-γ检测范围。
13.进一步地,试剂1中磁珠的包被量为10μg/mg,复溶比为1/50。
14.包被量含义为:10μg抗体对应1mg磁珠,包被量的意义在于将抗体按一定比例链接
到磁珠,这样的比例效果使得反应体系较好;稀释比例(复溶比)含义为:研发的裸磁珠是原倍,1/50就是在原倍的基础上进行50倍稀释,稀释比例的意义在于原倍的裸磁珠在反应体系中浓度过高,与抗体链接时会有所剩余,而稀释比过大却会导致链接抗体时缺失,经反复试验,稀释到1/50能使反应体系更加充分且效果更好。
15.进一步地,试剂1中第一基础缓冲液由以下组分组成:
16.tris、nacl、浓hcl、蔗糖、bsa、pc-950和tween-20。
17.进一步地,试剂1由以下组分组成:
18.12.11g/l tris、9.00g/l nacl、5.5ml/l浓hcl、20g/l蔗糖、10.00g/l bsa、1ml/l pc-950、0.5ml/l tween-20、2μg/ml的抗人ifn-γ单克隆抗体1、0.2mg/ml链亲和素磁珠和50ul/mg磁珠封闭液。
19.其中,磁珠封闭液配制步骤为:将生物素h放置室温(避光)平衡至室温(10-30min);取一张干净称量纸置天平上,调节零点;称量生物素h 244.5mg于适当容器中,并用50ml二甲基亚砜充分溶解,再加入50ml甘油,充分混匀,于-20℃存放,1mg磁珠加50ul封闭液。
20.进一步地,试剂2中第二基础缓冲液由以下组分组成:
21.tris、nacl、浓hcl、海藻糖、果绿色素、bsa、酪蛋白、tx-100、pc-300和丙三醇。
22.进一步地,试剂2由以下组分组成:
23.12.11g/l tris、9.00g/l nacl、5.5ml/l浓hcl,10.00g/l海藻糖、0.05g/l果绿色素、5.00g/l bsa、5.00g/l酪蛋白、0.1ml/l tx-100、3ml/l pc-300、10ml/l丙三醇和1mg/mg碱性磷酸酶活化的抗人ifn-γ单克隆抗体2。
24.其中,试剂2中包含的“碱性磷酸酶活化的抗人ifn-γ单克隆抗体2”是指被“可检测标记物”标记的“碱性磷酸酶活化的抗人ifn-γ单克隆抗体2”。用可检测标记物对抗体进行标记在领域众所周知的。被可检测标记物标记的抗人ifn-γ单克隆抗体2及其用量,本领域技术人员可根据实际情况进行选择,比如,采用碱性磷酸酶活化的抗人ifn-γ单克隆抗体2,其浓度可以采用例如0.1~1.0μg/ml,其浓度也可以是0.1μg/ml、0.2μg/ml、0.3μg/ml、0.4μg/ml、0.5μg/ml、0.6μg/ml、0.7μg/ml、0.8μg/ml、0.9μg/ml或1.0μg/ml。
25.进一步地,试剂3由以下组分组成:
26.100ml/l动物血清和3ml/l pc-300。
27.进一步地,试剂1的ph值为7.95-8.05。
28.进一步地,试剂2的ph值为7.95-8.05。
29.上述试剂盒的在测定干扰素-γ中应用,使用时,将待测样品与试剂1、试剂2和试剂3混合并孵育完成,所述试剂1、试剂2和试剂3在反应体系中的体积比为1:2:2。
30.本发明与现有技术相比,具有如下的优点和有益效果:
31.本发明通过试剂1和试剂2与试剂3为相互配合,具有稳定性好、灵敏性高、检测范围宽、测定周期短的优点,进而提高了干扰素-γ检测的准确性,易于临床推广。
附图说明
32.此处所说明的附图用来提供对本发明实施例的进一步理解,构成本技术的一部分,并不构成对本发明实施例的限定。在附图中:
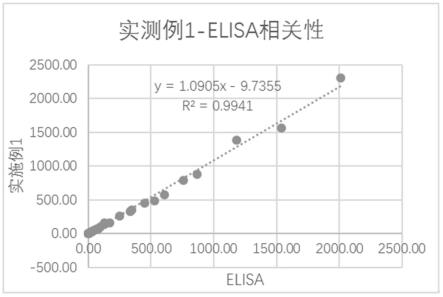
33.图1为实施例1所述试剂盒与elisa检测结果相关性示意图;
34.图2为实施例2所述试剂盒与elisa的检测结果相关性示意图;
35.图3为对比例3所述试剂盒与elisa的检测结果相关性示意图;
36.图4为实施例1所述试剂盒的实测浓度与理论浓度的线性关系图;
37.图5为实施例2所述试剂盒的实测浓度与理论浓度的线性关系图。
具体实施方式
38.为使本发明的目的、技术方案和优点更加清楚明白,下面结合实施例和附图,对本发明作进一步的详细说明,本发明的示意性实施方式及其说明仅用于解释本发明,并不作为对本发明的限定。
39.实施例1:
40.一种用于测定干扰素-γ的试剂盒,包括:
41.试剂1,包括抗人ifn-γ单克隆抗体1包被的磁珠和第一基础缓冲液,所述磁珠上标记有生物素;
42.试剂2,包括含有碱性磷酸酶标记的抗人ifn-γ单克隆抗体2和第二基础缓冲液;
43.试剂3,包括动物血清和防腐剂,所述动物血清为小牛血清。
44.试剂1、试剂2和试剂3分别按表1进行配制:
45.表1
[0046][0047]
其中,试剂1和试剂2的ph值均为7.95-8.05;使用时,所述试剂1、试剂2和试剂3的反应体系加入量比例为1:2:2。
[0048]
实施例2:
[0049]
本实施例基于实施例1,与实施例1的区别在于:
[0050]
动物血清为成牛血清。
[0051]
对比例1:
[0052]
本对比例基于实施例1,与实施例1的区别在于:
[0053]
试剂3为第一基础液。
[0054]
对比例2:
[0055]
本对比例基于实施例1,与实施例1的区别在于:
[0056]
试剂3为第二基础液。
[0057]
对比例3:
[0058]
本对比例基于实施例1,与实施例1的区别在于:
[0059]
不含试剂3。
[0060]
将实施例1、实施例2,对比例1-对比例3所述试剂盒,上机测定干扰素-γ校准品cal-1至cal-6,观察不同试剂盒的测定曲线及特异性,并测定样本y1-y41,与elisa值进行比较:
[0061]
实验材料:干扰素-γ校准品cal-1-cal-6(cal-1到cal-6的浓度为0,10,100,500,1000,3000pg/ml),样本y1-y41,底物液,清洗液,贝克曼access 2全自动化学发光测定仪,干扰素-γ试剂盒(bio-techne(elisa))
[0062]
反应模式为:先依次加入校准品或待测样本50μl、试剂3 100μl、试剂2 100μl、试剂1 50μl,37℃共同孵育30min后,加入清洗液在磁场中清洗分离三次后,加入底物液37℃孵育5min后,于贝克曼access 2全自动化学发光测定仪上检测,得到化学发光的信号值,用excel或medcalc等软件计算相关系数。
[0063]
1)、灵敏度评估
[0064]
将实施例1、实施例2和对比例1和对比例2所述试剂盒用于在同等情况下,试剂盒灵敏度比较实验,检测结果如表2所示:
[0065]
表2
[0066][0067]
2)、方法学比对评估
[0068]
将实施例1、实施例2和对比例3所述试剂盒用于在同等情况下,比较检测结果相关性,检测结果如表3及图1-图3所示:
[0069]
表3
[0070][0071][0072]
备注:干扰素-γ试剂盒(bio-techne(elisa))测定范围为2.91pg/ml-1000pg/ml,超出线性范围样本按照说明书稀释一定倍数后进行反算得到。
[0073]
由表2和表3的数据可知:
[0074]
采用不含第三试剂的试剂盒灵敏度和比对性均较差,存在干扰;采用第一基础液和第二基础液作为试剂3的试剂盒灵敏度相对而言比较差;采用小牛血清或成牛血清作为
试剂3的试剂盒曲线满足使用,测得样本结果与elisa法相关性较佳,免疫性一致,灵敏度较优。
[0075]
3)、线性评估
[0076]
将bio-techne(elisa)试剂盒定值的干扰素-γ浓度为3014pg/ml的临床样本作为原倍样本,使用校准品稀释液分别进行1:2、1:5、1:25、1:125、1:625、1:3125和1:15625倍稀释,用实施例1、实施例2所得试剂盒并配套使用贝克曼access 2全自动化学发光测定仪得到各样本的化学发光的信号值,用贝克曼access 2仪器自带软件计算测定浓度;结果如表4、图4-图5所示:
[0077]
表4
[0078][0079]
由表4、图4-图5可知:
[0080]
本发明试剂盒线性范围宽,在0.19pg/ml~3014pg/ml范围内,r2值达0.9995。
[0081]
4)、热稳定性评估:
[0082]
采用“标准曲线测定”记载的方法,使用于2~8℃和37℃保存6天的试剂1、试剂2和试剂3组合成整体共同测定校准品的信号值,并通过以下公式计算信号保留率:
[0083]
信号保留率=37℃下的信号值/2~8℃下的信号值
×
100%。
[0084]
将上述材料制成实施例1、实施例2所述试剂盒(各2盒),一份与2-8℃保存,一份于恒温培养箱中37℃保存,6天后取出。分别将磁珠于试剂3和酶工作液试剂2配合测定干扰素-γ校准品。第六天于贝克曼access 2全自动化学发光测定仪观察校准品的发光信号,计算信号保留率,验证试剂盒的稳定性。结果如表5所示:
[0085]
表5
[0086][0087]
由表5的数据可知:
[0088]
实施例1 37℃存放后信号保留率较高,稳定性好。
[0089]
综上,干扰素-γ测定试剂盒在采小牛血清或成牛血清作为试剂3时,灵敏度和特异性均有效提高,检测范围宽、稳定性好。
[0090]
与现有技术相比,本发明的干扰素-γ测定试剂盒稳定性好、灵敏度高,且检测范围宽,符合临床需求。
[0091]
以上所述的具体实施方式,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施方式而已,并不用于限定本发明的保护范围,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1