用于检测油脂型基质产品的前处理稀释液及检测方法与流程
1.本发明属于油脂型基质产品检测领域,更具体涉及一种油脂型基质产品的前处理稀释液及检测方法。
背景技术:
2.针对一些油脂型基质的产品,比如乳膏剂,两个重要检测是油脂含量检测和无菌检测。粗脂肪含量是粮食、油料、饲料等产品标准中重要的质量指标,是评价产品品质,组织生产的重要依据之一。国内外测定粗脂肪含量的方法有十余种之多,gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中提到了3种检测食品油脂含量的方法,分别是索氏抽提法、酸水解法、碱水解法,索氏抽提法是目前应用最广泛的测定方法,是公认的脂肪含量测定的经典方法,主要应用于食品中脂肪的测定。gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的索氏抽提法,样品的处理方法是称样后,将样品置于盛有石英砂的蒸发皿中,在沸水浴中蒸干,蒸干后在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内。gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中索氏抽提法的样品处理过程需要将样品在沸水浴中蒸干,蒸干后干燥,研细。该操作需要保证样品在沸水浴中蒸干,存在操作时间长,蒸干时间点的确定需要实验人员的经验,样品蒸干效果差抽提时间长的问题。
3.在非水溶性药品的无菌检查中,经常应用十四烷酸异丙酯来溶解非水溶性药品或其部分成分。例如文献《对几种抗生素眼膏无菌检查方法探讨》,该眼膏基质难以溶解,不能直接进行无菌检测。该文中记录前处理方法为:在2g眼膏中,加入十四烷酸异丙酯100ml,振动使供试品溶解,可在45℃水浴中加热使溶解完全。但也有文献报道称十四烷酸异丙酯无法将乳膏完全溶解。《盐酸米诺环素软膏无菌检查方法的建立》一文中采用十四烷酸异丙酯、10%吐温-80蛋白胨溶液、20%的乙醇溶液分别作溶剂,都不能将盐酸米诺环素软膏分散溶解。在样品的无菌检查中,需要将供试品通过过滤器,对于乳膏剂这类黏稠度高、难以穿透过滤器的样品检测来说,目前还没有一个较好的解决办法。
4.一些文献报道称,不易溶于水的乳膏剂可以使用吐温这种表面活性剂使其乳化分层,分离样品。例如文献《复方磺胺嘧啶锌乳膏无菌检查法的研究》中,样品的前处理方法是将吐温-80氯化钠-蛋白胨缓冲液加入样品中使其乳化,通过离心处理后,取沉淀进行检查。但是,对于配方较为复杂,尤其是含有增稠剂的乳膏剂来说,单独使用吐温进行乳化分层的效果并不明显,造成检测结果的偏差。所以,需要开发一种能够更加精确地检测粘度高、不易分离的油脂型基质产品的方法。
技术实现要素:
5.针对现有技术的上述缺陷和问题,本发明开发了一种用于检测油脂型基质产品的前处理稀释液,以及相应的油脂型基质产品检测的前处理方法、检测油脂型基质产品油脂含量的方法和对油脂型基质产品进行无菌检测的方法。
6.本发明第一方面提供了一种用于检测油脂型基质产品的前处理稀释液,其特征在于,所述稀释液包含钙盐水溶液和吐温,其中,所述钙盐水溶液中钙盐与水的质量比范围为1-30:99-70,所述稀释液中吐温与所述钙盐水溶液的体积比范围为1-30:99-70。
7.可选地,所述钙盐水溶液中钙盐与水的质量比范围为9-20:91-80,所述稀释液中吐温与所述钙盐水溶液的体积比范围为4-15:96-85。
8.可选地,所述吐温选自吐温-80、吐温-60、吐温-40、吐温-20中的一种或多种。
9.可选地,所述钙盐选自氯化钙、溴化钙、碘化钙、硝酸钙、硫酸钙中的一种或多种。
10.可选地,所述油脂型基质产品为乳膏剂。
11.本发明的发明人通过大量实验发现,单独加入吐温分离油相与水相,低速离心后,油相水相分界不明显;通过进一步加入了钙盐,例如氯化钙,能够得到完整的油脂层,可进行进一步的样品处理。
12.本发明另一方面提供了一种油脂型基质产品检测的前处理方法,其特征在于,使用上述的稀释液处理所述油脂型基质产品。
13.本发明另一方面提供了一种检测油脂型基质产品油脂含量的方法,其特征在于,在检测之前使用上述的稀释液处理所述油脂型基质产品。
14.可选地,所述的检测方法包括以下步骤:
15.(1)样品处理:将待测样品加入上述的稀释液中,混匀后离心,取出离心管中的油脂层;
16.(2)油脂含量测定:将油脂层放入索氏抽提器的抽提筒内,连接至接收瓶,进行抽提;将抽提物蒸干后进行称量。
17.优选地,在所述检测油脂型基质产品油脂含量的方法中,所述钙盐水溶液中钙盐与水的质量比范围为9-20:91-80,所述稀释液中吐温与所述钙盐水溶液的体积比范围为4-15:96-85。
18.本发明另一方面提供了一种对油脂型基质产品进行无菌检测的方法,其特征在于,在检测之前使用上述的稀释液进行处理。
19.可选地,所述的检测方法包括以下步骤:
20.(1)将待测样品加入上述的稀释液中,混匀后离心,取出离心管中的油脂层,涂抹在培养基上;
21.(2)对离心管中间层溶液进行过滤,过滤后每个滤膜使用缓冲液溶液冲洗,其中将滤膜接种于培养基中;
22.(3)离心管使用缓冲液溶解底部沉淀,溶解后将其接种于培养基中,然后对其进行无菌检测。
23.优选地,在所述对油脂型基质产品进行无菌检测的方法中,所述钙盐水溶液中钙盐与水的质量比范围为9-20:91-80,所述稀释液中吐温与所述钙盐水溶液的体积比范围为4-15:96-85;更优选地,所述稀释液中吐温与所述钙盐水溶液的体积比范围为4-6:96-94。
24.对于油脂型基质产品的无菌检测,选用低速离心后取水相,用薄膜过滤法检查,发明人发现无法通过滤膜。故尝试用十四烷酸异丙酯稀释样品,低速离心后取水相,用薄膜过滤法检查,过滤速度过慢,该方法依旧不理想。将稀释液更改为吐温-80,同样的操作过程,也无法满足过滤的需求。发明人通过大量实验,发现通过吐温和钙盐的合理配比,能够使乳
膏剂这类黏稠度高、不穿透过滤器的样品溶解,既保持了原料的安全性,又提高了过滤的速度。
25.本发明的检测方法以及前处理稀释液所适用的检测对象为油脂型基质产品。优选地,检测对象为不易溶于水的乳膏剂。优选地,检测对象为含有增稠剂的乳膏剂。更优选地,检测对象为包含油脂、乳化剂、增稠剂、保湿剂的产品。在本发明实施方案中,检测对象为专利申请202211104373.4中描述的无菌乳膏剂,其通过引用整体并入本文。本领域技术人员可在本发明适用的检测对象的范围内任意选择检测对象,并不被本发明的具体实施例所束缚。
26.相比现有技术,本发明提供了一种油脂型基质产品,例如乳膏剂产品的前处理稀释液和前处理及检测方法。发明人通过将吐温和钙盐合理配比,制备出一种稀释液,现溶现用,使乳膏剂这类黏稠度高、不易分离的样品油水分离,既保持了油脂原料的完整性,又提高了样品处理的速度以及过滤的速度。本发明的检测方法利用这种稀释液,能够更快速的收集样品中的油脂成分,避免油脂成分遗漏的同时缩短实验时间,并且解决了传统的样品在无菌检测时,存在样品难溶的问题,并培养检查,经系统方法验证,能更完全的收集乳膏剂中的微生物,可以避免漏检,提高检测结果的准确性。相较于现有技术方法,本发明的方法操作简单且耗时短,无原料损耗和流失,既提高了实验的准确率,又减少了操作时间,避免出现假阴性的结果。
具体实施方式
27.下面结合实施例进一步说明本发明,应当理解,实施例仅用于进一步说明和阐释本发明,并非用于限制本发明。
28.除非另外定义,本说明书中有关技术术语和科学术语与本领域内的技术人员所通常理解的意思相同。虽然在实验或实际应用中可以应用与此间所述相似或相同的方法和材料,本文还是在下文中对材料和方法做了描述。在相冲突的情况下,以本说明书包括其中的定义为准。另外,材料、方法和例子仅供说明,而不具限制性。
29.本发明实施例中所采用的试验方法、检测方法和常规实验试剂配制方法,如无特别说明,均按照本领域常规操作。本发明实施例中检测的样品为专利申请202211104373.4中描述的乳膏剂。
30.实施例1油脂含量测定
31.1.氯化钙溶液配置:取氯化钙和纯化水按照5:95的质量比配置,溶解;
32.2.吐温-氯化钙溶液配置:取吐温和氯化钙溶液,按照1:99的体积比配置成吐温-氯化钙溶液,混匀。
33.3.样品处理:称取样品5g,于50ml离心管中,准确至0.001g,加入45ml吐温-氯化钙溶液,混匀后离心(4000r/min,20min),取出离心管中上层油脂层。
34.4.油脂含量测定:将样品上层油脂层置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干,蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内,将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油
斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
35.实施例2油脂含量测定
36.1.氯化钙溶液配置:取氯化钙和纯化水按照8:92的质量比配置,溶解;
37.2.吐温-氯化钙溶液配置:取吐温和氯化钙溶液,按照3:97的体积比配置成吐温-氯化钙溶液,混匀。
38.3.样品处理:称取样品5g,于50ml离心管中,准确至0.001g,加入45ml吐温-氯化钙溶液,混匀后离心(4000r/min,20min),取出离心管中上层油脂层。
39.4.油脂含量测定:将样品上层油脂层置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干,蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内,将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
40.实施例3油脂含量测定
41.1.氯化钙溶液配置:取氯化钙和纯化水按照10:90的质量比配置,溶解;
42.2.吐温-氯化钙溶液配置:取吐温和氯化钙溶液,按照5:95的体积比配置成吐温-氯化钙溶液,混匀。
43.3.样品处理:称取样品5g,于50ml离心管中,准确至0.001g,加入45ml吐温-氯化钙溶液,混匀后离心(4000r/min,20min),取出离心管中上层油脂层。
44.4.油脂含量测定:将样品上层油脂层置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干,蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内,将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
45.实施例4油脂含量测定
46.1.氯化钙溶液配置:取氯化钙和纯化水按照12:88的质量比配置,溶解;
47.2.吐温-氯化钙溶液配置:取吐温和氯化钙溶液,按照7:93的体积比配置成吐温-氯化钙溶液,混匀。
48.3.样品处理:称取样品5g,于50ml离心管中,准确至0.001g,加入45ml吐温-氯化钙
溶液,混匀后离心(4000r/min,20min),取出离心管中上层油脂层。
49.4.油脂含量测定:将样品上层油脂层置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干,蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内,将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
50.实施例5油脂含量测定
51.1.氯化钙溶液配置:取氯化钙和纯化水按照15:85的质量比配置,溶解;
52.2.吐温-氯化钙溶液配置:取吐温和氯化钙溶液,按照10:90的体积比配置成吐温-氯化钙溶液,混匀。
53.3.样品处理:称取样品5g,于50ml离心管中,准确至0.001g,加入45ml吐温-氯化钙溶液,混匀后离心(4000r/min,20min),取出离心管中上层油脂层。
54.4.油脂含量测定:将样品上层油脂层置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干,蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内,将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
55.实施例6油脂含量测定
56.称取样品5g,准确至0.001g,置于蒸发皿中,加入约20g石英砂,于沸水浴上蒸干后,在电热鼓风干燥箱中于100℃
±
5℃干燥30min后,取出,研细,全部移入滤纸筒内。蒸发皿及粘有试样的玻璃棒,均用沾有乙醚的脱脂棉擦净,并将棉花放入滤纸筒内。将滤纸筒放入索氏抽提器的抽提筒内,连接已干燥至恒重的接收瓶,由抽提器冷凝管上端加入无水乙醚热水浴进行抽提。提取结束时,用磨砂玻璃棒接取1滴提取液,磨砂玻璃棒上无油斑表明提取完毕。取下接收瓶,回收无水乙醚或石油醚,待接收瓶内溶剂剩余1ml~2ml时在水浴上蒸干,再于100℃
±
5℃干燥1h,放干燥器内冷却0.5h后称量。重复以上操作直至恒重。通过gb5009.6-2016《食品安全国家标准食品中脂肪的测定》中的相关公式计算试样的脂肪含量。
57.实施例7样品无菌检测前处理
58.1)氯化钙溶液配置:取氯化钙和纯化水按照9:91的质量比配置,溶解,灭菌;
59.2)吐温-氯化钙溶液配置:取已灭菌吐温和上述已灭菌的氯化钙溶液,按照1:99的体积比配置成吐温-氯化钙溶液,混匀后备用;
60.供试品对照组
61.取20件未灭菌的样品,每管同法操作,操作如下:
62.每件样品称取20g于已灭菌的250ml蓝盖瓶中,加入180ml吐温-氯化钙溶液,混匀后分装于4个50ml无菌离心管中,37℃水浴30min后离心(4000rpm/min,20min),取出对离心管表面杀菌。取两个离心管油脂层分别涂抹在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上;分别对两个离心管中间层溶液进行过滤,过滤后每个滤膜使用100mlph7.0无菌氯化钠蛋白胨缓冲液溶液冲洗,一共冲洗三次,其中一个滤膜接种于装有硫乙醇酸盐流体培养基中,另外一个滤膜接种与胰酪大豆胨液体培养基中;每个离心管使用4mlph7.0无菌氯化钠蛋白胨缓冲液-蛋白胨缓冲液溶解底部沉淀,溶解后将其中一个离心管中的4ml溶液接种于装有50ml硫乙醇酸盐流体培养基的试管中,另一个离心管的4ml溶液接种于装有50ml胰酪大豆胨液体培养基的试管中。
63.实施例8样品无菌检测前处理
64.1)氯化钙溶液配置:取氯化钙和纯化水按照9:91的质量比配置,溶解,灭菌;
65.2)吐温-氯化钙溶液配置:取已灭菌吐温和上述已灭菌的氯化钙溶液,按照3:97的体积比配置成吐温-氯化钙溶液,混匀后备用;
66.供试品对照组
67.取20件未灭菌的样品,每管同法操作,操作如下:
68.每件样品称取20g于已灭菌的250ml蓝盖瓶中,加入180ml吐温-氯化钙溶液,混匀后分装于4个50ml无菌离心管中,37℃水浴30min后离心(4000rpm/min,20min),取出对离心管表面杀菌。取两个离心管油脂层分别涂抹在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上;分别对两个离心管中间层溶液进行过滤,过滤后每个滤膜使用100mlph7.0无菌氯化钠蛋白胨缓冲液溶液冲洗,一共冲洗三次,其中一个滤膜接种于装有硫乙醇酸盐流体培养基中,另外一个滤膜接种与胰酪大豆胨液体培养基中;每个离心管使用4mlph7.0无菌氯化钠蛋白胨缓冲液-蛋白胨缓冲液溶解底部沉淀,溶解后将其中一个离心管中的4ml溶液接种于装有50ml硫乙醇酸盐流体培养基的试管中,另一个离心管的4ml溶液接种于装有50ml胰酪大豆胨液体培养基的试管中。
69.实施例9样品无菌检测前处理
70.1)氯化钙溶液配置:取氯化钙和纯化水按照9:91的质量比配置,溶解,灭菌;
71.2)吐温-氯化钙溶液配置:取已灭菌吐温和上述已灭菌的氯化钙溶液,按照5:95的体积比配置成吐温-氯化钙溶液,混匀后备用;
72.供试品对照组
73.取20件未灭菌的样品,每管同法操作,操作如下:
74.每件样品称取20g于已灭菌的250ml蓝盖瓶中,加入180ml吐温-氯化钙溶液,混匀后分装于4个50ml无菌离心管中,37℃水浴30min后离心(4000rpm/min,20min),取出对离心管表面杀菌。取两个离心管油脂层分别涂抹在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上;分别对两个离心管中间层溶液进行过滤,过滤后每个滤膜使用100mlph7.0无菌氯化钠蛋白胨缓冲液溶液冲洗,一共冲洗三次,其中一个滤膜接种于装有硫乙醇酸盐流体培养基中,另外一个滤膜接种与胰酪大豆胨液体培养基中;每个离心管使用4mlph7.0无菌氯化钠蛋白胨缓冲液-蛋白胨缓冲液溶解底部沉淀,溶解后将其中一个离心管中的4ml溶液接
种于装有50ml硫乙醇酸盐流体培养基的试管中,另一个离心管的4ml溶液接种于装有50ml胰酪大豆胨液体培养基的试管中。
75.实施例10样品无菌检测前处理
76.1)氯化钙溶液配置:取氯化钙和纯化水按照9:91的质量比配置,溶解,灭菌;
77.2)吐温-氯化钙溶液配置:取已灭菌吐温和上述已灭菌的氯化钙溶液,按照7:93的体积比配置成吐温-氯化钙溶液,混匀后备用;
78.供试品对照组
79.取20件未灭菌的样品,每管同法操作,操作如下:
80.每件样品称取20g于已灭菌的250ml蓝盖瓶中,加入180ml吐温-氯化钙溶液,混匀后分装于4个50ml无菌离心管中,37℃水浴30min后离心(4000rpm/min,20min),取出对离心管表面杀菌。取两个离心管油脂层分别涂抹在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上;分别对两个离心管中间层溶液进行过滤,过滤后每个滤膜使用100mlph7.0无菌氯化钠蛋白胨缓冲液溶液冲洗,一共冲洗三次,其中一个滤膜接种于装有硫乙醇酸盐流体培养基中,另外一个滤膜接种与胰酪大豆胨液体培养基中;每个离心管使用4mlph7.0无菌氯化钠蛋白胨缓冲液-蛋白胨缓冲液溶解底部沉淀,溶解后将其中一个离心管中的4ml溶液接种于装有50ml硫乙醇酸盐流体培养基的试管中,另一个离心管的4ml溶液接种于装有50ml胰酪大豆胨液体培养基的试管中。
81.实施例11样品无菌检测前处理
82.1)氯化钙溶液配置:取氯化钙和纯化水按照9:91的质量比配置,溶解,灭菌;
83.2)吐温-氯化钙溶液配置:取已灭菌吐温和上述已灭菌的氯化钙溶液,按照1:9的体积比配置成吐温-氯化钙溶液,混匀后备用;
84.供试品对照组
85.取20件未灭菌的样品,每管同法操作,操作如下:
86.每件样品称取20g于已灭菌的250ml蓝盖瓶中,加入180ml吐温-氯化钙溶液,混匀后分装于4个50ml无菌离心管中,37℃水浴30min后离心(4000rpm/min,20min),取出对离心管表面杀菌。取两个离心管油脂层分别涂抹在胰酪大豆胨琼脂培养基和沙氏葡萄糖琼脂培养基上;分别对两个离心管中间层溶液进行过滤,过滤后每个滤膜使用100mlph7.0无菌氯化钠蛋白胨缓冲液溶液冲洗,一共冲洗三次,其中一个滤膜接种于装有硫乙醇酸盐流体培养基中,另外一个滤膜接种与胰酪大豆胨液体培养基中;每个离心管使用4mlph7.0无菌氯化钠蛋白胨缓冲液-蛋白胨缓冲液溶解底部沉淀,溶解后将其中一个离心管中的4ml溶液接种于装有50ml硫乙醇酸盐流体培养基的试管中,另一个离心管的4ml溶液接种于装有50ml胰酪大豆胨液体培养基的试管中。
87.实验例1油脂含量测定结果
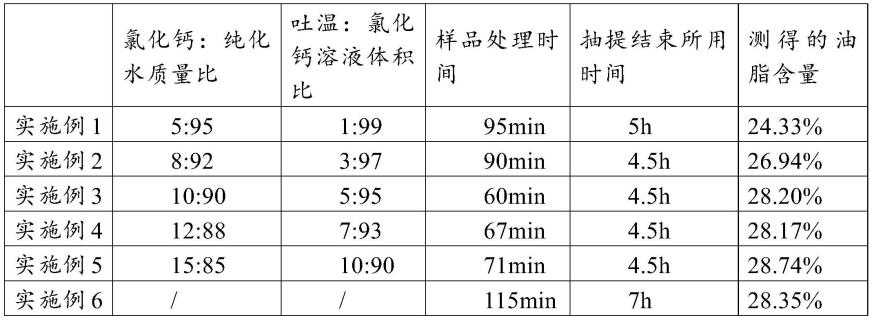
88.统计实施例1-6的样品处理时间、抽提结束所用时间和测得的油脂含量。结果如下表1所示。
89.表1
[0090][0091]
从表1可以看出,实施例1-5的样品处理时间和抽提结束所用时间相对于采用国标索氏抽提法的实施例6均有明显降低,同时油脂含量检测实验结果与国标中索氏抽提法的结果无显著性差异。其中,发明人出乎预料地发现,实施例3-5所花费的样品处理时间和抽提结束所用时间进一步降低,且油脂含量检测实验结果与国标检测方法的结果更加接近。故将实施例3-5作为本发明的优选实施例。
[0092]
实验例2样品无菌检测前处理实验结果
[0093]
统计实施例7-11中的过滤快慢和时间。结果如下表2所示。
[0094]
表2
[0095][0096]
在该实验中,实施例7和8的产品不能较好地使样品乳化分层,无法过滤;实施例9的产品分离效果最佳,过滤速度较快;实施例10和11的产品也可通过过滤器,但过滤速度慢于实施例9。
[0097]
应该理解到披露的本发明不仅仅限于描述的特定的方法、方案和物质,因为这些均可变化。还应理解这里所用的术语仅仅是为了描述特定的实施方式方案的目的,而不是意欲限制本发明的范围,本发明的范围仅受限于所附的权利要求。
[0098]
本领域的技术人员还将认识到,或者能够确认使用不超过常规实验,在本文中所述的本发明的具体的实施方案的许多等价物。这些等价物也包含在所附的权利要求中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1