HPLC测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的方法与流程
hplc测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的方法
技术领域
1.本发明属于葡萄糖酸根含量测定技术领域,尤其涉及一种使用edta-2na络合的样品溶液制备方法,实现采用hplc检测方法用单一对照品葡萄糖酸钙完成葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的准确测定。
背景技术:
2.葡萄糖酸钙锌口服溶液是由葡萄糖酸钙、葡萄糖酸锌、盐酸赖氨酸等组成的复方制剂。葡萄糖酸钙常用来维持神经肌肉的兴奋性、促进神经末梢分泌乙酰胆碱,也能改善细胞膜的通透性,增加毛细血管的致密性;葡萄糖酸锌与体内80多种酶的活性有关,具有促进器官发育和智力提高、促进伤口愈合以及提高免疫功能等作用。葡萄糖酸钙锌口服溶液的国家标准为ws1-xg-008-2001,对其中的含量测定项目仅进行了钙离子、锌离子及盐酸赖氨酸的含量进行了规定。2020年cde发布了葡萄糖酸钙锌口服溶液药学研究技术要求,新增葡萄糖酸根含量的控制要求。2021年国家药典委对葡萄糖酸钙口服溶液品种增订了葡萄糖酸根含量测定的要求。
3.采用《中国药典2020年版二部》增补版中葡萄糖酸钙口服溶液中葡萄糖酸根hplc含量测定方法,方法如下所述:色谱柱:caprisil c18-aq,4.6 *250mm,5μm;色谱条件:以10mmol/l磷酸二氢钾溶液-5mmol/l四丁基硫酸氢铵溶液(ph=7.0):甲醇=98:2为流动相,流速为每分钟1.0ml,柱温为30℃;检测波长为210nm,进样量25μl,采集时间为10min。
4.对照品溶液(2mg/ml)的配制:取葡萄糖酸钙对照品约20mg,精密称定,置10ml量瓶中,用水溶解并稀释至刻度,摇匀,即得;样品溶液的配制:精密量取本品3.0ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得。
5.精密移取对照品溶液和供试品溶液注入hplc系统,记录色谱图,以峰面积按外标法计算葡萄糖酸根的含量。以葡萄糖酸钙为对照品,测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量,结果葡萄糖酸根含量为标示量的92%;以葡萄糖酸锌为对照品,测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量,结果葡萄糖酸根含量为标示量的86%;按照供试品中比例配制葡萄糖酸钙和葡萄糖酸锌混合对照品溶液,测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量,结果葡萄糖酸根含量为标示量的88%。因此,采用药典方法测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量明显偏低。
技术实现要素:
6.本发明的目的在于提供一种hplc法测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的方法,供试品和对照品溶液配制方法简单,易操作,检测结果准确性高,检测的葡萄糖酸根含量偏差小,实现了使用单一的葡萄糖酸钙对照品即可完成对复方制剂葡萄糖酸钙锌
口服溶液中葡萄糖酸根总量进行测定。
7.为了实现本发明的目的,本发明提供了一种使用edta二钠溶液进行样品前处理后的葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的hplc测定方法,具体包括以下步骤:(1)葡萄糖酸钙对照品溶液的配制:取对照品葡萄糖酸钙加水溶解后,往葡萄糖酸钙溶液中加入氢氧化钠溶液调节ph值大于12,然后加入edta-2na溶液混合均匀后,静置至少5min,再加入稀盐酸调节ph值至4.7~9.6,得到每1ml中含葡萄糖酸钙2.0mg
±
0.2mg的对照品溶液;(2)供试品溶液的配制:取葡萄糖酸钙锌口服溶液,加入氢钠化钠溶液调节ph值大于12,然后加入edta-2na溶液混合均匀后,静置至少5min,再加入稀盐酸调节ph值至4.7~9.6,得到每1ml含葡萄糖酸钙浓度为1.8mg
±
0.2mg的供试品溶液;(3)样品检测:将上述对照品溶液和供试品溶液在hplc中进行检测,记录色谱图;(4)葡萄糖酸根含量的计算:按外标法以峰面积计算葡萄糖酸根的含量。
8.进一步的,所述步骤(1)中,每20mg
±
4mg葡萄糖酸钙中加入氢氧化钠的量为0.4mmol。
9.进一步的,所述葡萄糖酸钙对照品溶液和供试品溶液中,每10mg葡萄糖酸钙中加入的edta-2na的量不少于25
µ
mol。
10.进一步的,所述步骤(1)和所述步骤(2)中,所述加入稀盐酸的量中氯化氢的物质的量为加入氢氧化钠的物质的量的一半。
11.进一步的,所述步骤(2)中,每1.5ml
±
0.3ml葡萄糖酸钙锌口服溶液中加入氢氧化钠的量为2mmol。
12.进一步的,所述葡萄糖酸酸钙对照品溶液的配制过程为:取葡萄糖酸钙对照品约20mg,精密称定,用水溶解,置10ml量瓶中,加入1mol/l氢氧化钠溶液0.4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液1ml,摇匀,静置5min,加入1mol/l盐酸溶液0.2ml,加水稀释至刻度,摇匀,即得。
13.进一步的,所述样品溶液的配制过程为:精密量取葡萄糖酸钙锌口服溶液3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得。
14.进一步的,所述步骤(3)中,所述hplc色谱检测条件为:固定相的高效液相色谱柱为丙烯酰胺键合硅胶色谱柱;流动相为50mmol/l磷酸二氢钾-乙腈(26:74);流动相流速为0.9~1.1ml/min;色谱柱柱温为33~37℃;进样量为10
µ
l;检测波长为210nm。
15.进一步的,所述丙烯酰胺键合硅胶色谱柱为venusil hilic色谱柱,规格为4.6*250mm,填料粒径5μm。
16.进一步的,所述流动相流速为1.0ml/min,所述色谱柱柱温为35℃。
17.本发明取得了以下有益效果:1、本发明通过在样品和对照品溶液配制过程中,加入适量edta-2na(即edta二钠)
溶液在ph值大于12的碱性环境下进行络合反应,即使edta-2na络合葡萄糖酸钙对照品和葡萄糖酸钙锌口服溶液中的阳离子后,使葡萄糖酸根充分游离,然后再加入一定量的盐酸调节溶液至近中性(ph值4.7~9.6),进而实现hplc方法用葡萄糖酸钙对照品完成葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的准确测定,克服了采用《中国药典》中hplc方法测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量偏低的难题。
18.2、本发明使用edta-2na溶液可同等程度的络合葡萄糖酸钙对照品和葡萄糖酸钙锌口服溶液中的阳离子,不会导致葡萄糖酸根的损失,使得利用葡萄糖酸钙对照品标定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量。
19.3、本发明的检测方法操作简单,检测结果准确性高,实现了使用单一的葡萄糖酸钙对照品即可完成对复方制剂葡萄糖酸钙锌口服溶液中葡萄糖酸根总量进行测定。并且,本发明检测方法的准确性经专属性、线性与范围、准确度、精密度、耐用性等试验进行了验证。
20.4、本发明样品溶液配制过程中,调节样品溶液ph范围在4.7~9.6范围内,溶液均稳定;样品溶液浓度(以葡萄糖酸钙计)在1.6mg/ml~2.4mg/ml范围内,葡萄糖酸根含量检测结果均准确。
附图说明
21.图1为本发明一实施例的空白溶液hplc图;图2为本发明一实施例的辅料空白溶液hplc图;图3为本发明一实施例的葡萄糖酸钙对照品溶液hplc图;图4为本发明一实施例的辅料加葡萄糖酸根溶液hplc图;图5为本发明一实施例的葡萄糖酸钙锌口服液中葡萄糖酸根hplc图;图6为本发明一实施例的葡萄糖酸根线性图。
具体实施方式
22.下面对本发明的具体实施方式进行详细地描述。本说明书中公开的所有特征,或公开的所有方法或过程中的步骤,除了互相排斥的特征和/或步骤以外,均可以以任何方式组合。
23.本发明具体实施例中使用的检测设备、药品及条件如下:1、仪器hitachi高效液相色谱仪,采用的配置为:四元泵,uv检测器,在线脱气系统,自动进样器,agilent openlab数据处理系统。
24.2、hplc分析方法的测试条件色谱柱:venusil hilic,4.6 *250mm,5μm;色谱条件:以50mmol/l磷酸二氢钾溶液:乙腈=26:74为流动相,流速为每分钟1.0ml,柱温为35
°
c;检测波长为210nm,采集时间为30min。
25.3、试剂与试药葡萄糖酸钙对照品,批号:100082-201803,来源:中国食品药品检定研究院,含量:100.0%。
26.葡萄糖酸锌对照品,批号:100332-201102,来源:中国食品药品检定研究院,含量:90.3%。
27.乙二胺四乙酸二钠溶液,批号:tm-2020-8006.16,来源:坛墨质检-标准物质中心,0.05026mol/l。
28.纯化水,批号202010510h,来源:屈臣氏。
29.乙腈,批号:2021ah006,来源:天津市康科德科技有限公司。
30.乙腈,批号:shbn1565,来源:merck。
31.磷酸二氢钾,批号:201807202,来源:天津风船化学试剂科技有限公司。
32.下面结合具体实施例对本发明的hplc测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量的方法予以说明,并对检测方法的准确度、重复性、精密度、耐用性等进行验证。
33.实施例1 样品中葡萄糖酸根含量的检测本实施例1的hplc法测定葡萄糖酸钙锌口服溶液中葡萄糖酸根含量方法,具体包括如下步骤:(1)空白溶液的配制:精密量取纯化水3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得。
34.(2)葡萄糖酸钙对照品溶液(2mg/ml)的配制:取葡萄糖酸钙对照品约20mg,精密称定,用水溶解,置10ml量瓶中,加入1mol/l氢氧化钠溶液0.4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液1ml,摇匀,静置5min,加入1mol/l盐酸溶液0.2ml,加水稀释至刻度,摇匀,即得。
35.(3)辅料溶液的配制:分别取盐酸赖氨酸0.3g,三氯蔗糖0.04g,乳酸0.8ml,置100ml量瓶,用水溶解并定容至刻度,摇匀,即得。
36.(4)辅料空白溶液的配制:精密量取辅料溶液3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得。
37.(5)样品溶液的配制:精密量取本品3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得。
38.(6)样品检测:将步骤(1)~(5)得到的溶液在hplc中进样检测。
39.其中,色谱检测条件为:色谱柱:丙烯酰胺键合硅胶色谱柱为固定相的高效液相色谱柱,流动相为50mmol/l磷酸二氢钾-乙腈(26:74)为流动相,流动相流速:1.0ml/min,色谱柱柱温:35
°
c,进样量为10
µ
l,检测波长:210nm。
40.(7)葡萄糖酸根含量的计算:按外标法以峰面积计算葡萄糖酸根的含量。
41.得到的空白溶液hplc图、辅料空白溶液hplc图、葡萄糖酸钙对照品溶液hplc图、葡萄糖酸钙锌口服溶液样品hplc图、葡萄糖酸钙锌口服液中葡萄糖酸根hplc图,分别如图1~5所示,结果表明,空白溶液和辅料空白溶液在葡萄糖酸根出峰位置处无干扰,满足要求。按外标法以峰面积计算样品中葡萄糖酸根含量。样品中葡萄糖酸根含量计算公式如下:
上式中:a
样
为供试品溶液中葡萄糖酸根峰面积;a
对照
为对照品溶液中葡萄糖酸根峰面积;c
对照
为对照品溶液中葡萄糖酸根浓度(mg/ml);d
样
为供试品溶液稀释倍数;标示量为54.80mg/ml。
42.按下述公式计算对照品溶液葡萄糖酸根浓度(mg/ml):上式中:w
对照
为对照品称样量(mg);p为对照品含量(即对照品证书中标识含量);v
对照
为对照品配制体积(ml);0.8704为换算系数。
43.根据使用的葡萄糖酸钙锌口服溶液样品处方(【规格】10毫升;葡萄糖酸钙0.6克、葡萄糖酸锌0.03克与盐酸赖氨酸0.1克)计算得到的葡萄糖酸根标示量为54.80mg/ml。
44.本实施例1采用edta-2na溶液络合葡萄糖酸钙锌口服溶液中的钙离子和锌离子后,根据上述使用hplc法测定其中的总葡萄糖酸根含量,如图1~5的色谱图,按外标法以峰面积计算样品中葡萄糖酸根含量,计算得样品葡萄糖酸钙锌口服溶液中葡萄糖酸根含量为标示量的96.6%。
45.实施例2 专属性实验考察空白溶液、辅料空白溶液和样品溶液中其它成分对色谱峰是否干扰。
46.空白溶液:精密量取纯化水3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀。
47.葡萄糖酸钙对照品溶液:取葡萄糖酸钙对照品约20mg,精密称定,用水溶解,置10ml量瓶中,加入1mol/l氢氧化钠溶液0.4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液1ml,摇匀,静置5min,加入1mol/l盐酸溶液0.2ml,加水稀释至刻度,摇匀,即得。
48.辅料溶液:分别取盐酸赖氨酸0.3g,三氯蔗糖0.04g,乳酸0.8ml,置100ml量瓶,用水溶解并定容至刻度,摇匀,即得。
49.辅料空白溶液:精密量取辅料溶液3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得;样品溶液:精密量取本品3.0ml,置100ml量瓶中,加入1mol/l氢氧化钠溶液4ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液10ml,摇匀,静置5min,加入1mol/l盐酸溶液2ml,加水稀释至刻度,摇匀,即得。
50.取空白溶液、辅料空白溶液、葡萄糖酸钙对照品溶液和样品溶液各10
µ
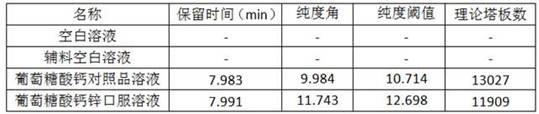
l,注入液相色谱仪,记录色谱图,并将专属性试验结果列于表1。
51.表1 专属性试验结果
从图1~4及表1可以看出,空白溶液及辅料空白不干扰主成分检测,结果葡萄糖酸根峰形良好,纯度角(9.984)小于纯度阈值(10.714),理论塔板数为13027,符合可接受的标准。其中,可接受的标准为:空白溶液及辅料空白溶液不干扰主成分出峰;葡萄糖酸根色谱峰理论塔板数应不小于5000,纯度角小于纯度阈值。
52.实施例3 系统精密度实验取浓度为2mg/ml葡萄糖酸钙对照品溶液连续进样6次,记录色谱图,计算葡萄糖酸根峰面积rsd。将连续6次进样的葡萄糖酸根峰面积rsd列于表2,从表2中可知,葡萄糖酸根峰面积rsd为0.1%,小于2%。因此,本方法系统精密度良好。
53.表2精密度检测结果实施例4 线性与范围配制葡萄糖酸根浓度分别为0.89mg/ml、1.43mg/ml、1.78mg/ml、2.14mg/ml和 2.67mg/ml的葡萄糖酸钙对照品溶液,将不同浓度的溶液由低到高依次进样,以浓度为横坐标,平均峰面积为纵坐标,进行线性回归,得到的葡萄糖酸根线性图,如图6所示,线性浓度和峰面积结果列于表3中,得到的葡萄糖酸根线性方程为y =1292226.3360x+7525.1655,相关系数r=0.9996>0.999。由此可知,葡萄糖酸根在0.89mg/ml~2.67mg/ml浓度范围内线性关系良好。
54.表3葡萄糖酸根线性浓度和峰面积结果实施例5 准确度实验分别制备低、中、高3个不同浓度的空白辅料加标溶液,每种浓度分别制备3份溶液考察方法的准确度。
55.葡萄糖酸钙对照品溶液:取葡萄糖酸钙对照品约10mg,精密称定,置5ml量瓶中,用水溶解,加入1mol/l氢氧化钠溶液0.2ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液0.5ml,摇匀,超声5min,加入1mol/l盐酸溶液0.1ml,用水稀释至刻度,摇匀,即得。
56.葡萄糖酸钙对照品储备液(简称钙储备液):取葡萄糖酸钙对照品约180mg,精密称
定,置10ml量瓶中,用水溶解并稀释至刻度,摇匀,即得。
57.葡萄糖酸锌对照品储备液(简称锌储备液):取葡萄糖酸锌对照品约18mg,精密称定,置20ml量瓶中,用水溶解并稀释至刻度,摇匀,即得。
58.辅料溶液:分别取盐酸赖氨酸0.3g,三氯蔗糖0.04g,乳酸0.8ml,置100ml量瓶,用水溶解并定容至刻度,摇匀即得。
59.按下表4的比例配制不同水平回收率溶液,每个水平溶液平行配制三份,将上述溶液进样分析。
60.表4准确度溶液配制可接受标准:各水平溶液平均回收率应在95%~102%范围内。其检测结果如下表5所示。
61.表5准确度试验结果 如上表5所示的检测结果为:80%水平溶液平均回收率98.1%,100%水平溶液平均回收率98.2%,120%水平溶液平均回收率97.0%,符合要求,因此,本发明的检测方法准确性良好,样品溶液浓度在0.024ml/ml~0.036ml/ml范围内,葡萄糖酸根含量检测准确。
62.实施例6 重复性实验葡萄糖酸钙对照品溶液:取葡萄糖酸钙对照品约10mg,精密称定,置5ml量瓶中,用水溶解,加入1mol/l氢氧化钠溶液0.2ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液0.5ml,摇匀,超声5min,加入1mol/l盐酸溶液0.1ml,用水稀释至刻度,摇匀,即得。
63.样品溶液:精密量取本品1.5ml,置50ml量瓶中,加入1mol/l氢氧化钠溶液2ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液5ml,摇匀,超声5min,加入1mol/l盐酸溶液1ml,加水稀释至刻度,摇匀,平行配制6份。进样分析,考察样品溶液中葡萄糖酸根含量与标示量
比值的rsd,如下表6。
64.可接受标准:6份样品溶液中测得葡萄糖酸根含量与标示量比值的rsd应不大于2%。
65.表6重复性结果从上述表6的检测结果可以看出:6份样品溶液中测得葡萄糖酸根含量与标示量比值的rsd 为0.3%,符合要求,因此,本发明的检测方法重复性良好。
66.实施例7 中间精密度实验由不同人员于不同日期配制样品溶液6份,考察样品溶液中葡萄糖酸根含量与标示量比值的rsd。
67.可接受标准:中间精密度6份测试溶液,测得葡萄糖酸根含量与标示量比值rsd≤2%;中间精密度与重复性共12份测试溶液,测得葡萄糖酸根含量与标示量比值的rsd≤2%。
68.检测结果:中间精密度6份测试溶液测得葡萄糖酸根含量与标示量比值rsd 为0.3%,符合要求,与重复性共12份测试溶液测得葡萄糖酸根含量与标示量比值的rsd为0.3%,如下表7。
69.表7中间精密度结果从上述表7的结果可以看出,本发明检测方法的中间精密度良好。
70.实施例8 耐用性实验参考葡萄糖酸根含量测定液相色谱方法,适度改变方法,调整柱温
±
2℃、流速
±
0.1ml/min情况下,验证本发明的检测方法是否适用。
71.配制葡萄糖酸钙对照品溶液和样品溶液,在不同耐用性条件下,分别进样分析,记录色谱图,按外标法以峰面积计算葡萄糖酸根的含量。调整柱温
±
2℃、流速
±
0.1ml/min情况下得到的耐用性试验结果见表8,由表8的数据可知,在改变本发明检测方法的柱温(35
±
2℃)、流速(1.0
±
0.1ml/min)条件下,葡萄糖酸根含量rsd值均小于2%。说明本发明的检测
方法耐用性良好。
72.表8耐用性实验结果实施例9 ph耐用性实验考察使用1mol/l盐酸溶液调节样品溶液ph后,样品溶液的稳定性。精密量取本品1.5ml,置50ml量瓶中,加入1mol/l氢氧化钠溶液2.0ml,摇匀,加入0.05mol/l乙二胺四乙酸二钠溶液5.0ml,超声5min,加入不同体积的1mol/l盐酸溶液,加水稀释至刻度,摇匀,进样分析,结果见表9。
73.表9样品溶液不同ph下稳定性结果结果:样品溶液配制过程中,调节样品溶液ph范围在4.7~9.6范围内,溶液均稳定。
74.以上所述实施例仅表达了本发明的具体实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1