一种工艺特异性宿主细胞蛋白残留的检测方法及试剂盒与流程
本发明涉及生物制药领域,特别涉及一种工艺特异性宿主细胞蛋白残留的检测方法及试剂盒。
背景技术:
1、生物制药是利用生物活体来生产药物的方法。随着生物技术的发展,人工制备的生物原料成为当前生物制药原料的主要来源。生物制药技术作为战略性新兴产业技术,发展迅猛,在制药工艺中广泛应用。现代生物制药特点是以基因工程为主导,包括细胞工程、发酵工程、酶工程和组织工程等技术的应用。
2、大多数生物药物是通过重组dna技术,使用宿主细胞来表达目标蛋白药物。由于宿主细胞本身的蛋白质也会大量表达,因此重组蛋白药物会受到宿主细胞蛋白( host cellprotein, hcp)的污染。宿主细胞中含有各种可能给生物制品造成污染的hpc、dna和内毒素等,即使经过复杂的纯化步骤,最终获得的生物药产品中仍有可能残留低浓度的hcp。
3、基因工程重组生物制品中残留的hcp作为外源蛋白,其潜在的免疫原性有可能诱导机体产生相应抗体;其潜在的“佐剂效应”也可能会引起机体对药物产生抗体,进而影响药物的疗效。灵敏度高、重复性好的宿主蛋白检测方法不仅是保证生物制品安全有效的关键,也是生产过程控制和工艺优化的重要参数。由于hcp可能会引起不可预测的免疫反应,因此相关法规要求对hcp进行鉴定和定量,以保障患者使用安全。hcp残留检测是生物药能否成功获批的重要因素之一。
4、由于伴随细胞凋亡、死亡、裂解等,除了目标蛋白外,其他非必需蛋白也可释放到细胞培养或发酵上清中。hcp构成了生物制品生产工艺过程与过程相关杂质的主要组成部分。生物制品中残余hcp含量通常被认为是产品的关键质量属性(cqa),因为hcp有可能影响产品的安全性和功效。hcp可以起免疫原性的作用而直接激发机体产生针对特定hcp杂质的抗体,同时也可以作为佐剂从而增加机体对治疗蛋白的免疫反应以及产生抗抗体,进而直接影响药物的生物分布、药代动力学和生物活性等。
5、目前,商品化的hcp试剂盒检测结果只代表通用的hcp含量和比例,但是每个项目都有其特异的hcp比例,而且各个蛋白对hcp的检测干扰程度不一样,所以建立专属的hcp检测方法是非常必要的。
技术实现思路
1、本发明的目的在于提供一种工艺特异性宿主细胞蛋白残留的检测方法及试剂盒,可以更有目的性地、更加准确地检测出目的重组蛋白药品中的宿主细胞蛋白残留,提高检测的灵敏性。
2、为了达到上述目的,本发明的一个方面提供了一种工艺特异性宿主细胞蛋白残留的检测方法,包括:
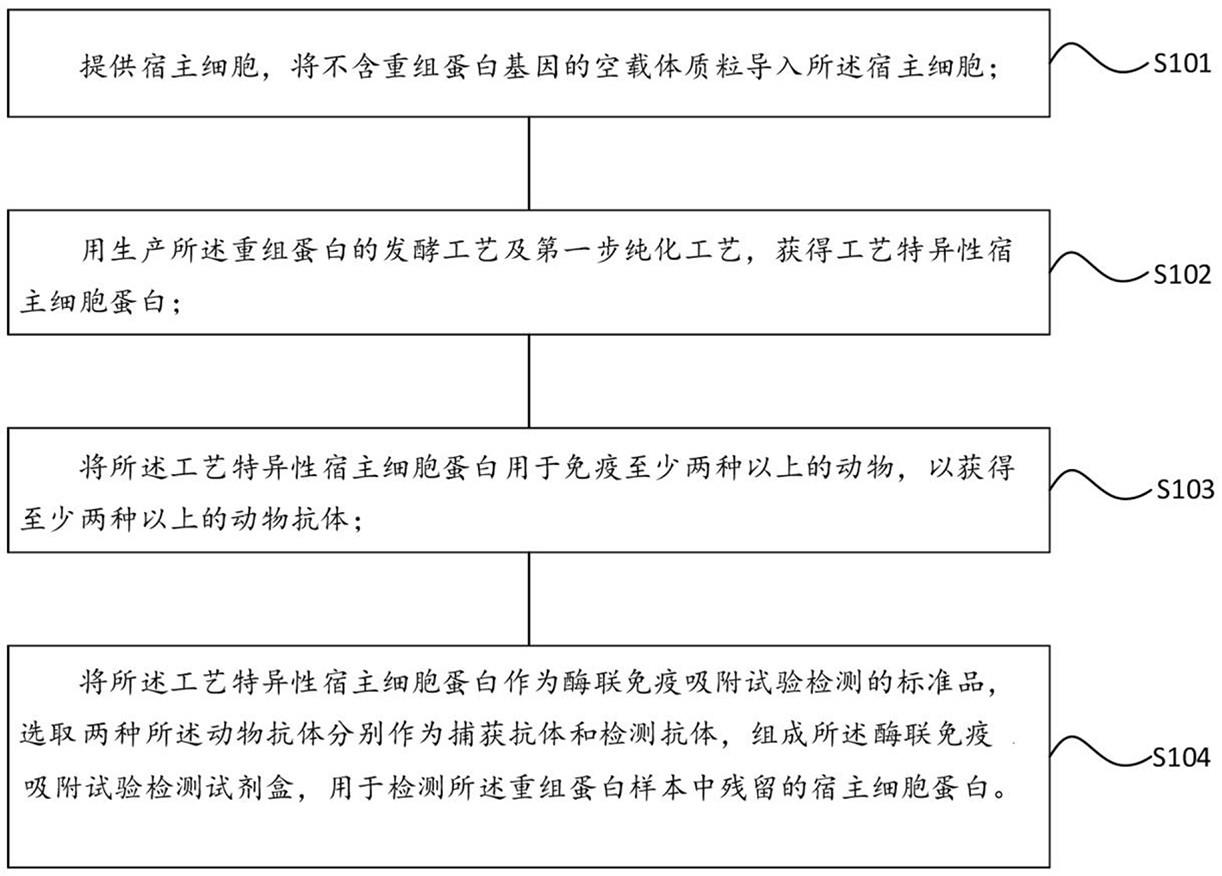
3、步骤s101:提供宿主细胞,将不含重组蛋白基因的空载体质粒导入所述宿主细胞;
4、步骤s102:用生产所述重组蛋白的发酵工艺及第一步纯化工艺,获得工艺特异性宿主细胞蛋白;
5、步骤s103:将所述工艺特异性宿主细胞蛋白用于免疫至少两种动物,以获得至少两种动物抗体;
6、步骤s104:将所述工艺特异性宿主细胞蛋白作为酶联免疫吸附试验检测的标准品,选取两种所述动物抗体分别作为捕获抗体和检测抗体,组成所述酶联免疫吸附试验检测试剂盒,用于检测待测样本中残留的宿主细胞蛋白;
7、其中,所述重组蛋白为利拉鲁肽前体,所述待测样本为利拉鲁肽前体产品或利拉鲁肽产品;
8、所述步骤s102包括:
9、步骤s102-1:将所述宿主细胞发酵及iptg诱导培养以获得原液;
10、步骤s102-2:将所述原液离心以获得菌体;
11、步骤s102-3:在所述菌体中加入裂解缓冲液获得菌体重悬液;
12、步骤s102-4:将所述菌体重悬液通过高压均质及离心后收集上清液,所述上清液经滤膜过滤后获得含所述工艺特异性宿主细胞蛋白的蛋白液;
13、步骤s102-5:将所述蛋白液经过镍柱纯化后,获得所述工艺特异性宿主细胞蛋白;
14、所述步骤s102-5包括:
15、所述镍柱为采用ni-nta亲和层析介质填充的层析柱;
16、依次采用平衡缓冲液、所述蛋白液、所述平衡缓冲液、洗脱缓冲液过柱;
17、所述平衡缓冲液的配方为:24~25mm咪唑、48~51mm磷酸盐、290~310mm氯化钠,ph调节为6.8-7.2;
18、洗脱缓冲液的配方为:390~410mm咪唑、48~51mm磷酸盐、290~310mm氯化钠,ph调节为8.0-8.2。
19、优选的,所述洗脱缓冲液的配方为:400mm咪唑、50mm磷酸钾、300mm氯化钠,ph调节为8.1。
20、优选的,取所述层析柱4~6倍柱体积的所述平衡缓冲液过柱,控制过柱的线性流速为85~90cm/h,以平衡所述层析柱;
21、取所述层析柱6~9倍柱体积的所述蛋白液过柱,控制过柱的线性流速为85~90cm/h,以使所述工艺特异性宿主细胞蛋白附着在所述ni-nta亲和层析介质;
22、取所述层析柱6~8倍柱体积的所述平衡缓冲液过柱,控制过柱的线性流速为85~90cm/h,以洗涤所述ni-nta亲和层析介质;
23、取所述层析柱6~9倍柱体积的所述洗脱缓冲液过柱;控制过柱的线性流速为85~90cm/h,以洗脱附着在所述ni-nta亲和层析介质的所述工艺特异性宿主细胞蛋白。
24、优选的,在所述步骤s103中,将所述工艺特异性宿主细胞蛋白用于免疫鼠和兔,以获得鼠抗体和兔抗体,获得所述鼠抗体和所述兔抗体的步骤包括:
25、对所述鼠进行4次免疫,第四次免疫与第三次免疫的间隔时间为4周,将0.5ml1mg/ml的所述工艺特异性宿主细胞蛋白与0.5 ml福氏完全佐剂混合用于第一次免疫,免疫剂量为0.1ml,使用1mg/ml的所述工艺特异性宿主细胞蛋白用于第二次和第三次免疫,第二次免疫和第三次免疫的用量分别为0.05ml、第四次免疫的用量为0.25ml,所述鼠第四次免疫后间隔1周对所述鼠进行采血,分离血清以获得所述鼠抗体;
26、对所述兔进行4次免疫,第一次免疫、第二次免疫和第三次免疫的间隔时间为2周,第四次免疫与第三次免疫的间隔时间为4周,将1ml 1mg/ml的所述工艺特异性宿主细胞蛋白与1.5 ml福氏完全佐剂混合用于第一次免疫,免疫剂量为1 ml,使用1mg/ml的所述工艺特异性宿主细胞蛋白用于第二次免疫、第三次免疫和第四次免疫,第二次免疫和第三次免疫的用量分别为0.5 ml、第四次免疫的用量为1 ml,所述兔第四次免疫后间隔1周对所述兔进行采血,分离血清后以获得所述兔抗体。
27、优选的,所述步骤s104包括:
28、提供酶标板,用19~21μg/ml第一所述动物抗体,在4℃的温度下,包被过夜,以形成第一阶段固相载体;
29、取300μl的1%浓度的bsa作为封闭液,加入至所述第一阶段固相载体后,在37℃的温度下,孵育1h,以形成第二阶段固相载体;
30、选取所述第二阶段固相载体中的若干个板孔,分别加入100μl的不同浓度的所述工艺特异性宿主细胞蛋白和所述重组蛋白样本,在37℃的温度下,孵育1h,以形成第三阶段固相载体;
31、将不同于第一所述动物抗体的第二所述动物抗体稀释500~1000倍,加入至所述第三阶段固相载体,在37℃的温度下,孵育1h,以形成第四阶段固相载体;
32、将与第二所述动物抗体结合的hrp偶联的二抗稀释5000-15000倍,加入至所述第四阶段固相载体,形成第五阶段固相载体;
33、向所述第五阶段固相载体加入tmb,显色时间为3-5min;
34、用酶标仪测定所述第五阶段固相载体中的所述板孔的a450吸光值。
35、优选的,第一所述动物抗体为兔抗体,第二所述动物抗体为鼠抗体,所述hrp偶联的二抗为hrp偶联的羊抗鼠抗体。
36、优选的,所述宿主细胞为大肠杆菌。
37、优选的,用于检测的所述待测样本的浓度为:所述利拉鲁肽前体产品的浓度为0.25mg/ml-0.0625mg/ml,所述利拉鲁肽产品的浓度为0.5mg/ml。
38、优选地,所述步骤s104中,所述工艺特异性宿主细胞蛋白的浓度梯度为:1000ng/ml、500ng/ml、250ng/ml、125ng/ml、62.5ng/ml、31.25ng/ml、15.625ng/ml、7.8125ng/ml、3.90625ng/ml。
39、本发明的另一方面在于提供一种用于上述检测方法的试剂盒,所述试剂盒包含所述工艺特异性宿主细胞蛋白、两种所述动物抗体分别作为捕获抗体和检测抗体、以及结合所述检测抗体的hrp偶联的二抗。
40、在本发明提供的工艺特异性宿主细胞蛋白残留的检测方法中,将不含重组蛋白基因的空载体质粒导入所述宿主细胞后,用生产所述重组蛋白的发酵工艺产生工艺特异性宿主细胞蛋白,及用生产所述重组蛋白的第一步纯化工艺进行纯化,获得所述工艺特异性宿主细胞蛋白。由于本发明的工艺特异性宿主细胞蛋白是在重组蛋白的发酵过程中产生,且在重组蛋白的纯化过程中不被完全去除的宿主细胞蛋白。因此,本发明的检测方法能够更加准确和灵敏地检测出基因工程重组蛋白样品中的宿主细胞蛋白残留。并且,通过使用生产所述重组蛋白的第一步纯化工艺进行纯化,与使用全部纯化工艺相比,能够得到适合数量的宿主细胞蛋白,由此构建的试剂盒以及检测方法的准确度及灵敏度更高。此外,将所述工艺特异性宿主细胞蛋白用于免疫至少两种动物,以获得至少两种动物抗体;将所述工艺特异性宿主细胞蛋白作为酶联免疫吸附试验检测的标准品,选取两种所述动物抗体分别作为捕获抗体和检测抗体,组成所述酶联免疫吸附试验检测试剂盒,用于检测所述重组蛋白样本中残留的宿主细胞蛋白。本发明采用两种所述动物抗体分别作为捕获抗体和检测抗体作为夹心酶联免疫吸附试验检测试剂盒,能够具有更高的检测灵敏度、更高的特异性和以及用于检测成分更复杂的重组蛋白样品。
- 还没有人留言评论。精彩留言会获得点赞!