作为电解质和电极保护层的硼硅酸锂玻璃的制作方法
本发明涉及硼硅酸锂电解质和包含该硼硅酸锂电解质的电池。
发明背景
本发明涉及硼硅酸锂玻璃组合物,其基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,并优选地基本上由氧化锂、氧化硅和氧化硼的三元体系组成。ren等人在journaloftheamericanceramicsociety,98[12](2015)3603-3623中限定了对于如果将在固态电池中使用的电解质而言所需要的一系列特性。电解质应该具有在室温下高的锂离子传导率、可忽略的电子传导率(锂离子迁移数接近于一(unity))、宽的电化学窗口、和对于相邻电极的稳定性。此外,如果将锂用作阳极,则电解质必须是对锂稳定的。
表现出这些特性中一些的固态电解质的一个实例是锂磷氧氮化物(lipon)。当与锂金属接触时其表现出高的稳定性,其具有充分宽的电化学窗口和可忽略的电子传导率。这使其成功地用于薄膜固态电池中。
固态电池发展中的显著挑战是可被用来替代lipon的新的固态电解质的确定。具有所需要特性的新的电解质的确定既不是简单的也不是可预测的。此外,具有固态电解质的所期望结构和离子传导率的材料当在固态电池装置中工作时可不必然证明是稳定的。
这限制了用于固态电池的新的电解质材料的设计并且导致材料设计的试错途径。已经提出了需要进一步研究以便更好地理解在不同种类锂离子导体中存在的趋势和机制以促进先进锂离子导体的设计。(bachman等人,chemicalreviews,116(2016)140-162。
具有组成li0.78b0.11si0.11和li0.77b0.18si0.05的硼硅酸锂化合物以及li0.78b0.06si0.16的氮掺杂变体已经公开于wo2015/104540,vapourdepositionmethodforpreparingamorphouslithiumcontainingcompounds中。根据目前公开内容的实施方案合成了材料。离子传导率为3.2×10-6s/cm并且该材料显示为无定形的。制备了包含硼硅酸锂电解质、锂锰氧化物(lmo)阴极和氧化锡(sno2)阳极的固态电池。该公开内容没有提供关于电化学稳定性随电势变化或当与锂接触时或在具有锂阳极的固态电池装置中工作时的电化学稳定性和反应性的任何教导。如bachman等人提出的,不可基于其结构和离子传导率预测硼硅酸锂特定组成的行为。
发明概述
根据本发明的第一方面,提供了电极,其包含电极活性材料;其中用硼硅酸锂组合物改性所述电极的表面,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第二方面,提供了电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中用硼硅酸锂组合物改性该正电极和/或该负电极的表面,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第三方面,提供了电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述负电极包含锂,其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第四方面,提供了电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃,且其中所述电池具有小于0.5μah的完全充电容量。
根据本发明的第五方面,提供了电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、li1-xvopo4、和li2fepo4f,且其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第六方面,提供了电池,其包含:正电极层、负电极层、在所述正电极层和所述负电极层之间的电解质层,和在所述正电极层和所述电解质层之间和/或在所述负电极层和所述电解质层之间的硼硅酸锂组合物的层,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第七方面,提供了电池,其包含:包含正电极活性材料颗粒的复合正电极层、负电极层、在所述正电极层和所述负电极层之间的电解质层、和涂覆所述正电极活性材料颗粒和/或在所述负电极层和所述电解质层之间的硼硅酸锂组合物的层,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
根据本发明的第八方面,提供了硼硅酸锂组合物,其基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中所述硼硅酸锂组合物包含基于锂、硼和硅的总原子百分比在81至83原子%之间的锂,且其中所述硼硅酸锂组合物是玻璃。
根据本发明的第九方面,提供了制作根据本发明第八方面的硼硅酸锂组合物的方法,其中通过真空沉积工艺形成该硼硅酸锂组合物,该方法包括:
对于硼硅酸锂玻璃的每种组分元素而言提供单独的蒸气源;其中该蒸气源包含锂源、氧源、硼源和硅源;和
将来自它们的单独的蒸气源的组分元素共沉积至加热的基材上,其中在该基材上组分元素反应以形成硼硅酸锂组合物。
根据本发明的第十方面,提供了通过真空沉积工艺制作根据本发明第一方面的电极的方法,该方法包括:
a)对于该电极的每种组分元素而言提供第一单独的蒸气源;和
将来自它们的单独的蒸气源的组分元素共沉积至加热的基材上,其中在该加热的基材上组分元素反应以形成电极;和
b)对于硼硅酸锂组合物的每种组分元素而言提供第二单独的蒸气源,其中该第二蒸气源包含锂源、氧源、硼源和硅源;和
c)将来自第二单独的蒸气源的组分元素共沉积至步骤a)的电极上,其中在该电极上组分元素反应以形成硼硅酸锂组合物。
根据本发明的第十一方面,提供了制作根据本发明第三至第五方面中的任一项的电池的方法,其中通过真空沉积工艺形成硼硅酸锂玻璃电解质,该方法包括:
提供第一蒸气源,其包含用于第一电极层的化合物中每种组分元素的单独的蒸气源,提供第二蒸气源,其包含用于硼硅酸锂玻璃电解质层的化合物中每种组分元素的单独的蒸气源,和提供第三蒸气源,其包含用于第二电极层的化合物中每种组分元素的单独的蒸气源;
加热基材至第一温度和将来自所述第一蒸气源的组分元素共沉积至该基材上,其中组分元素反应以形成该第一电极层;
加热该基材至第二温度和将来自所述第二蒸气源的组分元素共沉积至该第一电极层上,其中组分元素反应以形成硼硅酸锂玻璃电解质层;和
加热该基材至第三温度和将来自第三单独的蒸气源的组分元素共沉积至该硼硅酸锂玻璃电解质层上,其中组分元素反应以形成第二电极层。
根据本发明的第十二方面,提供了制作根据本发明第二方面的电池的方法,其中通过气相沉积工艺形成硼硅酸锂表面改性的电极,该方法包括:
对于硼硅酸锂玻璃的每种组分元素而言提供单独的蒸气源,其中该蒸气源包含锂源、氧源、硼源和硅源;和
将来自它们的单独的蒸气源的组分元素共沉积至加热的基材上,其中在该基材上组分元素反应以形成硼硅酸锂组合物。
根据本发明的第十三方面,提供了如本文限定的硼硅酸锂组合物作为电池中电极保护剂的用途。
如本文所用,术语“电池”被认为与术语“电芯”同义,并且是能够从化学反应产生电能或通过引入电能促进化学反应的装置。
硼硅酸锂组合物
本文所述为硼硅酸锂组合物,其中所述硼硅酸锂基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂。通常所述硼硅酸锂是玻璃。优选地,硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
另外,本文所述硼硅酸锂玻璃限定为氧化锂与氧化硅和/或氧化硼结合的体系,其中所述硼硅酸锂玻璃的摩尔%在以下之间:70.9摩尔%li2o-0.0摩尔%b2o3-29.1摩尔%sio2,53.8摩尔%li2o-0.0摩尔%b2o3-46.2摩尔%sio2,83.0摩尔%li2o-17.0摩尔%b2o3-0.0摩尔%sio2,和70.0摩尔%li2o-30.0摩尔%b2o3-0.0摩尔%sio2。在另外的实施方案中,硼硅酸锂玻璃在以下之间:79.6摩尔%li2o-12.2摩尔%b2o3-8.2摩尔%sio2,60.3摩尔%li2o-12.1摩尔%b2o3-27.6摩尔%sio2,73.8摩尔%li2o-3.8摩尔%b2o3-22.4摩尔%sio2,和62.2摩尔%li2o-15.6摩尔%b2o322.2摩尔%sio2。在另一个实施方案中,硼硅酸锂玻璃在以下之间:70.9摩尔%li2o-0.0摩尔%b2o3-29.1摩尔%sio2,66.7摩尔%li2o-0.0摩尔%b2o3-33.3摩尔%sio2,83.0摩尔%li2o-17.0摩尔%b2o3-0.0摩尔%sio2,和75.0摩尔%li2o-25.0摩尔%b2o30.0摩尔%sio2。
在一方面,本发明涉及硼硅酸锂组合物,其中所述硼硅酸锂基本上由氧化锂、氧化硅和氧化硼的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂。通常,所述硼硅酸锂是玻璃。在一个实施方案中,本发明涉及硼硅酸锂组合物,其中所述硼硅酸锂基本上由氧化锂、氧化硅和氧化硼的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在81至83原子%之间的锂。
在一方面,本发明涉及硼硅酸锂组合物,其中所述硼硅酸锂基本上由氧化锂、氧化硅和氧化硼的三元体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂。通常,所述硼硅酸锂是玻璃。在一个实施方案中,本发明涉及硼硅酸锂组合物,其中所述硼硅酸锂基本上由氧化锂、氧化硅和氧化硼的三元体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在81至83原子%之间的锂。
将领会在根据本发明的硼硅酸锂材料中可存在少量的其他原子,前提是其他原子的这样的量没有影响硼硅酸锂材料的性质。这种痕量的其他原子可取代li、b、o和/或si的任一种,优选取代b和/或si。
可取代硼硅酸锂材料的结构中的li、b、o和/或si(优选取代b和/或si)的原子的典型实例包括n、s、ge、al、p、ti、v、zr、pb、ga、as、sn、in、sb、bi、nb、ta和w。可取代硼硅酸锂材料的结构中的li、b、o和/或si(优选取代b和/或si)的原子的优选实例包括al、ti、ge、p、v、w、s和n。
在此方面,术语“基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成”意指硼硅酸锂材料中锂、硼和硅原子的总量(表示为材料中除氧之外的原子总量的摩尔百分比)为至少90%、优选至少95%、优选至少97%、更优选至少98%、甚至更优选至少99%、仍更优选至少99.5%、甚至更优选至少99.7%、仍更优选至少99.8%、甚至更优选至少99.9%、仍更优选至少99.95%、甚至更优选至少99.97%、仍更优选至少99.98%、甚至更优选至少99.99%、仍更优选至少99.995%、甚至更优选至少99.997%、仍更优选至少99.998%、甚至更优选至少99.999%、仍更优选至少99.9995%、甚至更优选至少99.9997%、仍更优选至少99.9998%、甚至更优选至少99.9999%、和最优选100%。
在一个实施方案中,本发明涉及硼硅酸锂组合物,其中所述硼硅酸锂由氧化锂、氧化硅和氧化硼的三元体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在81至83原子%之间的锂。通常所述硼硅酸锂是玻璃。
本发明人出乎预料地发现了如本文所述的硼硅酸锂玻璃表现出高的离子传导率同时还表现出较低的电子传导率。还出乎预料地发现了如本文所述的硼硅酸锂玻璃特别地在高电压下与锂接触是特别稳定的。这些出乎预料地改进的性质使硼硅酸锂玻璃组合物特别适合作为电极的保护剂,特别地在包括该组合物作为阳极上涂层的电池的阳极上。这是本领域没有预测过的。
本发明人还出乎预料地发现如本文所述的硼硅酸锂玻璃与锂接触是化学/电化学稳定的。这些出乎预料改进的性质使硼硅酸锂玻璃组合物特别适合作为与锂金属接触的电解质。这是本领域没有预测过的。
本发明人还出乎预料地发现如本文所述的硼硅酸锂玻璃当经受宽范围电势时具有电化学稳定性。特别地,硼硅酸锂电解质能够在高电压下工作。这是本领域没有预测过的。
在一个实施方案中,本发明提供硼硅酸锂玻璃与具有相对于li/li+的3.6-8.5v电势的正极阴极活性材料接触,其中所述硼硅酸锂玻璃是电化学稳定的。在另外的实施方案中,硼硅酸锂玻璃与具有相对于li/li+的5-8.5v电势的正极阴极活性材料接触,其中所述硼硅酸锂玻璃是电化学稳定的。在另外的实施方案中,硼硅酸锂玻璃与具有相对于li/li+的大于5.5v电势的正极阴极活性材料接触,其中所述硼硅酸锂玻璃是电化学稳定的。
在另一个实施方案中,在具有0和10v之间电势的铂和铂电极之间构造硼硅酸锂玻璃,其中所述硼硅酸锂玻璃是电化学稳定的。
在另外的实施方案中,在具有0和5v之间电势的铂和镍电极之间构造硼硅酸锂玻璃,其中所述硼硅酸锂玻璃是电化学稳定的。
在另一个实施方案中,硼硅酸锂玻璃具有在25℃下至少1.0×10-6s/cm的离子传导率。
在另一个实施方案中,本发明涉及具有低电子传导率的硼硅酸锂电解质。在另外的实施方案中,硼硅酸锂玻璃具有在25℃下小于2.0×10-13s/cm的电子传导率。在另外的实施方案中,硼硅酸锂玻璃具有在25℃下小于8.5×10-14s/cm的电子传导率。
在另一个实施方案中,硼硅酸锂玻璃是薄膜。在另外的实施方案中,该薄膜为在40nm至15微米之间厚。
用硼硅酸锂组合物表面改性的电极
本发明的第一方面提供包含电极活性材料的电极;其中用硼硅酸锂组合物改性所述电极的表面,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。优选地,该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。相对于未改性的电极,特别地但并不是仅在当相邻的液相电解质材料存在下工作时,libsio-表面改性的电极具有改进的稳定性和/或改进的循环。在一个实施方案中,libsio-表面改性的电极是libsio-表面改性的负电极。在另一个实施方案中,libsio-表面改性的电极是libsio-表面改性的正电极。
包含硼硅酸锂表面改性的电极的电池
本发明的第二方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中用本发明的libsio组合物改性该正电极和/或该负电极的表面。
在一个实施方案中,本发明涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中用本发明的libsio组合物的层涂覆该正电极和/或负电极。
在一个实施方案中,电池包含libsio-表面改性的负电极。在另一个实施方案中,电池包含libsio-表面改性的正电极。
按照本发明已经发现了包含根据本发明的libsio-表面改性的电极(特别地但不是仅负电极)的电池是特别有利的。不希望受理论的束缚,据信如本文所述的libsio组合物的性质使该组合物充当这样的电池(特别是锂离子电池和尤其是具有液体或聚合物电解质的锂离子电池)的电极上特别有效的电极保护层。
在一个实施方案中,本发明的这个方面涉及电池,其包含正集流体、正电极、电解质、负电极、和负集流体,其中用本发明的libsio组合物改性正电极和/或负电极的表面。在一个实施方案中,电池包含libsio-表面改性的负电极。在另一个实施方案中,电池包含libsio-表面改性的正电极。在另外的实施方案中,电池是锂离子二次电池。在另一个实施方案中,锂离子二次电池是薄膜电池。
包含硼硅酸锂电解质和含锂的负电极的电池
本发明的第三方面涉及电池,其包含正电极、负电极,其中所述负电极包含锂和在所述正电极和所述负电极之间的电解质,其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。优选地,该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
在一个实施方案中,电池是锂离子二次电池。本文将锂离子二次电池定义为通过来自负电极和正电极的锂离子的可逆移除和插入,伴随它们在电解质中传输同时相关的电子通过外电路来将在其活性材料中含有的化学能直接转化成电能的装置。所述负电极可在电化学循环之前或在电池的第一次充电过程中实现为电池结构的整体部件,因为将锂镀覆至包含与电解质的界面的负集流体的表面上。在另一个实施方案中,电池的正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、limn2o4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、livopo4、li2fepo4f。
在另一个实施方案中,电池还包含负电极集流体和正电极集流体。在另一个实施方案中,负电极集流体包含选自以下的负电极集流体材料:pt、ni、mo、cu、tin、al、au和不锈钢。在另一个实施方案中,正电极集流体材料选自由以下组成的组:pt、ni、mo、al、au、不锈钢、铟掺杂的氧化锡(ito)和其他导电金属氧化物。
在另一个实施方案中,电池是固态电池。在另外的实施方案中,固态电池包含:基材层、正集流体层、正电极层、负电极层、负集流体层和在所述正电极层和所述负电极层之间的硼硅酸锂玻璃电解质层。
在另一个实施方案中,电池还包含在基材和集流体之间的钝化层(例如si3n4)和/粘附层(例如tio2)。
在另一个实施方案中,电池包含封装层。在另外的实施方案中,封装层包含aln、si3n4、sio2、al2o3、al、cu、聚对二甲苯聚合物(parylenetm)、聚酰亚胺、或共聚聚(乙烯-共-甲基丙烯酸)
在另一个实施方案中,电池包含选自以下的基材材料:alopt(蓝宝石/tio2/pt)、sstop(si/sio2/tio2/pt)、si、sio2、si3n4、云母、和浮法玻璃。
在另一个实施方案中,电池是薄膜电池。在另外的实施方案中,正电极为在1和10微米之间厚,优选2-8微米厚。在另外的实施方案中,负电极为在50nm和5微米之间厚,优选0.15-3微米厚。在另外的实施方案中,硼硅酸锂玻璃电解质层为在40nm至15微米之间厚,优选0.4-5微米厚。
在另一个实施方案中,电池具有在充电状态下在1.0-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在3.6-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在5.5-8.5v之间的开路电压。
在另一个实施方案中,本发明涉及包含具有高离子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率。
在另一个实施方案中,本发明涉及包含具有低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含具有高离子传导率和低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含对锂电化学稳定的硼硅酸锂电解质的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质和锂阳极的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质的不含锂的电池。
在另一个实施方案中,本发明涉及包含能够在高电压下工作的硼硅酸锂电解质的电池。在另一个实施方案中,硼硅酸锂玻璃电解质在0和10v之间的所有电势下是电化学稳定的。在另一个实施方案中,硼硅酸锂玻璃电解质在从0和8v的所有电势下是电化学稳定的。
在另一个实施方案中,硼硅酸锂玻璃电解质在相对于li/li+在3.6和8.5v之间的所有电势下是电化学稳定的。
在另一个实施方案中,电池具有在0.04-5.0μah之间的完全充电容量。在另外的实施方案中,电池具有小于0.5μah的完全充电容量。在另外的实施方案中,电池具有小于0.1μah的完全充电容量。在另一个实施方案中,电池具有在2.0μah/cm2和300μah/cm2之间的完全充电容量。在另外的实施方案中,完全充电容量在2μah/cm2和200μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和100μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和50μah/cm2之间。在另外的实施方案中,完全充电容量在100μah/cm2和300μah/cm2之间。在另一个实施方案中,电池具有在3.25μah/cm2和650μah/cm2之间的完全充电容量并且libsio厚度在21μm和2.7nm之间。在另一个实施方案中,电池具有在3.25μah/cm2和32.5μah/cm2之间的完全充电容量并且libsio厚度在21μm和55nm之间。在另一个实施方案中,电池具有在32.5μah/cm2和65μah/cm2之间的完全充电容量并且libsio厚度在2.1μm和27nm之间。在另一个实施方案中,电池具有在65μah/cm2和650μah/cm2之间的完全充电容量并且libsio厚度在1.3μm和2.7nm之间。
另一个实施方案提供包含至少两个本发明电池的电池组。
具有小于0.5μah完全充电容量的电池,所述电池包含硼硅酸锂电解质
本发明的第四方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃,且其中所述电池具有小于0.5μah的完全充电容量。优选地,该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
在一个实施方案中,电池是锂离子二次电池。本文将锂离子二次电池定义为通过来自负电极和正电极的锂离子的可逆移除和插入,伴随它们在电解质中传输同时相关的电子通过外电路来将在其活性材料中含有的化学能直接转化成电能的装置。所述负电极可在电化学循环之前或在电池的第一次充电过程中实现为电池结构的整体部件,因为将锂镀覆至包含与电解质的界面的负集流体的表面上。在另一个实施方案中,电池的正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、limn2o4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、livopo4、li2fepo4f。在另一个实施方案中,电池的负电极包含选自以下的负电极活性材料:锂、硅、锡、镁、铝、锑、铟、钛、镍、钴、铬、锗、锌、氧、碳、钒、铌、铋、钨、硫、和铁。
在另外的实施方案中,正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、limn2o4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、livopo4、li2fepo4f,和负电极包含选自以下的负电极活性材料:锂、硅、锡、镁、铝。
在另一个实施方案中,电池还包含负电极集流体和正电极集流体。在另一个实施方案中,负电极集流体包含选自以下的负电极集流体材料:pt、ni、mo、cu、tin、al、au和不锈钢。在另一个实施方案中,正电极集流体材料选自由以下组成的组:pt、ni、mo、al、au、不锈钢、铟掺杂的氧化锡(ito)和其他导电金属氧化物。
在另一个实施方案中,电池是固态电池。在另外的实施方案中,固态电池包含:基材层、正集流体层、正电极层、负电极层、负集流体层和在所述正电极层和所述负电极层之间的硼硅酸锂玻璃电解质层。
在另一个实施方案中,电池还包含在基材和集流体之间的钝化层(例如si3n4)和/粘附层(例如tio2)。
在另一个实施方案中,电池包含封装层。在另外的实施方案中,封装层包含aln、si3n4、sio2、al2o3、al、cu、聚对二甲苯聚合物(parylenetm)、聚酰亚胺、或聚(乙烯-共-甲基丙烯酸)
在另一个实施方案中,电池包含选自以下的基材材料:alopt(蓝宝石/tio2/pt)、sstop(si/sio2/tio2/pt)、si、sio2、si3n4、云母、和浮法玻璃。
在另一个实施方案中,电池是薄膜电池。在另外的实施方案中,正电极为在1和10μm之间厚,优选2-8μm厚。在另外的实施方案中,负电极为在50nm和5μm之间厚,优选0.15-3μm厚。在另外的实施方案中,硼硅酸锂玻璃电解质层为在40nm至15μm之间厚,优选0.4-5μm厚。
在另一个实施方案中,电池具有在充电状态下在1.0-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在3.6-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在4.6-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在5.5-8.5v之间的开路电压。
在另一个实施方案中,本发明涉及包含具有高离子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率。
在另一个实施方案中,本发明涉及包含具有低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含具有高离子传导率和低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含对锂电化学稳定的硼硅酸锂电解质的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质和锂阳极的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质的不含锂的电池。
在另一个实施方案中,本发明涉及包含能够在高电压下工作的硼硅酸锂电解质的电池。在另一个实施方案中,硼硅酸锂玻璃电解质在0和10v之间的所有电势下是电化学稳定的。在另一个实施方案中,硼硅酸锂玻璃电解质在从0和8v的所有电势下是电化学稳定的。
在另一个实施方案中,硼硅酸锂玻璃电解质在相对于li/li+在3.6和8.5v之间的所有电势下是电化学稳定的。
在另一个实施方案中,电池具有小于0.1μah的完全充电容量。在另一个实施方案中,电池具有在2.0μah/cm2和300μah/cm2之间的完全充电容量。在另外的实施方案中,完全充电容量在2μah/cm2和200μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和100μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和50μah/cm2之间。在另外的实施方案中,完全充电容量在100μah/cm2和300μah/cm2之间。
另一个实施方案提供包含至少两个本发明电池的电池组。
包含硼硅酸锂电解质和高电压正电极的电池
第五方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、li1-xvopo4、和li2fepo4f,且其中所述电解质是硼硅酸锂组合物,其中该硼硅酸锂组合物基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。优选地,该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。
在一个实施方案中,电池是锂离子二次电池。本文将锂离子二次电池定义为通过来自负电极和正电极的锂离子的可逆移除和插入,伴随它们在电解质中传输同时相关的电子通过外电路来将在其活性材料中含有的化学能直接转化成电能的装置。所述负电极可在电化学循环之前或在电池的第一次充电过程中实现为电池结构的整体部件,因为将锂镀覆至包含与电解质的界面的负集流体的表面上。在另一个实施方案中,电池的负电极包含选自以下的负电极活性材料:锂、硅、锡、镁、铝、锑、铟、钛、镍、钴、铬、锗、锌、氧、碳、钒、铌、铋、钨、硫、和铁。
在另外的实施方案中,正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、livopo4、li2fepo4f,和负电极包含选自以下的负电极活性材料:锂、硅、锡、镁、铝。
在另一个实施方案中,电池还包含负电极集流体和正电极集流体。在另一个实施方案中,负电极集流体包含选自以下的负电极集流体材料:pt、ni、mo、cu、tin、al、au和不锈钢。在另一个实施方案中,正电极集流体材料选自由以下组成的组:pt、ni、mo、al、au、不锈钢、铟掺杂的氧化锡(ito)和其他导电金属氧化物。
在另一个实施方案中,电池是固态电池。在另外的实施方案中,固态电池包含:基材层、正集流体层、正电极层、负电极层、负集流体层和在所述正电极层和所述负电极层之间的硼硅酸锂玻璃电解质层。
在另一个实施方案中,电池还包含在基材和集流体之间的钝化层(例如si3n4)和/粘附层(例如tio2)。
在另一个实施方案中,电池包含封装层。在另外的实施方案中,封装层包含aln、si3n4、sio2、al2o3、al、cu、聚对二甲苯聚合物(parylenetm)、聚酰亚胺、或聚(乙烯-共-甲基丙烯酸)
在另一个实施方案中,电池包含选自以下的基材材料:alopt(蓝宝石/tio2/pt)、sstop(si/sio2/tio2/pt)、si、sio2、si3n4、云母、和浮法玻璃。
在另一个实施方案中,电池是薄膜电池。在另外的实施方案中,正电极为在1和10微米之间厚,优选2-8微米厚。在另外的实施方案中,负电极为在50nm和5微米之间厚,优选0.15-3微米厚。在另外的实施方案中,硼硅酸锂玻璃电解质层为在40nm至15微米之间厚,优选0.4-5微米厚。
在另一个实施方案中,电池具有在充电状态下在1.0-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在3.6-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在4.6-8.5v之间的开路电压。在另外的实施方案中,电池具有在充电状态下在5.5-8.5v之间的开路电压。
在另一个实施方案中,本发明涉及包含具有高离子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率。
在另一个实施方案中,本发明涉及包含具有低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含具有高离子传导率和低电子传导率的硼硅酸锂电解质的电池。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于2.0×10-13s/cm的电子传导率。
在另一个实施方案中,本发明涉及包含对锂电化学稳定的硼硅酸锂电解质的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质和锂阳极的电池。在另外的实施方案中,本发明涉及包含硼硅酸锂电解质的不含锂的电池。
在另一个实施方案中,本发明涉及包含能够在高电压下工作的硼硅酸锂电解质的电池。在另一个实施方案中,硼硅酸锂玻璃电解质在0和10v之间的所有电势下是电化学稳定的。在另一个实施方案中,硼硅酸锂玻璃电解质在从0至8v的所有电势下是电化学稳定的。
在另一个实施方案中,硼硅酸锂玻璃电解质在相对于li/li+在3.6和8.5v之间的所有电势下是电化学稳定的。
在另一个实施方案中,电池具有在0.04-5.0μah之间的完全充电容量。在另外的实施方案中,电池具有小于0.5μah的完全充电容量。在另外的实施方案中,电池具有小于0.1μah的完全充电容量。在另一个实施方案中,电池具有在2.0μah/cm2和300μah/cm2之间的完全充电容量。在另外的实施方案中,完全充电容量在2μah/cm2和200μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和100μah/cm2之间。在另外的实施方案中,完全充电容量在2μah/cm2和50μah/cm2之间。在另外的实施方案中,完全充电容量在100μah/cm2和300μah/cm2之间。
另一个实施方案提供包含至少两个本发明电池的电池组。
制作硼硅酸锂组合物的方法
第九方面提供制作如本文限定的硼硅酸锂组合物的方法。在一个实施方案中,通过真空沉积工艺形成硼硅酸锂组合物。在另外的实施方案中,通过物理气相沉积工艺形成硼硅酸锂组合物。
在一个实施方案中,本发明涉及制作对锂电化学稳定的硼硅酸锂电解质的方法。在另外的实施方案中,电池包含锂阳极。
在另一个实施方案中,本发明涉及制作能够在高电压下工作的硼硅酸锂电解质的方法。在另外的方面,电池适合用于较长期循环。
在另一个实施方案中,本发明涉及制作具有低电子传导率的硼硅酸锂电解质的方法。在另外的实施方案中,电池具有低容量。
制作硼硅酸锂表面改性的电极的方法
第十方面提供制作libsio-表面改性的电极的方法。只要制作本发明的libsio-表面改性的电极的方法能够提供改进稳定性或改进电极循环的期望的libsio-表面改性的电极,则不特别地限制该方法。该方法的实例包括如本文所述的pvd。在一个实施方案中,该方法是制作libsio-表面改性的负电极的方法。在另一个实施方案中,该方法是制作libsio-表面改性的正电极的方法。在一个实施方案中,通过物理气相沉积(pvd)制备libsio涂层。
制作包含硼硅酸锂电解质的电池的方法
本发明的第十一方面涉及制作包含硼硅酸锂电解质的电池的方法。
在一个实施方案中,本发明涉及制作包含对锂电化学稳定的硼硅酸锂电解质的电池的方法。在另外的实施方案中,电池包含锂阳极。
在另一个实施方案中,本发明涉及制作包含能够在高电压下工作的硼硅酸锂电解质的电池的方法。在另外的方面,电池适合用于较长期循环。
在另一个实施方案中,本发明涉及制作包含具有低电子传导率的硼硅酸锂电解质的电池的方法。在另外的实施方案中,电池具有低容量。
制作包含硼硅酸锂表面改性电极的电池的方法
另外的方面提供制作包含电极的电池的方法,其中用本发明的libsio材料改性该电极的表面。在一个实施方案中,该方法是制作包含libsio-表面改性的负电极的电池的方法。在另一个实施方案中,该方法是制作包含libsio-表面改性的正电极的电池的方法。在另外的实施方案中,电池是锂离子二次电池。在另一个实施方案中,锂离子二次电池是薄膜电池。
附图简要描述
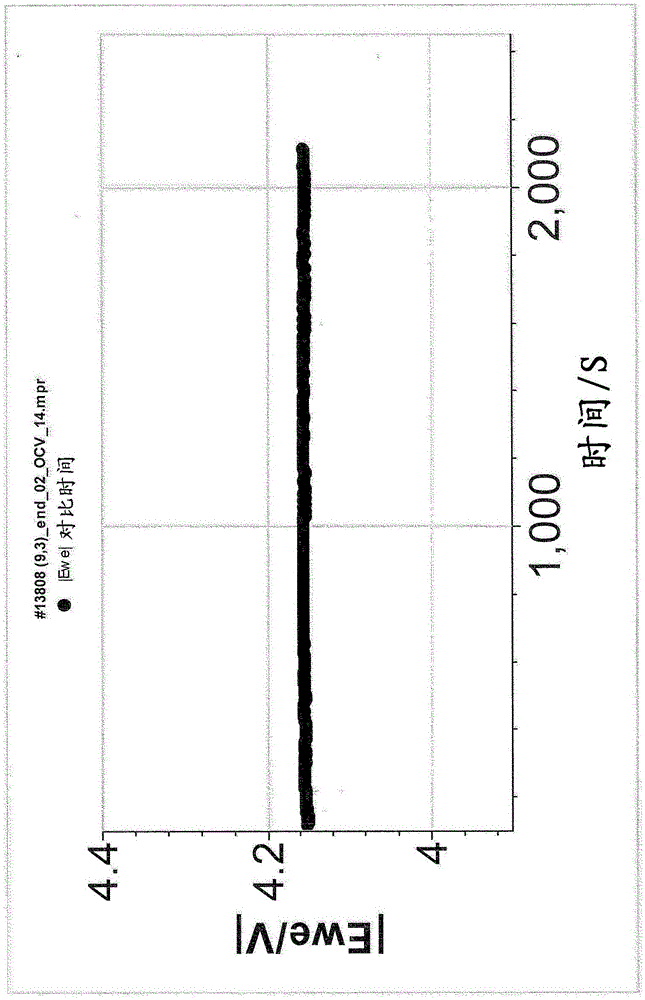
图1.在35分钟内每5秒测量的lmo/libsio/li电芯的开路电压。
图2.在充电最初15分钟的ocv监测。
图3.包含alopt基材、lmo阴极、libsio电解质和li金属阳极的固态电芯的循环伏安法。在3.6和4.25v之间使电芯循环100次。在0.5mv/s下循环最初的三次循环,而在0.25mv/s的扫描速率下进行剩下的97次循环。
图4a和4b.包含alopt基材、lmo阴极、libsio电解质和li金属阳极的固态电芯的阻抗。在电池经受10次在3.8和4.25v之间以0.1μa电流值的恒电流循环之前和之后相对于li/li+的3.8v电势下进行测量。测量的频率范围为261.0156khz至0.1hz,其中每个进位(decade)有七个数据点,并且ac幅度为10mv,且每个频率使用超过10次循环的平均值以产生每个频率下的点。图4a显示在整个实验范围内的数据点。图4b显示小于40kω的数据点。
图5.随锂含量变化的libsio样品的电子传导率(带三角形的虚线)和离子传导率(带圆形的实线)。
图6.随lmo中li原子百分比(x轴)变化的libsio涂覆的(空心圆形)与未涂覆的(实心正方形)lmo阴极样品对比的第1次放电的利用数(y轴)。
发明详细描述
电解质
电解质组合物
本文所述为硼硅酸锂(libsio)玻璃电解质。术语“玻璃”意指非晶的或无定形的固体,当通过x-射线衍射或拉曼光谱法表征时其没有表现出长程结构有序的迹象。本文所述的libsio玻璃优选是氧化锂、氧化硅和氧化硼的三元体系。
如本文所述,硼硅酸锂玻璃包含基于锂、硼和硅(即排除氧组分)的总原子百分比在70至83原子%之间的锂。在另外的实施方案中,硼硅酸锂玻璃包含基于li、b和si的在70和76原子%之间的li。在另外的实施方案中,硼硅酸锂玻璃包含在71和76原子%之间的li、在73和76原子%之间的li、在72和75原子%之间的li、在73和75原子%之间的li、或在79和83原子%之间的li,其每个基于li、b和si。在所有情况下,应理解氧以形成氧化物并维持电中性的量存在。
如本文所述,硼硅酸锂玻璃优选包含基于锂、硼和硅(即排除氧组分)的总原子百分比在1至25原子%之间的硼。优选地,硼硅酸锂玻璃包含基于li、b和si的在5和20原子%之间的b。优选地,硼硅酸锂玻璃包含基于li、b和si的在7.5和15原子%之间的b。在所有情况下,应理解氧以形成氧化物并维持电中性的量存在。
如本文所述,硼硅酸锂玻璃优选包含基于锂、硼和硅(即排除氧组分)的总原子百分比在1至25原子%之间的硅。优选地,硼硅酸锂玻璃包含基于li、b和si的在5和20原子%之间的si。优选地,硼硅酸锂玻璃包含基于li、b和si的在6和17原子%之间的si。在所有情况下,应理解氧以形成氧化物并维持电中性的量存在。
根据b和si,b:si的比率可为1:1+/-0.15。基于组分li、b和si,libsio电解质可包含74原子%li、14原子%si和12原子%b。
还可将本文所述的硼硅酸锂玻璃限定为氧化锂与氧化硅和/或氧化硼结合的体系,其中所述硼硅酸锂玻璃的摩尔%在以下之间:70.9摩尔%li2o-0.0摩尔%b2o3-29.1摩尔%sio2,53.8摩尔%li2o-0.0摩尔%b2o3-46.2摩尔%sio2,83.0摩尔%li2o-17.0摩尔%b2o3-0.0摩尔%sio2,和70.0摩尔%li2o-30.0摩尔%b2o3-0.0摩尔%sio2。
优选地,硼硅酸锂玻璃的摩尔%在以下之间:79.6摩尔%li2o-12.2摩尔%b2o3-8.2摩尔%sio2,60.3摩尔%li2o-12.1摩尔%b2o3-27.6摩尔%sio2,73.8摩尔%li2o-3.8摩尔%b2o3-22.4摩尔%sio2,和62.2摩尔%li2o-15.6摩尔%b2o322.2摩尔%sio2。
优选地,硼硅酸锂玻璃的摩尔%在以下之间:70.9摩尔%li2o-0.0摩尔%b2o3-29.1摩尔%sio2,66.7摩尔%li2o-0.0摩尔%b2o3-33.3摩尔%sio2,83.0摩尔%li2o-17.0摩尔%b2o3-0.0摩尔%sio2,和75.0摩尔%li2o-25.0摩尔%b2o30.0摩尔%sio2。
对锂的电化学稳定性
如本文所述的硼硅酸锂玻璃对锂是稳定的,其中稳定性特征在于不存在表明可检测的反应或降解的迹象(bates等人,journaloftheelectrochemicalsociety144[2](1997年)524-533)。使用阻抗频谱法和时间相关开路电压测量了硼硅酸锂玻璃电解质的稳定性。已经使用阻抗频谱法来表明在经受循环之前和之后电池的频率相关响应的可比性。在延长的沉积后储存之后和经受循环之后测量了开路电压以表明电解质的完整性及其承受阴极和阳极之间的电化学势差的能力,而没有维持可检测的反应或降解从而导致机械或化学失效,导致不能维持在所述正电极和负电极之间的非零电势。
发明人出乎预料地发现了可将包含libsio电解质和锂阳极的薄膜电池循环而没有在libsio电解质和阳极材料之间有害反应的迹象。此外,在电池的循环之前和之后都观察到相同薄膜电池系统的稳定的开路电压。这一发现的技术效果是其促进了在用沉积锂阳极构造的固态电池中或在不含锂的电芯内libsio电解质的使用,由此在固态libsio电解质和阳极集流体之间的界面处原位地形成锂阳极。
因此,在一个实施方案中,libsio玻璃与锂接触并且是电化学稳定的。
在另一个实施方案中,libsio玻璃对锂是稳定的并且与经受具有以下电势的正极阴极活性材料接触是化学稳定的:相对于li/li+至少+3.9v、相对于li/li+至少+4.5v、相对于li/li+至少+5.5v、或相对于li/li+至少+6.0v。
在高电压下的电化学稳定性
使用在两个电压限之间的循环伏安法测量相对于高电压的电化学稳定性,在循环伏安法中当跨样品电极施加随时间变化的固定速率电势改变时测定随电势变化的电流响应。电化学稳定性特征在于电势范围内的电流响应随提高的或降低的电势连续变化,也就是说在电势范围内没有电流幅度的增加或减少与电势值的改变无关的点。由于电化学不稳定性在测试期间电解质的失效将被观为在固定电势值下电流连续提高的幅度。
发明人还出乎预料地发现了当在范围从0至10v的电势之间在铂和铂或铂和镍之间构造时本文所述的libsio电解质是电化学稳定的。这一发现的技术效果是可在非常高的电压下工作并传输高能量密度的电池中使用libsio电解质。
因此,在另一个实施方案中,本发明涉及当经受宽范围电势时具有电化学稳定性的libsio电解质。
在另一个实施方案中,硼硅酸锂玻璃与经受3.6-5v电势、在另外的实施方案中4.5-5v电势、和在另外的实施方案中5.5-8.5v电势的正极阴极活性材料接触是电化学稳定的。在另一个实施方案中,硼硅酸锂玻璃对锂是稳定的并且与经受3.6-5v电势、在另外的实施方案中4.5-5v电势、和在另外的实施方案中5.5-8.5v电势的正极阴极活性材料接触是电化学稳定的。
高离子传导率和低电子传导率
发明人还出乎预料地发现如本文所述的libsio电解质的电子传导率非常低而离子传导率高。这一发现的技术效果是如本文所述的libsio电解质的电子传导率足够低使得由非常低的电子传导率性质(<2.0×10-13s/cm)所致基于它们维持充电状态的能力可将它们用于具有非常低理论容量(<0.04μah)的固态电池。
因此,在另一个实施方案中,本发明涉及具有高离子传导率和低电子传导率的libsio电解质。在另外的实施方案中,libsio电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于6.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于5.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于4×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少1.0×10-6s/cm的离子传导率和小于2.0×10-14s/cm的电子传导率。
在另外的实施方案中,libsio电解质具有在25℃下至少3.0×10-6s/cm的离子传导率和小于6.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少3.0×10-6s/cm的离子传导率和小于5.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少3.0×10-6s/cm的离子传导率和小于4×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少3.0×10-6s/cm的离子传导率和小于2.0×10-14s/cm的电子传导率。
在另外的实施方案中,libsio电解质具有在25℃下至少5.0×10-6s/cm的离子传导率和小于6.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少5.0×10-6s/cm的离子传导率和小于5.0×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少5.0×10-6s/cm的离子传导率和小于4×10-14s/cm的电子传导率。在另外的实施方案中,libsio电解质具有在25℃下至少5.0×10-6s/cm的离子传导率和小于2.0×10-14s/cm的电子传导率。
在另一个实施方案中,以上的libsio电解质对锂是稳定的。在另一个实施方案中,以上的libsio电解质对锂是电化学稳定的并且与经受3.6-5v电势的正极阴极活性材料接触是电化学稳定的。在另一个实施方案中,以上的libsio电解质对锂是电化学稳定的并且与经受5.5-8.5v电势的正极阴极活性材料接触是电化学稳定的。
硼硅酸锂表面改性的电极
可通过与电解质、电解质溶液或气氛反应,通过机械应力,或其他方式来引起电极活性材料的降解。例如,锂金属是高度反应性的。由于电解质中溶剂、活性物质或杂质的还原,在具有li基电极的电池循环过程中发生反应。这些和其他的反应导致电极的降解、电极容量的损失、电解质和活性材料的消耗、和最终的电池失效。额外的失效模式是在锂阳极的表面处枝晶锂的生长(由表面缺陷提供的不均匀的电流密度所致)导致容量损失、由分离的锂的产生引起、以及通过电极短路的电芯毁坏,可通过在锂和液体电解质之间的界面处放置固态电解质减轻这一过程。需要材料具有高离子传导率、低电子传导率,其与锂接触是稳定的,并且可用作电极的保护涂层。还需要电池具备具有改进的稳定性和循环的电极。
因此。本发明的第二方面提供电极,用如本文所述的libsio材料改性该电极的表面。libsio-表面改性的电极比未涂覆的电极具有改进的稳定性和/或改进的循环。在一个实施方案中,libsio-表面改性的电极是libsio-表面改性的负电极。在另一个实施方案中,libsio-表面改性的电极是libsio-表面改性的正电极。
如本文所用,术语“表面改性的”和“其表面通过改性的”意指电极表面的至少一部分与本文所述的libsio组合物机械或化学接触。
只要材料允许libsio连接至其表面并且能够储存和释放锂离子,则没有特别限制电极的电极活性材料。电极活性材料的实例包括但不限于在本说明书中其他地方描述的那些。在优选实施方案中,负电极活性材料是锂金属。
在一些实施方案中,电极是锂嵌入电极。如本文所用,术语“嵌入”是指分子或离子可逆的包含或插入至具有层状结构的化合物中。因此,锂嵌入电极可为其中可将锂离子可逆地包括或插入层状结构(例如石墨)中的电极。
在一些实施方案中,用如本文所述libsio材料层涂覆电极。在一些实施方案中,提供本文所述的硼硅酸锂组合物作为电极表面上的层。
在一些实施方案中,用如本文所述libsio材料层涂覆电极的表面。可通过首先在集流体上流延包含电极活性材料(和任选的碳添加剂、聚合物粘合剂和/或溶剂)的电极,并然后固化和干燥电极实现这种涂覆。流延电极的表面然后可具有沉积在其上的libsio材料保护层。在一些实施方案中,libsio完全涂覆电极的表面。在一些实施方案中,libsio部分地覆盖电极的表面。
在一些实施方案中,电极包含电极活性材料的颗粒,其中用如本文所述的libsio材料层涂覆该颗粒。这可通过用保护性libsio材料涂覆活性材料的每个颗粒的整体来实现。受保护的颗粒然后可任选地与碳添加剂、聚合物粘合剂和/或溶剂混合并形成为浆料。然后可将浆料流延至导电集流体上。
只要改进稳定性或改进电极的循环,则没有特别限制libsio-涂覆层的厚度。在一个实施方案中,libsio-涂覆层的厚度在2nm至100nm之间。在另外的实施方案中,该范围在2nm至50nm之间。
在一个实施方案中,libsio-表面改性的电极包含libsio-涂覆层,其涂覆电极的表面并且锂离子可移动通过该涂覆层。在一个实施方案中,用libsio完全涂覆电极表面。在另一个实施方案中,用libsio涂覆与电解质(尤其是非固态电解质)接触的电极表面。
电池
发明人出乎预料的发现如本文所述的硼硅酸锂玻璃具有1)与低电子传导率结合的高离子传导率,2)与非常还原性电极(例如金属性锂阳极)和非常氧化性电极(例如在相对于li/li+的4.2v下充电的li0.5coo2阴极)接触是电化学稳定的,和3)在高电压下是电化学稳定的。
因此,本发明的第三方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述负电极包含锂,且其中所述电解质是如本文所述的硼硅酸锂组合物。因此,本发明的第四方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述电解质是如本文所述的硼硅酸锂组合物,且其中所述电池具有小于0.5μah的完全充电容量。因此,本发明的第五方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中所述正电极包含选自以下的正电极活性材料:licopo4、lini0.5mn1.5o4、limnpo4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、li1-xvopo4、和li2fepo4f,且其中所述电解质是如本文所述的硼硅酸锂组合物。
在另外的实施方案中,电池还包含正电极集流体和负电极集流体。在另外的实施方案中,电池还包含基材。在另外的实施方案中,电池还是密封的。
在一个实施方案中,电池是锂离子电池。在另外的实施方案中,电池是锂离子二次电池。在另外的实施方案中,薄膜电池是全固态电池。在另外的实施方案中,电池是包含正电极、电解质和负电极的薄膜电池。
在一个实施方案中,电池包含多个正电极和多个负电极,例如以堆叠体形式。与电极接触的电解质通过在具有相反极性的电极之间的分隔体提供离子传导率。电池通常包含分别与负电极和正电极相关的集流体。通常将电极与它们相关的集流体和分隔体的堆叠体放置在具有硼硅酸锂电解质的容器内。
在一个实施方案中,电池是改进的锂离子电池,其包含负电极、正电极、和硼硅酸锂电解质,其中正电极包含具有以下电化学势的高电压正极活性材料:相对于li/li+至少3.5v、相对于li/li+至少4.0v、相对于li/li+至少4.5v、相对于li/li+至少5.5v、或相对于li/li+在6.0-8.5v之间。
具有如本文所述硼硅酸锂电解质和高电压正电极的锂离子电池允许高能量/功率密度锂离子电池的开发。此外,如本文所述的硼硅酸锂电解质具有非常高的离子传导率和低电子传导率,所以可提供改进的性能例如较高的功率和能量以及稳定的低容量。对于高电压工作而言,电解质性质的另一个重要方面是还原和氧化稳定性。改进的还原和氧化稳定性改进了本发明的电池寿命和循环性能。
提供具有硼硅酸锂电解质和高电压正电极的改进的电池系统,其可用于制备高能量和高功率锂离子电池。具有在相对于li/li+约3.6至8.5v范围内电势的正电极活性材料(阴极材料)的正电极提供与libsio电解质结合的优异性能。
负电极
使用负电极活性材料作为正电极的对电极。正电极活性材料和负电极活性材料的组成决定在放电过程中电池的电势,其为各自半反应的电势之差。
用于本发明电池中的负电极活性材料可选自li4ti5o12,si,ge,sn,sb,al,mg,bi,si-m(m=mg、al、sn、zn、ag、fe、ni、mn),insb,金属氧化物,其包括tio2,钒氧化物和钼氧化物,ti、nb氧化物(mgti2o5、tinb2o7),sno,sno2,sb氧化物,或锗酸盐。
用于本发明电池中的负电极活性材料可为锂或锂化的过渡金属氧化物,例如锂钛氧化物。负电极活性材料可为锂金属合金,包括lisi、lisb或lige。负电极活性材料还可为能够可逆地嵌入锂离子的含碳材料(例如活性炭)、含锡材料、含硅材料、或其他材料。
负电极活性材料还包括石墨、合成石墨、焦炭、富勒烯、五氧化二铌、锡合金、硅(包括无定形硅)、氧化钛、氧化锡、和锂钛氧化物。
包含碳单质材料的负电极活性材料包括石墨、合成石墨、焦炭、富勒烯、碳纳米管、其他石墨碳及其组合。石墨碳是指包含大量的石墨烯片区域的任何碳单质材料。
在一个实施方案中,负电极活性材料包含锂金属或其合金,并且电池是可充电(二次)锂离子电池。在另外的实施方案中,负电极可包含锂-铝合金或金属锂层。在另一个实施方案中,负电极是锂。在另一个实施方案中,负电极是不含锂的阳极。在另一个实施方案中,负电极是锂空气阳极。
在一些实施方案中,电极是锂嵌入电极。如本文所用,术语“嵌入”是指分子或离子可逆的包含或插入至具有层状结构的化合物中。因此,锂嵌入电极可为其中可将锂离子可逆地包括或插入层状结构(例如石墨)中的电极。
正电极
在负电极的对电极中使用正电极活性材料。在一些实施方案中,正电极可包括具有相对于li/li+大于3.6v电势的正极活性材料。
本发明电池的正电极活性材料包括锂化过渡金属化合物,例如锂镍锰氧化物、锂镍钒氧化物、锂钴钒氧化物、或锂钴磷酸盐,例如li2nimn3o8、linivo4、licovo4、licopo4等。其他实例包括锂镍磷酸盐、锂镍氟磷酸盐、和锂钴氟磷酸盐,即linipo4、li2nipo4f、li2copo4f等。锂含量通常取决于电池的电荷状态而变化。正极活性材料可包含其他的含氧材料,例如氧化物、锰酸盐、镍酸盐、钒酸盐、磷酸盐或氟磷酸盐。正极活性材料可具有式lixmynzo,其中m选自由ni、mn、v和co组成的组,且n是不同于m的杂原子物质,例如ni、mn、v、co、或p。可省略n。正极活性材料还可为氟化的,例如作为氟磷酸盐。
在一个实施方案中,本发明电池的正电极活性材料选自以下:licoo2、fes2、licopo4、lifepo4、li2fes2、li2fesio4、limn2o4、limnpo4、linipo4、liv3o8、liv6o13、livopo4、livopo4f、li3v2(po4)3、mno2、mos3、s、tis2、tis3、v2o5、v6o13、lini0.5mn1.5o4和limnnicoalo2。
在另一个实施方案中,本发明电池的正电极活性材料是高电压正电极活性材料。在另外的实施方案中,高电压正电极活性材料选自以下:licopo4、lini0.5mn1.5o4、limnpo4、limn2o4、licoo2、lini1/3mn1/3co1/3o2、lifepo4、linipo4、li2nipo4f、li2copo4f、limnpo4f、li2cosio4、li2mnsio4、fef3、limn0.8fe0.1ni0.1po4、li1-xvopo4和li2fepo4f。
在另一个实施方案中,正电极包含具有以下化学式的正电极活性材料:
lixm1-(d+t+q+r)ddttqqrr(xo4)
其中:
m是选自fe、mn、co、ti、ni或其混合物的金属的阳离子;
d是选自mg2+、ni2+、co2+、zn2+、cu2+、和ti2+的具有+2氧化态的金属;
t是选自al3+、ti3+、cr3+、fe3+、mn3+、ga3+、zn3+、和v3+的具有+3氧化态的金属;
q是选自ti4+、ge4+、sn4+、和v4+的具有+4氧化态的金属;
r是选自v5+、nb5+、和ta5+的具有+5氧化态的金属;
x包含si、s、p、v或其混合物;
0≤x≤1;和
0≤d、t、q、r≤1,其中d、t、q和r中至少一个不为0。
在另一个实施方案中,正电极活性材料包含正电极活性材料,其包含选自lifepo4、limnpo4、licopo4、linipo4的有序的橄榄石电极化合物,混合过渡金属化合物例如li1-2xfe1-xtixpo4或life1-xmnxpo4(其中0<x<1),或具有通式limpo4和有序的橄榄石结构的其他化合物。
通常,“等电荷取代”是指在给定结晶位点上的一种元素用具有相似电荷的元素取代。例如,mg2+被认为与fe2+相似地等电荷,和v5+与p5+相似地等电荷。同样地,可用vo43-四面体取代po43-四面体。“异价取代”是指给定结晶位点上的一种元素用具有不同价态或电荷的元素取代。异价取代的一个实例将是在fe2+位点上的cr3+或ti4+。另一个实例将是在fe2+位点上的li+。这些正电极活性材料通常将具有基于铁或锰衍生物的橄榄石结构,其通式为:
lix+ym1-(y+d+t+q+r)ddttqqrr[po4]1-(p+s+v)[so4]p[sio4]s[vo4]v
其中
m可为fe2+或mn2+或其混合物;
d可为+2氧化态的金属,优选为mg2+、ni2+、co2+、zn2+、cu2+、或ti2+;
t可为+3氧化态的金属,优选为al3+、ti3+、cr3+、fe3+、mn3+、ga3+、zn3+、或v3+;
q可为+4氧化态的金属,优选为ti4+、ge4+、sn4+、或v4+;
r可为+5氧化态的金属,优选为v5+、nb5+、或ta5+;
在这种另外的实施方案中,m、d、t、q和r存在于八面体位点。额外的系数可定义如下:x代表在电极材料的工作过程中嵌入的程度;y代表在初始fe2+位点上锂离子的分数;d代表在初始fe2+位点上二价离子(标为d)的分数;t代表在初始fe2+位点上三价离子(标为t)的分数;q代表在初始fe2+位点上四价离子(标为q)的分数;r代表在初始fe2+位点上五价离子(标为r)的分数;p代表在初始p5+位点上六价硫(作为离散的so42-四面体)的分数;s代表在初始p5+位点上四价硅(作为离散的sio42-四面体)的分数;和v代表在初始p5+位点上五价钒离子的分数。
位点占用和电中性的条件意味着以下:
0≤x≤1;
y+d+t+q+r≤1;
p+s+v<1;和
3+s-p=x-y+t+2q+3r。
x、y、d、t、q、r、p、s和v可在0(零)和1(一)之间,其中y、d、t、q、r、p、s或v中至少一个不为0。在优选实施方案中,y、d、t、q、r和v可在0(零)和0.2({分数(2/10)})之间变化并且r和s可在0(零)和0.5(1/2)之间变化。在一些实施方案中,电极是锂嵌入电极。如本文所用,术语“嵌入”是指分子或离子可逆的包含或插入至具有层状结构的化合物中。因此,锂嵌入电极可为其中可将锂离子可逆地包括或插入层状结构(例如石墨)中的电极。
本发明的电池可在含有所述lix+ym1-(y+d+t+q+r)ddttqqrr[po4]1-(p+s+v)[so4]p[sio4]s[vo4]v材料的正电极中含有具有快速扩散动力学的嵌入材料。短语“快速扩散动力学”在本领域通常理解为是指在工作温度下材料能够维持每克材料至少10ma的比电流与大于80%的容量利用。优选地,具有快速扩散动力学的嵌入材料可为薄片状的双硫属化物、氧化钒vox(其中2.1≤x≤2.5)、或nasicon相关材料例如li3fe2(po4)3或li3-xfe2-xtix(po4)3(其中x代表用ti4+取代fe3+的程度)。
当从8.5伏特放电至1伏特时,本文所述的正电极活性材料可具有室温下在第10次放电循环中在c/3的放电倍率下至少约50mah/g的放电比容量。
集流体
集流体(电子收集器)可为导电的部件,其包含金属、传导聚合物、或其他传导材料。本发明电池的集流体可包含金属例如cu、pt、au、al、ni、fe、ti、mo、不锈钢、或其他金属或合金。电子收集器可具有额外的层以减少腐蚀,例如包含钨(w)、铂(pt)、钯(pd)、碳化钛(tic)、碳化铊(tac)、氧化钛(例如tio2或ti4o7)、磷化铜(cu2p3)、磷化镍(ni2p3)、磷化铁(fep)等的额外的层,或可包含这种材料的颗粒。
电化学稳定性
可期望在高电压下操作电池以提供更高的容量和/或提供更大的功率输出。采用本文所述的改进的硼硅酸锂玻璃电解质,可显著改进高电压电池的性质。例如,电池可具有更长的循环寿命。
对于高电压工作而言,电解质的另一个重要方面是还原和氧化稳定性。改进的还原和氧化稳定性改进了相应电池的循环性能。本文所述的硼硅酸锂玻璃电解质在电池的工作电压下最终没有反应(还原或氧化)。硼硅酸锂玻璃电解质具有例如对锂或碳单质负电极活性材料在高电压下工作的能力。本文所述改进的电解质可有效地改进在大于4.45v的高充电电压下工作的锂离子电池的循环性能。
因此,在另一个实施方案中,本发明涉及包含能够在高电压下工作的硼硅酸锂玻璃电解质的电池。在另外的实施方案中,高电压电池包含能够在高至4.45v、至少5v、至少5.5v、至少6v、至少7v、至少8v、至少9v、或至少10v下工作的硼硅酸锂玻璃电解质。在另外的实施方案中,硼硅酸锂玻璃电解质具有在25℃下大于1.0×10-6s/cm的离子传导率。在另外的实施方案中,硼硅酸锂玻璃电解质对锂是稳定的。在另外的实施方案中,硼硅酸锂玻璃电解质为在0.05-15微米之间厚、在0.3-4微米之间厚、或在2-4微米之间厚。在另一个实施方案中,电池包含锂阳极或者是不含锂的电池。
高离子和低电子传导率
在另一个实施方案中,本发明提供包含具有高离子传导率和低电子传导率的硼硅酸锂玻璃电解质的电池。在一个实施方案中,硼硅酸锂玻璃电解质具有大于1.0×10-6s/cm的离子传导率和小于8.6×10-14s/cm的电子传导率。在另外的实施方案中,电池具有大于1.0×10-6s/cm的离子传导率和小于8.6×10-14s/cm的电子传导率并能够在高至4.45v、至少5v、至少5.5v、至少6v、至少7v、至少8v、至少9v、或至少10v下工作。在另外的实施方案中,电池具有大于1.0×10-6s/cm的离子传导率和小于8.6×10-14s/cm的电子传导率并能够在高至4.45v下工作,并包含锂阳极或者是不含锂的电池。在另外的实施方案中,电池是全固态电池、薄膜电池、锂离子电池。
在另一个实施方案中,包含硼硅酸锂玻璃电解质的电池具有大于1.0×10-6s/cm的离子传导率和小于8.6×10-14s/cm的电子传导率并具有在0.04-5μah之间的完全充电容量。在另外的实施方案中,电池具有小于0.5μah的完全充电容量。在另外的实施方案中,电池具有小于0.1μah的完全充电容量。
包含硼硅酸锂表面改性电极的电池
本发明的一个方面涉及电池,其包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中用本文所述的libsio组合物改性正电极和/或负电极的表面。libsio组合物可基本上由氧化锂与氧化硅和/或氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。优选地,该硼硅酸锂组合物基本上由氧化锂与氧化硅和氧化硼结合的体系组成,其中基于锂、硼和硅的总原子百分比所述硼硅酸锂包含在70至83原子%之间的锂,且其中所述硼硅酸锂是玻璃。在一个实施方案中,电池包含libsio-表面改性的负电极。在另一个实施方案中,电池包含libsio-表面改性的正电极。
在一个实施方案中,电池包含正电极、负电极、和在所述正电极和所述负电极之间的电解质,其中用本发明的libsio组合物层涂覆正电极和/或负电极。
在一个实施方案中,本发明提供电池,其包含正集流体、包含正电极活性材料的正电极、电解质、包含负电极活性材料的负电极、和负集流体,其中用本文所述的libsio材料改性正电极和/或负电极的表面。在一个实施方案中,电池包含libsio-表面改性的负电极。在另一个实施方案中,电池包含libsio-表面改性的正电极。在另一个实施方案中,电池包含libsio-表面改性的负电极和libsio-表面改性的正电极。在另外的实施方案中,电池是锂离子二次电池。在另一个实施方案中,锂离子二次电池是薄膜电池。
在一个实施方案中,本发明提供电池,其包含正集流体、包含正电极活性材料的正电极、电解质、包含负电极活性材料的负电极、和负集流体,其中用本发明的libsio材料涂覆正电极和/或负电极,例如根据第一方面。在一个实施方案中,电池包含libsio-涂覆的负电极。在另一个实施方案中,电池包含libsio-涂覆的正电极。在另一个实施方案中,电池包含libsio-涂覆的负电极和libsio-涂覆的正电极。在另外的实施方案中,电池是锂离子二次电池。在另一个实施方案中,锂离子二次电池是薄膜电池。
电解质可包含有机电解质、液体电解质、离子液体、凝胶电解质、室温熔融盐或固体电解质。如果电解质是液体或凝胶,则优选地其为非水性电解质。在一个实施方案中,电解质是有机电解质。在另一个实施方案中,电解质是液体电解质。在另外的实施方案中,液体电解质是非水性电解质。在另一个实施方案中,电解质是凝胶电解质。在另一个实施方案中,电解质是熔融盐电解质。在另一个实施方案中,电解质是固体电解质。
在另一个实施方案中,液体非水性电解质包含锂盐和非水性溶剂。锂盐的实例包括lipf6、libf4、双(三氟甲磺酰)胺锂(litfsa、lin(cf3so2)2)、licf3so3、lic4f9so3、lic(cf3so2)3、liclo4、双(草酸合)硼酸锂(libob)、双(三氟甲磺酰)亚胺锂(litfsi)、双(氟磺酰)胺锂(lifsa、lin(so2f)2)、和licf3co2。非水性溶剂能够溶解锂盐。非水性溶剂的实例包括碳酸亚丙酯、碳酸亚乙酯、碳酸二乙酯、碳酸二甲酯、碳酸甲乙酯、1,2-二甲氧基乙烷、1,2-二乙氧基乙烷、乙腈、丙腈、四氢呋喃、2-甲基四氢呋喃、二氧六环、1,3-二氧戊环、硝基甲烷、n,n-二甲基甲酰胺、二甲基亚砜、环丁砜、碳酸亚乙烯酯和γ-丁内酯。
在一些实施方案中,电解质包含添加剂。电解质添加剂可容易且经济地改性电极-电解质界面。在一些实施方案中,电解质包含选自以下的添加剂:4-(三氟甲基)-1,3-二氧戊环-2-酮(tfm-ec)、三(六氟-异丙基)磷酸酯(hfip)、3-己基噻吩、lidfob、三(三甲基甲硅烷基)磷酸酯(tmsp)、三(三甲基甲硅烷基)硼酸酯(tmsb)、及其组合。
制作硼硅酸锂的方法
第九方面提供了制作本文所述硼硅酸锂玻璃的方法。在一个实施方案中,通过真空沉积工艺形成硼硅酸锂玻璃。在另外的实施方案中,通过物理气相沉积工艺形成硼硅酸锂玻璃。
物理气相沉积工艺对本领域技术人员通常是已知的。在本发明中,该工艺通常包括使用物理工艺(例如加热)以制备包括组分元素li、b、si和o的蒸气,然后将该蒸气沉积在基材上。在一个实施方案中,在100和400℃之间、优选地150至300℃、且更优选地200至250℃的温度下进行物理气相沉积工艺。
在一个实施方案中,在4.0x10-4和6.7x10-3pa之间(3x10-6和5×10-5乇之间)、优选地在2.7x10-3和4.7x10-3pa之间(2x10-5和3.5×10-5乇之间)的压力下进行物理气相沉积工艺。
在一个实施方案中,氧源可为氧的臭氧来源、氧的原子来源、或氧的分子来源。
在一个实施方案中,本发明涉及制作对锂电化学稳定的硼硅酸锂电解质的方法。在另外的实施方案中,电池包含锂阳极。
在另一个实施方案中,本发明涉及制作能够在高电压下工作的硼硅酸锂电解质的方法。在另外的方面,电池适合用于较长期循环。
在另一个实施方案中,本发明涉及制作具有低电子传导率的硼硅酸锂电解质的方法。在另外的实施方案中,电池具有低容量。
制作硼硅酸锂涂覆电极的方法
另一个方面提供制作libsio-表面改性的电极的方法。只要方法能够提供改进稳定性或改进电极循环的期望的libsio-表面改性的电极,则没有特别限制制作本发明的libsio-表面改性的电极的方法。方法的实例包括如本文所述的pvd。在一个实施方案中,方法是制作libsio-表面改性的负电极的方法。在另一个实施方案中,方法是制作libsio-表面改性的正电极的方法。在一个实施方案中,通过物理气相沉积(pvd)制备libsio涂层。
制作包含硼硅酸锂玻璃电解质的电池的方法
本发明的另外的方面涉及制作包含硼硅酸锂玻璃电解质的电池的方法。
在另一个实施方案中,通过在全固态状态相继形成成分膜制备薄膜电池。
制作包含硼硅酸锂涂覆电极的电池的方法
另外的方面提供制作包含电极的电池的方法,其中用本文所述的libsio材料改性该电极的表面。在一个实施方案中,方法是制作包含libsio-表面改性的负电极的电池的方法。在另一个实施方案中,方法是制作包含libsio-表面改性的正电极的电池的方法。在另外的实施方案中,电池是锂离子二次电池。在另一个实施方案中,锂离子二次电池是薄膜电池。
实施例
实施例1-制备libsio电解质
按照本发明的实施方案,使用公开于题目为“vapourdepositionmethodforpreparingamorphouslithium-containingcompounds”的wo2015/104540(通过引用将其全文并入本文)中的方法由组分元素锂、氧和两种玻璃形成元素硼和硅形成硼硅酸锂材料。通过提供化合物的每种组分元素的蒸气源并在从2.7x10-3至4.3x10-3pa(2x10-5至3.2x10-5乇)压力下将来自蒸气源的组分元素共沉积至被加热至225℃的基材上。组分元素在基材上反应以形成无定形的硼硅酸锂化合物。制备的化合物具有在以下实施例5中所述的组成。
在之前描述于文献(guerin,s.和hayden,b.e.,journalofcombinatorialchemistry8(2006)66-73)中的物理气相沉积(pvd)系统中进行沉积。利用氧等离子体源作为原子氧来源沉积所有样品。氧化物材料(硅酸锂和硼酸锂)需要硅和硼两者的最高氧化态(分别为4+和3+),并因此原子氧而不是分子氧的使用去除了将o2断裂成2o所需要的分解步骤并提供高反应性物质以使硅和硼氧化成它们的最高氧化态(如在材料li4sio4和li3bo3中需要的)。由knudsen电芯来源沉积锂。由电子枪(e-gun)来源沉积硅和硼两者。
其他真空沉积方法的使用可用于制造阴极、阳极、集流体和第一阻挡层材料。这可包括但不限于物理气相沉积、化学气相沉积(cvd)、rf溅射、分子束外延固态反应、脉冲激光沉积(pld)、溶胶-凝胶和原子层沉积(ald)。
在本发明的情况下,可通过将适当的化合物相继沉积至合适的导电基材上来构造电池。例如,可进行阳极层(例如来自li蒸发源的li金属)、电解质层(例如使用本文公开的方法制备的硼硅酸锂)、阴极层(例如来自组分蒸发源的lmo)和导电顶层的相继沉积以提供薄膜电池的层状结构。
实施例2-libsio电解质的电化学稳定性
由铂阴极集流体、limn2o4阴极、硼硅酸锂玻璃电解质、和li阳极制成薄膜电池。以三种方式说明硼硅酸锂玻璃电解质的稳定性。
实施例3-对锂阳极的稳定性
首先,使用线性扫描伏安法以在0.5和0.25mv/s之间的速率使电池在3.6和4.25v之间循环,然后观察电解质和阳极材料之间的有害反应。在100次循环之后,在电流随电势变化的曲线中没有迹象表明在电解质和阳极材料之间有害反应的存在。
实施例4-稳定的ocv
其次,在所述电池的循环之前和之后都观察了相同的薄膜电池系统的稳定的开路电压(ocv)。测定在寿命开始时的开路电压(其在阳极沉积在libsio固态电解质上之后40天测量)范围相对于li/li+从2.36至2.92v。如果锂与固态电解质以持久的方式反应,则其在阳极和阴极之间连续通路的形成中最终消耗libsio,导致测量的ocv为0v。
在经受10次在0.1μa电流下3.8和4.25伏特之间的恒电流循环、12次循环伏安法循环和23次在0.2μa电流下3.8和4.25v之间的恒电流循环之后观察相对于li/li+的4.15v的稳定的寿命终止(eol)ocv。
在循环完成之后每5秒测量lmo/libsio/li电芯的开路电压持续35分钟(图1),其最后阶段是在充电开始监测ocv持续15分钟(图2)。在右图的数据中所观察的分散是由外部扰动的测量中断所致。
如图3中所示,在包含alopt(蓝宝石、钛或二氧化钛(20nm)、铂(100nm))基材、lmo阴极、libsio电解质和li金属阳极的固态电芯上进行循环伏安法。在3.6和4.25v之间使电芯循环100次。在0.25mv/s下循环最初的三次循环,而在0.5mv/s扫描速率下进行剩下的97次循环。可见依赖于电势的电流的特征曲线没有随着反映从循环开始到结束的行为的数据组内那样改变。与电流幅度减小相关的容量降低是与循环有关的老化效应的征兆,但并不意味着与电解质和电极之间的不相容性有关的降解或不稳定,但是可与在经受所施加循环条件时阴极材料的内在稳定性有关。
实施例5-阻抗
由bates等人,journaloftheelectrochemicalsociety144[2](1997)524-533使用阻抗作为稳定性量度的应用,其中进行了在铂电极之间夹层或一个锂电极和一个铂电极之间夹层的lipon的阻抗之间的对比。
采用类似于bates等人文献中描述的方法在10次在3.8和4.25v之间以0.1μa恒电流循环之前和之后相对于li/li+的3.8v电势下在libsio电解质(72.6摩尔%li2o-6.8摩尔%b2o3-20.6摩尔%sio2)样品上测量了阻抗。本文使用了在261.0156khz至0.1hz之间的频率范围,其中每个进位有七个数据点,并且ac幅度为10mv。如图4a和b所示,在数据组的高频范围(图4a)中循环之前和之后收集的阻抗谱之间几乎没有或没有差异,如图中纵坐标轴和横坐标轴上40kω以下的数据点(图4b)所提供的。正是在这一频率范围内,数据反映了电解质和在电解质与电极之间界面的贡献。因此,循环之前和之后的数据的再现性表明libsio固态电解质与相邻锂阳极之间的界面的稳定性。
第三,在循环之前和之后对比了阻抗并且显示了在反映来自电解质和在电解质与相邻电极之间界面的贡献的频率范围内其大部分未改变。
这一发现的技术效果是其促进了在用沉积状态的锂阳极构造的固态电池中和在不含锂的电芯内硼硅酸锂玻璃组合物的使用,由此在固态硼硅酸锂电解质和阳极集流体之间的界面处原位地形成锂阳极。
实施例6-在高电压下的电化学稳定性
如以下所示制作了许多硼硅酸锂组合物,其中li、b和si的值是关于li:b:si的原子百分比:
1.li=80.9、b=7.56、si=11.5
2.li=79.6、b=13.7、si=6.7
3.li=78.5、b=9.6、si=11.87
4.li=77.73、b=10.07、si=12.19
5.li=76.89、b=10.55、si=12.56
6.li=76.14、b=10.98、si=12.88
7.li=75.30、b=11.46、si=13.24
8.li=74.54、b=11.89、si=13.58
9.li=73.16、b=12.62、si=14.22
10.li=71.86、b=13.31、si=14.83
11.li=70.41、b=14.07、si=15.51
12.li=69.12、b=14.76、si=16.12;
其中氧以形成氧化物并维持电中性的量存在。
当沉积在铂涂覆的基材上(充当底部电极)而上部电极沉积在硼硅酸锂电解质上并由镍或铂组成时,libsio组合物表现出跨从0至5v范围的电势中的电化学稳定性。选择并测试并发现一个代表性样品表现出跨从0至10v范围的电势中的电化学稳定性。
这一发现的技术效果是对于如本文所述的硼硅酸锂组合物而言,可在非常高电压下工作传送高能量密度的固态电池组成中使用该材料。
实施例7-电子传导率和离子传导率
对于libsio体系中一系列组合物而言测量电子传导率和离子传导率随锂含量(基于组分li、b和si大约69-79%锂)的变化。从使用solartron1260频率响应分析仪在1mhz和1hz之间使用100mv的ac电势(每个频率一秒积分,每十个测量七个频率点)进行的阻抗测量来测定离子传导率值。通过使用在zview软件程序中构造的等效电路模型拟合实验数据来计算传导率值,以测定与薄膜电解质相关的电阻的实部,然后将其与几何因数结合使用以测定离子传导率。使用keithley2636系列数字源表测定电子传导率值。跨样品的电极施加1v的dc电势持续65小时,其中稳态电流、施加的电压和几何因数用于计算电子传导率值。在法拉第笼壳体中进行电子传导率值的测量。电子传导率在1.84×10-14和4.40×10-14s/cm之间而离子传导率在8.74×10-7和5.72×10-6s/cm之间。
这一发现的技术效果是电子传导率足够低,由非常低的电子传导率性质(<7×10-14s/cm)所致以它们维持充电状态的能力为基础,可在具有非常低理论容量(<0.5μah)的固态电池中使用lisbio玻璃电解质。
实施例8-用libsio涂覆的阴极材料的利用
图6显示随lmo中li原子百分比(x轴)变化的libsio涂覆的(空心圆形)与未涂覆的(实心圆形)lmo阴极样品对比的第一次放电的利用数(y轴)。从由10x10pt电极阵列所产生曲线的数据,电极上沉积具有锂含量在18.38和48.43原子%之间锂的lmo离散区域(由lmo膜的li和mn组分确定)。沉积在下面的pt集流体上的lmo活性阴极材料从元素沉积至维持在450℃的基材上,锂和锰熔剂源自knudsen电芯来源和通过具有3.5sccm的o2流速和500w功率的等离子源供应氧。在libsio涂层沉积在测试样品上之前,在o2下将包含单个lmo样品区域阵列的基材处理至550℃持续2小时。libsio膜沉积在十行中的七行上,而剩下的三行区域保持未涂覆。使用内部恒电势仪通过循环伏安法对电极阵列进行电化学测试。电压范围在3.25v和4.75v之间,扫描速率为0.104mv/sec。参比对电极是一片0.5mm厚的锂箔并且电解质包含在ec:dmc(1:1)中的1mlipf6。通过以下处理用于产生图像的数据:首先平均化样品上所有组成等效位点(对于具有libsio的那些而言7个/组成,对于没有libsio而言3个/组成,除非由于电极失效而存在空值),然后取所有值都落在该平均值的一个标准差内的平均值。
以上说明书中提及的所有出版物均通过引用并入本文。在不脱离本发明的范围和精神的情况下,本发明所述方法和系统的各种修改和变化对于本领域技术人员是明显的。尽管结合具体的优选实施方案已经描述了本发明,但是应理解要求保护的发明不应过于限制于这些具体的实施方案。实际上,对于化学和材料科学或相关领域的技术人员而言显而易见的用于实施本发明的所述模式的各种修改旨在落入以下权利要求的范围内。
- 还没有人留言评论。精彩留言会获得点赞!