一种安全无刺激可以入口的消毒剂配方及其生产工艺的制作方法
本发明涉及一种消毒液,具体为一种安全无刺激可以入口的消毒剂配方及其生产工艺,属于消毒液制备
技术领域:
。
背景技术:
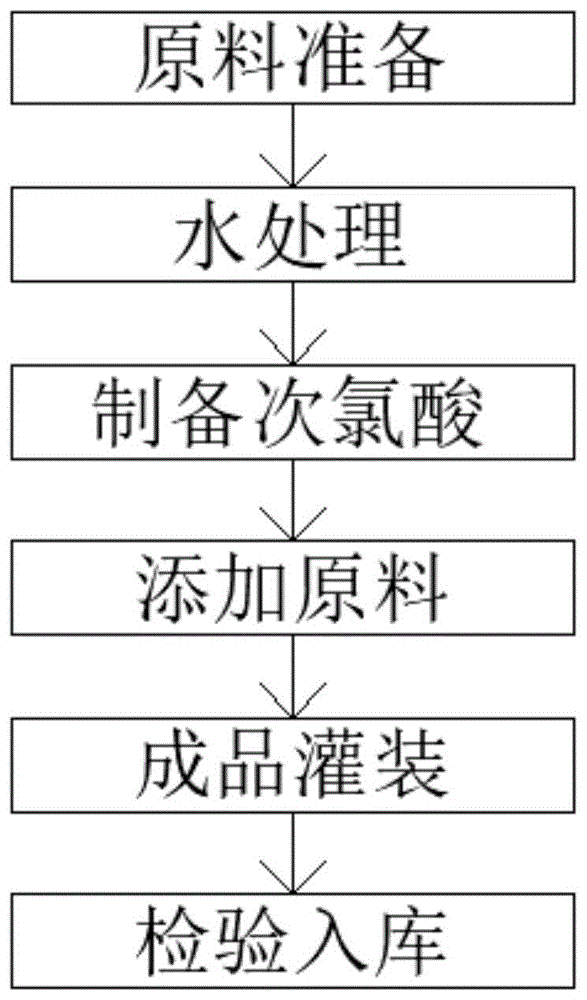
:84消毒液是一种以次氯酸钠为主要成分的含氯消毒剂,主要用于物体表面和环境等的消毒。次氯酸钠具有强氧化性,可水解生成具有强氧化性的次氯酸,能够将具有还原性的物质氧化,使微生物最终丧失机能,无法繁殖或感染。现在市场上的消毒产品大部分是以84消毒液和酒精为主,而84消毒液刺激味道太大,酒精又易燃易爆。技术实现要素:本发明的目的就在于为了解决上述问题而提供一种安全无刺激可以入口的消毒剂配方及其生产工艺。本发明通过以下技术方案来实现上述目的:一种安全无刺激可以入口的消毒剂配方,所述配方包括次氯酸钠、亚氯酸钠、氯化钠、纯化水、柠檬酸钠、edta二钠,所述纯化水的成份占比为80%-85%,所述次氯酸钠的成份占比为3%-4.5%,所述亚氯酸钠的成份占比为0.5%-0.8%,所述氯化钠的成份占比为5%-8%,所述柠檬酸钠以及edta二钠的成份占比为1.7%-11.5%;所述生产工艺包括以下步骤:步骤一、原料准备,根据所需制备的量,按照各成分占比分别称取相应重量的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠等原材料;步骤二、水处理,将自来水的出水端接入净化水设备的接入端,经过净化水设备处理生成纯化水;步骤三、制备次氯酸,量取定量的纯化水注入到次氯酸生成设备,生成次氯酸溶液;步骤四、添加原料,依次将所称取的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠加入到次氯酸溶液内,同时加入二氧化碳原液,生成次氯酸消毒液;步骤五、成品灌装,将制备好的次氯酸消毒液通过灌装机进行分瓶灌装;步骤六、检验入库。作为本发明再进一步的方案:所述次氯酸钠、亚氯酸钠、氯化钠、柠檬酸钠以及edta二钠均为无异味,无刺激性的原料。作为本发明再进一步的方案:所述步骤一中,进行称量时采用电子天平进行称取,且精度为0.01g。作为本发明再进一步的方案:所述步骤四中,添加的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠等原材料与次氯酸溶液构成混合溶液。本发明的有益效果是:该可以入口的消毒液设计合理,与市面上现有的消毒液相比具有无刺激、无异味、安全、不易燃、易运输等优点,且目前市面上的次氯酸大部分都是电解而成,本发明采用的是混合而成,加上在生产过程中加入了二氧化碳,具有与其他次氯酸相比具有稳定性好,含量高等优点市场上的次氯酸有效期一般是12个月,而本发明产品有效期可以达到24个月。附图说明图1为本发明制备流程示意图。具体实施方式下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。请参阅图1,一种安全无刺激可以入口的消毒剂配方,所述配方包括次氯酸钠、亚氯酸钠、氯化钠、纯化水、柠檬酸钠、edta二钠,所述纯化水的成份占比为80%-85%,所述次氯酸钠的成份占比为3%-4.5%,所述亚氯酸钠的成份占比为0.5%-0.8%,所述氯化钠的成份占比为5%-8%,所述柠檬酸钠以及edta二钠的成份占比为1.7%-11.5%;所述生产工艺包括以下步骤:步骤一、原料准备,根据所需制备的量,按照各成分占比分别称取相应重量的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠等原材料;步骤二、水处理,将自来水的出水端接入净化水设备的接入端,经过净化水设备处理生成纯化水;步骤三、制备次氯酸,量取定量的纯化水注入到次氯酸生成设备,生成次氯酸溶液;步骤四、添加原料,依次将所称取的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠加入到次氯酸溶液内,同时加入二氧化碳原液,生成次氯酸消毒液;步骤五、成品灌装,将制备好的次氯酸消毒液通过灌装机进行分瓶灌装;步骤六、检验入库。所述次氯酸钠、亚氯酸钠、氯化钠、柠檬酸钠以及edta二钠均为无异味,无刺激性的原料,很好的解决了味道大,刺激性强,不好运输的缺点。所述步骤一中,进行称量时采用电子天平进行称取,且精度为0.01g,确保原料称取的精准度较高,进而可使制备的消毒液符合配方标准。所述步骤四中,添加的次氯酸钠、亚氯酸钠、氯化钠、柠檬酸以及edta二钠等原材料与次氯酸溶液构成混合溶液,采用混合工艺制成的消毒液与其他次氯酸相比具有稳定性好,含量高等优点做出来的产品有效期更长。实施例一ph值检测一、器材1.样品:次氯酸消毒剂(批号为20190813)。2.试验仪器:phs-25ph计。3.试剂等级:分析纯。4.标准溶液:混合磷酸盐缓冲液ph=6.86,邻苯二甲酸氢钾缓冲液ph=4.00,硼酸钠缓冲液ph=9.18。二、方法1.检验依据:《消毒技术规范》(2002年版)2.2.1.4。2.检测环境:温度为22℃,相对湿度52%。三、结果次氯酸消毒剂ph值均值为6.59。四、结论次氯酸消毒剂(批号为20190813)ph值均值为6.59,检测结果符合企标q410183hly044—2019关于ph值的规定。实施例二有效氯一、器材1.样品:次氯酸消毒剂(批号为20190813),有效成分为有效氯。2.试验仪器:100ml容量瓶、10ml滴定管。3.试剂等级:分析纯。4.标准溶液:0.1008moll硫代硫酸钠滴定液。二、方法1.检验依据:《消毒技术规范》(2002年版)2.2.1.2.12。2.检测环境:温度为25℃,相对湿度43%。三、结果次氯酸消毒剂(批号为20190813)经容量法检测,有效氯含量为160mg/l;四、结论次氯酸消毒剂(批号为20190813)经容量法检测,有效氯含量为160mg/l,检测结果符合企标q/410183hly044—2019关于有效氯的规定。实施例三稳定性检测一、器材1.样品:次氯酸消毒剂(批号为20190813),有效成分为有效氯。2.试验仪器:100ml容量瓶、10ml滴定管、恒温恒湿箱(bsc-400)。3.试剂等级:分析纯。4.标准溶液:0.1008mol/l硫代硫酸钠滴定液。二、方法1.检验依据:《消毒技术规范》(2002年版)2.2.1.2.12。2.检测环境:温度为25℃,相对湿度46%。3.保存条件:温度37℃,时间90天。三、结果次氯酸消毒剂(批号为20190813)置37℃恒温恒湿箱储存90d后,经容量法检测其有效氯含量为145mgl,下降率为9.4%;四、结论次氯酸消毒剂(批号为20190813)置37℃恒温恒湿箱储存90d后,经容量法检测其有效氯含量为145mgl,下降率为9.4%,试验结果符合《消毒技术规范》(2002年版)的要求,该产品贮存有效期可定为2年。实施例四铅含量检验一、器材1.样品:次氯酸消毒剂(批号为20190813)。2.试验仪器:agilent280z原子吸收光谱仪。3.试剂等级:优级纯。4.标准溶液:铅标准溶液gbw08619(国家标准物质中心)。二、方法1.检验依据:国家食药局《化妆品安全技术规范》(2015年版)第四章(1.3)。2.检测环境:温度为25℃,相对湿度46%。三、结果次氯酸消毒剂(批号为20190813)经石墨炉原子吸收光谱法检测,铅含量为0.10mgkg。四、结论次氯酸消毒剂(批号为20190813)经石墨炉原子吸收光谱法检测,铅含量为0.10mgkg,检测结果符合《化妆品安全技术规范》(2015年版)关于铅限值的规定。实施例五砷含量检验一、器材1.样品:次氯酸消毒剂(批号为20190813)。2.试验仪器:afs-8220原子荧光光度计。3.试剂等级:优级纯。4.标准溶液:砷标准溶液gbw08611(国家标准物质中心)。二、方法1.检验依据:国家食药局《化妆品安全技术规范》(2015年版)第四章(1.4)。2.检测环境:温度为25℃,相对湿度47%。三、结果次氯酸消毒剂(批号为20190813)经氢化物原子荧光光度法检测,砷含量为<0.01mgkg。四、结论次氯酸消毒剂(批号为20190813)经氢化物原子荧光光度法检测,砷含量为<0.01mgkg,检测结果符合《化妆品安全技术规范》(2015年版)关于砷限值的规定。实施例六汞含量检验一、器材1.样品:次氯酸消毒剂(批号为20190813)。2.试验仪器:afs-8220原子荧光光度计。3.试剂等级:优级纯。4.标准溶液:汞标准溶液gbw08617(国家标准物质中心)。二、方法1.检验依据:国家食药局《化妆品安全技术规范》(2015年版)第四章(1.2)。2.检测环境:温度为25℃,相对湿度47%。三、结果次氯酸消毒剂(批号为20190813)经氢化物原子荧光光度法检测,汞含量为0.019mg/kg。四、结论次氯酸消毒剂(批号为20190813)经氢化物原子荧光光度法检测,汞含量为0.019mg/kg,检测结果符合《化妆品安全技术规范》(2015年版)关于汞限值的规定。实施例七细菌繁殖体定量杀菌检验一、器材1.试验菌株:金黄色葡萄球菌(atcc6538),培养至第9代;铜绿假单胞菌(atcc15442),培养至第9代;大肠杆菌8099,第7代,原始菌株购自广东环凯微生物科技有限公司。2.受试样品:次氯酸消毒剂,批号为20190813,有效成分为有效氯。3.中和剂:d/e中和肉汤。4.培养基:营养琼脂培养基,压力蒸汽灭菌后备用。5.有机干扰物:3%牛血清白蛋白。6.稀释液:无菌硬水、pbs缓冲液。二、方法1.检测依据:《消毒技术规范》(2002年版)2.1.1.2~2.1.1.7。2.金黄色葡萄球菌中和剂鉴定试验:次氯酸消毒剂,中和剂为d/e中和肉汤,第1、2组消毒作用时间为2min。试验重复3次。3.悬液定量杀菌试验:次氯酸消毒剂,试验重复3次。4.试验环境:温度23~25℃,湿度52~57%。三、结果1.金黄色葡萄球菌中和剂鉴定试验:次氯酸消毒剂,作用2min,第1组平均生长菌落数为0cfu/ml,第2组平均生长菌落数为39~fu/ml,第3、4和5组平均生长菌落数分别为2.04×107cfu/ml、2.01×107cfu/ml、1.85×107cfu/ml,组间误差率为3.81%,第6组无菌生长。2.对细菌繁殖体的杀菌效果:试验重复3次,所试次氯酸消毒剂(批号为20190813),作用2min,对金黄色葡萄球菌、铜绿假单胞菌及大肠杆菌平均平均杀菌率为99.999%。次氯酸消毒剂对金黄色葡萄球菌的杀菌效果次氯酸消毒剂对铜绿假单胞菌的杀菌效果次氯酸消毒剂对大肠杆菌的杀菌效果四、结论1.试验条件下,d/e中和肉汤中和剂在悬液定量杀菌试验中可有效中和次氯酸消毒剂(批号为20190813)对细菌繁殖体的抑制作用;且该中和剂及其与次氯酸消毒剂形成的中和产物对受试菌(金黄色葡萄球菌)生长及培养无影响。2.试验条件下,所试次氯酸消毒剂(批号为20190813),作用2min,对金黄色葡萄球菌、铜绿假单胞菌及大肠杆菌平均杀菌率为9.99%,符合《消毒技术规范》(2002年版)的要求,产品有杀菌作用。实施例八白色念珠菌定量杀菌试验一、器材1.试验菌株:白色念珠菌(atcc10231),培养至第5代,原始菌株购自广东环凯微生物科技有限公司。2.受试样品:次氯酸消毒剂,批号为20190813,有效成分为有效氯。3.中和剂:d/e中和肉汤。4.培养基∶沙氏琼脂培养基,压力蒸汽灭菌后备用。5.有机干扰物:3%牛血清白蛋白。6.稀释液:无菌硬水、pbs缓冲液。二、方法1.检测依据:《消毒技术规范》(2002年版)2.1.1.92.白色念珠菌中和剂鉴定试验:次氯酸消毒剂,中和剂为d/e中和肉汤,第1、2组消毒作用时间为2min,试验重复3次。3.悬液定量杀菌试验:次氯酸消毒剂,试验重复3次。4.试验环境:温度23~25℃,湿度52~57%。三、结果1.白色念珠菌中和剂鉴定试验:次氯酸消毒剂,作用2min,第1组平均生长菌落数为0cfu/ml,第2组平均生长菌落数为58cfu/ml,第3、4和5组平均生长菌落数分别为1.92×106cfu/ml、1.86×106cfu/ml、2.19×106cfu/ml,组间误差率为6.79%,第6组无菌生长。2.对白色念珠菌的杀菌效果:试验重复3次,所试次氯酸消毒剂,作用2min,对白色念珠菌平均杀菌率为99.999%四、结论1.试验条件下,d/e中和肉汤中和剂在悬液定量杀菌试验中可有效中和次氯酸消毒剂(批号为20190813)对白色念珠菌的抑制作用;且该中和剂及其与次氯酸消毒剂(批号为20190813)形成的中和产物对受试菌(白色念珠菌)生长及培养无影响。2.试验条件下,所试次氯酸消毒剂(批号为20190813),作用2min,对白色念珠菌平均杀菌率为99.999%,符合《消毒技术规范》(2002年版)的要求,产品有杀菌作用。实施例九微生物污染试验一、器材1.样品:次氯酸消毒剂(批号为20190813)。2.培养基:营养琼脂培养基,scdlp固体培养基,血琼脂平板,乳糖胆盐培养基,葡萄糖肉汤,沙氏琼脂培养基。3.培养箱:培养箱((fxb303-4)。二、方法1.检验依据:《消毒技术规范》(2002年版)。2.检测环境:温度24℃,相对湿度50%。三、结果该样品微生物污染检测结果均符合规定。检测指标标准值检测结果评价细菌菌落总数(cfu/ml)≤200<10符合规定大肠菌群不得检出未检出符合规定金黄色葡萄球菌不得检出未检出符合规定铜绿假单胞菌不得检出未检出符合规定溶血性链球菌不得检出未检出符合规定真菌菌落总数(cfu/ml)≤100<10符合规定四、结论次氯酸消毒剂(批号为20190813)微生物污染检测结果符合《一次性使用卫生用品卫生标准》(gb15979-2002)的要求。实施例十急性经口毒性试验一、器材1.样品:次氯酸消毒剂(批号20190813),液体。2.试验动物:昆明小鼠,spf级,体重18g~22g,20只,雌雄各半,由河南省实验动物中心提供,合格证号dw2019100082。3.饲养环境:普通环境+ivc,使用许可证号:syxk(豫)2018-0007。4.饲料:全价营养鼠饲料,由河南省实验动物中心提供,合格证号sl2019100048。5.饮水处理:无菌净水器过滤。二、方法1.检验依据:《消毒技术规范》(2002年版)中2.3.1"急性经口毒性试验"的"一次限量法"。2.环境温度:20℃~24℃,环境相对湿度:40%~70%。3.样品处理及剂量配制:取5.0g样品加蒸馏水溶解定容至20ml混匀作为灌胃液。4.给予方式:禁食过夜(自由饮水),次日早按剂量经口一次性给予受试物,灌胃量20ml/kg。5.实验步骤:20只小鼠(雌雄各半),一次灌胃剂量5000mg/kg体重,观察14天,记录死亡、中毒情况。三、结果20只小鼠(雌、雄各半)在14天观察期内未出现明显中毒症状,无死亡,试验结束尸检未见明显异常。四、结论依据《消毒技术规范》(2002年版)小鼠急性经口半数致死量lds0>5000mg/kg体重判定:次氯酸消毒剂(批号20190813)属实际无毒级。实施例十一多次完整皮肤刺激试验检验一、器材1.样品:次氯酸消毒剂(批号20190813),液体。2.试验动物:日本大耳白兔,普通级,雄性3只,体重约2kg,由武汉市万千佳兴生物科技有限公司提供,合格证号422020500005485。3.饲养环境:普通环境,使用许可证号:syxk(豫)2018-0007。4.饲料:由河南省实验动物中心提供c级兔饲料,合格证号sl2019100048。二、方法1.检测依据:《消毒技术规范》(2002年版)第2.3.3条“皮肤刺激试验”2.环境温度:20℃~24℃,环境相对湿度:40%~70%。3.染毒方式:经皮染毒。4.皮肤处理方法:用宠物修理剪去毛。5.试验操作步骤:试验前24h,用宠物用修理剪去除动物背部脊柱两侧的毛,去毛范围3cm×3cm,不可损伤表皮。取受试物0.5ml直接涂抹在动物一侧去毛皮肤上(另一侧作为空白对照),涂抹面积2.5cm×2.5cm,在涂抹后4h,用水或无刺激的适宜溶剂清洗,除去残留物。每天涂抹一次,连续涂抹14d。在每次涂抹后24h观察结果参照《消毒技术规范》(2002年版)皮肤刺激反应评分标准评分,结果汇总填入附表。三、结果试验结果及评分见附表。四、结论依据《消毒技术规范》(2002年版)皮肤刺激强度分级评价标准判定:次氯酸消毒剂工批材20190813)对家兔多次完整皮肤刺激试验属无刺激性。实施例十二阴道黏膜刺激试验一、器材1.样品:次氯酸消毒剂(批号20190813),液体。2.试验动物:日本大耳白兔,普通级,雌性6只,体重约2kg,由武汉市万千佳兴生物科技有限公司提供,合格证号422020500005484。3.饲养环境:普通环境,使用许可证号:syxk(豫)2018-0007。4.饲料:由河南省实验动物中心提供c级兔饲料,合格证号sl2019100048。二、方法1.检验依据:《消毒技术规范》(2002年版)中2.3.5"阴道黏膜刺激试验"2.环境温度:20℃~24℃,环境相对湿度:40%~70%。3.受试物浓度及配制:使用样品原液作为受试物。4.给予方式:经阴道注入。5.试验步骤:将8cm软导管用受试液(对照液)湿润后轻柔插入动物阴道4~5cm,并将受试物2ml注入动物阴道内(对照组用生理盐水)。染毒24h后采用气拴法处死动物,剖腹取出完整阴道组织,肉眼观察有无充血、水肿现象。然后将其放入10%福尔马林溶液中固定24h,选取两端和中央3个部位制片、he染色后,进行组织病理学检查。三、结果四、结论依据《消毒技术规范》(2002年版)2.3.5.5判定:次氯酸消毒剂(批号20190813)对家兔阴道黏膜刺激强度分级属无刺激性。实施例十三小鼠骨髓嗜多染红细胞微核试验一、器材1.样品:次氯酸消毒剂(批号20190813),液体。2.试验动物:昆明小鼠,spf级,体重25g~30g,50只,雌雄各半,由河南省实验动物中心提供,合格证号dw2019100082。3.饲养环境:普通环境+itvc,使用许可证号:syxk(豫)2018-0007。4.饲料:全价营养鼠饲料,由河南省实验动物中心提供,合格证号sl2019100048。5.饮水处理:无菌净水器过滤。二、方法1.检测依据:卫生部《消毒技术规范》(2002年版)2.3.8.4小鼠骨髓嗜多染红细胞微核试验。2.动物分组及剂量配制:设1.25g/kg、2.50g/kg、5.00g/kg作为低、中、高剂量组,每个剂量组用10只小鼠,雌雄各半。即分别称取1.25g、2.50g、5.00g样品加蒸馏水至20ml,混匀;溶剂对照组为蒸馏水,阳性对照组为环磷酰胺40mg/kgbw,称取环磷酰胺40mg加生理盐水至20ml。3.环境温度:20℃~24℃,环境相对湿度:40%~70%。4.受试物给予方式:经口灌胃,灌胃量20ml/kg。5.试验操作步骤:采用经口灌胃30h染毒法。即两次染毒间隔24h,第二次染毒6h后处死动物。取胸骨用止血钳挤出骨髓液与玻片一端的小牛血清混匀,常规涂片。涂片自然干燥后放入甲醇中固定10分钟,晾干后放入giemsa应用液中,染色15分钟,立即用ph6.8的磷酸缓冲液冲洗、晾干。显微镜下观察计数1000个pce,计算微核率(‰)和pce/nce值。三、结果:四、结论依据《消毒技术规范》(2002年版)判定:次氯酸消毒剂(批号20190813)小鼠骨髓嗜多染红细胞微核试验阴性。对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。不应将权利要求中的任何附图标记视为限制所涉及的权利要求。此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1